Пиколинат хрома(III)
 | |||
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Трис(пиколинат)хрома(III) | |||
| Идентификаторы | |||
3D model ( JSmol ) |
| ||
| ЧЭБИ | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.131.423 | ||
ПабХим CID | |||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| Cr(C 6 H 4 NO 2 ) 3 | |||
| Молярная масса | 418.33 g/mol | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Пиколинат хрома (III) представляет собой химическое соединение с формулой Cr(C 5 H 4 N(CO 2 H)) 3 , обычно сокращенно CrPic 3. Он продается в качестве пищевой добавки для лечения диабета 2 типа и способствует снижению веса. [1] Это ярко-красное координационное соединение является производным хрома (III) и пиколиновой кислоты . Следовые количества (25-35 мкг [2] ) хрома необходимы для глюкозы утилизации инсулином при нормальном состоянии здоровья, но дефицит встречается крайне редко и обычно наблюдается у людей, получающих 100% своих потребностей в питательных веществах внутривенно, т. е. на диетах с полным парентеральным питанием . [3] Было установлено, что хром регулирует инсулин, повышая чувствительность рецептора инсулина . [4] Таким образом, пиколинат хрома (III) был предложен для лечения диабета 2 типа , хотя его эффективность остается спорной из-за противоречивых данных испытаний на людях. [5]
История
[ редактировать ]Исследование, проведенное в 1989 году, показало, что пиколинат хрома (III) может способствовать снижению веса и увеличению мышечной массы, что привело к увеличению использования добавок пиколината хрома (III) , в результате чего он на какое-то время стал второй наиболее широко используемой добавкой после кальций. [5] 2013 года Кокрейновский обзор не смог найти «надежных доказательств для принятия твердых решений» в поддержку таких утверждений. [6] Исследования в целом показали, что он улучшает чувствительность к инсулину, либо продлевая его активность, либо повышая выработку мРНК для производства большего количества рецепторов инсулина . [ нужна ссылка ]
Среди переходных металлов Cr 3+ является наиболее спорным с точки зрения пищевой ценности и токсичности. [7] Этот спор сосредоточен на том, является ли Cr 3+ обеспечивает какие-либо питательные преимущества. [7] [8] Более того, это противоречие усугубляется тем фактом, что ни для одной Cr-содержащей биомолекулы не была охарактеризована структура и не был определен способ действия. Первый эксперимент, приведший к открытию Cr 3+ играя роль в метаболизме глюкозы, предположили, что биологически активная форма металла существует в белке, называемом фактором толерантности к глюкозе , однако новые данные свидетельствуют о том, что это просто артефакт, полученный в результате процедур выделения. [5] [7] [9] [10] Единственным общепринятым показателем дефицита хрома является изменение симптомов, которое происходит при введении добавок хрома (III) людям, находящимся на полном парентеральном питании . [11]
Физико-химические свойства
[ редактировать ]

Пиколинат хрома(III) представляет собой соединение розовато-красного цвета, о котором впервые сообщалось в 1917 году. [5] [12] Он плохо растворяется в воде, его растворимость составляет 600 мкМ в воде при pH, близком к нейтральному . [8] Подобно другим соединениям хрома (III), он относительно инертен и нереакционноспособен, а это означает, что этот комплекс стабилен в условиях окружающей среды, и необходимы высокие температуры . для разложения соединения [13] При более низких уровнях pH комплекс гидролизуется с высвобождением пиколиновой кислоты и свободного Cr. 3+ . [8]
Структура
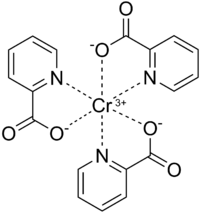
[ редактировать ]Пиколинат хрома (III) имеет искаженную октаэдрическую геометрию и изоструктурен аналогам кобальта (III) и марганца (III). [14] [15] Хром(III) представляет собой жесткую кислоту Льюиса и поэтому имеет высокое сродство к карбоксилатному кислороду и среднее сродство к пиридиновому азоту пиколината . [14] [16] Каждый пиколинатный лиганд действует как бидентатный хелатирующий агент и нейтрализует заряд +3 Cr. 3+ . Доказательства того, что Кр 3+ Координаты центра пиридинового азота происходят из-за сдвига в ИК-спектрах C=N колебания на 1602,4 см. −1 для свободной пиколиновой кислоты до 1565,9 см −1 для пиколината хрома(III). [14] Длина связи между Cr 3+ а атом азота пиридинового кольца пиколината находится в диапазоне от 2,047 до 2,048 Å . [15] Пиколинатный лиганд координируется с Cr 3+ только при депротонировании , о чем свидетельствует исчезновение ИК-полос в диапазоне от 2400 до 2800 см-1. −1 (центр 2500 см −1 ) и 1443 см. −1 , что соответствует растяжению и изгибу ОН карбоксильной функциональной группы соответственно. [13] [14] Кроме того, этот ИК-сдвиг также указывает на то, что только один атом кислорода из карбоксилата пиколината координируется с Cr 3+ центр. [13] [14] [16] Длина связи Cr-O колеблется от 1,949 до 1,957 Å . [15] Кристаллическая структура была описана совсем недавно, в 2013 году. [16] Вода не координируется с Cr 3+ Считается, что вместо этого он образует водородную связь между другими комплексами Cr(Pic) 3 , образуя сеть комплексов Cr(Pic) 3 . [16]
Биохимия пиколината хрома(III)
[ редактировать ]Хром был идентифицирован как необходимое питательное вещество для поддержания нормального уровня глюкозы в крови, и поэтому предполагается, что он взаимодействует с двумя естественными молекулами, обнаруженными в организме. [9] Эти взаимодействия, скорее всего, происходят посредством координации с жесткими лигандами, такими как аспартат и глутамат, поскольку Cr(III) сам по себе является твердым металлом.
Всасывание и выведение пиколината хрома(III)
[ редактировать ]При попадании пиколината хрома(III) в желудок происходит кислотный гидролиз комплекса при контакте со слизистой оболочкой желудка . [17] Гидролизованный Cr 3+ присутствует в форме гексааква и полимеризуется с образованием нерастворимого гидроксида-оксида Cr(III) (процесс олатирования ) , как только он достигает щелочного pH тонкого кишечника . [18] Примерно 2% Cr 3+ всасывается через кишечник в виде пиколината хрома (III) посредством ненасыщенного пассивного транспорта . [12] Хотя абсорбция низкая, CrPic 3 абсорбируется более эффективно, чем другие органические и неорганические источники (т.е. CrCl 3 и никотинат хрома) и, таким образом, накапливается в тканях в более высоких концентрациях. [10] [19] Это было одним из основных преимуществ пиколината хрома (III) по сравнению с другими добавками хрома (III). Органические источники имеют тенденцию лучше усваиваться, поскольку они имеют более липофильные лиганды и обычно нейтрализуют заряд металла, тем самым обеспечивая более легкое прохождение через кишечную мембрану. [19]
Также было показано, что диетические факторы влияют на Cr. 3+ поглощение. Крахмал , простые сахара , щавелевая кислота и некоторые аминокислоты имеют тенденцию увеличивать скорость всасывания хрома(III). Это результат хелатирования лиганда, превращающего гексааква Cr 3+ в более липофильные формы. [19] Напротив, кальций, магний, титан, цинк, ванадий и железо снижают скорость всасывания. [19] Предположительно, эти ионы вводят новое равновесие металл-лиганд, тем самым уменьшая пул липофильных лигандов, доступных для Cr. 3+ . После всасывания в кровоток 80% Cr 3+ из CrPic 3 передается трансферрину. [17] [19] [20] высвобождения Точный механизм в настоящее время неизвестен, однако считается, что он не происходит путем одноэлектронного восстановления, как в случае с Fe. 3+ , из-за высокой нестабильности Cr 2+ . [18] Администрирование Cr 3+ обнаруживается во всех тканях в пределах от 10 до 100 мкг/кг массы тела. [19] Выводится преимущественно с мочой (80%), остальная часть выводится с потом и калом. [19]
Связывание хрома(III) с трансферрином
[ редактировать ]
Трансферрин , помимо хромодулина, был идентифицирован как основной физиологический агент транспорта хрома. [20] [22] хотя недавнее исследование показало, что Cr 3+ фактически лишает трансферрин функции транспорта ионов металлов. [23] Хотя трансферрин очень специфичен к ионам трехвалентного железа, в нормальных условиях только 30% молекул трансферрина насыщены ионами трехвалентного железа, что позволяет связываться и другим металлам, особенно тем, у которых большое соотношение заряда к размеру. [8] [12] [21] Сайты связывания состоят из C-доли и N-доли, которые практически идентичны по структуре. [21] Каждая доля содержит аспарагиновую кислоту , гистидин , 2 остатка тирозина и ион бикарбоната , который действует как бидентатный лиганд, позволяя железу или другим металлам связываться с трансферрином в искаженной октаэдрической геометрии . [20] [21] [22] Доказательства, подтверждающие связывание Cr 3+ Трансферрин основан на обширных клинических исследованиях, которые показали положительную корреляцию между уровнями ферритина и уровнями глюкозы натощак , инсулина и гликированного гемоглобина (Hb1Ac). [8] Более того, исследование in vivo на крысах показало, что 80% изотопно-меченного Cr 3+ в итоге оказались на трансферрине, а остальные были связаны с альбумином . Исследование in vitro показало, что при добавлении хлорида хрома (III) к выделенному трансферрину Cr 3+ легко связываемый трансферрин из-за изменений в УФ-Вид спектре. [12] [20] [24] образования Константа Cr 3+ в С-доле составляет 1,41 х 10. 10 М −1 и 2,04 х 10 5 М −1 в N-доле, что указывает на то, что Cr 3+ преимущественно связывает C-долю. [8] [20] [21] В целом константа образования хрома (III) ниже, чем у иона трехвалентного железа. [20] Бикарбонатный лиганд играет решающую роль в связывании Cr. 3+ как и при очень низких концентрациях бикарбоната, аффинность связывания также значительно ниже. [20] Исследования электронного парамагнитного резонанса (ЭПР) показали, что при pH ниже 6 хром (III) связывается только с N-долей, а при pH, близком к нейтральному, хром (III) также связывается с C-долей. [8] Хром(III) может конкурировать с ионом трехвалентного железа за связывание с C-долей, когда насыщение значительно превышает 30%. [21] Таким образом, эти эффекты наблюдаются только у пациентов с гемохроматозом , заболеванием накопления железа, характеризующимся чрезмерным насыщением железа в трансферрине. [24]
Механизм действия
[ редактировать ]
Низкомолекулярное хромсвязывающее вещество (LMWCr; также известное как хромодулин) представляет собой олигопептид, который, по-видимому, связывает хром (III) в организме. [25] Он состоит из четырех аминокислотных остатков; аспартат , цистеин , глутамат и глицин , связанные четырьмя (Cr 3+ ) центры. [8] [11] [26] Он взаимодействует с рецептором инсулина, продлевая активность киназы за счет стимуляции тирозинкиназного пути, что приводит к улучшению абсорбции глюкозы. [20] [27] Его путают с фактором толерантности к глюкозе . Несмотря на недавние попытки охарактеризовать хромодулин, точная структура до сих пор относительно неизвестна. [28]
Хотя точный механизм действия хромодулина на рецептор инсулина в настоящее время неизвестен, один из обычно описываемых механизмов представлен ниже. Этот предложенный механизм имеет наибольшее согласие с различными экспериментами с участием хромодулина. [7] [12] [18] [24]
В норме хромодулин существует в форме апохромодулина, которая не содержит ионов Cr(III) и обладает минимальной активностью в отношении инсулиновых рецепторов. [24] Апохромодулин хранится в чувствительных к инсулину клетках ядра. Когда уровень глюкозы в крови повышается, инсулин высвобождается в кровоток и связывается с внешней α-субъединицей инсулинового рецептора, трансмембранным белком . [26] Рецептор инсулина состоит из 2 внеклеточных α-субъединиц и 2 трансмембранных β-субъединиц. [24] Как только инсулин связывается с инсулиновым рецептором, происходит конформационное изменение рецептора, вызывающее тирозина фосфорилирование всех трех остатков (расположенных в β-субъединицах). Это активирует рецептор и позволяет ему передавать сигнал от инсулина в клетку. [11] [24] [26] Как упоминалось выше, абсорбированный пиколинат хрома(III) со временем отдает Cr. 3+ трансферрину. В свою очередь трансферрин транспортирует Cr 3+ к чувствительным к инсулину клеткам (т.е. адипоцитам ), где он связывается с апохромодулин с образованием голохромодулина. [24] Холохромодулин связывается с рецептором инсулина, что помогает поддерживать активную конформацию рецептора инсулина за счет продления киназной активности киназ или повышения уровня мРНК рецептора инсулина , тем самым снижая уровень глюкозы в крови. [11]
Эксперименты смогли показать, что хром(III) способен усиливать стимулируемую инсулином передачу сигнала инсулина, воздействуя на нижестоящие молекулы IR, о чем свидетельствуют повышенные уровни фосфорилирования тирозина IRS-1 , повышенное Thr308 и Ser473 фосфорилирование Akt . и повышенная активность PI3-K на различных клеточных и животных моделях. [29] Повышенное фосфорилирование IRS-1 приводило к повышению чувствительности рецепторов инсулина, тогда как Akt и PI3-K приводили к усилению транслокации GLUT4 на поверхность клетки, вызывая тем самым большее поглощение глюкозы. [29]
Также было показано, что хром(III) может облегчить резистентность к инсулину за счет снижения стресса эндоплазматической сети (ЭР). [29] Стресс ЭР определяется как накопление неправильно свернутых и развернутых белков в просвете ЭР. [29] Стресс ER приводит к стимуляции терминальной киназы c-Jun ( JNK ), которая, в свою очередь, фосфорилирует сериновый остаток IRS, что приводит к подавлению сигнального каскада инсулина и меньшему поглощению глюкозы. [30] Экспериментальные данные показывают, что хром ингибирует стресс ER и, следовательно, усиливается подавление передачи сигналов инсулина. [30] Точный механизм неизвестен. [30]

Другой способ, которым Cr(III) может продлить киназную активность инсулинового рецептора, заключается в окислении критическом активном центре остатка цистеина в протеин-тирозинфосфатазы 1B (PTP1B). Обычно PTP1B дефосфорилирует остатки фосфотирозина, осуществляя нуклеофильную атаку на фосфатную группу через ее остаток цистеина, тем самым инактивируя рецептор инсулина. [31] Этот процесс удаляет фосфатную группу из остатка тирозина с образованием Cys–S–PO 3 2− группа, которая впоследствии гидролизуется водой для регенерации остатка цистеина, что позволяет выполнить следующий цикл действия. [31] Исследования показали, что хром(III) может фактически вызывать необратимое ингибирование PTP1B. Считается, что Cr(III) превращается в Cr(VI) или Cr(V) (под действием оксидоредуктаз ) , которые затем окисляют тиол цистеинового остатка на PTP1B до сульфеновой кислоты , что делает его неспособным атаковать фосфат. группа фосфотирозина. [32] Однако это лишь вероятный механизм, и прямых доказательств в поддержку этой гипотезы не было показано. [31] При выключении сигнального каскада голохромодулин выводится с мочой, поскольку константа образования слишком велика для прямого удаления Cr(III). [8] Экспериментальные данные показали, что потеря хромодулина из клеток коррелирует с увеличением концентрации хрома в моче после приема пищи, богатой углеводами (например, глюкозой). [26]
Заявления и дебаты о здоровье
[ редактировать ]Вес тела
[ редактировать ]Пиколинат хрома (III) продается в Соединенных Штатах как средство для развития тела спортсменов и как средство для похудения . Обзоры сообщают об отсутствии влияния ни на рост мышц, ни на потерю жира. [33] или же умеренная, но статистически значимая потеря веса -1,1 кг (2,4 фунта) в исследованиях продолжительностью более 12 недель. [6] Европейское управление по безопасности пищевых продуктов изучило литературу и пришло к выводу, что доказательств в поддержку утверждения недостаточно. [34]
Диабет
[ редактировать ]Есть утверждения, что пиколинатная форма добавки хрома помогает снизить резистентность к инсулину и улучшить метаболизм глюкозы 2 типа , особенно у диабетиков , но обзоры не выявили связи между хромом и концентрацией глюкозы или инсулина у недиабетиков, а результаты для диабетиков неубедительны. [35] [36] Авторы второго обзора отметили, что пиколинат хрома снижал уровень HbA1c на 0,7% у пациентов с диабетом 2 типа. Они заметили, что исследования низкого качества дали более положительные результаты, чем исследования более высокого качества. [36] [37] В двух обзорах сделан вывод, что пиколинат хрома (III) может быть более эффективным в снижении уровня глюкозы в крови по сравнению с другими хромсодержащими пищевыми добавками. [36] [38]
США В 2005 году Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) одобрило квалифицированное заявление о полезности для здоровья пиколината хрома в качестве пищевой добавки, связанное с резистентностью к инсулину и риском развития диабета 2 типа. Любая компания, желающая сделать такое заявление, должна использовать точную формулировку: «Одно небольшое исследование предполагает, что пиколинат хрома может снизить риск резистентности к инсулину и, следовательно, возможно, может снизить риск диабета 2 типа. Однако FDA приходит к выводу, что существование такая связь между пиколинатом хрома и резистентностью к инсулину или диабетом 2 типа весьма неопределенна». В рамках процесса рассмотрения петиции FDA отклонило другие заявления о снижении аномально повышенного уровня сахара в крови, риска сердечно-сосудистых заболеваний, риска ретинопатии или риска заболеваний почек. [39] В 2006 году FDA добавило, что «взаимосвязь между потреблением пиколината хрома (III) и резистентностью к инсулину весьма неопределенна». [40]
Вариативность исследований
[ редактировать ]В клинических результатах, касающихся пиколината хрома(III) и адекватного лечения диабета 2 типа, не наблюдалось единообразия. Это связано со степенью непереносимости глюкозы у пациентов, участвующих в клинических исследованиях. [10] Непереносимость глюкозы является градиентной, и на ее интенсивность влияют этническая принадлежность, степень ожирения, возраст, распределение жира в организме и многие другие факторы. [10] В некоторых исследованиях давались низкие дозы добавки, однако человеку необходимо ввести подходящее количество пиколината хрома (III), прежде чем будет наблюдаться какое-либо заметное снижение уровня глюкозы из-за различных уровней резистентности к инсулину. Еще один важный момент, о котором следует упомянуть, заключается в том, что диабет не всегда вызван непереносимостью глюкозы. [10] Как упоминалось ранее, было показано, что Cr(III) влияет только на непереносимость глюкозы, но не на уровень инсулина. Кроме того, условия, в которых проводились исследования, не были одинаковыми. Уровни стресса, диеты, которую употребляли пациенты, и генетика пациентов были разными среди участников исследования. [10] Это также верно для контрольной группы в различных исследованиях, в которых субъекты, страдающие диабетом, уже получали широкий спектр противодиабетических препаратов, которые могут снизить влияние хрома на активность инсулина. [30] Это может объяснить, почему исследования на животных имеют тенденцию давать более положительные результаты из-за того, что этих животных с диабетом не лечили противодиабетическими препаратами в контрольной группе. [30] Кроме того, как упоминалось в разделе «Всасывание и выведение», на всасывание/биодоступность пиколината хрома(III) влияет диета. В совокупности эти различные факторы способствовали вариабельности исследований.
Безопасность и токсичность
[ редактировать ]Первоначально были высказаны опасения, что пиколинат хрома (III) с большей вероятностью вызовет повреждение и мутацию ДНК, чем другие формы трехвалентного хрома. [41] но эти результаты также обсуждаются. [42] Эти опасения были частично основаны на исследованиях на плодовых мухах, где добавка пиколината хрома (III) вызывает хромосомные аберрации, препятствует развитию потомства, [43] и вызывает бесплодие и летальные мутации. [44]
Было опубликовано исследование по оценке токсичности пиколината Cr(III) для человека. [45] Исследователи, проводившие это исследование, использовали предыдущие знания о том, что Cr(III) восстанавливается до Cr(II) клеточными восстановителями, такими как НАДН или цистеин . [45] Показано, что эта восстановленная форма Cr(II) реагирует с H 2 O 2 с образованием радикалов , которые, в свою очередь, окисляют пары оснований ДНК . [46] [47] Помня об этом, исследователи вводили десяти женщинам по 400 мкг пиколината хрома (III) в день в течение восьминедельного периода. [45] Измеряя количество окисленной пары оснований ДНК, 5-гидроксиметилурацила, с использованием титров антител , группа могла сделать вывод о степени окисления пары оснований ДНК, происходящей в прямой зависимости от пиколината хрома (III). [45] Результаты исследования показали, что пиколинат хрома(III) сам по себе не вызывает значительных хромосомных повреждений in vivo . [45]
В целом было показано, что пиколинат хрома(III) не токсичен для человека. Большинству взрослых его можно принимать внутрь в дозе до 1000 мкг в день. [48] Эта низкая токсичность обычно связана с низкой абсорбцией Cr(III) в организме через легкие , кожу и желудочно-кишечный тракт . [49] в сочетании с высокой экскрецией. Обычно 99% принятого хрома(III) может быть восстановлено с фекалиями пользователя. Были отдельные случаи, когда прием добавок хрома(III) приводил к почечной недостаточности, однако эта связь неясна и еще не проверена. [50]
Регулирование пиколината хрома(III)
[ редактировать ]В 2004 году Агентство по пищевым стандартам Великобритании рекомендовало потребителям использовать другие формы трехвалентного хрома вместо пиколината хрома (III) до тех пор, пока не будет получена рекомендация специалиста от Комитета по мутагенности. Это произошло из-за опасений, высказанных Экспертной группой по витаминам и минералам, что пиколинат хрома (III) может быть генотоксичным (вызывать рак). Комитет также отметил два сообщения о случаях почечной недостаточности , которые могли быть вызваны этой добавкой, и призвал к дальнейшим исследованиям ее безопасности. [51] [52] В декабре 2004 года Комитет по мутагенности опубликовал свои выводы, в которых пришел к выводу, что «в целом можно сделать вывод, что баланс данных позволяет предположить, что пиколинат хрома (III) следует рассматривать как не обладающий мутагенными свойствами in vitro» и что «доступный в -vivo тесты на млекопитающих с пиколинатом хрома(III) отрицательны». [53] После этих выводов Агентство по пищевым стандартам Великобритании отозвало свои рекомендации избегать пиколината хрома (III), хотя оно планирует держать свои рекомендации о добавках хрома под контролем. [54]
В 2010 году пиколинат хрома (III) был одобрен Министерством здравоохранения Канады для использования в пищевых добавках. Утвержденные заявления на маркировке включают: фактор поддержания хорошего здоровья, обеспечивает поддержку здорового метаболизма глюкозы, помогает организму усваивать углеводы и помогает организму усваивать жиры. [55]
Ссылки
[ редактировать ]- ^ Пройсс, Х.Г.; Эчард, Б.; Перриконе, Невада; Багчи, Д.; Ясмин, Т.; Стохс, С.Дж. (2008). «Сравнение метаболических эффектов шести различных коммерческих соединений трехвалентного хрома». Журнал неорганической биохимии . 102 (11): 1986–1990. дои : 10.1016/j.jinorgbio.2008.07.012 . ПМИД 18774175 .
- ^ «Источник питания: хром» . Школа общественного здравоохранения Гарвардского университета. 28 января 2021 г.
- ^ Обзор хрома. Архивировано 7 февраля 2012 г., в Экспертной группе Wayback Machine по обзору хрома по витаминам и минералам, 12 августа 2002 г.
- ^ Стернс ДМ (2000). «Является ли хром незаменимым металлом?». Биофакторы . 11 (3): 149–62. дои : 10.1002/biof.5520110301 . ПМИД 10875302 . S2CID 19417496 .
- ^ Перейти обратно: а б с д Винсент, Джон (2010). «Хром: празднование 50-летия как важнейшего элемента?». Транзакции Далтона . 39 (16): 3787–3794. дои : 10.1039/B920480F . ПМИД 20372701 .
- ^ Перейти обратно: а б Тянь, Х; Го, Х; Ван, X; Он, З; Солнце, Р; Ге, С; Чжан, Z (2013). «Добавка пиколината хрома для взрослых с избыточным весом или ожирением» . Кокрановская база данных систематических обзоров . 2013 (11): CD010063. дои : 10.1002/14651858.CD010063.pub2 . ПМЦ 7433292 . ПМИД 24293292 . CD010063.
- ^ Перейти обратно: а б с д Левина, Авива; Лэй, Питер (2008). «Химические свойства и токсичность пищевых добавок хрома (III)». Химические исследования в токсикологии . 21 (3): 563–571. дои : 10.1021/tx700385t . ПМИД 18237145 .
- ^ Перейти обратно: а б с д и ж г час я Фэн, Вэйюэ (2007). «Глава 6 – Транспорт хрома (III) в организме: влияние на функцию» (PDF) . Винсент, Джон (ред.). Пищевая биохимия хрома (III) . Амстердам: Elsevier BV, стр. 121–137. ISBN 978-0444530714 . Проверено 20 марта 2015 г. [ постоянная мертвая ссылка ]
- ^ Перейти обратно: а б Чефалу, Уильям; Ху, Фрэнк (2004). «Роль хрома в здоровье человека и при диабете» . Уход при диабете . 27 (11): 2741–2751. дои : 10.2337/diacare.27.11.2741 . ПМИД 15505017 . Проверено 20 марта 2015 г.
- ^ Перейти обратно: а б с д и ж Андерсон, Ричард (1998). «Хром, непереносимость глюкозы и диабет». Журнал Американского колледжа питания . 17 (6): 548–555. дои : 10.1080/07315724.1998.10718802 . ПМИД 9853533 . S2CID 19532052 .
- ^ Перейти обратно: а б с д Винсент, Джон (2004). «Последние достижения в биохимии питания трехвалентного хрома» . Труды Общества питания . 63 (1): 41–47. дои : 10.1079/PNS2003315 . ПМИД 15070438 .
- ^ Перейти обратно: а б с д и Винсент, Джон (2001). «Бионеорганическая химия хрома (III)». Многогранник . 20 (1–2): 1–26. дои : 10.1016/S0277-5387(00)00624-0 .
- ^ Перейти обратно: а б с Абу-Гамра, Зейнаб; Абдель-Мессих, Мишель (2014). «Корреляция термических и спектральных свойств пиколинатного комплекса хрома(III) и кинетическое исследование его термической деструкции». Журнал термического анализа и калориметрии . 117 (2): 993–1000. дои : 10.1007/s10973-014-3768-5 . S2CID 93050541 .
- ^ Перейти обратно: а б с д и Парахон-Коста, Беатрис; Вагнер, Клаудия; Баран, Энрике (2003). «Вольтамперометрическое и спектроскопическое исследование комплексов хрома (III)/пиколината». Журнал неорганической и общей химии . 629 (6): 1085–1090. дои : 10.1002/zaac.200300050 .
- ^ Перейти обратно: а б с Стернс, Дайан; Армстронг, Уильям (1992). «Моноядерные и биядерные пиколинатные комплексы хрома (III)». Неорганическая химия . 31 (25): 5178–5184. дои : 10.1021/ic00051a007 .
- ^ Перейти обратно: а б с д Хакими, Мохаммед (2013). «Структурная и спектральная характеристика комплекса пиколината хрома (III): введение новой окислительно-восстановительной реакции» . Журнал Корейского химического общества . 57 (6): 721–725. дои : 10.5012/jkcs.2013.57.6.721 . Проверено 1 апреля 2015 г.
- ^ Перейти обратно: а б Лукаски, Генри (2007). «Глава 4 – Влияние хрома (III) в качестве пищевой добавки» (PDF) . Винсент, Джон (ред.). Пищевая биохимия хрома (III) . Амстердам: Elsevier BV, стр. 57–70. ISBN 978-0444530714 . Проверено 20 марта 2015 г. [ постоянная мертвая ссылка ]
- ^ Перейти обратно: а б с Лащинский, Нильс; Котвитц, Карин; Фройнд, Барбара; Дресов, Бернд; Фишер, Роланд; Нильсен, Питер (2012). «Биодоступность добавок хрома (III) у крыс и людей». Биометаллы . 25 (5): 1051–1060. дои : 10.1007/s10534-012-9571-5 . ПМИД 22814636 . S2CID 1533593 .
- ^ Перейти обратно: а б с д и ж г Дебски, Б.; Гоневич, М.; Кшизовскал, М.; Левица, А.; Левикил, С.; Нимцевиз, М.; Здановскил, Р. (2014). «Роль хрома III в организме и возможности его использования при лечении диабета и ожирения» . Анналы сельскохозяйственной и экологической медицины . 21 (2): 331–335. дои : 10.5604/1232-1966.1108599 . ПМИД 24959784 .
- ^ Перейти обратно: а б с д и ж г час Винсент, Джон (2015). «Является ли фармакологический механизм действия хрома (III) вторичным мессенджером?». Исследование биологических микроэлементов . 166 (1): 7–12. дои : 10.1007/s12011-015-0231-9 . ПМИД 25595680 . S2CID 16895342 .
- ^ Перейти обратно: а б с д и ж Куорлз, К.; Маркус, Р.; Брумагим, Джулия (2011). «Конкурентное связывание Fe 3+ , Кр 3+ и Ни 2+ к трансферрину». Журнал биологической неорганической химии . 16 (6): 913–921. : 10.1007 /s00775-011-0792-9 . PMID 21678080. . S2CID 24302252 doi
- ^ Перейти обратно: а б Винсент, Джон (2012). «Связывание и транспорт альтернативных металлов трансферрином». Biochimica et Biophysical Acta (BBA) – Общие предметы . 1820 (3): 362–378. дои : 10.1016/j.bbagen.2011.07.003 . ПМИД 21782896 .
- ^ Левина, Авива; Фам, Т. Д. Нгуен; Лэй, Питер А. (01 мая 2016 г.). «Связывание хрома (III) с трансферрином может участвовать в детоксикации пищевого хрома (III), а не в транспорте незаменимого микроэлемента» . Angewandte Chemie, международное издание . 55 (28): 8104–8107. дои : 10.1002/anie.201602996 . ISSN 1521-3773 . ПМИД 27197571 .
- ^ Перейти обратно: а б с д и ж г Винсент, Джон (2012). «Биохимические механизмы». Винсент, Джон (ред.). Бионеорганическая химия хрома . Чичестер, Великобритания: John Wiley & Sons. стр. 125–167. дои : 10.1002/9781118458891.ch6 . ISBN 978-0470664827 .
- ^ Виера М., Дэвис-МакГибони CM (2008). «Выделение и характеристика низкомолекулярного хромсвязывающего вещества (LMWCr) из куриной печени». Протеин Дж . 27 (6): 371–375. дои : 10.1007/s10930-008-9146-z . ПМИД 18769887 . S2CID 32564084 .
- ^ Перейти обратно: а б с д Винсент, Джон (2000). «Биохимия хрома» . Журнал питания . 130 (4): 715–718. дои : 10.1093/jn/130.4.715 . ПМИД 10736319 .
- ^ Клодфелдер Б.Дж., Эмамаулли Дж., Хепберн Д.Д., Чаков Н.Е., Неттлз Х.С., Винсент Дж.Б. (2001). «След хрома (III) in vivo из крови в мочу: роль трансферрина и хромодулина». Ж. Биол. Неорг. Хим . 6 (5–6): 608–617. дои : 10.1007/s007750100238 . ПМИД 11472024 . S2CID 8956685 .
- ^ Винсент Дж. Б. (1994). «Связь между фактором толерантности к глюкозе и низкомолекулярным хромсвязывающим веществом» (PDF) . Дж. Нутр . 124 (1): 117–9. дои : 10.1093/jn/124.1.117 . ПМИД 8283288 .
- ^ Перейти обратно: а б с д Китамура, Масанори (2008). «Стресс эндоплазматической сети и реакция развернутого белка в патофизиологии почек: лица Януса». Американский журнал физиологии . 295 (2): 323–334. дои : 10.1152/ajprenal.00050.2008 . ПМИД 18367660 .
- ^ Перейти обратно: а б с д и Хуа, Инань; Кларк, Сюзанна; Рен, Джун; Шриджаян, Наир (2012). «Молекулярные механизмы хрома в снижении резистентности к инсулину» . Журнал пищевой биохимии . 23 (4): 313–319. дои : 10.1016/j.jnutbio.2011.11.001 . ПМК 3308119 . ПМИД 22423897 .
- ^ Перейти обратно: а б с Тонкс, Николас (2003). «PTP1B: С боков на передовую!» . Письма ФЭБС . 546 (1): 140–148. Бибкод : 2003FEBSL.546..140T . дои : 10.1016/S0014-5793(03)00603-3 . ПМИД 12829250 . S2CID 21205538 .
- ^ Левина, Авива (2011). «Противодиабетические препараты на основе металлов: достижения и проблемы». Транзакции Далтона . 40 (44): 11675–1686. дои : 10.1039/C1DT10380F . ПМИД 21750828 .
- ^ Винсент Дж.Б.; Сак, Д.А.; Роффман, М; Финч, М; Коморовский, младший (2003). «Потенциальная ценность и токсичность пиколината хрома в качестве пищевой добавки, средства для снижения веса и средства для развития мышц». Спортивная медицина . 33 (3): 213–230. дои : 10.2165/00007256-200333030-00004 . ПМИД 12656641 . S2CID 9981172 .
- ^ «Научное заключение по обоснованию утверждений о пользе хрома для здоровья и его вкладе в нормальный метаболизм макронутриентов (ID 260, 401, 4665, 4666, 4667), поддержании нормальной концентрации глюкозы в крови (ID 262, 4667), вкладе в поддержание или достижение нормальной массы тела (ID 339, 4665, 4666) и снижения усталости и усталости (ID 261) в соответствии со статьей 13(1) Регламента (ЕС) № 1924/2006» . Журнал EFSA . 8 (10). 2010. doi : 10.2903/j.efsa.2010.1732 .
- ^ Алтуис, доктор медицинских наук, Джордан, штат Нью-Йорк, Лудингтон, Э.А., Виттес, Дж.Т. (1 июля 2002 г.). «Реакция глюкозы и инсулина на пищевые добавки хрома: метаанализ» . Американский журнал клинического питания . 76 (1): 148–155. дои : 10.1093/ajcn/76.1.148 . ПМИД 12081828 .
- ^ Перейти обратно: а б с Балк Э.М., Тациони А., Лихтенштейн А.Х. , Лау Дж., Питтас А.Г. (2007). «Влияние добавок хрома на метаболизм глюкозы и липидов: систематический обзор рандомизированных контролируемых исследований» . Уход при диабете . 30 (8): 2154–2163. дои : 10.2337/dc06-0996 . ПМИД 17519436 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Суксомбун, Н.; Пулсап, Н.; Юванаком, А. (2014). «Систематический обзор и метаанализ эффективности и безопасности добавок хрома при диабете» . Журнал клинической фармации и терапии . 39 (3): 292–306. дои : 10.1111/jcpt.12147 . ПМИД 24635480 . S2CID 22326435 .
- ^ Бродхерст CL, Доменико П. (декабрь 2006 г.). «Клинические исследования добавок пиколината хрома при сахарном диабете – обзор». Диабетическая технология. Там . 8 (6): 677–87. дои : 10.1089/диа.2006.8.677 . ПМИД 17109600 .
- ^ Квалифицированные заявления о вреде для здоровья: Письмо о принудительном исполнении по усмотрению - пиколинат хрома и резистентность к инсулину (регистрационный номер 2004Q-0144) (2005) Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США.
- ^ Трамбо PR, Эллвуд KC (август 2006 г.). «Потребление пиколината хрома и риск развития диабета 2 типа: научно обоснованный обзор Управления по контролю за продуктами и лекарствами США» . Нутр. Преподобный . 64 (8): 357–63. дои : 10.1111/j.1753-4887.2006.tb00220.x . ПМИД 16958312 .
- ^ Чаудхари С., Пинкстон Дж., Рабиле М.М., Ван Хорн Дж.Д. (2005). «Необычная реакционная способность коммерческой добавки хрома по сравнению с базовым расщеплением ДНК синтетическими комплексами хрома». Журнал неорганической биохимии . 99 (3): 787–794. дои : 10.1016/j.jinorgbio.2004.12.009 . PMID 15708800 .
- ^ Хинингер И., Бенараба Р., Осман М., Фор Х., Мари Руссель А., Андерсон Р.А. (2007). «Безопасность комплексов трехвалентного хрома: нет доказательств повреждения ДНК в кератиноцитах HaCaT человека» . Свободный Радик. Биол. Мед . 42 (12): 1759–65. doi : 10.1016/j.freeradbiomed.2007.02.034 . ПМИД 17512455 .
- ^ Столлингс Д.М., Хепберн Д.Д., Ханна М., Винсент Дж.Б., О'Доннелл Дж. (2006). «Пищевая добавка пиколинат хрома вызывает хромосомные аберрации и препятствует развитию потомства у Drosophila melanogaster». Мутат. Рез . 610 (1–2): 101–13. Бибкод : 2006MRGTE.610..101S . doi : 10.1016/j.mrgentox.2006.06.019 . ПМИД 16887379 .
- ^ Хепберн Д.Д., Сяо Дж., Биндом С., Винсент Дж.Б., О'Доннелл Дж. (2003). «Пищевая добавка пиколинат хрома вызывает стерильность и летальные мутации у Drosophila melanogaster» . Учеб. Натл. акад. наук. США . 100 (7): 3766–71. дои : 10.1073/pnas.0636646100 . ПМК 152996 . ПМИД 12649323 .
- ^ Перейти обратно: а б с д и Като, Икуко; Фогельман, Джозеф; Дильман, Владимир; Каркошка, Ежи; Френкель, Кристина; Дурр, Нэнси; Орентрейх, Норман; Тониоло, Паоло (1998). «Влияние добавок пиколината хрома на титры антител к 5-гидроксиметилурацилу». Европейский журнал эпидемиологии . 14 (6): 621–626. дои : 10.1023/A:1007442203258 . ПМИД 9794131 . S2CID 19071972 .
- ^ Цоу, Цуй-Чун; Чен, Чиу-лань; Лю, Цунг-Юнь; Ян, Цзя-Лин (1996). «Индукция 8-гидроксидезоксигуанозина в ДНК хромом (III) плюс перекисью водорода и ее предотвращение с помощью поглотителей» (PDF) . Канцерогенез . 17 (1): 103–108. дои : 10.1093/carcin/17.1.103 . ПМИД 8565117 . Проверено 20 марта 2015 г.
- ^ Одзава, Т.; Ханаки, А. (1990). «Исследование спиновых ловушек реакций Cr(III) с перекисью водорода в присутствии биологических восстановителей: нетоксичен ли Cr(III)?». Биохимия Интернэшнл . 22 (2): 343–352. ПМИД 1965278 .
- ^ Джиджибхой, Хуршид (2009). «Роль хрома в питании и терапии, а также как потенциальный токсин» . Обзоры питания . 57 (11): 329–335. дои : 10.1111/j.1753-4887.1999.tb06909.x . ПМИД 10628183 .
- ^ Фэрхерст, С.; Минти, К. (1989). Токсичность хрома и неорганических соединений хрома . Обзор токсичности; 21. Лондон: HMSO, стр. 1–243. ISBN 978-0118855211 .
- ^ Вассер, Уолтер; Фельдман, Натаниэль; Д'Агати, Виветт (1997). «Хроническая почечная недостаточность после приема безрецептурного пиколината хрома». Анналы внутренней медицины . 126 (5): 410. дои : 10.7326/0003-4819-126-5-199703010-00019 . ПМИД 9054292 . S2CID 27418296 .
- ^ Безопасные верхние уровни витаминов и минералов. Архивировано 4 июля 2008 г. в Wayback Machine - май 2003 г. Агентстве по пищевым стандартам
- ^ Оценка риска: Экспертная группа по хрому по витаминам и минералам, 2003 г.
- ^ Заявление о мутагенности трехвалентного хрома и пиколината хрома. Архивировано 16 мая 2008 г. на Wayback Machine COM/04/S3 - декабрь 2004 г.
- ^ Агентство пересматривает рекомендации Агентства по пищевым стандартам по пиколинату хрома - 13 декабря 2004 г.
- ^ «Монография: Хром (из пиколината хрома)» . Здоровье Канады. 9 декабря 2009 года . Проверено 24 марта 2015 г.
Внешние ссылки
[ редактировать ] СМИ, связанные с пиколинатом хрома (III), на Викискладе?
СМИ, связанные с пиколинатом хрома (III), на Викискладе? - Руководство Мерк

