Субталамическое ядро
| Субталамическое ядро | |
|---|---|
 Корональные срезы человеческого мозга, показывающие базальные ганглии ( внешний бледный шар (GPe) и внутренний бледный шар (GPi)), субталамическое ядро (STN) и черную субстанцию (SN). | |
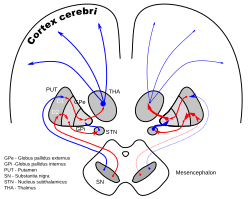 DA-петли при болезни Паркинсона | |
| Подробности | |
| Часть | Субталамус (физически); базальные ганглии (функционально) |
| Идентификаторы | |
| латинский | субталамическое ядро |
| Акроним(ы) | СТН |
| МеШ | D020531 |
| Нейроимена | 435 |
| НейроЛекс ID | nlx_anat_1010002 |
| ТА98 | A14.1.08.702 |
| ТА2 | 5709 |
| ФМА | 62035 |
| Анатомические термины нейроанатомии | |
Субталамическое ядро ( STN ) представляет собой небольшое ядро головного мозга в форме линзы , которое с функциональной точки зрения является частью системы базальных ганглиев . С точки зрения анатомии это основная часть субталамуса . названия, субталамическое ядро расположено вентральнее таламуса Как следует из . Он также расположен дорсально от черной субстанции и медиальнее внутренней капсулы . Впервые он был описан Жюлем Бернаром Люисом в 1865 году. [1] и термин corpus Luysi или тело Луиса до сих пор иногда используется.
Анатомия
[ редактировать ]Структура
[ редактировать ]Основной тип нейронов , обнаруженный в субталамическом ядре, имеет довольно длинные, редко шиповатые дендриты . [2] [3] В нейронах, расположенных более центрально, дендритные ветви имеют более эллипсоидную форму. [4] Размеры этих беседок (1200 мкм, 600 мкм и 300 мкм) одинаковы у многих видов, включая крысу, кошку, обезьяну и человека, что необычно. Однако количество нейронов увеличивается с размером мозга, а также с внешними размерами ядра. Основные нейроны являются глутаматергическими , что придает им особое функциональное положение в системе базальных ганглиев. У человека также имеется небольшое количество (около 7,5%) ГАМКергических интернейронов , участвующих в локальных цепях; однако дендритные ветви субталамических нейронов уклоняются от границы и преимущественно взаимодействуют друг с другом. [5]
Структура субталамического ядра еще не полностью изучена и понята, но, вероятно, оно состоит из нескольких внутренних доменов. Субталамическое ядро приматов часто делится на три внутренних анатомо-функциональных домена. Однако эта так называемая трехсторонняя модель обсуждается, поскольку она не полностью объясняет сложность субталамического ядра в функционировании мозга. [6] [7]
Афферентные аксоны
[ редактировать ]Субталамическое ядро получает основную информацию от внешнего бледного шара (GPe), [8] не столько через чечевицеобразную мышцу , как часто говорят, сколько через отходящие «гребенчатые» волокна, пересекающие сначала медиальное паллидум и внутреннюю капсулу (составляющую часть гребешковой системы Эдингера , см. рисунок), а также субталамическую ансу. [9] . Эти афференты являются ГАМКергическими и тормозят нейроны субталамического ядра. Возбуждающие, глутаматергические входы поступают из коры головного мозга (вся лобная кора с преобладанием моторного, премоторного и глазодвигательного входа в заднелатеральную часть ядра) и из парафасцикулярной части центрального комплекса . Субталамическое ядро также получает нейромодулирующие сигналы, в частности дофаминергические аксоны от черной субстанции . компактной части [10] Он также получает сигналы от педункулопонтинного ядра .
Эфферентные цели
[ редактировать ]Аксоны нейронов субталамического ядра покидают ядро дорсально. Эфферентные аксоны являются глутаматергическими (возбуждающими). За исключением связи с полосатым телом (17,3% у макак), большинство главных субталамических нейронов являются мультимишенными и направлены к другим элементам ядра базальных ганглиев. [11] Некоторые посылают аксоны к черной субстанции медиально и к медиальному и латеральному ядрам паллидума латерально (3-мишень, 21,3%). Некоторые из них двухмишеневые с латеральным паллидумом и черной субстанцией (2,7%) или латеральным паллидумом и медиальной (48%). Реже встречаются одиночные мишени для латерального паллидума. В паллидуме субталамические окончания заканчиваются полосами, параллельными краю паллида. [11] [12] Когда добавляются все аксоны, достигающие этой цели, основным эффектом субталамического ядра в 82,7% случаев явно является внутренний бледный шар (GPi).
Некоторые исследователи сообщили о внутренних коллатералях аксонов . [13] Однако функциональных доказательств этому мало.
Физиология
[ редактировать ]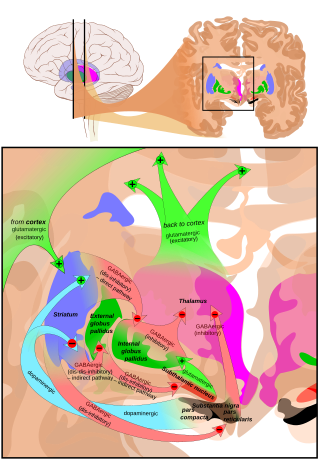
Субталамическое ядро
[ редактировать ]Первые внутриклеточные электрические записи субталамических нейронов были выполнены с использованием острых электродов на препарате среза крысы. [ нужна ссылка ] В этих записях были сделаны три ключевых наблюдения, все три из которых доминировали в последующих сообщениях о свойствах субталамической активации. Первое наблюдение заключалось в том, что в отсутствие подачи тока или синаптической стимуляции большинство клеток активировались спонтанно. Второе наблюдение заключается в том, что эти клетки способны кратковременно срабатывать на очень высоких частотах. Третье наблюдение касается нелинейного поведения, когда клетки временно деполяризуются после гиперполяризации ниже –65 мВ. Затем они способны задействовать потенциалзависимые токи кальция и натрия, чтобы вызвать всплески потенциалов действия.
Несколько недавних исследований были сосредоточены на способности субталамических нейронов к автономной стимуляции. Эти клетки часто называют «быстродействующими кардиостимуляторами». [14] поскольку они могут генерировать спонтанные потенциалы действия с частотой от 80 до 90 Гц у приматов.
Колебательная и синхронная активность [15] [16] Вероятно, это типичный образец разряда в субталамических нейронах, зарегистрированный у пациентов и на животных моделях, характеризующийся потерей дофаминергических клеток в компактной части черной субстанции , что является основной патологией, лежащей в основе болезни Паркинсона .
Латеропаллидо-субталамическая система
[ редактировать ]Прочные реципрокные связи связывают субталамическое ядро и наружный сегмент бледного шара . Оба являются кардиостимуляторами с быстрым импульсом. Считается, что вместе они составляют «центральный водитель ритма базальных ганглиев». [17] с синхронными всплесками.
Связь латерального паллидума с субталамическим ядром также наблюдается в системе базальных ганглиев , где сокращение между излучающими/принимающими элементами, вероятно, является самым сильным. В объемном отношении латеральный паллидум у человека составляет 808 мм. 3 , субталамическое ядро всего 158 мм 3 . [18] Это преобразованное количество нейронов представляет собой сильное сжатие с потерей точности карты.
Некоторые аксоны латерального паллидума переходят в полосатое тело. [19] На активность медиального паллидума влияют влияния латерального паллидума и субталамического ядра. [20] То же самое и с сетчатой частью черной субстанции . [12] Субталамическое ядро посылает аксоны к другому регулятору: ножко-мостовому комплексу (id).
Считается, что латеропаллидо-субталамическая система играет ключевую роль в формировании паттернов активности, наблюдаемых при болезни Паркинсона . [21]
Патофизиология
[ редактировать ]Поражение STN приводит к облегчению двигательных симптомов, таких как акинезия , ригидность и тремор при болезни Паркинсона . Впервые это было показано на модели приматов MPTP в статье Бергмана и его коллег. [22] . Это вдохновило Беназуза и его коллег исследовать глубокую стимуляцию ядра мозга, которая, как известно, оказывает эффект, аналогичный абляционным поражениям. [23] . Вскоре после этого команда Алима Луиса Бенабида показала, что глубокая стимуляция ядра мозга приводит к облегчению симптомов у пациентов с болезнью Паркинсона, а также [24] , что привело к созданию в настоящее время одобренной FDA и широко применяемой формы глубокой стимуляции мозга . В первую очередь стимулируются терминальные разветвления афферентных аксонов, которые изменяют активность субталамических нейронов. Однако это было показано на срезах таламуса мышей. [25] что стимул также заставляет близлежащие астроциты высвобождать аденозинтрифосфат (АТФ), предшественник аденозина (посредством катаболического процесса). В свою очередь, активация аденозинового рецептора А1 подавляет передачу возбуждения в таламусе, имитируя тем самым абляцию субталамического ядра.
До статьи Бергмана стереотаксическое поле не повреждало ядро, поскольку было известно, что одностороннее разрушение или разрушение субталамического ядра, которое может возникнуть в результате естественных инсультов, может привести к гемибаллизму . Хотя в целом это остается верным, ятрогенное поражение STN проводилось много раз и недавно приобрело новый виток с появлением фокусированного ультразвука под контролем МРТ , который также исследовался на предмет субталамической нуклеотомии для лечения болезни Паркинсона. [26] . Любопытно, что команда под руководством Майкла Фокса недавно смогла показать, что, хотя некоторые поражения, которые привели к гемибаллизму, действительно находились внутри и вокруг STN, большинство зарегистрированных случаев были в других областях мозга. [27] .
Поскольку одной из предполагаемых функций STN является контроль импульсов, дисфункция этой области связана с обсессивно-компульсивным расстройством . [28] Применение высокочастотных импульсов посредством глубокой стимуляции мозга показало некоторые многообещающие результаты в коррекции тяжелого импульсивного поведения и было одобрено FDA для лечения резистентных случаев этого расстройства. [29]
Функция
[ редактировать ]Функция STN неизвестна, но современные теории рассматривают ее как компонент системы контроля базальных ганглиев , который может выполнять выбор действий. Он играет роль в так называемых «гиперпрямых» и «непрямых» путях моторного контроля, в отличие от прямого пути, который, как считается, обходит STN на пути от полосатого тела к внутреннему паллидуму. Дисфункция STN связана с двигательными симптомами, такими как ригидность, брадикинезия и тремор. [30] поведенческие особенности, такие как остановка текущих движений [31] или импульсивность у людей, которым предъявлены два одинаково полезных стимула. [32]
Физиологическая роль СТН долгое время была скрыта за ее патологической ролью. Но недавно исследования физиологии STN привели к открытию, что STN необходим для достижения запланированного движения, включая передвижение, равновесие и координацию движений. Он участвует в остановке или прерывании текущих двигательных задач. Более того, возбуждение STN обычно коррелировало со значительным снижением двигательной активности, тогда как ингибирование STN, напротив, усиливало локомоцию. [33] [34] [35]
Дополнительные изображения
[ редактировать ]- Корональный срез мозга непосредственно перед мостом. Субталамическое ядро, названное «Ядро Люйса».
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Луйс Ж. Б. (1865). Исследования спинномозговой системы, ее строения, функций и заболеваний (на французском языке). Париж: Байьер.
- ^ Афшарпур С. (июнь 1985 г.). «Светомикроскопический анализ субталамических нейронов крысы, пропитанных аппаратом Гольджи». Журнал сравнительной неврологии . 236 (1): 1–13. дои : 10.1002/cne.902360102 . ПМИД 4056088 . S2CID 12482772 .
- ^ Рафолс Дж. А., Фокс, Калифорния (июль 1976 г.). «Нейроны субталамического ядра приматов: исследование Гольджи и электронная микроскопия». Журнал сравнительной неврологии . 168 (1): 75–111. дои : 10.1002/cne.901680105 . ПМИД 819471 . S2CID 11962279 .
- ^ Ельник Дж., Першерон Г. (1979). «Субталамические нейроны у приматов: количественный и сравнительный анализ». Нейронаука . 4 (11): 1717–1743. дои : 10.1016/0306-4522(79)90030-7 . ПМИД 117397 . S2CID 40909863 .
- ^ Левеск Ж.К., родитель А (май 2005 г.). «ГАМКергические интернейроны в субталамическом ядре человека». Двигательные расстройства . 20 (5): 574–584. дои : 10.1002/mds.20374 . PMID 15645534 . S2CID 9551517 .
- ^ Алкемаде А., Форстманн БУ (июль 2014 г.). «Нужно ли нам пересмотреть гипотезу трехчастного подразделения субталамического ядра человека (STN)?». НейроИмидж . 95 : 326–329. doi : 10.1016/j.neuroimage.2014.03.010 . ПМИД 24642281 . S2CID 11010595 .
- ^ Ламберт С., Зринзо Л., Надь З., Лютти А., Хариз М., Фолтини Т. и др. (март 2012 г.). «Подтверждение функциональных зон в субталамическом ядре человека: закономерности соединения и субпарцелляции с использованием диффузионно-взвешенной визуализации» . НейроИмидж . 60 (1): 83–94. doi : 10.1016/j.neuroimage.2011.11.082 . ПМК 3315017 . ПМИД 22173294 .
- ^ Кантерас Н.С., Шамма-Лагнадо С.Дж., Сильва Б.А., Рикардо Х.А. (апрель 1990 г.). «Афферентные связи субталамического ядра: комбинированное ретроградное и антероградное исследование пероксидазы хрена на крысах». Исследования мозга . 513 (1): 43–59. дои : 10.1016/0006-8993(90)91087-W . ПМИД 2350684 . S2CID 22996045 .
- ^ Алхо Э.Дж., Алхо А.Т., Хорн А., Мартин М.Д., Эдлоу Б.Л., Фишл Б. и др. (январь 2020 г.). «Ansa Subthalamica: забытый участок волокон». Двигательные расстройства . 35 (1): 75–80. дои : 10.1002/mds.27901 . ПМИД 31758733 .
- ^ Крэгг С.Дж., Бауфретон Дж., Сюэ Ю., Болам Дж.П., Беван, доктор медицинских наук (октябрь 2004 г.). «Синаптическое высвобождение дофамина в субталамическом ядре» . Европейский журнал неврологии . 20 (7): 1788–1802. дои : 10.1111/j.1460-9568.2004.03629.x . ПМИД 15380000 . S2CID 14698708 .
- ^ Перейти обратно: а б Наута Х.Дж., Коул М. (июль 1978 г.). «Эфферентные проекции субталамического ядра: авторадиографическое исследование на обезьянах и кошках». Журнал сравнительной неврологии . 180 (1): 1–16. дои : 10.1002/cne.901800102 . ПМИД 418083 . S2CID 43046462 .
- ^ Перейти обратно: а б Смит Ю., Хазрати Л.Н., Родитель А (апрель 1990 г.). «Эфферентные проекции субталамического ядра у беличьей обезьяны, изученные с помощью метода антероградного отслеживания PHA-L». Журнал сравнительной неврологии . 294 (2): 306–323. дои : 10.1002/cne.902940213 . ПМИД 2332533 . S2CID 9667393 .
- ^ Кита Х., Чанг Х.Т., Китай С.Т. (апрель 1983 г.). «Морфология внутриклеточно меченных субталамических нейронов крыс: световой микроскопический анализ». Журнал сравнительной неврологии . 215 (3): 245–257. дои : 10.1002/cne.902150302 . ПМИД 6304154 . S2CID 32152785 .
- ^ Сюрмейер DJ , Мерсер Дж. Н., Чан К. С. (июнь 2005 г.). «Автономные кардиостимуляторы в базальных ганглиях: кому вообще нужны возбуждающие синапсы?». Современное мнение в нейробиологии . 15 (3): 312–318. дои : 10.1016/j.conb.2005.05.007 . ПМИД 15916893 . S2CID 42900941 .
- ^ Леви Р., Хатчисон В.Д., Лозано А.М., Достровский Дж.О. (октябрь 2000 г.). «Высокочастотная синхронизация активности нейронов субталамического ядра у больных паркинсонизмом с тремором конечностей» . Журнал неврологии . 20 (20): 7766–7775. doi : 10.1523/JNEUROSCI.20-20-07766.2000 . ПМЦ 6772896 . ПМИД 11027240 .
- ^ Линтас А., Силкис И.Г., Альбери Л., Вилла А.Е. (январь 2012 г.). «Дефицит дофамина увеличивает синхронизированную активность субталамического ядра крысы» (PDF) . Исследования мозга . 1434 (3): 142–151. дои : 10.1016/j.brainres.2011.09.005 . ПМИД 21959175 . S2CID 14636489 .
- ^ Пленц Д., Китал С.Т. (август 1999 г.). «Кардиостимулятор базальных ганглиев, образованный субталамическим ядром и наружным бледным шаром». Природа . 400 (6745): 677–682. Бибкод : 1999Natur.400..677P . дои : 10.1038/23281 . ПМИД 10458164 . S2CID 4356230 .
- ^ Ельник Ю. (2002). «Функциональная анатомия базальных ганглиев». Двигательные расстройства . 17 (Приложение 3): С15–С21. дои : 10.1002/mds.10138 . ПМИД 11948751 . S2CID 40925638 .
- ^ Сато Ф., Лавалле П., Левеск М., Родитель А (январь 2000 г.). «Исследование одноаксонного отслеживания нейронов наружного сегмента бледного шара у приматов». Журнал сравнительной неврологии . 417 (1): 17–31. doi : 10.1002/(SICI)1096-9861(20000131)417:1<17::AID-CNE2>3.0.CO;2-I . PMID 10660885 . S2CID 84665164 .
- ^ Смит Ю., Вичманн Т., Делонг М.Р. (май 1994 г.). «Синапсическая иннервация нейронов внутреннего паллидного сегмента субталамическим ядром и внешнего паллидума у обезьян». Журнал сравнительной неврологии . 343 (2): 297–318. дои : 10.1002/cne.903430209 . ПМИД 8027445 . S2CID 24968074 .
- ^ Беван, доктор медицинских наук, Мэгилл П.Дж., Терман Д., Болам Дж.П., Уилсон С.Дж. (октябрь 2002 г.). «Двигайтесь в ритме: колебания субталамического ядра — сети наружного бледного шара». Тенденции в нейронауках . 25 (10): 525–531. дои : 10.1016/S0166-2236(02)02235-X . ПМИД 12220881 . S2CID 8127062 .
- ^ Бергман Х., Вичманн Т., Делонг М.Р. (сентябрь 1990 г.). «Обращение экспериментального паркинсонизма путем поражения субталамического ядра». Наука . 249 (4975): 1436–1438. Бибкод : 1990Sci...249.1436B . дои : 10.1126/science.2402638 . ПМИД 2402638 .
- ^ Бенацуз А., Гросс С., Фегер Дж., Боро Т., Биулак Б. (апрель 1993 г.). «Изменение ригидности и улучшение двигательных качеств путем субталамической высокочастотной стимуляции у обезьян, получавших MPTP». Европейский журнал неврологии . 5 (4): 382–389. дои : 10.1111/j.1460-9568.1993.tb00505.x . ПМИД 8261116 .
- ^ Поллак П., Бенабид А.Л., Гросс С., Гао Д.М., Лоран А., Бенацуз А. и др. (1993). «[Эффекты стимуляции субталамического ядра при болезни Паркинсона]» . Ревю Неврологии . 149 (3): 175–176. ПМИД 8235208 .
- ^ Бекар Л., Либионка В., Тиан Г.Ф., Сюй К., Торрес А., Ван Х. и др. (январь 2008 г.). «Аденозин имеет решающее значение для ослабления тремора, опосредованного глубокой стимуляцией мозга». Природная медицина . 14 (1): 75–80. дои : 10.1038/nm1693 . ПМИД 18157140 . S2CID 7107064 .
- ^ Мартинес-Фернандес Р., Маньес-Миро Х.Ю., Родригес-Рохас Р., Дель Аламо М., Шах Б.Б., Эрнандес-Фернандес Ф. и др. (декабрь 2020 г.). «Рандомизированное исследование субталамотомии с помощью фокусированного ультразвука при болезни Паркинсона». Медицинский журнал Новой Англии . 383 (26): 2501–2513. дои : 10.1056/NEJMoa2016311 . ПМИД 33369354 .
- ^ Лаганьер С., Боес А.Д., Фокс, доктор медицины (июнь 2016 г.). «Сетевая локализация гемихореи-гемибаллизма» . Неврология . 86 (23): 2187–2195. дои : 10.1212/WNL.0000000000002741 . ПМЦ 4898318 . ПМИД 27170566 .
- ^ Картер Р. Книга «Человеческий мозг» . стр. 58, 233.
- ^ Маллет Л., Полосан М., Джаафари Н., Бауп Н., Велтер М.Л., Фонтейн Д. и др. (ноябрь 2008 г.). «Стимуляция субталамического ядра при тяжелом обсессивно-компульсивном расстройстве» . Медицинский журнал Новой Англии . 359 (20): 2121–2134. doi : 10.1056/NEJMoa0708514 . ПМИД 19005196 .
- ^ Бергман Х., Вичманн Т., Делонг М.Р. (сентябрь 1990 г.). «Обращение экспериментального паркинсонизма путем поражения субталамического ядра». Наука . 249 (4975): 1436–1438. Бибкод : 1990Sci...249.1436B . дои : 10.1126/science.2402638 . ПМИД 2402638 .
- ^ Лофреди Р., Ауерниг Г.К., Ирмен Ф., Нивелер Дж., Нойманн В.Дж., Хорн А. и др. (февраль 2021 г.). «Субталамическая стимуляция ухудшает остановку текущих движений». Мозг . 144 (1): 44–52. дои : 10.1093/brain/awaa341 . ПМИД 33253351 .
- ^ Фрэнк М.Дж., Саманта Дж., Мустафа А.А., Шерман С.Дж. (ноябрь 2007 г.). «Придержите лошадей: импульсивность, глубокая стимуляция мозга и лекарства при паркинсонизме» . Наука . 318 (5854): 1309–1312. Бибкод : 2007Sci...318.1309F . дои : 10.1126/science.1146157 . ПМИД 17962524 . S2CID 2718110 .
- ^ Арон А.Р., Беренс Т.Э., Смит С., Фрэнк М.Дж., Полдрак Р.А. (апрель 2007 г.). «Триангуляция сети когнитивного контроля с использованием диффузионно-взвешенной магнитно-резонансной томографии (МРТ) и функциональной МРТ» . Журнал неврологии . 27 (14): 3743–3752. doi : 10.1523/JNEUROSCI.0519-07.2007 . ПМК 6672420 . ПМИД 17409238 .
- ^ Файф К.Х., Гутьеррес-Рид Н.А., Зелл В., Бейли Дж., Льюис СМ, Арон А.Р. и др. (июль 2017 г.). Учида Н (ред.). «Причинная роль субталамического ядра в прерывании поведения» . электронная жизнь . 6 : e27689. дои : 10.7554/eLife.27689 . ПМК 5526663 . ПМИД 28742497 .
- ^ Гийомен А., Серра ГП, Жорж Ф., Валлен-Маккензи О (март 2021 г.). «Экспериментальное исследование роли субталамического ядра (СТЯ) в двигательном контроле с использованием оптогенетики на мышах» . Исследования мозга . 1755 : 147226. doi : 10.1016/j.brainres.2020.147226 . ПМИД 33358727 .
