Аденоассоциированный вирус
| Аденоассоциированный вирус | |
|---|---|
| |
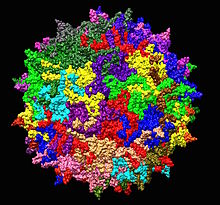
| Структура аденоассоциированного вируса серотипа 2 из 1LP3. Одна пятикратная ось показана в центре. | |
| Научная классификация | |
| (без рейтинга): | Вирус |
| Область : | Моноднавирия |
| Королевство: | Шотокувираэ |
| Тип: | Коссавирикота |
| Сорт: | Квинтовирицеты |
| Заказ: | Пикковираллез |
| Семья: | Парвовирусиды |
| Подсемейство: | Парвовирины |
| Род: | Депендопарвовирус |
| В состав вирусов вошли: | |
| |
Аденоассоциированные вирусы ( ААВ ) — это небольшие вирусы, которые заражают человека и некоторые другие виды приматов . Они принадлежат к роду Dependoparvovirus , который, в свою очередь, относится к семейству Parvoviridae . Это небольшие (примерно 26 нм в диаметре) по репликации дефектные вирусы без оболочки и имеющие геном линейной одноцепочечной ДНК (оцДНК) длиной примерно 4,8 тысяч нуклеотидов (т.п.н.). [ 1 ] [ 2 ]
Некоторые особенности делают AAV привлекательным кандидатом для создания вирусных векторов для генной терапии , а также для создания моделей изогенных заболеваний человека . [ 3 ] генной терапии Векторы с использованием AAV могут инфицировать как делящиеся, так и покоящиеся клетки и персистировать во внехромосомном состоянии, не интегрируясь в геном клетки-хозяина. Однако в нативном вирусе происходит интеграция переносимых вирусом генов в геном хозяина. [ 4 ] Интеграция может быть важна для определенных приложений, но также может иметь нежелательные последствия. Недавние клинические испытания на людях с использованием AAV для генной терапии сетчатки показали многообещающие результаты. [ 5 ]
В марте 2023 года в серии статей Nature были обнаружены высокие титры аденоассоциированного вируса 2 (AAV2), наряду с аденовирусом и герпесвирусом, в образцах, взятых из волны детского гепатита. [ 6 ] В одной статье предполагается, что коинфекция AAV2 может способствовать более серьезным заболеваниям печени, чем инфекция только адено- или герпесвирусами, и что причинно-следственная связь еще предстоит установить. [ 7 ]
История
[ редактировать ]Аденоассоциированный вирус (ААВ), который ранее считался примесью аденовирусных препаратов, был впервые идентифицирован как зависимый парвовирус в 1960-х годах в лабораториях Боба Атчисона в Питтсбурге и Уоллеса Роу в НИЗ . Серологические исследования на людях впоследствии показали, что, несмотря на присутствие у людей, инфицированных вирусами-помощниками , такими как аденовирус или вирус герпеса, сам AAV не вызывает никаких заболеваний. [ 8 ]
Использование в генной терапии
[ редактировать ]Преимущества и недостатки
[ редактировать ]AAV дикого типа привлекли значительный интерес исследователей генной терапии из-за ряда особенностей. Главным среди них было очевидное отсутствие патогенности вируса. Он также может инфицировать неделящиеся клетки и обладает способностью стабильно интегрироваться в геном клетки-хозяина в специфическом сайте (обозначенном AAVS1) в хромосоме человека 19 . [ 9 ] [ 10 ] Эта особенность делает его несколько более предсказуемым, чем ретровирусы , которые представляют угрозу случайного внедрения и мутагенеза, который иногда сопровождается развитием рака. Геном AAV чаще всего интегрируется в указанный сайт, тогда как случайные включения в геном происходят с незначительной частотой. Однако развитие AAV в качестве векторов генной терапии устранило эту интегративную способность за счет удаления повтора и кэпа из ДНК вектора . Желаемый ген вместе с промотором, управляющим транскрипцией гена, вставляется между инвертированными концевыми повторами (ITR), которые способствуют образованию конкатемера в ядре после того, как одноцепочечная векторная ДНК преобразуется комплексами ДНК-полимеразы клетки-хозяина в двухцепочечную. ДНК. Векторы генной терапии на основе AAV образуют эписомальные конкатемеры в ядре клетки-хозяина. В неделящихся клетках эти конкатемеры остаются интактными на протяжении всей жизни клетки-хозяина. В делящихся клетках ДНК AAV теряется в результате клеточного деления, поскольку эписомальная ДНК не реплицируется вместе с ДНК клетки-хозяина. [ 11 ] Случайную интеграцию ДНК AAV в геном хозяина можно обнаружить, но происходит с очень низкой частотой. [ 11 ] AAV также обладают очень низкой иммуногенностью , по-видимому, ограничивающейся выработкой нейтрализующих антител , в то время как они не вызывают четко определенного цитотоксического ответа . [ 12 ] [ 13 ] [ 14 ] Эта особенность, наряду со способностью инфицировать покоящиеся клетки, свидетельствует об их доминировании над аденовирусами как векторами генной терапии человека . [ нужна ссылка ]
Использование вируса действительно имеет некоторые недостатки. Возможности клонирования вектора относительно ограничены, и большинство терапевтических генов требуют полной замены генома вируса длиной 4,8 тыс. оснований. Поэтому большие гены не подходят для использования в стандартном векторе AAV. В настоящее время изучаются варианты преодоления ограниченных возможностей кодирования. [ 15 ] ITR AAV двух геномов могут отжигаться с образованием конкатемеров «голова к хвосту», что почти удваивает емкость вектора. Вставка сайтов сплайсинга позволяет удалить ITR из транскрипта. [ нужна ссылка ]
Из-за преимуществ специализированной генной терапии AAV исследователи создали измененную версию AAV, названную самокомплементарным аденоассоциированным вирусом (scAAV) . В то время как AAV упаковывает одну цепь ДНК и должен ждать синтеза второй цепи, scAAV упаковывает две более короткие цепи, которые комплементарны друг другу. Избегая синтеза второй цепи, scAAV может экспрессироваться быстрее, хотя следует предостеречь, scAAV может кодировать только половину и без того ограниченной способности AAV. [ 16 ] Недавние сообщения показывают, что векторы scAAV более иммуногенны, чем одноцепочечные аденовирусные векторы, индуцируя более сильную активацию цитотоксических Т-лимфоцитов . [ 17 ]
Считается, что гуморальный иммунитет, вызванный инфекцией дикого типа, является обычным явлением. Сопутствующая нейтрализующая активность ограничивает полезность наиболее часто используемого серотипа AAV2 в определенных приложениях. Соответственно, большинство проводимых клинических испытаний включают доставку AAV2 в мозг, относительно иммунологически привилегированный орган. В мозге AAV2 сильно нейрон-специфичен. [ нужна ссылка ]
Клинические испытания
[ редактировать ]По состоянию на 2019 год векторы AAV использовались в более чем 250 клинических исследованиях по всему миру, что составляет примерно 8,3% исследований генной терапии с использованием вирусных векторов. [ 18 ] Недавно были получены многообещающие результаты исследований фазы 1 и фазы 2 для ряда заболеваний, включая врожденный амавроз Лебера , [ 5 ] [ 19 ] [ 20 ] гемофилия , [ 21 ] застойная сердечная недостаточность , [ 22 ] спинальная мышечная атрофия , [ 23 ] дефицит липопротеинлипазы , [ 24 ] и болезнь Паркинсона . [ 25 ]
| Индикация | Ген | Путь введения | Фаза | Номер субъекта | Статус |
| Муковисцидоз | ЦФТР | Легкие, через аэрозоль | я | 12 | Полный |
| ЦФТР | Легкие, через аэрозоль | II | 38 | Полный | |
| ЦФТР | Легкие, через аэрозоль | II | 100 | Полный | |
| Гемофилия Б | ИСПРАВИТЬ | Внутримышечный | я | 9 | Полный |
| ИСПРАВИТЬ | Печеночная артерия | я | 6 | Закончено | |
| Артрит | ТНФР:ФК | Внутрисуставной | я | 1 | Непрерывный |
| Наследственная эмфизема | ААТ | Внутримышечный | я | 12 | Непрерывный |
| Врожденный амороз Лебера | РПЭ65 | Субретинал | I – II | Несколько | Несколько текущих и полных ( voretigene neparvovec ) |
| Возрастная дегенерация желтого пятна | sFlt-1 | Субретинал | I – II | 24 | Непрерывный |
| мышечная дистрофия Дюшенна | SGCA | Внутримышечный | я | 10 | Непрерывный |
| болезнь Паркинсона | ГАД65 , ГАД67 | внутричерепной | я | 12 | Полный [ 27 ] |
| болезнь Канавана | ААС | внутричерепной | я | 21 | Непрерывный |
| Болезнь Баттена | CLN2 | внутричерепной | я | 10 | Непрерывный |
| болезнь Альцгеймера | НФР | внутричерепной | я | 6 | Непрерывный |
| Спинальная мышечная атрофия | СМН1 | Внутривенно, интратекально | I – III | 150+ | Несколько продолжающихся и полных ( onasemnogene abeparvovec ) |
| Застойная сердечная недостаточность | СЕРКА 2а | Внутрикоронарный | IIб | 250 | Непрерывный |
Фундаментальная биология
[ редактировать ]
Геномика, транскриптомика и протеомика
[ редактировать ]Геном AAV построен из одноцепочечной дезоксирибонуклеиновой кислоты (оц- ДНК ), как положительной, так и отрицательной, длиной около 4,7 тысяч оснований. Геном содержит ITR на обоих концах цепи ДНК и две открытые рамки считывания (ORF): Rep и Cap . Первый состоит из четырех перекрывающихся генов, кодирующих белки Rep, необходимые для жизненного цикла AAV, а второй содержит перекрывающиеся нуклеотидные последовательности капсидных белков: VP1, VP2 и VP3, которые взаимодействуют с образованием капсида с икосаэдрической симметрией. [ 28 ]
ITR-последовательности
[ редактировать ]Последовательности инвертированных терминальных повторов (ITR) содержат по 145 оснований каждая. Они были названы так из-за их симметрии, которая, как было показано, необходима для эффективного размножения генома AAV. [ 29 ] Особенностью этих последовательностей, придающей им это свойство, является их способность образовывать шпильку , что способствует так называемому самовсасыванию, позволяющему примазо -независимый синтез второй цепи ДНК. Также было показано, что ITR необходимы как для интеграции ДНК AAV в геном клетки-хозяина (19-я хромосома у человека), так и для спасения от него. [ 30 ] [ 31 ] а также для эффективной инкапсидации ДНК AAV в сочетании с образованием полностью собранных, устойчивых к дезоксирибонуклеазе частиц AAV. [ 32 ]
Что касается генной терапии, ITR, по-видимому, являются единственными последовательностями, необходимыми в цис-последовательности рядом с терапевтическим геном: структурные ( cap ) и упаковочные ( rep ) белки могут доставляться в транс . Благодаря этому предположению было создано множество методов эффективного получения рекомбинантных векторов AAV (rAAV), содержащих репортерный или терапевтический ген. Однако также было опубликовано, что ITR не являются единственными элементами, необходимыми в цис-системе для эффективной репликации и инкапсидации. Несколько исследовательских групп идентифицировали последовательность, обозначенную цис-действующим Rep-зависимым элементом (CARE), внутри кодирующей последовательности гена Rep . Было показано, что CARE усиливает репликацию и инкапсидацию, когда присутствует в цис-форме . [ 33 ] [ 34 ] [ 35 ] [ 36 ]
ген Rep и белки Rep
[ редактировать ]На «левой стороне» генома расположены два промотора, называемые p5 и p19, из которых две перекрывающиеся информационные рибонуклеиновые кислоты ( мРНК могут образовываться ) разной длины. Каждый из них содержит интрон , который может быть либо подвергнут сплайсингу , либо нет. Учитывая эти возможности, можно синтезировать четыре различных мРНК и, следовательно, четыре различных белка Rep с перекрывающейся последовательностью. Их названия отражают их размеры в килодальтонах (кДа): Rep78, Rep68, Rep52 и Rep40. [ 37 ] Rep78 и 68 могут специфически связывать шпильку, образованную ITR, в процессе самовсасывания и расщеплять в определенной области, обозначенной терминальным сайтом разрешения, внутри шпильки. Также было показано, что они необходимы для специфической для AAVS1 интеграции генома AAV. Показано, что все четыре белка Rep связывают АТФ и обладают геликазной активностью. Также было показано, что они усиливают транскрипцию промотора p40 (упомянутого ниже), но подавляют промоторы p5 и p19. [ 31 ] [ 37 ] [ 38 ] [ 39 ] [ 40 ] [ 41 ]
ген cap и белки VP
[ редактировать ]Правая сторона положительно воспринимаемого генома AAV кодирует перекрывающиеся последовательности трех капсидных белков, VP1, VP2 и VP3, и двух вспомогательных белков, MAAP и AAP, которые начинаются с одного промотора, обозначенного p40. Молекулярная масса этих белков составляет 87, 72 и 62 кДа соответственно. [ 42 ] Капсид AAV состоит из смеси VP1, VP2 и VP3, всего 60 мономеров, расположенных в икосаэдрической симметрии в соотношении 1:1:10. [ 43 ] с пустой массой примерно 3,8 МДа . [ 44 ] Кристаллическая структура белка VP3 была определена Xie, Bue и соавт. [ 45 ]

Ген cap производит дополнительный неструктурный белок, называемый белком, активирующим сборку (AAP). Этот белок вырабатывается из ORF2 и необходим для процесса сборки капсида. [ 46 ] Точная функция этого белка в процессе сборки и его структура до сих пор не решены. [ нужна ссылка ]
Все три ВП транслируются с одной мРНК. После синтеза этой мРНК ее можно сплайсировать двумя различными способами: можно вырезать более длинный или более короткий интрон, что приводит к образованию двух пулов мРНК: пула мРНК длиной 2,3 т.п.н. и пула мРНК длиной 2,6 т.п.н. Обычно, особенно в присутствии аденовируса, более длинный интрон является предпочтительным, поэтому мРНК длиной 2,3 т.п.н. представляет собой так называемый «основной сплайсинг». первый кодон AUG В этой форме вырезается , с которого начинается синтез белка VP1, что приводит к снижению общего уровня синтеза белка VP1. Первый кодон AUG, остающийся в основном сплайсинге, является инициирующим кодоном белка VP3. Однако выше этого кодона в той же открытой рамке считывания находится последовательность ACG (кодирующая треонин), окруженная оптимальным контекстом Козака . Это способствует низкому уровню синтеза белка VP2, который на самом деле является белком VP3 с дополнительными N-концевыми остатками, как и VP1. [ 47 ] [ 48 ] [ 49 ] [ 50 ]
Поскольку более крупный интрон предпочтителен для сплайсинга и поскольку в главном сплайсинге кодон ACG является гораздо более слабым сигналом инициации трансляции , соотношение, при котором структурные белки AAV синтезируются in vivo, составляет примерно 1:1:20, что составляет то же, что и в зрелой вирусной частице. [ 51 ] Было показано, что уникальный фрагмент на N-конце белка VP1 обладает активностью фосфолипазы А2 (PLA2), которая, вероятно, необходима для высвобождения частиц AAV из поздних эндосом . [ 52 ] Муралидхар и др. сообщили, что VP2 и VP3 имеют решающее значение для правильной сборки вириона. [ 49 ] Однако совсем недавно Warrington et al. показали, что VP2 не требуется для полного формирования вирусных частиц и эффективной инфекционности, а также показали, что VP2 может переносить большие вставки на своем N-конце, тогда как VP1 не может, вероятно, из-за присутствия домена PLA2. [ 53 ]
Посттрансляционные модификации
[ редактировать ]Недавние открытия, сделанные с использованием высокопроизводительных подходов омики, включают тот факт, что капсиды AAV подвергаются посттрансляционной модификации (PTM) во время производства, например ацетилирование, метилирование, фосфорилирование, дезамидирование, O-GlycNAcylation. [ 54 ] и СУМОилирование по капсидным белкам VP1, VP2 и VP3. Эти ПТМ различаются в зависимости от производственной платформы изготовления. Еще одним таким открытием является тот факт, что геномы AAV эпигенетически метилируются во время производства. Помимо цены, эти результаты могут повлиять на кинетику экспрессии, связывание рецептора rAAV, транспортировку, иммуногенность вектора и долговечность экспрессии. [ 55 ] [ 56 ]
Классификация, серотипы, рецепторы и нативный тропизм
[ редактировать ]| Серотип | Тканевой тропизм [ 57 ] | Пройти гематоэнцефалический барьер | Клеточный тропизм | Синтетический | Комментарий | Опубликовано шапка/реп. |
|---|---|---|---|---|---|---|
| 2 | гладкие мышцы, ЦНС, печень | Нет | Нет | |||
| 5 | ЦНС, гладкие мышцы | Нет | Нет | |||
| 8 | ЦНС, мозг, печень, гладкие мышцы | Нет | Нет | |||
| 9 | ЦНС, печень, гладкие мышцы | Да | Нет | |||
| ПАЛ2 | ЦНС | Да | Да | Экспрессия печени составляет 1/4 от AAV9. | Нет | |
| 9P1/ААВМЁ | ЦНС | Да | астроциты | Да | высокая мускулатура, включая скелетные мышцы, сердце и диафрагму, скелетная трансдукция | Нет |
Два вида AAV были признаны Международным комитетом по таксономии вирусов в 2013 году: аденоассоциированный зависимопарвовирус A (ранее AAV-1, -2, -3 и -4) и аденоассоциированный зависимопарвовирус B (ранее AAV-5). [ 58 ]
До 1990-х годов практически вся биология AAV изучалась с использованием серотипа 2 AAV. Однако AAV широко распространен у людей и других приматов, и несколько серотипов были выделены из различных образцов тканей. Серотипы 2, 3, 5 и 6 были обнаружены в клетках человека, серотипы 1, 4 и 7–11 AAV - в образцах приматов, не являющихся человеком. [ 59 ] По состоянию на 2006 г. описано 11 серотипов AAV , в 2004 г. – 11-й. [ 60 ] Капсидные белки AAV содержат 12 гипервариабельных поверхностных областей, при этом наибольшая вариабельность приходится на тройные проксимальные пики, но геном парвовируса в целом представляет собой высококонсервативные репликационные и структурные гены для всех серотипов. [ 59 ] Все известные серотипы могут инфицировать клетки различных типов тканей. Специфичность ткани определяется серотипом капсида, и псевдотипирование векторов AAV для изменения диапазона их тропизма, вероятно, будет важно для их использования в терапии.
Серотип 2
[ редактировать ]Серотип 2 (AAV2) на данный момент изучен наиболее тщательно. [ 61 ] [ 62 ] [ 63 ] [ 64 ] [ 65 ] [ 66 ] AAV2 обладает естественным тропизмом к скелетным мышцам . [ 67 ] нейроны , [ 61 ] сосудов гладкомышечные клетки [ 68 ] и гепатоциты . [ 69 ]
Для AAV2 описаны три клеточных рецептора: гепарансульфат-протеогликан (HSPG), V β 5 интегрин и рецептор 1 фактора роста фибробластов (FGFR-1). Первый действует как первичный рецептор, тогда как два последних обладают корецепторной активностью и позволяют AAV проникать в клетку путем рецептор-опосредованного эндоцитоза . [ 70 ] [ 71 ] [ 72 ] Эти результаты исследования были оспорены Цю, Хандой и др. [ 73 ] HSPG действует как первичный рецептор, хотя его обилие во внеклеточном матриксе может поглощать частицы AAV и снижать эффективность инфекции. [ 74 ]
Исследования показали, что серотип 2 вируса (AAV-2), очевидно, убивает раковые клетки, не причиняя вреда здоровым. «Наши результаты показывают, что аденоассоциированный вирус типа 2, который заражает большую часть населения, но не имеет известных побочных эффектов, убивает несколько типов раковых клеток, но не оказывает никакого воздействия на здоровые клетки», — сказал Крейг Мейерс, [ 75 ] профессор иммунологии и микробиологии Пенсильвании в Медицинского колледжа штата Пенсильвания в 2005 году. [ 76 ] Это может привести к созданию нового противоракового агента.
В марте 2023 года серия статей Nature связала заражение аденоассоциированным вирусом 2 (AAV2) с волной детского гепатита. [ 6 ]
Другие серотипы
[ редактировать ]Этот раздел необходимо обновить . ( декабрь 2023 г. ) |
Хотя AAV2 является наиболее популярным серотипом в различных исследованиях, основанных на AAV, было показано, что другие серотипы могут быть более эффективными в качестве векторов доставки генов. AAV9 преодолевает гематоэнцефалический барьер у человека, AAV6 гораздо лучше заражает эпителиальные клетки дыхательных путей. [ 77 ] [ 78 ] AAV7 демонстрирует очень высокую скорость трансдукции клеток скелетных мышц мыши (аналогично AAV1 и AAV5), AAV8 трансдуцирует гепатоциты. [ 79 ] [ 80 ] [ 81 ] и было показано, что AAV1 и 5 очень эффективны в доставке генов в эндотелиальные клетки сосудов. [ 82 ] В головном мозге большинство серотипов AAV демонстрируют нейрональный тропизм, тогда как AAV5 также трансдуцирует астроциты. [ 83 ] AAV6, гибрид AAV1 и AAV2, [ 81 ] также демонстрирует более низкую иммуногенность, чем AAV2. [ 80 ]
Серотипы могут различаться в зависимости от рецепторов, с которыми они связаны. Например, трансдукцию AAV4 и AAV5 можно ингибировать растворимыми сиаловыми кислотами (разной формы для каждого из этих серотипов). [ 84 ] и было показано, что AAV5 проникает в клетки через рецептор тромбоцитарного фактора роста . [ 85 ]
Синтетические серотипы
[ редактировать ]Было предпринято много усилий по разработке и улучшению новых вариантов AAV как для клинических, так и для исследовательских целей. Такие модификации включают новые тропизмы, нацеленные на определенные ткани, и модифицированные поверхностные остатки, позволяющие избежать обнаружения иммунной системой. Помимо выбора конкретных штаммов рекомбинантного AAV (rAAV) для воздействия на определенные клетки, исследователи также изучили псевдотипирование AAV — практику создания гибридов определенных штаммов AAV для достижения еще более точной цели. Гибрид создается путем взятия капсида одного штамма и генома другого штамма. Например, исследования с использованием AAV2/5, гибрида генома AAV2 и капсида AAV5, позволили достичь большей точности и диапазона в клетках мозга, чем негибридный AAV2. Исследователи продолжили экспериментировать с псевдотипированием, создавая штаммы с гибридными капсидами. AAV-DJ имеет гибридный капсид восьми различных штаммов AAV; как таковой, он может инфицировать различные клетки во многих областях тела - свойство, которым не обладал бы одиночный штамм AAV с ограниченным тропизмом. [ 86 ] Другие усилия по разработке и улучшению новых вариантов AAV включали предковую реконструкцию вариантов вируса для создания новых векторов с улучшенными свойствами для клинического применения и изучения биологии AAV. [ 87 ]
Иммунология
[ редактировать ]AAV представляет особый интерес для генных терапевтов из-за его очевидной ограниченной способности вызывать иммунные реакции у людей, фактора, который должен положительно влиять на эффективность векторной трансдукции, одновременно снижая риск любой иммуноассоциированной патологии .
Считается, что AAV не играет какой-либо известной роли в заболевании. [ 88 ] Однако реакция иммунной системы хозяина и иммунная толерантность снижают эффективность генной терапии, опосредованной AAV. Было показано, что иммунный ответ хозяина отвечает на векторы AAV, трансдуцированные клетки и трансдуцированные белки. [ 89 ] Иммунный ответ можно разделить на две категории: врожденный и адаптивный, последняя из которых подразделяется на гуморальный и клеточно-опосредованный. [ 90 ] [ 91 ]
Врожденный
[ редактировать ]Врожденный . иммунный ответ на векторы AAV был охарактеризован на животных моделях Внутривенное введение мышам вызывает временную выработку провоспалительных цитокинов и некоторую инфильтрацию нейтрофилов и других лейкоцитов в печень, которая, по-видимому, изолирует большой процент введенных вирусных частиц. Уровни растворимого фактора и клеточной инфильтрации возвращаются к исходному уровню в течение шести часов. Напротив, более агрессивные вирусы вызывают врожденные реакции, продолжающиеся 24 часа или дольше. [ 92 ]
Исследования in vivo показывают, что векторы AAV взаимодействуют с путями Toll-подобного рецептора (TLR)9 и TLR2-MyD88, запуская врожденный иммунный ответ путем стимуляции выработки интерферонов. [ 93 ] Показано, что мыши с дефицитом TLR9 более восприимчивы к лечению AAV и демонстрируют более высокий уровень экспрессии трансгена. [ 94 ]
Гуморальный
[ редактировать ]Из-за предшествующей естественной инфекции у многих людей уже имеются нейтрализующие антитела (NAb) против AAV, что может существенно затруднить его применение в генной терапии. [ 95 ] Несмотря на то, что AAV сильно варьируют среди дикого типа и синтетических вариантов, сайты узнавания антител могут быть консервативными в ходе эволюции. [ 96 ]
Известно, что вирус вызывает сильный гуморальный иммунитет на животных моделях и в человеческой популяции, где считается, что до 80% людей являются серопозитивными к AAV2. антитела Известно, что обладают нейтрализующим действием, и при применении в генной терапии они действительно влияют на эффективность векторной трансдукции при некоторых путях введения. Как показывают исследования с прайм-бустер на животных, а также клинические испытания, наряду с постоянным уровнем антител, специфичных к AAV, B-клеточная память также сильна. [ 97 ] У серопозитивных людей циркулирующие антитела IgG к AAV2, по-видимому, в основном состоят из подклассов IgG1 и IgG2 с небольшим присутствием или отсутствием IgG3 или IgG4. [ 98 ]
клеточно-опосредованный
[ редактировать ]Клеточно -опосредованный ответ на вирус и векторы плохо изучен и в значительной степени игнорировался в литературе еще в 2005 году. [ 97 ] Клинические испытания с использованием вектора на основе AAV2 для лечения гемофилии B, по-видимому, указывают на то, что может происходить целенаправленное разрушение трансдуцированных клеток. [ 99 ] В сочетании с данными, показывающими, что CD8+ Т-клетки могут распознавать элементы капсида AAV in vitro , [ 100 ] Похоже, что может существовать цитотоксический ответ Т-лимфоцитов на векторы AAV. Цитотоксические реакции предполагают участие CD4+ Т-хелперных клеток в ответ на AAV, а данные исследований in vitro на людях позволяют предположить, что вирус действительно может индуцировать такие реакции, включая реакции памяти как Th1, так и Th2. [ 98 ] В капсидном белке VP1 AAV был идентифицирован ряд эпитопов -кандидатов, стимулирующих Т-клетки , которые могут быть привлекательными мишенями для модификации капсида, если вирус будет использоваться в качестве вектора для генной терапии. [ 98 ] [ 99 ]
Цикл заражения
[ редактировать ]Цикл заражения AAV состоит из нескольких этапов: от заражения клетки до производства новых инфекционных частиц: [ нужна ссылка ]
- прикрепление к клеточной мембране
- рецептор-опосредованный эндоцитоз
- эндосомальный транспорт
- выход из поздней эндосомы или лизосомы
- транслокация в ядро
- удаление покрытия
- образование двухцепочечной репликативной формы ДНК генома AAV
- экспрессия Rep- генов
- генома репликация
- экспрессия кэп -генов, синтез частиц оцДНК потомства
- сборка полных вирионов и
- выход из зараженной клетки.
Некоторые из этих этапов могут выглядеть по-разному в разных типах клеток, что отчасти способствует определенному и довольно ограниченному нативному тропизму AAV. Репликация вируса также может различаться в одном типе клеток в зависимости от текущей фазы клеточного цикла . [ 101 ]
Характерной особенностью аденоассоциированного вируса является нарушение репликации и, следовательно, его неспособность размножаться в непораженных клетках. Аденоассоциированный вирус распространяется путем совместного заражения клетки вирусом-помощником. Первым вирусом-помощником, который был описан как обеспечивающий успешную генерацию новых частиц AAV, был аденовирус, от которого произошло название AAV. Затем было показано, что репликации AAV могут способствовать избранные белки, полученные из генома аденовируса. [ 102 ] [ 103 ] другими вирусами, такими как HSV [ 104 ] или коровьей оспы, или генотоксичными агентами, такими как УФ- облучение или гидроксимочевина . [ 105 ] [ 106 ] [ 107 ] В зависимости от присутствия или отсутствия вируса-хелпера жизненный цикл AAV проходит либо по литическому, либо по лизогенному пути соответственно. [ 108 ] Если есть вирус-помощник, экспрессия гена AAV активируется, позволяя вирусу реплицироваться с использованием полимеразы клетки-хозяина. Когда вирус-помощник убивает клетку-хозяина, высвобождаются новые вирионы AAV. Если вирус-помощник отсутствует, AAV проявляет лизогенное поведение. Когда AAV инфицирует клетку в одиночку, экспрессия его гена подавляется (AAV не реплицируется), и его геном включается в геном хозяина (в хромосому 19 человека). В редких случаях лизис может происходить без вируса-помощника, но обычно AAV не может реплицироваться и убивать клетку самостоятельно. [ 109 ]
Минимальный набор аденовирусных генов, необходимый для эффективной генерации дочерних частиц AAV, был обнаружен Мацуситой, Эллингером и др. [ 102 ] Это открытие позволило разработать новые методы производства рекомбинантного AAV, которые не требуют коинфекции аденовирусом клеток, продуцирующих AAV. В отсутствие вируса-помощника или генотоксических факторов ДНК AAV может либо интегрироваться в геном хозяина, либо сохраняться в эписомальной форме. В первом случае интеграция опосредуется белками Rep78 и Rep68 и требует присутствия ITR, фланкирующих интегрируемую область. У мышей геном AAV сохраняется в течение длительного периода времени в покоящихся тканях, таких как скелетные мышцы, в эписомальной форме (круглая конформация «голова к хвосту»). [ 110 ]
См. также
[ редактировать ]- Модели изогенных заболеваний человека
- Онколитический ААВ
- Рекомбинантная геномная инженерия, опосредованная AAV
Ссылки
[ редактировать ]- ^ Насо М.Ф., Томкович Б., Перри В.Л., Строл В.Р. (август 2017 г.). «Аденоассоциированный вирус (AAV) как вектор для генной терапии» . Биопрепараты . 31 (4): 317–334. дои : 10.1007/s40259-017-0234-5 . ПМЦ 5548848 . ПМИД 28669112 .
- ^ Ву З, Ян Х, Колози П. (январь 2010 г.). «Влияние размера генома на упаковку вектора AAV» . Молекулярная терапия . 18 (1): 80–86. дои : 10.1038/mt.2009.255 . ПМК 2839202 . ПМИД 19904234 .
- ^ Григер Дж. К., Самульский Р. Дж. (2005). «Адено-ассоциированный вирус как вектор генной терапии: разработка, производство и клиническое применение вектора». Аденоассоциированный вирус как вектор генной терапии: разработка, производство и клиническое применение вектора . Достижения в области биохимической инженерии/биотехнологии. Том. 99. стр. 119–45. дои : 10.1007/10_005 . ISBN 978-3-540-28404-8 . PMID 16568890 .
- ^ Дейл Д.Р., Рассел Д.В. (август 2009 г.). «Интеграция аденоассоциированных вирусных векторов» . Современное мнение о молекулярной терапии . 11 (4): 442–7. ПМЦ 2929125 . ПМИД 19649989 .
- ^ Перейти обратно: а б Магуайр А.М., Симонелли Ф., Пирс Э.А., Пью Э.Н., Мингоцци Ф., Бенничелли Дж. и др. (май 2008 г.). «Безопасность и эффективность переноса генов при врожденном амаврозе Лебера» . Медицинский журнал Новой Англии . 358 (21): 2240–8. doi : 10.1056/NEJMoa0802315 . ПМЦ 2829748 . ПМИД 18441370 .
- ^ Перейти обратно: а б Таке Ф (май 2023 г.). «Вспышка тяжелого гепатита у детей, связанная с вирусом AAV2». Природа . 617 (7961): 471–472. Бибкод : 2023Natur.617..471T . дои : 10.1038/d41586-023-00570-8 . ПМИД 36997704 .
- ^ Сервеллита В., Сотомайор Гонсалес А., Ламсон Д.М., Форсайт А., Ха Х.Дж., Базинет А.Л. и др. (май 2023 г.). «Аденоассоциированный вирус типа 2 у детей в США с острым тяжелым гепатитом» . Природа . 617 (7961): 574–580. Бибкод : 2023Natur.617..574S . дои : 10.1038/s41586-023-05949-1 . ПМК 10170441 . ПМИД 36996871 .
- ^ Картер Би Джей (декабрь 2004 г.). «Адено-ассоциированный вирус и развитие адено-ассоциированных вирусных векторов: историческая перспектива» . Молекулярная терапия . 10 (6): 981–9. дои : 10.1016/j.ymthe.2004.09.011 . ПМИД 15564130 .
- ^ Котин Р.М., Синискалько М., Самульски Р.Дж., Чжу К.Д., Хантер Л., Лафлин К.А. и др. (март 1990 г.). «Сайт-специфическая интеграция аденоассоциированного вируса» . Труды Национальной академии наук Соединенных Штатов Америки . 87 (6): 2211–5. Бибкод : 1990PNAS...87.2211K . дои : 10.1073/pnas.87.6.2211 . ПМК 53656 . ПМИД 2156265 .
- ^ Суроски Р.Т., Урабе М., Годвин С.Г., МакКвистон С.А., Курцман Г.Дж., Озава К. и др. (октябрь 1997 г.). «Аденоассоциированные вирусные белки Rep нацеливают последовательности ДНК на уникальный локус в геноме человека» . Журнал вирусологии . 71 (10): 7951–9. doi : 10.1128/JVI.71.10.7951–7959.1997 . ЧВК 192153 . ПМИД 9311886 .
- ^ Перейти обратно: а б Дая С., Бернс К.И. (октябрь 2008 г.). «Генная терапия с использованием аденоассоциированных вирусных векторов» . Обзоры клинической микробиологии . 21 (4): 583–93. дои : 10.1128/CMR.00008-08 . ПМК 2570152 . ПМИД 18854481 .
- ^ Чирмул Н., Проперт К., Магосин С., Цянь Ю, Цянь Р., Уилсон Дж (сентябрь 1999 г.). «Иммунные реакции на аденовирус и аденоассоциированный вирус у человека» . Генная терапия . 6 (9): 1574–83. дои : 10.1038/sj.gt.3300994 . ПМИД 10490767 .
- ^ Эрнандес Ю.Дж., Ван Дж., Кернс В.Г., Лойлер С., Пуарье А., Флотт Т.Р. (октябрь 1999 г.). «Латентная аденоассоциированная вирусная инфекция вызывает гуморальные, но не клеточно-опосредованные иммунные реакции на модели приматов, не являющихся человеком» . Журнал вирусологии . 73 (10): 8549–58. doi : 10.1128/JVI.73.10.8549-8558.1999 . ПМЦ 112875 . ПМИД 10482608 .
- ^ Поннажаган С., Мукерджи П., Йодер М.С., Ван К.С., Чжоу С.З., Каплан Дж. и др. (апрель 1997 г.). «Перенос гена, опосредованный аденоассоциированным вирусом 2, in vivo: органотропизм и экспрессия трансдуцированных последовательностей у мышей». Джин . 190 (1): 203–10. дои : 10.1016/S0378-1119(96)00576-8 . ПМИД 9185868 .
- ^ Бак Р.О., Портеус М.Х. (июль 2017 г.). «CRISPR-опосредованная интеграция больших кассет генов с использованием донорских векторов AAV» . Отчеты по ячейкам . 20 (3): 750–756. дои : 10.1016/j.celrep.2017.06.064 . ПМЦ 5568673 . ПМИД 28723575 .
- ^ Маккарти Д.М., Монахан П.Е., Самульски Р.Дж. (август 2001 г.). «Векторы самокомплементарного рекомбинантного аденоассоциированного вируса (scAAV) способствуют эффективной трансдукции независимо от синтеза ДНК» . Генная терапия . 8 (16): 1248–54. дои : 10.1038/sj.gt.3301514 . ПМИД 11509958 .
- ^ Роджерс Г.Л., Мартино А.Т., Золотухин И., Эртл Х.К., Херцог Р.В. (январь 2014 г.). «Роль векторного генома и лежащей в его основе мутации фактора IX в иммунных ответах на генную терапию AAV при гемофилии B» . Журнал трансляционной медицины . 12:25 . дои : 10.1186/1479-5876-12-25 . ПМЦ 3904690 . ПМИД 24460861 .
- ^ «Векторы, используемые в клинических испытаниях генной терапии» . Журнал генной медицины . Уайли. Декабрь 2018. Архивировано из оригинала 21 октября 2019 года . Проверено 4 января 2012 г.
- ^ Бейнбридж Дж.В., Смит А.Дж., Баркер С.С., Робби С., Хендерсон Р., Балагган К. и др. (май 2008 г.). «Влияние генной терапии на зрительную функцию при врожденном амаврозе Лебера». Медицинский журнал Новой Англии . 358 (21): 2231–9. CiteSeerX 10.1.1.574.4003 . doi : 10.1056/NEJMoa0802268 . ПМИД 18441371 .
- ^ Хаусвирт В.В., Алеман Т.С., Каушал С., Цидециан А.В., Шварц С.Б., Ван Л. и др. (октябрь 2008 г.). «Лечение врожденного амавроза Лебера, вызванного мутациями RPE65, путем субретинальной инъекции вектора гена аденоассоциированного вируса: краткосрочные результаты исследования фазы I» . Генная терапия человека . 19 (10): 979–90. дои : 10.1089/hum.2008.107 . ПМЦ 2940541 . ПМИД 18774912 .
- ^ Натвани А.С., Тадденхэм Э.Г., Рангараджан С., Розалес С., Макинтош Дж., Линч Д.С. и др. (декабрь 2011 г.). «Перенос генов, опосредованный аденовирус-ассоциированным вирусным вектором, при гемофилии B» . Медицинский журнал Новой Англии . 365 (25): 2357–65. дои : 10.1056/NEJMoa1108046 . ПМК 3265081 . ПМИД 22149959 .
- ^ Джессап М., Гринберг Б., Манчини Д., Каппола Т., Поли Д.Ф., Яски Б. и др. (июль 2011 г.). «Повышение уровня кальция путем чрескожного применения генной терапии при сердечно-сосудистых заболеваниях (CUPID): исследование фазы 2 интракоронарной генной терапии Ca2+-АТФазы саркоплазматического ретикулума у пациентов с выраженной сердечной недостаточностью» . Тираж . 124 (3): 304–13. doi : 10.1161/CIRCULATIONAHA.111.022889 . ПМЦ 5843948 . ПМИД 21709064 .
- ^ «AveXis сообщает о данных продолжающегося исследования фазы 1 AVXS-101 при спинальной мышечной атрофии типа 1» . Авексис . 6 мая 2016 года. Архивировано из оригинала 11 июня 2017 года . Проверено 8 мая 2016 г.
- ^ Годе Д., Мето Ж., Дери С., Бриссон Д., Эссембре С., Трембле Г. и др. (апрель 2013 г.). «Эффективность и долгосрочная безопасность генной терапии алипогена типарвовека (AAV1-LPLS447X) при дефиците липопротеинлипазы: открытое исследование» . Джин Тер . 20 (4): 361–9. дои : 10.1038/gt.2012.43 . ПМЦ 4956470 . ПМИД 22717743 .
- ^ Левитт П.А., Резай А.Р., Лихи М.А., Ожеманн С.Г., Флаэрти А.В., Эскандар Э.Н. и др. (апрель 2011 г.). «Генная терапия AAV2-GAD для лечения прогрессирующей болезни Паркинсона: двойное слепое рандомизированное исследование, контролируемое ложной хирургической операцией». «Ланцет». Неврология . 10 (4): 309–19. дои : 10.1016/S1474-4422(11)70039-4 . ПМИД 21419704 . S2CID 37154043 .
- ^ Картер Би Джей (май 2005 г.). «Адено-ассоциированные вирусные векторы в клинических испытаниях». Генная терапия человека . 16 (5): 541–50. дои : 10.1089/hum.2005.16.541 . ПМИД 15916479 .
- ^ Каплитт М.Г., Фейгин А., Тан С., Фицсаймонс Х.Л., Мэттис П., Лоулор П.А. и др. (июнь 2007 г.). «Безопасность и переносимость генной терапии с использованием гена GAD, переносимого аденоассоциированным вирусом (AAV), при болезни Паркинсона: открытое исследование, фаза I». Ланцет . 369 (9579): 2097–105. дои : 10.1016/S0140-6736(07)60982-9 . ПМИД 17586305 . S2CID 24491886 .
- ^ Картер Би Джей (2000). «Адено-ассоциированный вирус и адено-ассоциированные вирусные векторы для доставки генов». В Лассик Д.Д., Темплтон Н.С. (ред.). Генная терапия: терапевтические механизмы и стратегии . Нью-Йорк: Marcel Dekker, Inc., стр. 41–59. ISBN 978-0-585-39515-9 .
- ^ Бохенцки Р.А., Лефевр Р.Б., Бернс К.И. (октябрь 1988 г.). «Требования к последовательности и симметрии внутренних палиндромных последовательностей терминального повтора аденоассоциированного вируса». Вирусология . 166 (2): 316–27. дои : 10.1016/0042-6822(88)90502-8 . ПМИД 2845646 .
- ^ Ван XS, Поннажаган С, Шривастава А (июль 1995 г.). «Сигналы спасения и репликации генома аденоассоциированного вируса 2». Журнал молекулярной биологии . 250 (5): 573–80. дои : 10.1006/jmbi.1995.0398 . ПМИД 7623375 .
- ^ Перейти обратно: а б Вейцман, доктор медицинских наук, Кёстиё С.Р., Котин Р.М., Оуэнс Р.А. (июнь 1994 г.). «Белки Rep аденоассоциированного вируса (AAV) опосредуют образование комплекса между ДНК AAV и местом его интеграции в ДНК человека» . Труды Национальной академии наук Соединенных Штатов Америки . 91 (13): 5808–12. Бибкод : 1994PNAS...91.5808W . дои : 10.1073/pnas.91.13.5808 . ПМК 44086 . ПМИД 8016070 .
- ^ Чжоу X, Музыка Н (апрель 1998 г.). «Упаковка аденоассоциированной вирусной ДНК in vitro» . Журнал вирусологии . 72 (4): 3241–7. doi : 10.1128/JVI.72.4.3241–3247.1998 . ПМЦ 109794 . ПМИД 9525651 .
- ^ Нони П., Тессье Дж., Шадеф Г., Уорд П., Жиро А., Дюгаст М. и др. (октябрь 2001 г.). «Новый цис-действующий элемент репликации в геноме аденоассоциированного вируса типа 2 участвует в амплификации интегрированных последовательностей Rep-Cap» . Журнал вирусологии . 75 (20): 9991–4. doi : 10.1128/JVI.75.20.9991-9994.2001 . ПМЦ 114572 . ПМИД 11559833 .
- ^ Нони П., Шадеф Г., Тессье Дж., Мулье П., Салветти А. (январь 2003 г.). «Доказательства упаковки последовательностей Rep-Cap в капсиды аденоассоциированного вируса (AAV) типа 2 в отсутствие инвертированных концевых повторов: модель генерации повтор-положительных частиц AAV» . Журнал вирусологии . 77 (1): 776–81. doi : 10.1128/JVI.77.1.776-781.2003 . ПМК 140600 . ПМИД 12477885 .
- ^ Филпотт, Нью-Джерси, Жиро-Вали С., Дюпюи С., Гомос Дж., Гамильтон Х., Бернс К.И. и др. (июнь 2002 г.). «Эффективная интеграция векторов ДНК рекомбинантных аденоассоциированных вирусов требует цис-последовательности p5-rep» . Журнал вирусологии . 76 (11): 5411–21. doi : 10.1128/JVI.76.11.5411-5421.2002 . ПМК 137060 . ПМИД 11991970 .
- ^ Таллис Г.Е., Шенк Т. (декабрь 2000 г.). «Эффективная репликация векторов аденоассоциированного вируса 2 типа: цис-действующий элемент вне концевых повторов и минимальный размер» . Журнал вирусологии . 74 (24): 11511–21. doi : 10.1128/JVI.74.24.11511-11521.2000 . ПМК 112431 . ПМИД 11090148 .
- ^ Перейти обратно: а б Кьёстиё С.Р., Оуэнс Р.А., Вайцман М.Д., Антони Б.А., Чеяновский Н., Картер Б.Дж. (май 1994 г.). «Анализ аденоассоциированных вирусов (AAV) дикого типа и мутантных белков Rep на предмет их способности отрицательно регулировать уровни мРНК p5 и p19 AAV» . Журнал вирусологии . 68 (5): 2947–57. doi : 10.1128/JVI.68.5.2947-2957.1994 . ПМК 236783 . ПМИД 8151765 .
- ^ Im DS, Muzyczka N (май 1990 г.). «Белок Rep68, связывающий происхождение AAV, представляет собой АТФ-зависимую сайт-специфическую эндонуклеазу с ДНК-хеликазной активностью». Клетка . 61 (3): 447–57. дои : 10.1016/0092-8674(90)90526-К . ПМИД 2159383 . S2CID 27997617 .
- ^ Im DS, Muzyczka N (февраль 1992 г.). «Частичная очистка аденоассоциированных вирусов Rep78, Rep52 и Rep40 и их биохимическая характеристика» . Журнал вирусологии . 66 (2): 1119–28. doi : 10.1128/JVI.66.2.1119-1128.1992 . ПМК 240816 . ПМИД 1309894 .
- ^ Самульский Р.Дж. (2003). «Векторы AAV, будущая рабочая лошадка генной терапии человека». Семинар Исследовательского фонда Эрнста Шеринга . Генная терапия человека: текущие возможности и будущие тенденции. стр. 25–40. дои : 10.1007/978-3-662-05352-2_3 . ISBN 978-3-662-05354-6 . ПМИД 12894449 .
- ^ Тремпе Дж.П., Картер Б.Дж. (январь 1988 г.). «Регуляция экспрессии генов аденоассоциированного вируса в клетках 293: контроль количества и трансляции мРНК» . Журнал вирусологии . 62 (1): 68–74. doi : 10.1128/JVI.62.1.68-74.1988 . ПМК 250502 . ПМИД 2824856 .
- ^ Джей Ф.Т., Лафлин Калифорния, Картер Б.Дж. (май 1981 г.). «Эукариотический контроль трансляции: на синтез белка аденоассоциированного вируса влияет мутация в ДНК-связывающем белке аденовируса» . Труды Национальной академии наук Соединенных Штатов Америки . 78 (5): 2927–31. Бибкод : 1981PNAS...78.2927J . дои : 10.1073/pnas.78.5.2927 . ПМК 319472 . ПМИД 6265925 .
- ^ Зоннтаг Ф., Шмидт К., Кляйншмидт Дж.А. (июнь 2010 г.). «Фактор сборки вируса способствует образованию капсида AAV2 в ядрышке» . Труды Национальной академии наук Соединенных Штатов Америки . 107 (22): 10220–5. Бибкод : 2010PNAS..10710220S . дои : 10.1073/pnas.1001673107 . ПМК 2890453 . ПМИД 20479244 .
- ^ Пирсон Э.Э., Кейфер Д.З., Асокан А., Джарролд М.Ф. (июль 2016 г.). «Выявление разнообразия аденоассоциированных вирусных частиц с помощью масс-спектрометрии с обнаружением заряда» . Аналитическая химия . 88 (13). Американское химическое общество (ACS): 6718–6725. дои : 10.1021/acs.analchem.6b00883 . ПМК 6537880 . ПМИД 27310298 .
- ^ Се Кью, Бу В., Бхатия С., Харе Дж., Сомасундарам Т., Аззи А. и др. (август 2002 г.). «Атомная структура аденоассоциированного вируса (AAV-2), вектора для генной терапии человека» . Труды Национальной академии наук Соединенных Штатов Америки . 99 (16): 10405–10. Бибкод : 2002PNAS...9910405X . дои : 10.1073/pnas.162250899 . ПМЦ 124927 . ПМИД 12136130 .
- ^ Зоннтаг Ф., Кетер К., Шмидт К., Вегхофер М., Раупп С., Ньето К. и др. (декабрь 2011 г.). «Белок, активирующий сборку, способствует сборке капсида различных серотипов аденоассоциированных вирусов» . Журнал вирусологии . 85 (23): 12686–97. дои : 10.1128/JVI.05359-11 . ПМК 3209379 . ПМИД 21917944 .
- ^ Бесерра С.П., Роуз Дж.А., Харди М., Баруди Б.М., Андерсон К.В. (декабрь 1985 г.). «Прямое картирование аденоассоциированных белков капсида вируса B и C: возможный кодон инициации ACG» . Труды Национальной академии наук Соединенных Штатов Америки . 82 (23): 7919–23. Бибкод : 1985PNAS...82.7919B . дои : 10.1073/pnas.82.23.7919 . ПМК 390881 . ПМИД 2999784 .
- ^ Кассинотти П., Вайц М., Трачин Дж.Д. (ноябрь 1988 г.). «Организация капсидного гена аденоассоциированного вируса (AAV): картирование минорной сплайсированной мРНК, кодирующей капсидный белок 1 вируса». Вирусология . 167 (1): 176–84. дои : 10.1016/0042-6822(88)90067-0 . ПМИД 2847413 .
- ^ Перейти обратно: а б Муралидхар С., Бесерра С.П., Роуз Дж.А. (январь 1994 г.). «Сайт-направленный мутагенез кодонов инициации структурного белка аденоассоциированного вируса 2 типа: влияние на регуляцию синтеза и биологическую активность» . Журнал вирусологии . 68 (1): 170–6. doi : 10.1128/JVI.68.1.170-176.1994 . ПМК 236275 . ПМИД 8254726 .
- ^ Тремпе Дж.П., Картер Б.Дж. (сентябрь 1988 г.). «Альтернативный сплайсинг мРНК необходим для синтеза капсидного белка аденоассоциированного вируса VP1» . Журнал вирусологии . 62 (9): 3356–63. doi : 10.1128/JVI.62.9.3356-3363.1988 . ПМК 253458 . ПМИД 2841488 .
- ^ Рабиновиц Дж. Э., Самульский Р. Дж. (декабрь 2000 г.). «Создание лучшего вектора: манипулирование вирионами AAV» . Вирусология . 278 (2): 301–8. дои : 10.1006/виро.2000.0707 . ПМИД 11118354 .
- ^ Жирод А., Вобус С.Э., Задори З., Рид М., Лейке К., Тийссен П. и др. (май 2002 г.). «Капсидный белок VP1 аденоассоциированного вируса типа 2 несет домен фосфолипазы А2, необходимый для инфекционности вируса» . Журнал общей вирусологии . 83 (Часть 5): 973–8. дои : 10.1099/0022-1317-83-5-973 . ПМИД 11961250 .
- ^ Уоррингтон К.Х., Горбатюк О.С., Харрисон Дж.К., Опи С.Р., Золотухин С., Музычка Н. (июнь 2004 г.). «Капсидный белок VP2 аденоассоциированного вируса типа 2 не является необходимым и может переносить большие пептидные вставки на своем N-конце» . Журнал вирусологии . 78 (12): 6595–609. doi : 10.1128/JVI.78.12.6595-6609.2004 . ПМК 416546 . ПМИД 15163751 .
- ^ Румачик Н.Г., Малакер С.А., Павелейт Н., Мейнард Л.Х., Адамс CM, Лейб Р.Д. и др. (май 2020 г.). «Методы имеют значение: стандартные производственные платформы для получения рекомбинантных AAV химически и функционально различных векторов» . Молекулярная терапия – методы и клиническое развитие . 18 : 98–118. дои : 10.1016/j.omtm.2020.05.018 . ПМЦ 7488757 . ПМИД 32995354 .
- ^ Чен К., Ньенга Р., Лойхс Б., Чиокка С., Кляйншмидт Дж., Мюллер М. (сентябрь 2020 г.). «СУМОилирование нацелено на аденоассоциированные вирусные капсиды, но в основном ограничивает трансдукцию клеточными механизмами» . Журнал вирусологии . 94 (19): e00871-20. дои : 10.1128/JVI.00871-20 . ПМЦ 7495375 . ПМИД 32669341 .
- ^ Джайлс А.Р., Симс Дж.Дж., Тернер К.Б., Говиндасами Л., Альвира М.Р., Лок М. и др. (декабрь 2018 г.). «Деамидирование аминокислот на поверхности аденоассоциированных вирусных капсидов приводит к неоднородности заряда и изменению векторной функции» . Молекулярная терапия . 26 (12): 2848–2862. дои : 10.1016/j.ymthe.2018.09.013 . ПМК 6277538 . ПМИД 30343890 .
- ^ «Тропизмы AAV» . ВекторСтроитель .
- ^ «Подсемейство: Parvovirinae, род: Dependoparvovirus» . Международный комитет по таксономии вирусов (ICTV) . Проверено 31 января 2020 г.
- ^ Перейти обратно: а б Вейцман, доктор медицинских наук, Линден Р.М. (2011). «Биология аденоассоциированных вирусов». В Снайдер Р.О., Мулье П. (ред.). Методы и протоколы аденоассоциированных вирусов . Тотова, Нью-Джерси: Humana Press. ISBN 978-1-61779-370-7 .
- ^ Мори С., Ван Л., Такеучи Т., Канда Т. (декабрь 2004 г.). «Два новых аденоассоциированных вируса яванских обезьян: характеристика псевдотипирования капсидного белка» . Вирусология . 330 (2): 375–83. дои : 10.1016/j.virol.2004.10.012 . ПМИД 15567432 .
- ^ Перейти обратно: а б Бартлетт Дж. С., Самульски Р. Дж., МакКаун Т. Дж. (май 1998 г.). «Селективное и быстрое поглощение аденоассоциированного вируса типа 2 в мозге». Генная терапия человека . 9 (8): 1181–6. дои : 10.1089/hum.1998.9.8-1181 . ПМИД 9625257 .
- ^ Фишер А.С., Бек С.Е., Смит С.И., Лаубе Б.Л., Аскин Ф.Б., Гуггино С.Е. и др. (декабрь 2003 г.). «Успешная экспрессия трансгена с помощью серийных доз аэрозольных векторов rAAV2 у макак-резус» . Молекулярная терапия . 8 (6): 918–26. дои : 10.1016/j.ymthe.2003.08.015 . PMID 14664794 .
- ^ Никлин С.А., Бюнинг Х., Дишарт К.Л., де Алвис М., Жирод А., Хакер У. и др. (сентябрь 2001 г.). «Эффективный и селективный перенос гена, опосредованный AAV2, направленный на сосудистые эндотелиальные клетки человека» . Молекулярная терапия . 4 (3): 174–81. дои : 10.1006/mthe.2001.0424 . ПМИД 11545607 .
- ^ Рабиновиц Дж. Э., Сяо В., Самульский Р. Дж. (декабрь 1999 г.). «Инсерционный мутагенез капсида AAV2 и получение рекомбинантного вируса» . Вирусология 265 (2): 274–85. дои : 10.1006/virus.1999.0045 . ПМИД 10600599 .
- ^ Ши В., Бартлетт Дж.С. (апрель 2003 г.). «Включение RGD в VP3 обеспечивает векторы на основе аденоассоциированного вируса типа 2 (AAV2) с независимым от гепарансульфата механизмом проникновения в клетку» . Молекулярная терапия . 7 (4): 515–25. дои : 10.1016/S1525-0016(03)00042-X . ПМИД 12727115 .
- ^ Ву П., Сяо В., Конлон Т., Хьюз Дж., Агбандже-МакКенна М., Феркол Т. и др. (сентябрь 2000 г.). «Мутационный анализ капсидного гена аденоассоциированного вируса типа 2 (AAV2) и конструирование векторов AAV2 с измененным тропизмом» . Журнал вирусологии . 74 (18): 8635–47. doi : 10.1128/JVI.74.18.8635-8647.2000 . ПМК 102071 . ПМИД 10954565 .
- ^ Манно К.С., Чу А.Дж., Хатчисон С., Ларсон П.Дж., Херцог Р.В., Арруда В.Р. и др. (апрель 2003 г.). «AAV-опосредованный перенос гена фактора IX в скелетные мышцы у пациентов с тяжелой гемофилией B» . Кровь . 101 (8): 2963–72. дои : 10.1182/кровь-2002-10-3296 . ПМИД 12515715 .
- ^ Рихтер М., Ивата А., Нюхейс Дж., Нитта Ю., Миллер А.Д., Халберт К.Л. и др. (апрель 2000 г.). «Аденоассоциированная вирусная векторная трансдукция гладкомышечных клеток сосудов in vivo». Физиологическая геномика . 2 (3): 117–27. doi : 10.1152/физиологгеномика.2000.2.3.117 . ПМИД 11015590 . S2CID 14150468 .
- ^ Кеберл Д.Д., Александр И.Е., Халберт К.Л., Рассел Д.В., Миллер А.Д. (февраль 1997 г.). «Постоянная экспрессия человеческого фактора свертывания крови IX в печени мышей после внутривенной инъекции векторов аденоассоциированного вируса» . Труды Национальной академии наук Соединенных Штатов Америки . 94 (4): 1426–31. Бибкод : 1997PNAS...94.1426K . дои : 10.1073/pnas.94.4.1426 . ЧВК 19807 . ПМИД 9037069 .
- ^ Цин К., Мах С., Хансен Дж., Чжоу С., Дварки В., Шривастава А. (январь 1999 г.). «Рецептор 1 фактора роста фибробластов человека является корецептором инфекции аденоассоциированным вирусом 2». Природная медицина . 5 (1): 71–7. дои : 10.1038/4758 . ПМИД 9883842 . S2CID 31602526 .
- ^ Саммерфорд С., Самульски Р.Дж. (февраль 1998 г.). «Мембранассоциированный протеогликан гепарансульфата является рецептором для вирионов аденоассоциированного вируса 2 типа» . Журнал вирусологии . 72 (2): 1438–45. doi : 10.1128/JVI.72.2.1438-1445.1998 . ПМК 124624 . ПМИД 9445046 .
- ^ Саммерфорд С., Бартлетт Дж.С., Самульски Р.Дж. (январь 1999 г.). «Интегрин AlphaVbeta5: корецептор аденоассоциированной вирусной инфекции типа 2». Природная медицина . 5 (1): 78–82. дои : 10.1038/4768 . ПМИД 9883843 . S2CID 23326070 .
- ^ Цю Дж., Ханда А., Кирби М., Браун К.Э. (март 2000 г.). «Взаимодействие гепаринсульфата и аденоассоциированного вируса 2» . Вирусология . 269 (1): 137–47. дои : 10.1006/виро.2000.0205 . ПМИД 10725206 .
- ^ Паюсола К., Гручала М., Йох Х., Люшер Т.Ф., Юля-Херттуала С., Бюелер Х. (ноябрь 2002 г.). «Специфические для типа клеток характеристики модулируют эффективность трансдукции аденоассоциированного вируса типа 2 и сдерживают инфицирование эндотелиальных клеток» . Журнал вирусологии . 76 (22): 11530–40. doi : 10.1128/JVI.76.22.11530-11540.2002 . ПМК 136795 . ПМИД 12388714 .
- ^ «Обычный вирус «убивает рак» » . CNN . 22 июня 2005 г. Проверено 5 августа 2009 г.
- ^ Пенн Стейт (23 июня 2005 г.). «Безобидный вирус убивает некоторые виды рака» . Наука Дейли.
- ^ Лимберис М.П., Ванденберге Л.Х., Чжан Л., Пиклз Р.Дж., Уилсон Дж.М. (февраль 2009 г.). «Эффективность трансдукции новых векторов AAV в эпителии дыхательных путей мыши in vivo и мерцательном эпителии дыхательных путей человека in vitro» . Молекулярная терапия . 17 (2): 294–301. дои : 10.1038/mt.2008.261 . ПМЦ 2835069 . ПМИД 19066597 .
- ^ Стробель Б., Дуекс М.Дж., Шмид Р., Штирсторфер Б.Е., Бухер Х., Кваст К. и др. (сентябрь 2015 г.). «Моделирование путей легочных заболеваний с использованием рекомбинантного аденоассоциированного вируса 6.2». Американский журнал респираторной клеточной и молекулярной биологии . 53 (3): 291–302. doi : 10.1165/rcmb.2014-0338MA . ПМИД 25845025 .
- ^ Гао Г.П., Альвира М.Р., Ван Л., Кальседо Р., Джонстон Дж., Уилсон Дж.М. (сентябрь 2002 г.). «Новые аденоассоциированные вирусы макак-резус как векторы для генной терапии человека» . Труды Национальной академии наук Соединенных Штатов Америки . 99 (18): 11854–9. Бибкод : 2002PNAS...9911854G . дои : 10.1073/pnas.182412299 . ПМК 129358 . ПМИД 12192090 .
- ^ Перейти обратно: а б Халберт К.Л., Аллен Дж.М., Миллер А.Д. (июль 2001 г.). «Векторы аденоассоциированного вируса типа 6 (AAV6) опосредуют эффективную трансдукцию эпителиальных клеток дыхательных путей в легких мышей по сравнению с векторами AAV2» . Журнал вирусологии . 75 (14): 6615–24. doi : 10.1128/JVI.75.14.6615-6624.2001 . ПМЦ 114385 . ПМИД 11413329 .
- ^ Перейти обратно: а б Рабиновиц Дж. Э., Боулз Д. Е., Фауст С. М., Ледфорд Дж. Г., Каннингем С. Е., Самульски Р. Дж. (май 2004 г.). «Перекрестное переодевание вириона: транскапсидация серотипов аденоассоциированных вирусов функционально определяет подгруппы» . Журнал вирусологии . 78 (9): 4421–32. doi : 10.1128/JVI.78.9.4421-4432.2004 . ПМЦ 387689 . ПМИД 15078923 .
- ^ Чен С., Каптурчак М., Лойлер С.А., Золотухин С., Глушакова О.Ю., Мадсен К.М. и др. (февраль 2005 г.). «Эффективная трансдукция сосудистых эндотелиальных клеток рекомбинантными аденоассоциированными вирусными векторами серотипов 1 и 5» . Генная терапия человека . 16 (2): 235–47. дои : 10.1089/hum.2005.16.235 . ПМЦ 1364465 . ПМИД 15761263 .
- ^ Ортински П.И., Донг Дж., Мунгенаст А., Юэ С., Такано Х., Уотсон DJ и др. (май 2010 г.). «Селективная индукция астроцитарного глиоза вызывает дефицит нейронального торможения» . Природная неврология . 13 (5): 584–91. дои : 10.1038/nn.2535 . ПМК 3225960 . ПМИД 20418874 .
- ^ Калудов Н., Браун К.Е., Уолтерс Р.В., Забнер Дж., Чиорини Дж.А. (август 2001 г.). «Аденоассоциированный вирус серотипа 4 (AAV4) и AAV5 требует связывания сиаловой кислоты для гемагглютинации и эффективной трансдукции, но различаются по специфичности связывания сиаловой кислоты» . Журнал вирусологии . 75 (15): 6884–93. doi : 10.1128/JVI.75.15.6884-6893.2001 . ПМК 114416 . ПМИД 11435568 .
- ^ Ди Паскуале Дж., Дэвидсон Б.Л., Стейн К.С., Мартинс И., Скудьеро Д., Монкс А. и др. (октябрь 2003 г.). «Идентификация PDGFR как рецептора трансдукции AAV-5» . Природная медицина . 9 (10): 1306–12. дои : 10.1038/нм929 . ПМИД 14502277 . S2CID 32547188 .
- ^ «Руководство по аденоассоциированным вирусам (AAV)» . Аддген . Уотертаун, Массачусетс.
- ^ Зинн Э., Пакуре С., Хайчук В., Турунен Х.Т., Карвалью Л.С., Андрес-Матеос Э. и др. (август 2015 г.). «In Silico реконструкция эволюционной линии вируса дает мощный вектор генной терапии» . Отчеты по ячейкам . 12 (6): 1056–68. дои : 10.1016/j.celrep.2015.07.019 . ПМЦ 4536165 . ПМИД 26235624 .
- ^ Флотт Т.Р., Бернс К.И. (апрель 2005 г.). «Адено-ассоциированный вирус: повсеместный комменсал млекопитающих». Генная терапия человека . 16 (4): 401–407. дои : 10.1089/hum.2005.16.401 . ПМИД 15871671 .
- ^ Ронзитти Дж., Гросс Д.А., Мингоцци Ф. (2020). «Иммунные реакции человека на векторы аденоассоциированного вируса (AAV)» . Границы в иммунологии . 11 : 670. дои : 10.3389/fimmu.2020.00670 . ПМЦ 7181373 . ПМИД 32362898 .
- ^ Вандамм К., Аджали О., Мингоцци Ф. (ноябрь 2017 г.). «Раскрытие сложной истории иммунных ответов на векторы AAV, испытание за испытанием» . Генная терапия человека . 28 (11): 1061–1074. дои : 10.1089/hum.2017.150 . ПМК 5649404 . ПМИД 28835127 .
- ^ Барнс С., Шайделер О., Шаффер Д. (декабрь 2019 г.). «Разработка капсида AAV для уклонения от иммунных реакций» . Современное мнение в области биотехнологии . 60 : 99–103. doi : 10.1016/j.copbio.2019.01.002 . ПМЦ 7117822 . ПМИД 30807882 .
- ^ Зайсс А.К., Лю Кью, Боуэн Г.П., Вонг Н.К., Бартлетт Дж.С., Муруве Д.А. (май 2002 г.). «Дифференциальная активация врожденных иммунных ответов аденовирусными и аденоассоциированными вирусными векторами» . Журнал вирусологии . 76 (9): 4580–90. doi : 10.1128/JVI.76.9.4580-4590.2002 . ПМК 155101 . ПМИД 11932423 .
- ^ Чжу Дж, Хуан Х, Ян Ю (август 2009 г.). «Путь TLR9-MyD88 имеет решающее значение для адаптивного иммунного ответа на векторы генной терапии аденоассоциированных вирусов у мышей» . Журнал клинических исследований . 119 (8): 2388–2398. дои : 10.1172/JCI37607 . ПМК 2719948 . ПМИД 19587448 .
- ^ Мартино А.Т., Сузуки М., Маркусик Д.М., Золотухин И., Риалс Р.К., Могими Б. и др. (июнь 2011 г.). «Геном самокомплементарных аденоассоциированных вирусных векторов усиливает Toll-подобный рецептор 9-зависимые врожденные иммунные реакции в печени» . Кровь . 117 (24): 6459–6468. дои : 10.1182/кровь-2010-10-314518 . ПМК 3123017 . ПМИД 21474674 .
- ^ Кальседо Р., Моризоно Х., Ван Л., МакКартер Р., Хе Дж., Джонс Д. и др. (сентябрь 2011 г.). «Профили антител к аденоассоциированному вирусу у новорожденных, детей и подростков» . Клиническая и вакциноиммунология . 18 (9): 1586–1588. дои : 10.1128/CVI.05107-11 . ПМК 3165215 . ПМИД 21775517 .
- ^ Це Л.В., Клинк К.А., Мэдиган В.Дж., Кастельянос Ривера Р.М., Уэллс Л.Ф., Хавлик Л.П. и др. (июнь 2017 г.). «Структурно-ориентированная эволюция антигенно различных вариантов аденоассоциированного вируса для уклонения от иммунитета» . Труды Национальной академии наук Соединенных Штатов Америки . 114 (24): Е4812–Е4821. Бибкод : 2017PNAS..114E4812T . дои : 10.1073/pnas.1704766114 . ПМК 5474820 . ПМИД 28559317 .
- ^ Перейти обратно: а б Заисс А.К., Муруве Д.А. (июнь 2005 г.). «Иммунные ответы на аденоассоциированные вирусные векторы». Современная генная терапия . 5 (3): 323–31. дои : 10.2174/1566523054065039 . ПМИД 15975009 .
- ^ Перейти обратно: а б с Мэдсен Д., Кантвелл Э.Р., О'Брайен Т., Джонсон П.А., Махон Б.П. (ноябрь 2009 г.). «Аденоассоциированный вирус серотипа 2 индуцирует клеточно-опосредованный иммунный ответ, направленный против множества эпитопов капсидного белка VP1» . Журнал общей вирусологии . 90 (Часть 11): 2622–33. дои : 10.1099/vir.0.014175-0 . ПМЦ 2885037 . ПМИД 19641045 .
- ^ Перейти обратно: а б Манно К.С., Пирс Г.Ф., Арруда В.Р., Глэйдер Б., Рагни М., Раско Дж.Дж. и др. (март 2006 г.). «Успешная трансдукция печени при гемофилии с помощью AAV-фактора IX и ограничения, налагаемые иммунным ответом хозяина». Природная медицина . 12 (3): 342–7. дои : 10.1038/nm1358 . ПМИД 16474400 . S2CID 14664182 .
- ^ Сабатино Д.Э., Мингоцци Ф., Хуэй Дж., Чен Х., Колози П., Эртл Х.К. и др. (декабрь 2005 г.). «Идентификация эпитопов CD8+ Т-клеток, специфичных для капсида AAV мыши» . Молекулярная терапия . 12 (6): 1023–33. дои : 10.1016/j.ymthe.2005.09.009 . ПМИД 16263332 .
- ^ Рор У.П., Кроненветт Р., Гримм Д., Кляйншмидт Дж., Хаас Р. (сентябрь 2002 г.). «Первичные клетки человека различаются по своей восприимчивости к переносу генов, опосредованному rAAV-2, и продолжительности экспрессии репортерного гена». Журнал вирусологических методов . 105 (2): 265–75. дои : 10.1016/S0166-0934(02)00117-9 . ПМИД 12270659 .
- ^ Перейти обратно: а б Мацусита Т., Эллигер С., Эллигер С., Подсакофф Г., Вильярреал Л., Курцман Г.Дж. и др. (июль 1998 г.). «Векторы аденоассоциированных вирусов можно эффективно получать без вируса-помощника» . Генная терапия . 5 (7): 938–45. дои : 10.1038/sj.gt.3300680 . ПМИД 9813665 .
- ^ Майерс М.В., Лафлин Калифорния, Джей Ф.Т., Картер Б.Дж. (июль 1980 г.). «Вспомогательная функция аденовируса для роста аденоассоциированного вируса: влияние чувствительных к температуре мутаций в области 2 раннего гена аденовируса» . Журнал вирусологии . 35 (1): 65–75. doi : 10.1128/JVI.35.1.65-75.1980 . ПМЦ 288783 . ПМИД 6251278 .
- ^ Ханда Х., Картер Б.Дж. (июль 1979 г.). «Комплексы репликации ДНК аденоассоциированного вируса в вирусе простого герпеса или клетках, инфицированных аденовирусом» . Журнал биологической химии . 254 (14): 6603–10. дои : 10.1016/S0021-9258(18)50411-7 . ПМИД 221504 .
- ^ Ялкиноглу А.О., Хайльбронн Р., Бюркле А., Шлехофер-младший, Цур Хаузен Х. (июнь 1988 г.). «Амплификация ДНК аденоассоциированного вируса как ответ на клеточный генотоксический стресс» . Исследования рака . 48 (11): 3123–9. ПМИД 2835153 .
- ^ Якобсон Б., Кох Т., Винокур Э. (апрель 1987 г.). «Репликация аденоассоциированного вируса в синхронизированных клетках без добавления вируса-помощника» . Журнал вирусологии . 61 (4): 972–81. doi : 10.1128/JVI.61.4.972-981.1987 . ПМК 254052 . ПМИД 3029431 .
- ^ Якобсон Б., Гринько Т.А., Пик М.Дж., Винокур Э. (март 1989 г.). «Репликация аденоассоциированного вируса в клетках, облученных УФ-светом с длиной волны 254 нм» . Журнал вирусологии . 63 (3): 1023–30. doi : 10.1128/JVI.63.3.1023-1030.1989 . ПМК 247794 . ПМИД 2536816 .
- ^ «Введение в аденоассоциированный вирус (AAV)» . Векторные биолаборатории . Малверн, Пенсильвания.
- ^ «Адено-ассоциированный вирус и адено-ассоциированные вирусные векторы» . Экологическая безопасность и гигиена . Университет Айовы. Архивировано из оригинала 20 сентября 2018 года . Проверено 19 сентября 2018 г.
- ^ Дуань Д., Шарма П., Ян Дж., Юэ Ю., Дудус Л., Чжан Ю. и др. (ноябрь 1998 г.). «Циркулярные промежуточные соединения рекомбинантного аденоассоциированного вируса имеют определенные структурные характеристики, ответственные за долгосрочную эписомальную персистенцию в мышечной ткани» . Журнал вирусологии . 72 (11): 8568–77. doi : 10.1128/JVI.72.11.8568-8577.1998 . ПМК 110267 . ПМИД 9765395 .
Внешние ссылки
[ редактировать ]- Кимбалл Дж.В. (17 мая 2015 г.). «Генная терапия II» . Страницы биологии Кимбалла . Архивировано из оригинала 18 марта 2005 года . Проверено 13 мая 2005 г.
- « Аденоассоциированный вирус » . Браузер таксономии NCBI . 272636.