Антинейтрофильное цитоплазматическое антитело

Антинейтрофильные цитоплазматические антитела АНЦА ) — группа аутоантител , преимущественно типа IgG , против антигенов в цитоплазме нейтрофилов ( (наиболее распространенный тип лейкоцитов ) и моноцитов . Они выявляются при анализе крови при ряде аутоиммунных заболеваний , но особенно связаны с системными васкулитами , так называемыми ANCA-ассоциированными васкулитами (AAV). [ 1 ]
Шаблоны ANCA IF
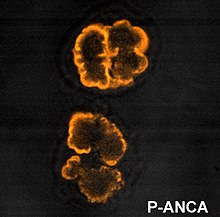
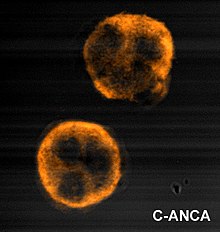
[ редактировать ]Иммунофлуоресценция (IF) нейтрофилов, фиксированных этанолом, используется для обнаружения ANCA, хотя нейтрофилы, фиксированные формалином, могут использоваться для дифференциации паттернов ANCA. ANCA можно разделить на четыре модели, если их визуализировать с помощью IF; цитоплазматическая ANCA (c-ANCA), C-ANCA (атипичная), перинуклеарная ANCA (p-ANCA) и атипичная ANCA (a-ANCA), также известная как x-ANCA. c-ANCA показывает цитоплазматическую гранулярную флуоресценцию с центральной междольковой акцентуацией. C-ANCA (атипичный) демонстрирует окрашивание цитоплазмы, которое обычно однородное и без междольковой акцентуации. p-ANCA имеет три подтипа: классический p-ANCA, p-ANCA без расширения ядра и гранулоцитарно-специфическое антинуклеарное антитело (GS-ANA). Классический p-ANCA показывает перинуклеарное окрашивание с расширением ядра, p-ANCA без расширения ядра имеет перинуклеарное окрашивание без расширения ядра, а GS-ANA показывает ядерное окрашивание только на гранулоцитах. a-ANCA часто демонстрирует сочетание цитоплазматического и перинуклеарного окрашивания. [ 2 ]
АНЦА-антигены
[ редактировать ]Антиген c-ANCA представляет собой протеиназу 3 (PR3). Антигены p-ANCA включают миелопероксидазу (МПО) и фактор, повышающий бактериальную проницаемость, бактерицидный/белок, повышающий проницаемость (BPI). Существуют и другие антигены c-ANCA (атипичные), однако многие из них пока неизвестны. Классический p-ANCA возникает при наличии антител, направленных к МПО. p-ANCA без ядерного расширения встречается с антителами к BPI, катепсину G , эластазе , лактоферрину и лизоциму . GS-ANA представляют собой антитела, направленные к специфическим ядерным антигенам гранулоцитов. Считается, что атипичные ANCA представляют собой антигены, аналогичные антигенам p-ANCA, однако они могут возникать из-за различий в процессинге нейтрофилов. [ 2 ]
Другие менее распространенные антигены включают HMG1 (паттерн p-ANCA), HMG2 (паттерн p-ANCA), альфа-енолазу (паттерн p и c-ANCA), каталазу (паттерн p и c-ANCA), бета-глюкуронидазу (паттерн p-ANCA). , азуроцидин (паттерн p и c-ANCA), актин (p и a-ANCA) и h-лампа-2 (c-ANCA). [ 2 ]
ИФА
[ редактировать ]Иммуноферментный анализ (ИФА) используется в диагностических лабораториях для выявления АНЦА. Хотя ИФ можно использовать для скрининга многих АНЦА, ИФА используется для выявления антител к отдельным антигенам. Наиболее распространенными антигенами, используемыми на микротитровальном планшете ELISA, являются MPO и PR3, которые обычно проверяются после положительного теста IF. [ 3 ]
Разработка
[ редактировать ]Малопонятно, как развиваются ANCA, хотя было предложено несколько гипотез. Вероятно, существует генетический вклад, особенно в генах, контролирующих уровень иммунного ответа – хотя генетическая восприимчивость, вероятно, будет связана с фактором окружающей среды, некоторыми возможными факторами, включая вакцинацию или воздействие силикатов. Постулируются два возможных механизма развития ANCA, хотя ни одна из этих теорий не отвечает на вопрос о том, как развиваются различные особенности ANCA, и по развитию ANCA все еще проводится много исследований. [ 4 ]
Теория молекулярной мимикрии
[ редактировать ]Микробные суперантигены — это молекулы, экспрессируемые бактериями и другими микроорганизмами, которые способны стимулировать сильный иммунный ответ путем активации Т-клеток . Эти молекулы обычно имеют области, напоминающие аутоантигены, которые способствуют остаточному аутоиммунному ответу – это теория молекулярной мимикрии. Стафилококковые и стрептококковые суперантигены были охарактеризованы при аутоиммунных заболеваниях – классический пример стрептококковой ревматической болезни сердца группы А , где существует сходство М-белков Streptococcus pyogenes с сердечным миозином и ламинином . Показано также, что до 70% больных гранулематозом с полиангиитом являются хроническими назальными носителями Staphylococcus aureus у носителей увеличивается в восемь раз , при этом риск рецидива . [ 4 ] Следовательно, это можно рассматривать как реакцию гиперчувствительности II типа . [ нужна ссылка ]
Теория дефектного апоптоза
[ редактировать ]нейтрофилов Апоптоз , или запрограммированная гибель клеток, имеет жизненно важное значение для контроля продолжительности ранней воспалительной реакции, тем самым ограничивая повреждение тканей нейтрофилами. ANCA может развиваться либо посредством неэффективного апоптоза, либо неэффективного удаления фрагментов апоптотических клеток, что приводит к воздействию на иммунную систему молекул, обычно секвестрированных внутри клеток. Эта теория решает парадокс того, как возможно образование антител против внутриклеточных антигенных мишеней ANCA. [ 4 ]
Роль в болезни
[ редактировать ]Ассоциации заболеваний
[ редактировать ]АНЦА связаны с васкулитами мелких сосудов, включая гранулематоз с полиангиитом , микроскопический полиангиит , первичный слабоиммунный некротический серповидный гломерулонефрит (тип микроскопического полиангиита, ограниченного почками), эозинофильный гранулематоз с полиангиитом и васкулиты, вызванные лекарственными препаратами. АНЦА-ассоциированные васкулиты (ААВ) имеют новые критерии классификации, обновленные в 2022 году. [ 5 ] [ 6 ] PR3-направленная c-ANCA присутствует в 80-90% гранулематоза с полиангиитом, в 20-40% микроскопического полиангиита, в 20-40% малоиммунного серповидного гломерулонефрита и в 35% эозинофильного гранулематоза с полиангиитом. c-ANCA (атипичный) присутствует в 80% случаев муковисцидоза (с BPI в качестве антигена-мишени), а также при воспалительных заболеваниях кишечника , первичном склерозирующем холангите и ревматоидном артрите (с антителами к множественным антигенным мишеням). p-АНЦА со специфичностью МПО обнаруживают в 50% микроскопических полиангиитов, в 50% первичного малоиммунного некротического серповидного гломерулонефрита и в 35% эозинофильного гранулематоза с полиангиитом. p-ANCA со специфичностью к другим антигенам связаны с воспалительными заболеваниями кишечника, ревматоидным артритом, лекарственным васкулитом, аутоиммунным заболеванием печени , лекарственными синдромами и паразитарными инфекциями. Атипичный ANCA связан с лекарственным системным васкулитом, воспалительными заболеваниями кишечника и ревматоидным артритом. [ 3 ] [ 7 ] Частота ANCA-положительных результатов значительно выше у пациентов с сахарным диабетом 1 типа, чем у здоровых людей. [ 8 ]
Левамизол , который является распространенной примесью кокаина , может вызвать ANCA-положительный васкулит. [ 9 ]
Наличие или отсутствие ANCA не может указывать на наличие или отсутствие заболевания, и результаты коррелируют с клиническими особенностями. Связь ANCA и активности заболевания остается спорной; однако повторное появление ANCA после лечения может указывать на рецидив. [ 10 ] [ 11 ]
Патогенез
[ редактировать ]Хотя патогенная роль ANCA все еще остается спорной, модели in vitro и на животных подтверждают идею о том, что антитела играют прямую патологическую роль в формировании васкулитов мелких сосудов. ANCA, специфичные для MPO и PR3, могут активировать нейтрофилы и моноциты через их рецепторы Fc и Fab'2, что может усиливаться цитокинами , которые заставляют нейтрофилы отображать MPO и PR3 на своей поверхности. Аберрантное гликозилирование специфичных для MPO и PR3 ANCA усиливает их способность взаимодействовать с активирующими Fc-рецепторами на нейтрофилах. [ 12 ] Активированные нейтрофилы могут затем прикрепляться к эндотелиальным клеткам , где происходит дегрануляция. При этом высвобождаются свободные радикалы кислорода и литические ферменты, что приводит к повреждению эндотелия посредством индукции некроза и апоптоза . Кроме того, нейтрофилы высвобождают хемоаттрактивные сигнальные молекулы, которые привлекают больше нейтрофилов к эндотелию, действуя как петля положительной обратной связи. Модели на животных показали, что антитела к МПО могут вызывать некротический серповидный гломерулонефрит и системный васкулит мелких сосудов. В этих животных моделях формирование гломерулонефрита и васкулита может происходить в отсутствие Т-клеток, однако нейтрофилы должны присутствовать. [ 13 ] [ 14 ] [ 15 ] [ 16 ] Хотя было отмечено, что титры ANCA имеют ограниченную корреляцию с активностью заболевания, за исключением заболеваний почек, и с риском рецидива, это объясняется различиями в эпитопах и сродстве ANCA. [ 17 ] ANCA вызывают избыточную активацию нейтрофилов , что приводит к образованию нейтрофильных внеклеточных ловушек (NET), которые вызывают повреждение мелких кровеносных сосудов. [ 17 ] Кроме того, у пациентов с активным заболеванием, получающих ритуксимаб , антитело против CD20 , которое удаляет циркулирующие В-клетки, клиническая ремиссия больше коррелирует со снижением количества циркулирующих В-клеток, чем со снижением титра ANCA, что у некоторых пациентов не происходит. изменения во время лечения. В том же исследовании было обнаружено, что клинический рецидив у некоторых пациентов был связан с возвращением циркулирующих B-клеток. [ 18 ] На основании вышеизложенных наблюдений и того, что ANCA-реактивные B-клетки могут быть обнаружены в кровообращении у пациентов с AAV, была предложена альтернативная гипотеза, предполагающая прямую патогенную роль этих клеток, при которой активированные нейтрофилы и ANCA-реактивные B-клетки участвуют в межклеточных процессах. перекрестные помехи, которые приводят не только к дегрануляции и воспалению нейтрофилов, но также к пролиферации и дифференцировке ANCA-реактивных B-клеток. [ 19 ] Однако эту гипотезу еще предстоит проверить.
Уход
[ редактировать ]Авакопан был одобрен для медицинского применения в США для лечения васкулита, связанного с антинейтрофильными цитоплазматическими аутоантителами, в октябре 2021 года. [ 20 ]
История
[ редактировать ]ANCA были первоначально описаны Davies et al. в 1982 году при сегментарно-некротическом гломерулонефрите . [ 17 ] [ 21 ] Второй международный семинар ANCA, состоявшийся в Нидерландах в мае 1989 года, зафиксировал номенклатуру перинуклеарных и цитоплазматических паттернов, а антигены MPO и PR3 были открыты в 1988 и 1989 годах соответственно. [ 22 ] Международные семинары ANCA проводятся каждые два года. [ нужна ссылка ]
Ссылки
[ редактировать ]- ^ Шарма П., Зонози Р., Гита Д. ANCA-ассоциированный васкулит. Adv Почки Dis Health. Май 2024 г.;31(3):194–205. doi: 10.1053/j.akdh.2024.04.005. PMID: 39004459.
- ^ Jump up to: а б с Мид А.Р. Брэдвелл, Р.П. Стоукс, врач общей практики (1999). Расширенный атлас структуры аутоантител . Бирмингем: Связующее место. ISBN 978-0-7044-8510-5 .
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Jump up to: а б Сэвидж Дж., Дэвис Д., Фальк Р.Дж., Дженнетт Дж.К., Вийк А. (март 2000 г.). «Антинейтрофильные цитоплазматические антитела и ассоциированные заболевания: обзор клинических и лабораторных особенностей» . Почки Интернешнл . 57 (3): 846–62. дои : 10.1046/j.1523-1755.2000.057003846.x . ПМИД 10720938 . S2CID 14521707 .
- ^ Jump up to: а б с Ремо Д., Дютийёль П., Роос Д. (2004). «Патогенез заболеваний, связанных с аутоантителами антинейтрофильной цитоплазмы». Хум Иммунол . 65 (1): 1–12. дои : 10.1016/j.humimm.2003.09.013 . ПМИД 14700590 .
- ^ Робсон Джей Си (2022). «Критерии классификации гранулематоза с полиангиитом Американского колледжа ревматологии/Европейского альянса ревматологических ассоциаций 2022 года» . Анналы ревматических болезней . 81 (3): 315–320. doi : 10.1136/annrheumdis-2021-221795 . hdl : 1983/ba2d3ba8-c9a1-4606-a765-459e1eb54e36 . ПМИД 35110333 . Проверено 27 сентября 2023 г.
- ^ Суппиа Р., Робсон Дж.К., Грейсон П.С., Понте С., Крэйвен А., Халид С. и др. (2022). «Критерии классификации микроскопического полиангиита Американского колледжа ревматологии/Европейского альянса ревматологических ассоциаций 2022 года» . Анналы ревматических болезней . 81 (3): 321–326. doi : 10.1136/annrheumdis-2021-221796 . hdl : 1983/129ff4b5-ffde-474d-abc0-339895d912d9 . ПМИД 35110332 .
- ^ Боссайт X (февраль 2006 г.). «Серологические маркеры воспалительных заболеваний кишечника» . Клиническая химия . 52 (2): 171–81. дои : 10.1373/clinchem.2005.058560 . ПМИД 16339302 .
- ^ Омура Т. (сентябрь 2019 г.). «Самый старый пациент с диабетом 1 типа, получающий лечение инсулиновой помпой с положительным осложнением на миелопероксидазу-антинейтрофильные цитоплазматические антитела: отчет о случае». Международная гериатрия и геронтология . 19 (9): 957–58. дои : 10.1111/ggi.13683 . ПМИД 31490005 . S2CID 201845957 .
- ^ Тран Х., Тан Д., Марнехон Т.П. (февраль 2013 г.). «Кожная васкулопатия, связанная с кокаином, фальсифицированным левамизолом» . Клиническая медицина и исследования . 11 (1): 26–30. дои : 10.3121/cmr.2012.1085 . ПМК 3573092 . ПМИД 22723468 .
- ^ Синклер Д., Стивенс Дж. М. (сентябрь 2007 г.). «Роль антинейтрофильных цитоплазматических антител и антител к базальной мембране клубочков в диагностике и мониторинге системных васкулитов». Анналы клинической биохимии . 44 (Часть 5): 432–42. дои : 10.1258/000456307781646049 . ПМИД 17761028 . S2CID 28849057 .
- ^ Стегеман, Калифорния (ноябрь 2005 г.). «Прогностическая ценность антинейтрофильных цитоплазматических антител при васкулите мелких сосудов: стакан наполовину полон или наполовину пуст?». Журнал ревматологии . 32 (11): 2075–7. ПМИД 16265681 .
- ^ Маверакис Э., Ким К., Шимода М., Гершвин М., Патель Ф., Уилкен Р. и др. (2015). «Гликаны в иммунной системе и теория аутоиммунитета с измененными гликанами» . Дж. Аутоиммун . 57 (6): 1–13. дои : 10.1016/j.jaut.2014.12.002 . ПМЦ 4340844 . ПМИД 25578468 .
- ^ Фальк Р.Дж., Дженнетт, Дж.К. (май 2010 г.). «Болезнь ANCA: куда движется эта область?» . Журнал Американского общества нефрологов . 21 (5): 745–52. дои : 10.1681/ASN.2009121238 . ПМИД 20395376 .
- ^ Со П., Стоун, Дж. Х. (1 июля 2004 г.). «Васкулиты, связанные с антинейтрофильными цитоплазматическими антителами». Американский медицинский журнал . 117 (1): 39–50. doi : 10.1016/j.amjmed.2004.02.030 . ПМИД 15210387 .
- ^ Дженнетт Дж.С., Сяо Х., Фальк Р.Дж. (май 2006 г.). «Патогенез сосудистого воспаления антинейтрофильными цитоплазматическими антителами» . Журнал Американского общества нефрологов . 17 (5): 1235–42. дои : 10.1681/ASN.2005101048 . ПМИД 16624929 .
- ^ Фальк Р.Дж. , Террелл Р.С., Чарльз Л.А., Дженнетт Дж.К. (1990). «Антинейтрофильные цитоплазматические аутоантитела вызывают дегрануляцию нейтрофилов и выработку кислородных радикалов in vitro» . Proc Natl Acad Sci США . 87 (11): 4115–4119. Бибкод : 1990PNAS...87.4115F . дои : 10.1073/pnas.87.11.4115 . ПМК 54058 . ПМИД 2161532 .
- ^ Jump up to: а б с Наказава Д., Масуда С., Томару У., Исидзу А. (февраль 2019 г.). «Патогенез и терапевтические вмешательства при ANCA-ассоциированном васкулите» (PDF) . Обзоры природы Ревматология . 15 (2): 91–101. дои : 10.1038/s41584-018-0145-y . hdl : 2115/74654 . ПМИД 30542206 . S2CID 54474335 .
- ^ Джейн Д.Р.-младший, Ферраро А.Дж., Чаудри А.Н., Броган П., Салама А.Д., Смит К.Г. и др. (01 июля 2009 г.). «Многоцентровое исследование терапии ритуксимабом рефрактерного васкулита, связанного с антинейтрофильными цитоплазматическими антителами». Ревмирующий артрит . 60 (7): 2156–68. дои : 10.1002/арт.24637 . ПМИД 19565480 .
- ^ Уртадо П., Нитшке Дж., Уртадо-Перес Э., Пе К. (апрель 2013 г.). «ANCA-реактивные B-клетки и нейтрофилы взаимодействуют в патогенезе AAV: модельное предложение». Ла Пресс Медицинский . 42 (4 Часть 2): 720. doi : 10.1016/j.lpm.2013.02.256 .
- ^ «ChemoCentryx объявляет об одобрении FDA тавнеоса (авакопана) при ANCA-ассоциированном васкулите» . ChemoCentryx, Inc. (Пресс-релиз). 8 октября 2021 года. Архивировано из оригинала 8 октября 2021 года . Проверено 11 октября 2021 г.
- ^ Дэвис DJ, Моран, Дж. Э., Найл, Дж. Ф., Райан, Великобритания (28 августа – 4 сентября 1982 г.). «Сегментарно-некротизирующий гломерулонефрит с антинейтрофильными антителами: возможная арбовирусная этиология?» . Британский медицинский журнал (под ред. Клинических исследований) . 285 (6342): 606. дои : 10.1136/bmj.285.6342.606 . ПМЦ 1499415 . ПМИД 6297657 .
- ^ Дженнетт Дж.С., Хойдал-младший, Фальк Р.Дж. (1 июня 1990 г.). «Специфичность антинейтрофильных цитоплазматических аутоантител к протеиназе 3» . Кровь . 75 (11): 2263–4. дои : 10.1182/blood.V75.11.2263.2263 . ПМИД 2189509 .
Внешние ссылки
[ редактировать ]- изображения pANCA и cANCA, заархивированные 27 сентября 2012 г. на Wayback Machine.
- флуоресцентные изображения ANCA, заархивированные 26 марта 2007 г. в Wayback Machine.
- Антинейтрофильные + цитоплазматические + антитела Национальной медицинской библиотеки США в медицинских предметных рубриках (MeSH)