Вирусные квазивиды
Вирусный квазивид — это структура вирусов популяционная с большим количеством вариантов геномов (связанных мутациями). Квазивиды возникают в результате высокой частоты мутаций , поскольку мутанты возникают постоянно, а их относительная частота меняется по мере вируса репликации и отбора . [1]
Теория предсказывает, что вирусный квазивид, находящийся на низком, но эволюционно нейтральном и сильно связанном (то есть плоском) участке ландшафта приспособленности, вытеснит квазивид, находящийся на более высоком, но более узком пике приспособленности, к которому окружающие мутанты непригодны. [2] [3] Это явление получило название «квазивидовой эффект» или, с недавних пор, «выживание самых плоских». [4]
Термин «квазивид» был заимствован из теории происхождения жизни , в которой примитивные репликоны состояли из мутантных дистрибутивов, как это было обнаружено экспериментально на современных РНК-вирусах внутри их хозяина . [5] [6] Теория предоставила новое определение дикого типа при описании вирусов и концептуальную основу для более глубокого понимания адаптивного потенциала РНК-вирусов, чем это предлагается классическими исследованиями, основанными на упрощенных консенсусных последовательностях . [1]
Модель квазивидов наиболее применима, когда размер генома ограничен и частота мутаций высока, и поэтому она наиболее актуальна для РНК-вирусов (включая важные патогены ), поскольку они имеют высокую частоту мутаций (приблизительно одна ошибка на раунд репликации) . [7] хотя эти концепции могут применяться и к другим биологическим объектам, таким как вирусы ДНК с обратной транскрипцией, такие как гепатит B. [8] В таких сценариях сложное распределение близкородственных вариантов геномов подвергается генетическим вариациям , конкуренции и отбору и может выступать в качестве единицы отбора . Следовательно, эволюционную траекторию вирусной инфекции нельзя предсказать исключительно на основе характеристик наиболее подходящей последовательности. Высокая частота мутаций также устанавливает верхний предел , совместимый с наследственной информацией. Превышение такого предела приводит к вымиранию РНК-вируса , переходу, который лежит в основе противовирусной конструкции, называемой летальным мутагенезом , и имеет отношение к противовирусной медицине. [1]
Актуальность квазивидов в вирусологии стала предметом обширных дискуссий. Однако стандартные клональные анализы и методологии глубокого секвенирования подтвердили наличие множества мутантных геномов в вирусных популяциях и их участие в адаптивных процессах . [1]
История
[ редактировать ]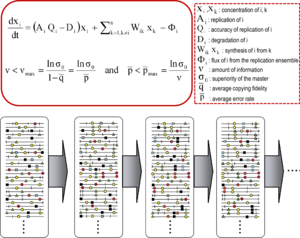
Теория квазивидов была разработана в 1970-х годах Манфредом Эйгеном и Питером Шустером для объяснения самоорганизации и адаптивности примитивных репликонов (термин, используемый для обозначения любого реплицирующегося объекта) как ингредиента гиперциклических организаций, связывающих генотипическую и фенотипическую информацию, как важный шаг в зарождении жизни. [11] [9] Теория изображала ранние популяции репликонов как организованные мутантные спектры, в которых доминирует мастер-последовательность, наделенная наивысшей приспособленностью (репликативной способностью) в распределении. Он ввел понятие мутантного ансамбля как единицы отбора, тем самым подчеркнув значимость внутрипопуляционных взаимодействий для понимания реакции на селективные ограничения . Одним из его следствий является соотношение порога ошибки , которое отмечает максимальную частоту мутаций, при которой мастер-(или доминантная) последовательность может стабилизировать мутантный ансамбль. Нарушение порога ошибки приводит к потере доминирования мастер-последовательности и дрейфу популяции в пространстве последовательностей . [9] [12] [13] [14]
Основные концепции квазивидов описываются двумя фундаментальными уравнениями: репликацией с созданием ошибочных копий и соотношением порога ошибки. Они отражают две основные особенности РНК-вирусов на популяционном уровне: наличие мутантного спектра и неблагоприятное влияние увеличения частоты мутаций на выживаемость вируса, каждая из которых имеет несколько производных. [1]
Существование мутантного спектра было сначала подтверждено экспериментально с помощью клонального анализа популяций РНК-бактериофага Qβ, репликация которых была инициирована одной вирусной частицей. Отдельные геномы отличались от консенсусной последовательности в среднем от одной до двух мутаций на отдельный геном. [15] Приспособленность биологических клонов была хуже, чем у родительской неклонированной популяции; разница также зафиксирована для вируса везикулярного стоматита (ВВС). [16] Репликативная способность популяционного ансамбля не обязательно должна совпадать со способностью его отдельных компонентов. Открытие того, что вирусная популяция представляет собой, по сути, пул мутантов, было сделано в то время, когда мутации в общей генетике считались редкими событиями, и вирусологи связывали вирусный геном с определенной нуклеотидной последовательностью , что до сих пор подразумевается в содержимом банков данных . [17] Облачная природа Qβ была понята как следствие его высокой частоты мутаций, рассчитанной за 10 лет. −4 мутации, вносимые на каждый копируемый нуклеотид, [18] вместе с толерантностью отдельных геномов к принятию неопределенной доли вновь возникающих мутаций, несмотря на затраты на приспособленность. Уровень ошибок, рассчитанный для бактериофага Qβ, был подтвержден и сопоставим со значениями, рассчитанными для других РНК-вирусов. [7] [19]
Высокие уровни мутаций и квазивиды были подтверждены для других РНК-вирусов на основе анализа вирусных популяций путем молекулярного или биологического клонирования и анализа последовательностей отдельных клонов. Джон Холланд и его коллеги были первыми, кто осознал, что быстро развивающийся мир РНК, внедренный в биосферу, основанную на ДНК, имеет множество эволюционных и медицинских последствий. [1] [16] [20] [21] [22] О пластичности генома РНК-вирусов подозревали многие десятилетия. Ключевыми ранними наблюдениями были вариации вирусных признаков, описанные Финдли в 1930-х годах, исследования Граноффа по изменениям бляшек морфологии вируса болезни Ньюкасла или высокая частота конверсий между лекарственной устойчивостью и зависимостью у вируса Коксаки А9 , а также другие исследования на животных. и вирусы растений в середине 20 века. [23] Если рассматривать их в контексте современных знаний, мы понимаем, что эти наблюдения фенотипических изменений были верхушкой айсберга чрезвычайно сложной реальности вирусных популяций. Высокая частота мутаций и гетерогенность популяции характеризуют РНК-вирусы, что имеет последствия для вирусного патогенеза и контроля вирусных заболеваний. Детальные исследования квазивидовой динамики in vivo были проведены с вирусом иммунодефицита человека типа 1 (ВИЧ-1) и вирусом гепатита С. [10] [24] [25]
Текущий объем
[ редактировать ]Первая математическая формулировка квазивидов была детерминистской; он предполагал устойчивое распределение мутантов в генетическом равновесии без возмущений, вызванных модификациями окружающей среды или размера популяции . [26] Эти условия часто встречаются в первоначальных теоретических формулировках сложных явлений, поскольку они обеспечивают математическую управляемость. С тех пор было разработано несколько расширений теории на неравновесные условия со стохастическими компонентами с целью найти общие решения для многопиковых ландшафтов приспособленности . Эти цели приближают квазивиды к реальному случаю РНК-вирусов, которые вынуждены иметь дело с резкими различиями в размерах популяций и окружающей среде. [27] Исследования квазивидов проводились по нескольким теоретическим и экспериментальным направлениям, включая продолжающиеся исследования эволюционной оптимизации и происхождения жизни, взаимодействий РНК-РНК и сетей репликаторов, порога ошибки в изменяющихся ландшафтах приспособленности, рассмотрение механизмов химического мутагенеза и корректуры, эволюции опухолевые клетки , бактериальные популяции или стволовые клетки , хромосомная нестабильность , устойчивость к лекарствам и распределение конформаций в прионах (класс белков с конформационно-зависимым патогенным потенциалом; в этом случае квазивид определяется распределением конформаций). [10] [28] Новые данные в экспериментальные исследования квазивидов были внесены благодаря глубокому секвенированию для исследования вирусных и клеточных популяций, распознаванию взаимодействий в пределах мутантного спектра, моделям динамики вирусных популяций, связанных с прогрессированием заболевания и передачей патогенов, а также новым знаниям, основанным на верных вариантах вирусов. [28] Здесь мы суммируем основные аспекты динамики квазивидов и недавние разработки, имеющие отношение к эволюции и патогенезу вирусов.
Динамическая неоднородность
[ редактировать ]Молекулярной основой высокой частоты ошибок является ограниченная точность копирования матрицы РНК-зависимыми РНК-полимеразами (RdRps) и РНК-зависимыми ДНК-полимеразами (также называемыми обратными транскриптазами, RT). Кроме того, эти ферменты дефектны в корректуре. [29] домен от 3' до 5', потому что у них отсутствует экзонуклеазный присутствующий в репликативных клеточных ДНК-полимеразах. [30] Кроме того, пути пострепликативной репарации, которые широко используются для коррекции генетических повреждений при репликации клеточной ДНК, оказываются неэффективными для двухцепочечных РНК или гибридов РНК-ДНК. Наличие корректорско-восстановительной активности у коронавирусов повышает точность их копирования примерно в 15 раз. [31] Эта и другие действия по восстановлению, которые могут воздействовать на стандартные РНК или ретровирусные геномы, [32] [33] [34] [35] не препятствуют образованию мутантных спектров, хотя их амплитуда может быть ниже, чем у других РНК-вирусов, по крайней мере, в популяциях, близких к клональному (одногеномному) происхождению. Динамика квазивидов будет действовать в любой вирусной или клеточной системе, в которой из-за высокой скорости мутаций (в результате полимераз нуклеиновых кислот низкой точности или изменений окружающей среды) быстро генерируются мутантные спектры. [10] [36] [37] [38] [39] [40]
Исследования различных систем вирус-хозяин позволили установить некоторые общие наблюдения о механизмах образования мутантов и последствиях динамики квазивидов. [10] [41] [42] [43] [44] [45] [46] [47] [48] [49] [50] В генетике РНК-вирусов, когда мы говорим о «мутанте», мы имеем дело с облаком мутантов, в котором конкретная мутация, на которую мы обращаем наше внимание, присутствует во всех (или в подавляющем большинстве) индивидуальных геномах. Не существует такого понятия, как вирус дикого типа или вирус-мутант. Это всегда тучи мутантов. Изменения относительного доминирования компонентов мутантного спектра особенно выражены при in vivo инфекциях , со сложной динамикой внутрихозяинной гетерогенности и вариаций. биоинформационные Были разработаны анализ могут предполагать некоторый иерархический порядок приобретения мутаций или идентификации кластеров передачи (примеры : разделов квазивидов процедуры для раскрытия связей между различными, но тесно связанными типами генома, которые , PAQ [51] или QU asispecies Evolution , , основе сети передаче на вывод о QUENTIN [52] ).
Фенотипические резервуары
[ редактировать ]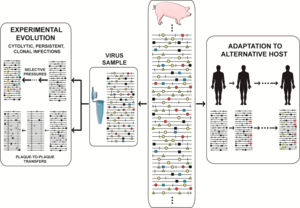
Суть вопроса о квазивидовых последствиях заключается в том, что в любой момент времени вирусная популяция включает в себя резервуар не только генотипических , но и фенотипических вариантов, наделяющих популяцию некоторой адаптивной плюрипотентностью . Накопление лабораторных и клинических данных делает несостоятельным утверждение о том, что меньшинства компонентов мутантного спектра следует отбрасывать на том основании, что они нейтральны . Они могут участвовать в избирательных процессах и не могут быть исключены из интерпретации поведения вируса. Вариации повсеместно включают точечные мутации , а также могут включать рекомбинацию (в ее репликативном и нерепликативном режимах) и реассортацию сегментов генома . [42] Все способы молекулярных вариаций совместимы, но ограничены только объемом механизмов, доступных репликативному аппарату, и необходимостью сохранения функциональности вирусных геномов. Дэвид Эванс и его коллеги выявили множество событий рекомбинации, связанных с репликацией энтеровируса , и лишь немногим рекомбинантам удалось продолжить репликацию. [53] Рекомбинация может опосредовать адаптивность и вирулентность . [54] Высокие уровни мутаций и рекомбинаций привели к концептуальному различию между механически неизбежными и эволюционно значимыми вариациями в связи с проблемой клональной и неклональной природы эволюции вируса (микробной эволюции в целом). [55] [56] Только незначительная часть возникающих во время репликации вариаций может быть успешно размножена. В пределах, установленных биологическими ограничениями , каждая популяция состоит из множества вариантов геномов, общее количество которых соизмеримо с размером популяции вируса. Заразить растение, животное или культуру клеток 10 3 инфекционные единицы могут иметь совсем другие последствия, чем заражение 10 10 инфекционные единицы не только потому, что защитные системы хозяина могут быть подавлены высокой инфекционной дозой, но и потому, что репертуар мутантов, участвующих в адаптивных исследованиях, шире. Часть вариантов мутантного спектра, изолированно или в консорциуме с другими, [57] могут работать лучше, чем другие члены той же популяции, в случае изменения окружающей среды. Избирательное давление благоприятствует репликации одних компонентов мутантного спектра по сравнению с другими, несмотря на то, что все они связаны между собой мутациями. Дифференциальная эффективность может быть на уровне вирусных геномов (при репликации, внутриклеточной экспрессии генов , взаимодействии с факторами хозяина и т. д.) или вирусных частиц (по термостабильности, входу в клетки или выходу из них, устойчивости к нейтрализующим антителам и т. д.). [22] [10] [23] [24] [25] [42] [43] [44] Адаптивность РНК-вирусов связана с параметрами, которые облегчают исследование пространства последовательностей: размер генома (от 1,8 до 33 КБ), размер популяции (переменный, но может достигать впечатляющих 10 КБ). 12 отдельных геномов инфицированного хозяина в данный момент времени), скорость репликации, скорость мутаций, плодовитость (выход вирусных частиц на клетку) и количество мутаций, необходимых для фенотипического изменения (на удивление низкое для некоторых важных признаков). [58] ).
Динамика мутантного спектра изображалась по-разному, и мы выбрали тот, который охватывает частые события в природных популяциях и дизайне исследований, такие как изоляция вируса от инфицированного хозяина, адаптация к клеточной культуре для изучения экспериментальной эволюции или адаптация к альтернативным хозяевам. в естественных условиях. Реальность еще более сложна, учитывая большие размеры популяции, с неопределенной долей геномов, активно реплицирующихся в любой момент времени (иногда приравнивается к эффективному размеру популяции в общей генетике) и содержащим множество мутаций на геном. Сценарии, предлагаемые современными экспериментальными данными, бросают вызов нашему воображению. Относительная частота отдельных мутаций колеблется в ходе непрерывного исследования пространства последовательностей. [59] [60] [10] при этом фенотипические изменения (не только генотипические) происходят гораздо чаще, чем считалось ранее. План экспериментальной эволюции , заключающийся в передаче вирусных популяций в течение длительных периодов времени (множество последовательных инфекций), часто бывает чрезвычайно показательным. В случае вируса ящура (Ящур) такой дизайн привел к заметной фенотипической диверсификации на субпопуляции колонизаторов и конкурентов, что модулировало вирулентность мутантного ансамбля. [61] В случае с вирусом гепатита С такой дизайн позволил выявить непрерывные волны мутаций и более точное понимание типов фитнес-ландшафтов, занимаемых вирусами с высокой приспособленностью. [60] [62]
Ограничения и неопределенности
[ редактировать ]Нуклеотидная последовательность отдельного генома из популяции (независимо от степени сложности популяции) может быть определена либо в результате биологического или молекулярного клонирования, либо путем глубокого секвенирования целых вирусных геномов таким образом, чтобы установить связь мутаций ( можно установить отнесение разных мутаций к одной и той же молекуле генома). Каждая из этих процедур подразумевает некоторые ограничения: биологическое клонирование может исказить представление в пользу инфекционных геномов, тогда как молекулярное клонирование может ввести в анализ неинфекционные (дефектные) геномы. [22] [58] [59] Полногеномное описание квазивидов по-прежнему технически сложно из-за искусственного введения мутаций. Большинство современных платформ глубокого секвенирования дают последовательности коротких прочтений для данного ампликона (анализируемой последовательности); миноритарные мутации в ампликоне не могут быть надежно связаны с мутациями в другом ампликоне того же генома; самое большее, можно предложить статистические выводы о связи. Несмотря на эти ограничения, контрольные эксперименты и усовершенствования биоинформатических процедур подтверждают, что большая часть гетерогенности последовательностей, проанализированной в вирусных популяциях, действительно отражает различия в природных матричных популяциях. Если связь мутаций можно будет решить в рутинном порядке, на сцену выйдет новая волна молекулярной информации, имеющей отношение к эпистатическим взаимодействиям.
Существуют дополнительные уровни неопределенности при последовательном анализе вирусных популяций, особенно тех, которые реплицируются in vivo. Компоненты мутантного спектра, представленные в данный момент в образце, взятом для секвенирования, могут отличаться от таковых в следующий момент времени либо из-за неопределенностей выборки, либо из-за реальных колебаний частот генома. Неоправданно принимать грубое сходство, поскольку даже одна мутация в данном контексте последовательности может повлиять на биологические свойства. [10] По словам Джона Холланда и его коллег: «Важно помнить, что каждый рой квазивидовых геномов у инфицированного человека уникален и «нов» в том смысле, что ни одна идентичная популяция геномов никогда раньше не существовала, и ни одна такая никогда не будет существовать снова. ". [63] Несмотря на мимолетный характер любого распространения мутантов, стандартные методы, доступные для характеристики квазивидов, позволяют получить геномные последовательности меньшинства популяции (по оценкам, в 10 −8 до 10 −13 для молекулярного клонирования-секвенирования по Сэнгеру и в 10 −6 до 10 −11 для глубокого секвенирования). [58] Мы можем иметь лишь приблизительное представление о вирусных популяциях и их динамике, о чем свидетельствуют многие экспериментальные исследования. [15] [20] [10] [43] [44] [58] [60] [64]
Дескрипторы, не основанные на консенсусе
[ редактировать ]Тезисы, изложенные в предыдущих разделах, полностью оправдывают обращение к аналитическим инструментам спектра мутантов, а не их игнорирование или рассмотрение его присутствия как второстепенную проблему. Использование консенсусных последовательностей для описания генома изолята вируса, несмотря на то, что оно оправдано трудностями передачи информации, обобщенной в мутантном спектре, размывает и ослабляет биологические интерпретации. Экспериментальные результаты показали, что миноритарные геномы из мутантного спектра (которые не могут быть идентифицированы путем изучения консенсусной последовательности) могут включать мутации, которые придают устойчивость к противовирусным ингибиторам , нейтрализующим антителам или цитотоксическим Т-клеткам или могут изменять способность индуцировать интерферон (ИФН). ) или реагировать на ИФН, вирулентность или стабильность частиц, среди других фенотипических признаков. [10] [42] [46] [60] [64] [65] [66] [67] Мутантные спектры также могут опосредовать циклическую адаптацию к различным типам клеток. [41] Мутантный спектр определяет консенсус, но консенсус — это абстракция; оно может быть не представлено среди населения. Многие события в вирусном патогенезе и эволюции происходят из-за модификаций или взаимодействий мутантного спектра, которые нельзя правильно интерпретировать исключительно на основе консенсусных последовательностей. [15] [10] [22] [23] [28] [41] [40] [43] [44] [53] [54] [57] [60] [63]
Коллективный ответ
[ редактировать ]Спектры мутантов — это не просто совокупность мутантов, действующих независимо. Они часто участвуют в коллективных ответах. [1] Двумя основными типами являются те, которые зависят от присутствия наборов вариантов, и те, которые полагаются на взаимодействия внутримутантного спектра.
Варианты, которые стимулируют реакцию на выборочные ограничения
[ редактировать ]Поведение реконструированных квазивидов
[ редактировать ]В некоторых случаях радикального отбора (очень сильный отбор по признаку) особь (или ограниченное число особей), кодирующая сигнатуры, склонные к отбору, может приблизиться к доминированию, став при этом основателем мутантного облака (поскольку формирование облака свойственна репликации). Условия доминирования (в данном случае в ответ на отбор) заключаются в том, что геном ощущает избирательный охват и разрешена его репликация в новой селективной среде. В остальных случаях отбирают коллекцию мутантов. Это было проиллюстрировано на примере квазивида вируса ящура, который был реконструирован в лаборатории с множеством антигенных вариантов (каждый с низкой частотой), которые принадлежали к двум различным категориям и имели общую устойчивость к одному и тому же моноклональному антителу . [68] Одна категория включала мутанты с аминокислотной заменой, которая влияла на узнавание рецептора (поскольку антигенная детерминанта перекрывалась с сайтом узнавания рецептора интегрина ); в другой категории замены затрагивали антигенную детерминанту, но не сайт узнавания рецептора. Пассажи вируса в отсутствие моноклональных антител приводили к доминированию антигенных вариантов, которые сохраняли способность распознавания рецепторов, но доминантные варианты были окружены облаком мутантов другой категории антигенных вариантов. И наоборот, пассажи в присутствии антитела привели к отбору вариантов с измененным распознаванием рецептора, окруженных облаком антигенных вариантов, которые поддерживали распознавание рецептора. Результаты подчеркнули роль мутантных облаков в селективных событиях и открыли новый механизм антигенной гибкости. [68]
Квазивидовая память
[ редактировать ]Квазивидовая память — это тип молекулярной памяти, зависящий от недавней истории эволюционного происхождения и целостности мутантного спектра. [69] [70] Поиск памяти был вызван сложным адаптивным системным поведением вирусного квазивида, о чем свидетельствует наличие основной информации (считающейся той, которая определяет вирусную идентичность), несмотря на вариации конститутивных элементов (мутантный спектр). Хорошо известным примером является память иммунной системы , которая мобилизует и расширяет компоненты меньшинства в ответ на стимулы, с которыми ранее сталкивалась система. [71] В экспериментах, направленных на выявление памяти у вирусных квазивидов, частота членов мутантного спектра увеличивалась вследствие их репликации во время отбора, который привел их к доминированию. Когда селективное ограничение было снято, геномы памяти остались на уровнях, которые были в 10-100 раз выше базальных уровней, что можно было объяснить исключительно их возникновением путем мутации, как документально подтверждено независимыми генетическими маркерами вируса ящура и ВИЧ-1 in vivo . [69] [70] [72] [73] Таким образом, память — это исторически-зависимое коллективное свойство квазивидов, которое дает избирательное преимущество в реагировании на изменения окружающей среды, ранее испытанные той же эволюционной линией. Это может проявиться только в том случае, если спектр мутантов сохраняет свою полноту, поскольку память теряется, когда популяция подвергается узким местам, исключающим меньшинства. Соответствующий пример последствий памяти возникает в противовирусной фармакологии при повторном введении того же или родственного противовирусного агента (способного вызывать мутации общей резистентности), использованного при предыдущем лечении. Второе вмешательство может столкнуться с устойчивыми к ингибиторам геномами памяти от предыдущего лечения, что будет способствовать бегству вируса. [69] Это аспект, которому не уделялось должного внимания при планировании противовирусных вмешательств для пациентов, у которых первый курс лечения оказался неэффективным и которые должны пройти второй курс лечения.
Взаимодействия внутримутантного спектра для интерференции, комплементации или сотрудничества
[ редактировать ]Отдельные геномы, окруженные облаком родственных мутантов, можно либо подавить, чтобы сохранить низкую частоту, либо помочь сохранить в популяции. Две альтернативные судьбы зависят от нескольких факторов, одним из которых является окружающий спектр мутантов на тех этапах инфекционного цикла, на которых устанавливается эффективная конкуренция между вариантами, например, внутри репликационных комплексов. Это важное понятие было впервые выведено теоретически. [12] [74] а затем экспериментально подошел к нескольким вирусам. В раннем исследовании Хуан Карлос де ла Торре и Джон Холланд описали подавление VSV с высокой приспособленностью с помощью мутантных спектров с низкой приспособленностью. [12] С тех пор подавляющие эффекты были зарегистрированы на стандартных и мутагенизированных вирусных популяциях. Некоторые примеры:
- Подавление антигенных вариантов вируса ящура с высокой приспособленностью с помощью мутантов с низкой приспособленностью, ускользающих от антител. [75]
- Подавление вирулентного полиовируса (PV) аттенуированным вирусом в полиовирусных вакцинах . [65]
- Подавление патогенного вируса лимфоцитарного хориоменгита (LCMV) (вызывающего дефицит гормона роста у мышей) непатогенными вариантами LCMV. [76]
- Подавление ящура мутагенизированной популяцией вируса ящура. [77]
- Подавление ящура мутантами капсида и полимеразы ящура. [78]
- Подавление лекарственно-устойчивых вирусных мутантов во время противовирусной терапии. [79] [80]
Противоположностью подавлению является поддержание мутанта либо за счет благоприятного положения в ландшафте приспособленности, либо за счет взаимодействия комплементации или сотрудничества с членами мутантного спектра. Положение в ландшафте приспособленности влияет на уязвимость к мутациям, что популяризируется терминами «преимущество самого плоского» или «выживание самого плоского», что указывает на то, что вариант, расположенный на вершине острого пика приспособленности, имеет более высокую вероятность снижения приспособленности, поскольку результат новых мутаций, чем тот же вариант, расположенный на плато приспособленности . [3] [81] [82] Выживание самого плоского варианта также было предложено в качестве компонента некоторых моделей порога ошибки. [83]
Коллективное поведение вирусов было документировано с помощью мутантных РНК-вирусов, устойчивых к нуклеотидным аналогам. Изучение этого класса мутантов сыграло важную роль для понимания молекулярной основы точности копирования матрицы и последствий изменений точности в адаптивной способности и патогенном потенциале РНК-вирусов. [84] [85] [86] У первого изученного мутанта замена аминокислоты G46S в PV-полимеразе привела примерно к четырехкратному увеличению точности копирования матрицы. Эта модификация снизила адаптивность и инфекционный потенциал ПВ in vivo. [84] [85] Изолированный мутант не реплицировался эффективно в мозге восприимчивых мышей, но это происходило, когда его мутантный спектр был расширен за счет мутагенеза 5-фторурацила или когда он был совместно инокулирован с PV дикого типа. [85]
Комплементация (часто возникающая, когда функциональный белок, кодируемый набором геномов, используется другим набором геномов, кодируемый белок которого не является функциональным) может лежать в основе некоторых коллективных реакций квазивидов, таких как приспособленность особей, изолированных от популяции, уступающая приспособленности особей, выделенных из популяции. население. [15] [30] Была описана комплементация между двумя укороченными геномными формами вируса ящура. [87] Геномы с внутренними делециями стали обнаруживаться при высокой множественности пассажа клональной популяции стандартного вируса ящура, имеющего моночастный геном из одноцепочечной РНК. Инфекционность была вызвана комплементацией двух укороченных форм в отсутствие стандартных полноразмерных геномов вируса ящура. Чтобы комплементация была эффективной, требовалось предварительное исследование пространства последовательностей посредством точечных мутаций. [88] Система претерпела замечательный эволюционный переход, похожий на сегментацию генома. Серьезные генетические нарушения в вирусных геномах трудно наблюдать, если на помощь девиантным геномам не придет такой механизм, как комплементация. Сообщалось о дополнительных примерах комплементации среди РНК-вирусов. [89] [90] [91] [42] [44] Комплементация — это средство поддержания обнаруживаемых частот дефектных геномов в вирусных популяциях.
Было проведено различие между комплементацией и кооперацией, при которых два разных генома порождают новый фенотип посредством взаимодействия между двумя вариантными белками. [92] Пример сотрудничества был охарактеризован в ходе исследований с вирусом кори по слиянию мембран, которое необходимо для проникновения вируса в клетки. Для этого вируса слияние опосредовано двумя белками, называемыми H и F. Усеченный H был недостаточен для слияния клеток, но активность восстанавливалась, когда усеченный H сопровождался двумя формами F, но не одной из форм по отдельности. [92]
Следовательно, комплементация, кооперация, интерференция и подавление могут возникать в результате взаимодействий между компонентами мутантного спектра, возникающими в результате случайных мутаций. Отбор действует на любые наборы мутантов, которые могут обеспечить полезный признак, чтобы превратить случайные явления в биологический смысл.
Узкие места
[ редактировать ]
Способом прервать участие отдельных геномов во взаимодействиях с их мутантным спектром является резкое сокращение размера популяции квазивидов, которое изолирует один или несколько отдельных геномов от их окружения. Такие сокращения называются узкими местами, и они играют важную роль в формировании эволюционных линий всех видов организмов, а также вирусов. Они часто возникают не только при передаче данных между хостами, но и внутри зараженных хостов. [93] [94] [95] и они могут нарушать положительные и отрицательные события отбора в процессах, которые трудно идентифицировать и охарактеризовать.
Серьезные узкие места были воспроизведены с лабораторными популяциями вирусов в форме переноса от бляшки к бляшке. [96] [97] Эта конструкция служила для экспериментальной проверки действия храповика Мюллера или снижения приспособленности за счет необратимого внедрения мутаций в бесполые организмы в отсутствие компенсаторных механизмов. [98] Серийные переносы выявили наличие редких мутаций, не наблюдаемых в стандартных лабораторных или естественных вирусных популяциях. В отсутствие вынужденных узких мест такие редкие мутации были бы потеряны в результате отрицательного отбора из-за затрат на их приспособленность. [99] Исследование того, как клоны ящура, ослабленные храповым механизмом Мюллера, восстановили репликативную приспособленность, выявило несколько альтернативных молекулярных путей восстановления приспособленности. [100] Последствия этого наблюдения оставались в основном незамеченными до тех пор, пока недавние результаты с вирусом гепатита С (ВГС) также не показали наличие нескольких путей улучшения физической формы. [60] [62] Кроме того, обширное пассаж биологического клона вируса ящура в клетках BHK-21 обеспечил способность инфицировать несколько линий клеток человека в дополнение к ожидаемому увеличению приспособленности к размножению в клетках BHK-21. [101] Таким образом, некоторые данные свидетельствуют о том, что повышение приспособленности в конкретной среде может парадоксальным образом расширить фенотипический потенциал вируса. Будет интересно выяснить, может ли целенаправленная адаптация других вирусов к конкретной среде также повлечь за собой расширение разнообразия, при этом многие фенотипические варианты достигают схожих уровней приспособленности. В обобщенном виде это расширение фенотипического пространства могло бы обеспечить новую интерпретацию молекулярной основы адаптации и объяснить, почему адаптация к альтернативной среде может не привести к ослаблению .
Лишение отдельного вируса возможности подавления, дополнения или сотрудничества может представлять собой освобождение для инициирования нового эволюционного процесса или приговор к вымиранию. В случае освобождения от подавления изолированный геном должен реплицироваться и иметь возможность реконструировать облако мутантов, чтобы восстановить адаптивные способности. Это привело к предположению, что высокая частота мутаций позволила восстановить такой мутантный спектр после узких мест. Другие модели объясняют высокую частоту мутаций адаптивной оптимизацией, независимой от узких мест, или механистическим следствием быстрой репликации. [58] Каковы бы ни были их первопричины, высокие темпы мутаций служат цели адаптации во многих обстоятельствах, а не только при устранении узких мест. Вирус-основатель может привнести другой фенотип для последующей эволюции. Эволюцию вирусов в природе и как возбудителей болезней можно рассматривать как последовательность изменений мутантного спектра, подвергающихся расширению и сокращению размера популяции в непрерывном взаимодействии положительного и отрицательного отбора и случайного дрейфа. Хотя краткосрочная (например, внутрихозяинная) эволюция поддается наблюдению и измерению, вирусы могут оказаться относительно статичными в долгосрочной перспективе на протяжении десятилетий (как это видно на примере антигенных вариантов вируса ящура). [102] ) или дольше. Эволюция внутри хоста обычно происходит быстрее, чем эволюция между хостами, что документально подтверждено вирусами. [10] и другие биологические системы. [103] Кажущаяся инвариантность может быть результатом отбора на долгосрочное выживание популяций, которые ранее лихорадочно проверяли результаты эволюции в краткосрочных процессах. [58]
Вирусное заболевание
[ редактировать ]Вскоре после того, как были обнаружены квазивиды вирусов, стали очевидны некоторые медицинские последствия. [20] [104] Несколько конкретных и общих моментов ниже. [10] [43] [66] [28]
- Высокая частота мутаций и гетерогенность популяции наделяют вирусы способностью избегать иммунного давления (в том числе вызванного вакцинацией ) и противовирусных ингибиторов, используемых в терапии. Вопрос о том, может ли вакцинация способствовать долгосрочной эволюции антигенных детерминант, остается открытым.
- Вакцины с ослабленным РНК-вирусом могут вернуться в вирулентные формы. РНК-вирусы, выпущенные в природу для целей борьбы с вредителями, могут мутировать и приобретать новые фенотипы.
- Ослабление и вирулентность вируса зависят от генетических особенностей вируса. Вариантные формы данного вируса могут проявлять повышенную вирулентность или атипичное заболевание.
- Компоненты мутантного спектра могут демонстрировать другой клеточный тропизм или диапазон хозяев , чем большинство геномов в той же популяции, что может иметь значение для возникновения и повторного возникновения вирусных заболеваний.
- На вирусный патогенез влияют микроэволюционные процессы, при которых одни вирусные субпопуляции заменяются другими, сохраняясь или проникая в новые типы клеток, ткани или органы.
- Чем больше размер активно реплицирующейся (эффективной) популяции и скорость репликации, тем эффективнее исследование пространства последовательностей для фенотипического расширения, которое способствует выживанию и персистенции.
- Существует связь между четырьмя параметрами, которые характеризуют вирусы во время инфекционных процессов: скорость репликации (скорость, с которой вирусная РНК или ДНК синтезируется внутриклеточно для производства вирусного потомства), вирусная нагрузка (общее количество вируса, определенное количественно в инфицированном хозяине или компартменте хозяина). ), генетическая гетерогенность и репликативная приспособленность (выход инфекционных частиц, которые могут способствовать появлению следующего поколения). Они могут влиять на прогрессирование заболевания, и любой из них может быть направлен на борьбу с заболеванием.
Во всех взаимодействиях, ведущих к заболеванию, решающую роль играют клетки-хозяева по отдельности и в виде групп в тканях и органах. Последствия вирусной инфекции всегда зависят от хозяина. Однако сам вирус представляет собой серьезную проблему, решить которую помогает более глубокое понимание динамики квазивидов. [28]
Противовирусные стратегии
[ редактировать ]Растет мнение, что дарвиновские принципы должны помочь в планировании противовирусных разработок. [105] Цель вакцинации — вызвать защитную реакцию, которая либо предотвращает репликацию вируса, либо заболевание. Целью противовирусного фармакологического вмешательства является подавление репликации вируса, чтобы дать иммунной системе возможность уничтожить вирус. Проще говоря, прямая опасность для вакцинации и лечения заключается в том, что вирус может уйти в результате отбора мутантов, устойчивых к компонентам защиты, запускаемым вакциной, или к ингибиторам, вводимым извне. Это привело к появлению нескольких предложений по борьбе с вирусными заболеваниями, которые можно резюмировать ниже. [58]
Воздействие вакцины на множественные эпитопы В- и Т-клеток
[ редактировать ]Вакцины должны включать репертуар эпитопов В- и Т-клеток, чтобы вызвать сильный иммунный ответ . Широкий ответ должен свести к минимуму отбор ускользающих мутантов, которые могут присутствовать в качестве компонентов меньшинства в мутантном спектре, как неоднократно документировалось экспериментально. [10] [22] [44] [69] При существующих типах доступных вакцин те вакцины, которые лучше всего соответствуют требованию наличия множественных эпитопов , в порядке ожидаемой эффективности обеспечивают защиту от высоковариабельных вирусов: аттенуированный > инактивированный цельный вирус > несколько экспрессируемых белков > один экспрессируемый белок > несколько синтетических пептидов. антигены > одиночный пептидный антиген. Нехватка эффективных синтетических вакцин против РНК-вирусных патогенов, несмотря на огромные научные и экономические усилия, является отражением основных проблем.
Противовирусные средства, используемые в комбинации
[ редактировать ]противовирусной монотерапии Следует избегать (использования одного противовирусного препарата). Следующие рекомендации были сделаны и в некоторых случаях успешно реализованы:
- Ингибиторы, используемые в комбинации, должны быть нацелены на различные вирусные генные продукты.
- Разделение лечения на два этапа: первый режим индукции и второй поддерживающий режим. Лекарственные препараты, вводимые на двух этапах, должны быть разными.
- Нацеливание на клеточные функции, необходимые для жизненного цикла вируса.
- Применение препаратов, стимулирующих врожденный иммунный ответ (например, ингибиторов ферментов, участвующих в биосинтезе пиримидинов).
- Комбинированное применение иммунотерапии и химиотерапии .
- Летальный мутагенез или вымирание вируса из-за избыточного количества мутаций, возникших во время репликации вируса.
Основная цель этих стратегий состоит в том, чтобы избежать отбора мутантов, избегающих лечения, с помощью множества селективных ограничений, которые вирус не может преодолеть. [58] [106] Контроль эффективен либо потому, что исследование пространства последовательностей не может достичь необходимых множественных мутаций (даже когда доступна рекомбинация), либо потому, что множественные мутации приводят к серьезным затратам на приспособленность. [106] Вакцины, подвергающие воздействию множественных эпитопов, и комбинированная терапия следуют одной и той же стратегии, цель которой состоит в том, чтобы ограничить возможные пути бегства квазивидов вируса перед лицом супрессивных ограничений.
Летальный мутагенез
[ редактировать ]Летальный мутагенез — это процесс вымирания вируса с частотой ошибок, при которой вирус больше не может сохранять свою генетическую информацию. [10] [28] [44] [58] [62] [83] [107] [108] Применение летального мутагенеза в качестве противовирусной стратегии заслуживает внимания в контексте настоящей статьи, поскольку его истоки лежат в квазивидовой теории, в форме соотношения порога ошибки. И порог ошибки, и летальный мутагенез сильно зависят от ландшафта приспособленности, но оба могут возникать в сложных ландшафтах приспособленности, как и те, которые имеют отношение к вирусным популяциям. [83] Термин «летальный мутагенез» был придуман Лоуренсом Лебом и его коллегами. [107] и в настоящее время он широко используется для описания противовирусной активности аналогов оснований и нуклеозидов, которые увеличивают частоту вирусных мутаций. Хотя было предложено несколько моделей, объясняющих вымирание вируса избыточными мутациями, [83] Вероятным механизмом является расширение нарушения порога ошибки. [109] [108] Интересно, что некоторые противовирусные агенты, лицензированные для использования у людей, которые первоначально считались действующими только как ингибиторы репликации вируса, на самом деле могут проявлять свою противовирусную активность против некоторых РНК-вирусов, по крайней мере частично, путем летального мутагенеза. Так обстоит дело с фавипиравиром (Т-705; 6-фтор-3-гидрокси-2-пиразинкарбоксамид) и рибавирином (1-β-D-рибофуранозил-1-H-1,2,4-триазол-3-карбоксамид). которые в настоящее время интенсивно исследуются как смертельные мутагены. [108]
Защитные механизмы, основанные на модификации генома вторгшихся генетических паразитов, таких как редактирование клеточной активности, которая задействуется как часть врожденного иммунного ответа ( ADAR , APOBEC , RIP и т. д.). [110] представляют собой естественный аналог принципа летального мутагенеза. Применимость к патогенным клеточным элементам вполне реальна, а летальный мутагенез для контроля опухолевых клеток является активной областью исследований. [111] [112] Таким образом, признание динамики квазивидов позволило предложить некоторые фундаментальные рекомендации по профилактике и контролю заболеваний, которые постепенно проникают в клиническую практику. Это соответствует признанной необходимости применения дарвиновских принципов для борьбы с инфекционными заболеваниями.
Порог ошибки
[ редактировать ]Это можно определить как «неспособность генетического элемента поддерживаться в популяции, поскольку точность механизма его репликации снижается за пределы определенного порогового значения». [113]
Теоретически, если бы уровень мутаций был достаточно высоким, вирусная популяция не смогла бы поддерживать генотип с максимальной приспособленностью, и, следовательно, способность популяции адаптироваться к окружающей среде была бы поставлена под угрозу. Практическое применение этой динамики можно найти в противовирусных препаратах, использующих летальный мутагенез. Например, повышенные дозы мутагена рибавирина снижают инфекционность полиовируса. [114]
Однако эти модели предполагают, что вредными являются только мутации, возникающие в наиболее подходящей последовательности, и, более того, они не смертельны. Утверждалось, что если принять во внимание вредное воздействие мутаций на популяцию вариантов и тот факт, что многие мутации летальны, то порог ошибки исчезает, т. е. наиболее приспособленная последовательность всегда сохраняется. [115] [113] [116] Эмпирические данные о влиянии мутаций на вирусы редки, но, похоже, соответствуют этому сценарию. [117]
Возможные эволюционные последствия
[ редактировать ]
Мутационная устойчивость
[ редактировать ]На долгосрочную эволюцию вируса может повлиять то, что эволюционно стабильной стратегией может оказаться создание широкого квазивида с членами примерно одинаковой приспособленности, чем создание четко определенного «наиболее подходящего» единственного генотипа (с мутационными соседями, существенно меньшими). соответствовать). Это назвали «выживанием самого плоского» — имея в виду профили приспособленности двух стратегий соответственно. [3]
В долгосрочной перспективе более плоский профиль приспособленности может позволить квазивиду лучше использовать изменения в давлении отбора , аналогично тому, как половые организмы используют рекомбинацию для сохранения разнообразия в популяции. По крайней мере, в ходе моделирования можно показать, что более медленный репликатор способен превзойти более быстрый репликатор в тех случаях, когда он более устойчив и частота мутаций высока. [2]
Однако неизвестно, возникла ли мутационная устойчивость или она присуща генетическим системам, поскольку основной механизм устойчивости будет зависеть от особенностей каждой системы. [4]
Сотрудничество
[ редактировать ]Экспериментальные манипуляции с полиовирусами более высокой точности с целью придания им полимеразы – и, следовательно, снижения частоты их мутаций – показали, что эти варианты имеют меньшую патогенность, чем последовательности дикого типа . [85] Патогенность затем можно было восстановить применением мутагена. Это было интерпретировано как означающее, что более низкая частота мутаций снизила адаптивность (или широту) квазивида. Мутантные вирусы, выделенные из ткани головного мозга, сами по себе не были патогенными, и авторы предполагают, что между вариантными представителями квазивидов может существовать комплементация, которая могла бы позволить вирусам колонизировать различные ткани и системы хозяина.
Ссылки
[ редактировать ]![]() Эта статья была адаптирована из следующего источника под лицензией CC BY 4.0 ( 2000 г. ) ( отчеты рецензента ):
Эстебан Доминго Соланс, Селия Пералес (17 октября 2019 г.). «Вирусные квазивиды» . ПЛОС Генетика . 15 (10): e1008271. doi : 10.1371/JOURNAL.PGEN.1008271 . ISSN 1553-7390 . ПМК 6797082 . ПМИД 31622336 . Викиданные Q86320171 .
Эта статья была адаптирована из следующего источника под лицензией CC BY 4.0 ( 2000 г. ) ( отчеты рецензента ):
Эстебан Доминго Соланс, Селия Пералес (17 октября 2019 г.). «Вирусные квазивиды» . ПЛОС Генетика . 15 (10): e1008271. doi : 10.1371/JOURNAL.PGEN.1008271 . ISSN 1553-7390 . ПМК 6797082 . ПМИД 31622336 . Викиданные Q86320171 .
- ^ Jump up to: а б с д и ж г Доминго Э, Гарсиа-Креспо К, Пералес К (29 сентября 2021 г.). «Исторический взгляд на открытие концепции квазивида» . Ежегодный обзор вирусологии . 8 (1): 51–72. doi : 10.1146/annurev-virology-091919-105900 . hdl : 10261/265663 . ISSN 2327-056X . ПМИД 34586874 .
- ^ Jump up to: а б ван Нимвеген Э., Кратчфилд Дж. П., Хайнен М. (август 1999 г.). «Нейтральная эволюция мутационной устойчивости» . Труды Национальной академии наук Соединенных Штатов Америки . 96 (17): 9716–20. arXiv : adap-org/9903006 . Бибкод : 1999PNAS...96.9716V . дои : 10.1073/pnas.96.17.9716 . ПМК 22276 . ПМИД 10449760 .
- ^ Jump up to: а б с Уилке С.О., Ван Дж.Л., Офриа С., Ленски Р.Э., Адами С. (июль 2001 г.). «Эволюция цифровых организмов при высоких темпах мутаций приводит к выживанию самых плоских» . Природа . 412 (6844): 331–3. Бибкод : 2001Natur.412..331W . дои : 10.1038/35085569 . ПМИД 11460163 . S2CID 1482925 .
- ^ Jump up to: а б Елена С.Ф., Агудело-Ромеро П., Карраско П., Кодоньер Ф.М., Мартин С., Торрес-Барсело К., Санхуан Р. (май 2008 г.). «Экспериментальная эволюция растительных РНК-вирусов» . Наследственность . 100 (5): 478–83. дои : 10.1038/sj.hdy.6801088 . ПМК 7094686 . ПМИД 18253158 .
- ^ Эйген М., Маккаскилл Дж., Шустер П. (1988). «Молекулярные квазивиды». Журнал физической химии . 92 (24): 6881–6891. дои : 10.1021/j100335a010 . hdl : 11858/00-001M-0000-002C-84A7-C . S2CID 96727272 .
- ^ Новак М.А. (апрель 1992 г.). «Что такое квазивид?». Тенденции в экологии и эволюции . 7 (4): 118–21. дои : 10.1016/0169-5347(92)90145-2 . ПМИД 21235976 .
- ^ Jump up to: а б Дрейк Дж.В., Холланд Дж.Дж. (ноябрь 1999 г.). «Степень мутаций среди РНК-вирусов» . Труды Национальной академии наук Соединенных Штатов Америки . 96 (24): 13910–3. Бибкод : 1999PNAS...9613910D . дои : 10.1073/pnas.96.24.13910 . ПМК 24164 . ПМИД 10570172 .
- ^ Ле Клерк Л.С. (18 июня 2014 г.). Молекулярная характеристика полногеномных последовательностей вируса гепатита В из когорты городской больницы в Претории, Южная Африка . Претория, Южная Африка: Университет Претории. OCLC 958495192 .
- ^ Jump up to: а б с Эйген М., Шустер П. (1979). «Гиперцикл». естественные науки . 65 (1): 7–41. дои : 10.1007/bf00420631 . ISSN 0028-1042 . S2CID 1812273 .
- ^ Jump up to: а б с д и ж г час я дж к л м н тот Доминго Э., Шелдон Дж., Пералес К. (июнь 2012 г.). «Эволюция вирусных квазивидов» . Обзоры микробиологии и молекулярной биологии . 76 (2): 159–216. дои : 10.1128/MMBR.05023-11 . ПМЦ 3372249 . ПМИД 22688811 .
- ^ Эйген М. (октябрь 1971 г.). «Самоорганизация материи и эволюция биологических макромолекул». Die Naturwissenschaften . 58 (10): 465–523. Бибкод : 1971NW.....58..465E . дои : 10.1007/bf00623322 . ПМИД 4942363 . S2CID 38296619 .
- ^ Jump up to: а б с Светина Дж., Шустер П. (декабрь 1982 г.). «Самовоспроизведение с ошибками. Модель репликации полинуклеотидов». Биофизическая химия . 16 (4): 329–45. дои : 10.1016/0301-4622(82)87037-3 . ПМИД 7159681 .
- ^ Форнес Х, Томас Ласаро Х, Аларкон Т, Елена СФ, Сарданьес Х (январь 2019 г.). «Режимы репликации вируса в однопиковых ландшафтах приспособленности: анализ динамических систем». Журнал теоретической биологии . 460 : 170–183. Бибкод : 2019JThBi.460..170F . дои : 10.1016/j.jtbi.2018.10.007 . hdl : 2072/378023 . ПМИД 30300648 . S2CID 52947045 .
- ^ Шустер П. (2016). «Квазивиды на фитнес-ландшафтах». Квазивиды: от теории к экспериментальным системам . Актуальные темы микробиологии и иммунологии. Том. 392. Международное издательство Спрингер. стр. 61–120. дои : 10.1007/82_2015_469 . ISBN 9783319238975 . ПМИД 26597856 .
- ^ Jump up to: а б с д Доминго Э., Сабо Д., Танигучи Т., Вайсманн К. (апрель 1978 г.). «Гетерогенность нуклеотидной последовательности популяции РНК-фагов». Клетка . 13 (4): 735–44. дои : 10.1016/0092-8674(78)90223-4 . ПМИД 657273 . S2CID 19109157 .
- ^ Jump up to: а б Дуарте Э.А., Новелла И.С., Ледесма С., Кларк Д.К., Моя А., Елена С.Ф. и др. (июль 1994 г.). «Субклональные компоненты консенсусной приспособленности в клоне РНК-вируса» . Журнал вирусологии . 68 (7): 4295–301. doi : 10.1128/JVI.68.7.4295-4301.1994 . ПМК 236352 . ПМИД 8207804 .
- ^ Доминго Э., Брун А., Нуньес Х.И., Кристина Х., Брионес К., Эскармас К. (10 мая 2006 г.). «Геномика вирусов». Патогеномика . Wiley-VCH Verlag GmbH & Co. КГаА: 367–388. дои : 10.1002/352760801x.ch17 . ISBN 9783527608010 .
- ^ Батшелет Э., Доминго Э., Вайсман К. (январь 1976 г.). «Доля ревертантных и мутантных фагов в растущей популяции в зависимости от мутации и скорости роста». Джин . 1 (1): 27–32. дои : 10.1016/0378-1119(76)90004-4 . ПМИД 1052321 .
- ^ Брэдвелл К., Комб М., Доминго-Калап П., Санхуан Р. (сентябрь 2013 г.). «Корреляция между скоростью мутаций и размером генома рибовирусов: скорость мутаций бактериофага Qβ» . Генетика . 195 (1): 243–51. дои : 10.1534/genetics.113.154963 . ПМЦ 3761305 . ПМИД 23852383 .
- ^ Jump up to: а б с Холланд Дж., Шпиндлер К., Городиски Ф., Грабау Э., Никол С., ВандеПол С. (март 1982 г.). «Быстрая эволюция геномов РНК». Наука . 215 (4540): 1577–85. Бибкод : 1982Sci...215.1577H . дои : 10.1126/science.7041255 . ПМИД 7041255 .
- ^ Доминго Э., Мартинес-Салас Э., Собрино Ф., де ла Торре Х.К., Портела А., Ортин Дж. и др. (январь 1985 г.). «Квазивидовая (чрезвычайно гетерогенная) природа популяций генома вирусной РНК: биологическая значимость - обзор». Джин . 40 (1): 1–8. дои : 10.1016/0378-1119(85)90017-4 . ПМИД 3912262 .
- ^ Jump up to: а б с д и Доминго Э., Холланд Дж. Дж., Алквист П. (1988). Доминго Э., Холланд Дж.Дж., Алквист П. (ред.). РНК-генетика . дои : 10.1201/9781351076432 . ISBN 9781351076432 .
- ^ Jump up to: а б с Холланд Джей-Джей (2006). «Переходы в понимании РНК-вирусов: историческая перспектива» . Квазивиды: концепция и значение для вирусологии . Актуальные темы микробиологии и иммунологии. Том. 299. Шпрингер-Верлаг. стр. 371–401 . дои : 10.1007/3-540-26397-7_14 . ISBN 3540263950 . ПМИД 16568907 .
- ^ Jump up to: а б Мейерханс А., Чейнер Р., Альберт Дж., Сет М., Квок С., Снински Дж. и др. (сентябрь 1989 г.). «Временные колебания квазивидов ВИЧ in vivo не отражаются последовательными выделениями ВИЧ». Клетка . 58 (5): 901–10. дои : 10.1016/0092-8674(89)90942-2 . ПМИД 2550139 . S2CID 35903181 .
- ^ Jump up to: а б Фарси П. (ноябрь 2011 г.). «Новый взгляд на квазивиды и компартментализацию ВГС». Семинары по заболеваниям печени . 31 (4): 356–74. дои : 10.1055/s-0031-1297925 . ПМИД 22189976 . S2CID 260313185 .
- ^ Эйген М., Шустер П. (ноябрь 1977 г.). «Гиперцикл. Принцип естественной самоорганизации. Часть А: Возникновение гиперцикла». Die Naturwissenschaften . 64 (11): 541–65. дои : 10.1007/bf00450633 . ПМИД 593400 . S2CID 42131267 .
- ^ Саакян Д.Б., Ху К.К. (2016). «Математические модели теории квазивидов и точные результаты для динамики». Квазивиды: от теории к экспериментальным системам . Актуальные темы микробиологии и иммунологии. Том. 392. Международное издательство Спрингер. стр. 121–39. дои : 10.1007/82_2015_471 . ISBN 9783319238975 . ПМИД 26342705 .
- ^ Jump up to: а б с д и ж Доминго Э., Шустер П., ред. (2016). Квазивиды: от теории к экспериментальным системам . Актуальные темы микробиологии и иммунологии. Том. 392. дои : 10.1007/978-3-319-23898-2 . ISBN 978-3-319-23897-5 . S2CID 19514308 .
- ^ Штайнхауэр Д.А., Доминго Э., Холланд Дж.Дж. (декабрь 1992 г.). «Отсутствие доказательств механизмов корректуры, связанных с РНК-полимеразой вируса». Джин . 122 (2): 281–8. дои : 10.1016/0378-1119(92)90216-c . ПМИД 1336756 .
- ^ Jump up to: а б Бернад А., Бланко Л., Ласаро Х.М., Мартин Г., Салас М. (октябрь 1989 г.). «Консервативный 3'----5'-активный сайт экзонуклеазы в прокариотических и эукариотических ДНК-полимеразах». Клетка . 59 (1): 219–28. дои : 10.1016/0092-8674(89)90883-0 . ПМИД 2790959 . S2CID 23203156 .
- ^ Экерл Л.Д., Лу X, Сперри С.М., Чой Л., Денисон М.Р. (ноябрь 2007 г.). «Высокая точность репликации вируса мышиного гепатита снижается у мутантов экзорибонуклеазы nsp14» . Журнал вирусологии . 81 (22): 12135–44. дои : 10.1128/jvi.01296-07 . ПМК 2169014 . ПМИД 17804504 .
- ^ Надь П.Д., Карпентер К.Д., Саймон А.Е. (февраль 1997 г.). «Новый механизм восстановления 3'-конца РНК-вируса» . Труды Национальной академии наук Соединенных Штатов Америки . 94 (4): 1113–8. Бибкод : 1997PNAS...94.1113N . дои : 10.1073/pnas.94.4.1113 . ЧВК 19753 . ПМИД 9037015 .
- ^ Баханашвили М (апрель 2001 г.). «Экзонуклеолитическая корректура по белку р53» . Европейский журнал биохимии . 268 (7): 2047–54. дои : 10.1046/j.1432-1327.2001.02075.x . ПМИД 11277927 .
- ^ Смит Э.К., Денисон М.Р. (5 декабря 2013 г.). «Коронавирусы как подражатели ДНК: новая модель регуляции точности репликации РНК-вируса» . ПЛОС Патогены . 9 (12): e1003760. дои : 10.1371/journal.ppat.1003760 . ПМЦ 3857799 . ПМИД 24348241 .
- ^ Смит Э.К., Секстон Н.Р., Денисон М.Р. (ноябрь 2014 г.). «Мышление вне треугольника: точность репликации крупнейших РНК-вирусов» . Ежегодный обзор вирусологии . 1 (1): 111–32. doi : 10.1146/annurev-virology-031413-085507 . ПМИД 26958717 .
- ^ Вагнер Н., Ацмон-Раз Ю., Ашкенаси Г. (2016). «Теоретические модели обобщенных квазивидов». Квазивиды: от теории к экспериментальным системам . Актуальные темы микробиологии и иммунологии. Том. 392. Международное издательство Спрингер. стр. 141–59. дои : 10.1007/82_2015_456 . ISBN 9783319238975 . ПМИД 26373410 .
- ^ Шмидт Т.Т., Рейес Г., Грис К., Джейлан Кю, Шарма С., Мёрер М. и др. (май 2017 г.). «Инактивация GLN3 вызывает несбалансированные пулы dNTP и усиление мутагенеза» . Труды Национальной академии наук Соединенных Штатов Америки . 114 (22): Е4442–Е4451. дои : 10.1073/pnas.1618714114 . ПМЦ 5465912 . ПМИД 28416670 .
- ^ Такахаши К., Секизука Т., Фукумото Х., Накамичи К., Сузуки Т., Сато Ю. и др. (январь 2017 г.). «Идентификация глубоких последовательностей и роль в репликации вируса квазивида вируса JC у пациентов с прогрессирующей мультифокальной лейкоэнцефалопатией» . Журнал вирусологии . 91 (1). дои : 10.1128/jvi.01335-16 . ПМК 5165223 . ПМИД 27795410 .
- ^ Доминго-Калап П., Шуберт Б., Жоли М., Солис М., Унтрау М., Карапито Р. и др. (октябрь 2018 г.). «Необычайно высокий уровень замен в полиомавирусе BK, ассоциированном с трансплантатом, in vivo дополнительно концентрируется в HLA-C-связанных вирусных пептидах» . ПЛОС Патогены . 14 (10): e1007368. дои : 10.1371/journal.ppat.1007368 . ПМК 6207329 . ПМИД 30335851 .
- ^ Jump up to: а б Санчес-Кампос С., Домингес-Уэрта Г., Диас-Мартинес Л., Томас Д.М., Навас-Кастильо Х., Морионес Е., Гранде-Перес А. (02.07.2018). «Дифференциальная форма спектров мутантов геминивирусов у культивируемых и диких хозяев с инвариантными вирусными консенсусными последовательностями» . Границы в науке о растениях . 9 :932.дои : 10.3389 / fpls.2018.00932 . ПМК 6036239 . ПМИД 30013589 .
- ^ Jump up to: а б с Донохью Р.К., Пфаллер К.К., Каттанео Р. (февраль 2019 г.). «Циклическая адаптация квазивидов вируса кори к эпителиальным и лимфоцитарным клеткам: к V или не к V» . ПЛОС Патогены . 15 (2): e1007605. дои : 10.1371/journal.ppat.1007605 . ПМК 6395005 . PMID 30768648 .
- ^ Jump up to: а б с д и Агол VI, Gmyl AP (июнь 2018 г.). «Скорая помощь вирусным РНК: восстановление и ремоделирование» . Обзоры микробиологии и молекулярной биологии . 82 (2): e00067-1. дои : 10.1128/mmbr.00067-17 . ПМЦ 5968460 . ПМИД 29540453 .
- ^ Jump up to: а б с д и Фиглерович М, Алейска М, Куржинска-Кокорняк А, Фиглерович М (23 сентября 2003 г.). «Генетическая изменчивость: ключевая проблема профилактики и терапии РНК-вирусных инфекций». ХимИнформ . 34 (38). дои : 10.1002/chin.200338243 . ISSN 0931-7597 .
- ^ Jump up to: а б с д и ж г Доминго Э., Пералес К. (май 2018 г.). «Квазивиды и вирус». Европейский биофизический журнал . 47 (4): 443–457. дои : 10.1007/s00249-018-1282-6 . ПМИД 29397419 . S2CID 13239618 .
- ^ Санхуан Р., Доминго-Калап П. (декабрь 2016 г.). «Механизмы вирусной мутации» . Клеточные и молекулярные науки о жизни . 73 (23): 4433–4448. дои : 10.1007/s00018-016-2299-6 . ПМК 5075021 . ПМИД 27392606 .
- ^ Jump up to: а б Лауринг А.С., Андино Р. (июль 2010 г.). «Квазивидовая теория и поведение РНК-вирусов» . ПЛОС Патогены . 6 (7): е1001005. дои : 10.1371/journal.ppat.1001005 . ПМЦ 2908548 . ПМИД 20661479 .
- ^ ван Бохемен С., Тас А., Анвар С.Ю., ван Гротвельд Р., Албулеску И.К., Бауэр М.П. и др. (май 2017 г.). «Квазивидовой состав и эволюция типичного клинического изолята вируса Зика из Суринама» . Научные отчеты 7 (1): 2368. Бибкод : 2017НатСР...7.2368В . дои : 10.1038/s41598-017-02652-w . ПМК 5443807 . ПМИД 28539654 .
- ^ Влок М., Ланг А.С., Саттл, Калифорния (апрель 2019 г.). «Квазивиды морских РНК-вирусов распространены по всему океану» . мСфера . 4 (2): e00157-19. дои : 10.1128/mspheredirect.00157-19 . ПМК 6449609 . ПМИД 30944212 .
- ^ Хиросе Ю., Онуки М., Тенджимбаяши Ю., Мори С., Исии Ю., Такеучи Т. и др. (июнь 2018 г.). «Внутрихозяинные вариации вируса папилломы человека, выявленные с помощью сигнатурного мутагенеза APOBEC в вирусном геноме» . Журнал вирусологии . 92 (12):e00017-1 дои : 10.1128/jvi.00017-18 . ПМЦ 5974501 . ПМИД 29593040 .
- ^ Гисдер С., Мёкель Н., Эйзенхардт Д., Генерш Э. (декабрь 2018 г.). «Эволюция вирусной вирулентности in vivo: переключение вируса с деформированным крылом между хозяевами приводит к изменениям вирулентности и сдвигам последовательности» . Экологическая микробиология . 20 (12): 4612–4628. Бибкод : 2018EnvMi..20.4612G . дои : 10.1111/1462-2920.14481 . ПМИД 30452113 .
- ^ Баккам П., Томпсон Р.Дж., Федриго О., Карпентер С., Корнетт Дж.Л. (январь 2001 г.). «PAQ: Анализ распределения квазивидов». Биоинформатика . 17 (1): 16–22. дои : 10.1093/биоинформатика/17.1.16 . ПМИД 11222259 .
- ^ Скумс П., Зеликовский А., Сингх Р., Гасслер В., Димитрова З., Князев С. и др. (январь 2018 г.). «КВЕНТИН: реконструкция передачи болезней на основе геномных данных вирусных квазивидов» . Биоинформатика . 34 (1): 163–170. doi : 10.1093/биоинформатика/btx402 . ПМК 6355096 . ПМИД 29304222 .
- ^ Jump up to: а б Лоури К., Вудман А., Кук Дж., Эванс DJ (июнь 2014 г.). «Рекомбинация в энтеровирусах представляет собой двухфазный репликационный процесс, включающий образование «неточных» промежуточных продуктов, длина которых превышает длину генома» . ПЛОС Патогены . 10 (6): e1004191. дои : 10.1371/journal.ppat.1004191 . ПМЦ 4055744 . ПМИД 24945141 .
- ^ Jump up to: а б Сяо Ю., Рузин И.М., Бьянко С., Асеведо А., Гольдштейн Э.Ф., Фарков М. и др. (сентябрь 2017 г.). «Рекомбинация РНК повышает адаптивность и необходима для распространения и вирулентности вируса» . Клетка-хозяин и микроб . 22 (3): 420. doi : 10.1016/j.chom.2017.08.006 . ПМК 5807061 . ПМИД 28910639 .
- ^ Тибайренц М., Аяла Ф.Дж. (ноябрь 2012 г.). «Репродуктивная клональность патогенов: взгляд на патогенные вирусы, бактерии, грибы и паразитические простейшие» . Труды Национальной академии наук Соединенных Штатов Америки . 109 (48): Е3305-13. дои : 10.1073/pnas.1212452109 . ПМК 3511763 . ПМИД 22949662 .
- ^ Пералес К., Морено Э., Доминго Э. (июль 2015 г.). «Клональность и внутриклеточная полиплоидия в эволюции и патогенезе вирусов» . Труды Национальной академии наук Соединенных Штатов Америки . 112 (29): 8887–92. Бибкод : 2015PNAS..112.8887P . дои : 10.1073/pnas.1501715112 . ПМЦ 4517279 . ПМИД 26195777 .
- ^ Jump up to: а б Вильярреал LP, Вицани Дж (ноябрь 2013 г.). «Переосмысление теории квазивидов: от наиболее приспособленного типа к кооперативным консорциумам» . Всемирный журнал биологической химии . 4 (4): 79–90. дои : 10.4331/wjbc.v4.i4.79 . ПМК 3856310 . ПМИД 24340131 .
- ^ Jump up to: а б с д и ж г час я Доминго Э (сентябрь 2015 г.). Вирус как популяция: состав, сложность, динамика и биологические последствия . Академическая пресса. ISBN 978-0-12-800837-9 .
- ^ Jump up to: а б Асеведо А., Бродский Л., Андино Р. (январь 2014 г.). «Мутационные и фитнес-ландшафты РНК-вируса, выявленные посредством популяционного секвенирования» . Природа . 505 (7485): 686–90. Бибкод : 2014Natur.505..686A . дои : 10.1038/nature12861 . ПМК 4111796 . ПМИД 24284629 .
- ^ Jump up to: а б с д и ж Морено Э., Гальего И., Грегори Дж., Люсия-Санс А., Сория М.Е., Кастро В. и др. (май 2017 г.). «Внутренние неравновесия и фенотипическая диверсификация во время репликации вируса гепатита С в некоэволюционирующей клеточной среде» . Журнал вирусологии . 91 (10). дои : 10.1128/jvi.02505-16 . ПМК 5411618 . ПМИД 28275194 .
- ^ Охоснегрос С., Беренвинкель Н., Антал Т., Новак М.А., Эскармас К., Доминго Э. (февраль 2010 г.). «Динамика конкуренции-колонизации в РНК-вирусе» . Труды Национальной академии наук Соединенных Штатов Америки . 107 (5): 2108–12. Бибкод : 2010PNAS..107.2108O . дои : 10.1073/pnas.0909787107 . ПМЦ 2836666 . ПМИД 20080701 .
- ^ Jump up to: а б с Гальего И., Грегори Дж., Сория М.Е., Гарсия-Креспо С., Гарсиа-Альварес М., Гомес-Гонсалес А. и др. (октябрь 2018 г.). «Устойчивость вируса гепатита С высокой пригодности к летальному мутагенезу». Вирусология 523 : 100–109. дои : 10.1016/j.virol.2018.07.030 . ПМИД 30107298 . S2CID 52006443 .
- ^ Jump up to: а б Холланд Дж. Дж., Де Ла Торре Дж. К., Штайнхауэр Д. А. (1992). «Популяции РНК-вирусов как квазивиды». Генетическое разнообразие РНК-вирусов . Актуальные темы микробиологии и иммунологии. Том. 176. Берлин, Гейдельберг: Шпрингер. стр. 1–20. дои : 10.1007/978-3-642-77011-1_1 . ISBN 9783642770111 . OCLC 851813241 . ПМИД 1600747 . S2CID 46530529 .
- ^ Jump up to: а б Гарсиа-Арриаса Х., Охоснегрос С., Давила М., Доминго Э., Эскармас К. (июль 2006 г.). «Динамика мутаций и рекомбинации в реплицирующейся популяции дополняющих дефектных вирусных геномов». Журнал молекулярной биологии . 360 (3): 558–72. дои : 10.1016/j.jmb.2006.05.027 . ПМИД 16797586 .
- ^ Jump up to: а б Чумаков К.М., Пауэрс Л.Б., Нунан К.Э., Ронинсон И.Б., Левенбук И.С. (январь 1991 г.). «Корреляция между количеством вируса с измененной нуклеотидной последовательностью и тестом на обезьянах приемлемости пероральной полиовирусной вакцины» . Труды Национальной академии наук Соединенных Штатов Америки . 88 (1): 199–203. Бибкод : 1991PNAS...88..199C . дои : 10.1073/pnas.88.1.199 . ПМК 50777 . ПМИД 1846038 .
- ^ Jump up to: а б Холланд Джей-Джей (1992). Генетическое разнообразие РНК-вирусов . Берлин, Гейдельберг: Springer Berlin Heidelberg. ISBN 9783642770111 . OCLC 851813241 .
- ^ Пералес С (октябрь 2018 г.). «Квазивидовая динамика и клиническое значение противовирусной устойчивости вируса гепатита С (ВГС)». Международный журнал противомикробных средств . 56 (1): 105562. doi : 10.1016/j.ijantimicag.2018.10.005 . ПМИД 30315919 . S2CID 52980171 .
- ^ Jump up to: а б Мартин В., Доминго Э. (август 2008 г.). «Влияние мутантного спектра на эволюцию вирусов: целенаправленный отбор антигенных вариантов в реконструированном квазивиде вируса» . Молекулярная биология и эволюция . 25 (8): 1544–54. дои : 10.1093/molbev/msn099 . ПМИД 18436553 .
- ^ Jump up to: а б с д Брионес С., Доминго Э (2008). «Отчет меньшинства: скрытые геномы памяти у квазивидов ВИЧ-1 и возможные клинические последствия» . Обзоры по СПИДу . 10 (2): 93–109. ПМИД 18615120 .
- ^ Jump up to: а б Руис-Харабо СМ, Ариас А, Барановский Э, Эскармас С, Доминго Э (апрель 2000 г.). «Память у вирусных квазивидов» . Журнал вирусологии . 74 (8): 3543–7. дои : 10.1128/jvi.74.8.3543-3547.2000 . ПМЦ 111862 . ПМИД 10729128 .
- ^ Фарбер Д.Л., Нетеа М.Г., Радбрух А., Раевски К., Цинкернагель Р.М. (февраль 2016 г.). «Иммунологическая память: уроки прошлого и взгляд в будущее». Обзоры природы. Иммунология . 16 (2): 124–8. дои : 10.1038/nri.2016.13 . ПМИД 26831526 . S2CID 8000538 .
- ^ Брионес К., Доминго Э., Молина-Парис К. (август 2003 г.). «Память ретровирусных квазивидов: экспериментальные данные и теоретическая модель вируса иммунодефицита человека» . Журнал молекулярной биологии . 331 (1): 213–29. дои : 10.1016/s0022-2836(03)00661-2 . ПМЦ 7173031 . ПМИД 12875847 .
- ^ Ариас А., Руис-Харабо С.М., Эскармас С., Доминго Э. (май 2004 г.). «Повышение приспособленности геномов памяти у вирусного квазивида». Журнал молекулярной биологии . 339 (2): 405–12. дои : 10.1016/j.jmb.2004.03.061 . ПМИД 15136042 .
- ^ Эйген М., Бибрихер К.К. (1988). Пространство последовательностей и распределение квазивидов . ЦРК Пресс. стр. 211–245. дои : 10.1201/9781351076449-12 . ISBN 9781351076449 .
{{cite book}}:|journal=игнорируется ( помогите ) - ^ Боррего Б., Новелла И.С., Жиральт Э., Андреу Д., Доминго Э. (октябрь 1993 г.). «Различный репертуар антигенных вариантов вируса ящура при наличии или отсутствии иммунного отбора» . Журнал вирусологии . 67 (10): 6071–9. doi : 10.1128/JVI.67.10.6071-6079.1993 . ПМК 238028 . ПМИД 7690417 .
- ^ Тенг М.Н., Олдстоун М.Б., де ла Торре Дж.К. (сентябрь 1996 г.). «Подавление синдрома дефицита гормона роста, вызванного вирусом лимфоцитарного хориоменингита, с помощью отрицательных по заболеванию вариантов вируса» . Вирусология . 223 (1): 113–9. дои : 10.1006/виро.1996.0460 . ПМИД 8806545 .
- ^ Гонсалес-Лопес С, Ариас А, Парьенте Н, Гомес-Мариано Г, Доминго Э (апрель 2004 г.). «Вирусная предварительная тушащая РНК может препятствовать инфекции» . Журнал вирусологии . 78 (7): 3319–24. дои : 10.1128/jvi.78.7.3319-3324.2004 . ПМК 371084 . ПМИД 15016853 .
- ^ Пералес С., Матео Р., Матеу М.Г., Доминго Э. (июнь 2007 г.). «Изучение спектра мутантных РНК-вирусов и событий летального мутагенеза: репликативная интерференция и комплементация множественными точечными мутантами». Журнал молекулярной биологии . 369 (4): 985–1000. дои : 10.1016/j.jmb.2007.03.074 . ПМИД 17481660 .
- ^ Краудер С., Киркегор К. (июль 2005 г.). «Транс-доминантное ингибирование репликации вирусной РНК может замедлить рост устойчивых к лекарствам вирусов». Природная генетика . 37 (7): 701–9. дои : 10.1038/ng1583 . ПМИД 15965477 . S2CID 16501575 .
- ^ Киркегор К., ван Бюрен, Нью-Джерси, Матео Р. (октябрь 2016 г.). «Мой кузен, мой враг: квазивидовое подавление лекарственной устойчивости» . Современное мнение в вирусологии . 20 : 106–111. дои : 10.1016/j.coviro.2016.09.011 . ПМЦ 5298929 . ПМИД 27764731 .
- ^ Кер Дж., Херши К.Л., Доминго Э., Холланд Дж.Дж., Новелла И.С. (август 2001 г.). «Условная нейтральность в конкурирующих вирусных популяциях» . Журнал вирусологии . 75 (16): 7315–20. doi : 10.1128/jvi.75.16.7315-7320.2001 . ПМК 114966 . ПМИД 11462003 .
- ^ Кодоньер FM, Дарос Х.А., Соле Р.В., Елена С.Ф. (декабрь 2006 г.). «Самый приспособленный против самого плоского: экспериментальное подтверждение квазивидового эффекта с субвирусными патогенами» . ПЛОС Патогены . 2 (12): е136. дои : 10.1371/journal.ppat.0020136 . ПМК 1757203 . ПМИД 17196038 .
- ^ Jump up to: а б с д Техеро Х., Монтеро Ф., Нуньо Х.К. (2016). «Теории летального мутагенеза: от катастрофы ошибок к летальному дезертирству». Квазивиды: от теории к экспериментальным системам . Актуальные темы микробиологии и иммунологии. Том. 392. Международное издательство Спрингер. стр. 161–79. дои : 10.1007/82_2015_463 . ISBN 9783319238975 . ПМИД 26210988 .
- ^ Jump up to: а б Пфайффер Дж. К., Киркегор К. (октябрь 2005 г.). «Повышенная точность снижает приспособленность и вирулентность полиовируса под давлением отбора у мышей» . ПЛОС Патогены . 1 (2): е11. дои : 10.1371/journal.ppat.0010011 . ПМЦ 1250929 . ПМИД 16220146 .
- ^ Jump up to: а б с д Виньуцци М., Стоун Дж.К., Арнольд Дж.Дж., Кэмерон К.Э., Андино Р. (январь 2006 г.). «Квазивидовое разнообразие определяет патогенез посредством кооперативных взаимодействий в вирусной популяции» . Природа . 439 (7074): 344–8. Бибкод : 2006Natur.439..344V . дои : 10.1038/nature04388 . ПМК 1569948 . ПМИД 16327776 .
- ^ Бордерия А.В., Розен-Ганьон К., Виньюцци М. (2016). «Варианты точности и квазивиды РНК». Квазивиды: от теории к экспериментальным системам . Актуальные темы микробиологии и иммунологии. Том. 392. Международное издательство Спрингер. стр. 303–22. дои : 10.1007/82_2015_483 . ISBN 9783319238982 . ПМК 7121553 . ПМИД 26499340 .
- ^ Гарсиа-Арриаса Х., Манрубия СК, Тоха М., Доминго Э., Эскармас К. (ноябрь 2004 г.). «Эволюционный переход к дефектным РНК, заразным за счет комплементации» . Журнал вирусологии . 78 (21): 11678–85. doi : 10.1128/JVI.78.21.11678-11685.2004 . ПМК 523252 . ПМИД 15479809 .
- ^ Морено Э., Охоснегрос С., Гарсиа-Арриаса Х., Эскармас К., Доминго Э., Пералес К. (май 2014 г.). «Исследование пространства последовательностей как основа сегментации генома вирусной РНК» . Труды Национальной академии наук Соединенных Штатов Америки . 111 (18): 6678–83. Бибкод : 2014PNAS..111.6678M . дои : 10.1073/pnas.1323136111 . ПМК 4020086 . ПМИД 24757055 .
- ^ Аасков Дж., Бузакотт К., Тху Х.М., Лоури К., Холмс Э.К. (январь 2006 г.). «Долгосрочная передача вирусов с дефектной РНК у людей и комаров Aedes». Наука . 311 (5758): 236–8. Бибкод : 2006Sci...311..236A . дои : 10.1126/science.1115030 . ПМИД 16410525 . S2CID 21605827 .
- ^ Сиота А.Т., Эрбар DJ, Ван Слайк Г.А., Уиллси Г.Г., Крамер Л.Д. (май 2012 г.). «Кооперативные взаимодействия в рое мутантов вируса Западного Нила» . Эволюционная биология BMC . 12 (1): 58. Бибкод : 2012BMCEE..12...58C . дои : 10.1186/1471-2148-12-58 . ПМЦ 3358237 . ПМИД 22541042 .
- ^ Сюэ К.С., Хупер К.А., Оллодарт А.Р., Дингенс А.С., Блум Дж.Д. (март 2016 г.). «Сотрудничество между различными вариантами вируса способствует росту гриппа H3N2 в клеточной культуре» . электронная жизнь . 5 : е13974. дои : 10.7554/elife.13974 . ПМЦ 4805539 . ПМИД 26978794 .
- ^ Jump up to: а б Широгане Ю, Ватанабэ С, Янаги Ю (2016). «Кооперативное взаимодействие в спектрах мутантных РНК-вирусов». Квазивиды: от теории к экспериментальным системам . Актуальные темы микробиологии и иммунологии. Том. 392. Международное издательство Спрингер. стр. 219–29. дои : 10.1007/82_2015_461 . ISBN 9783319238975 . ПМИД 26162566 .
- ^ Пфайффер Дж. К., Киркегор К. (апрель 2006 г.). «Ограничение квазивидов, опосредованное узким местом, при распространении РНК-вируса из места прививки в мозг» . Труды Национальной академии наук Соединенных Штатов Америки . 103 (14): 5520–5. Бибкод : 2006PNAS..103.5520P . дои : 10.1073/pnas.0600834103 . ПМЦ 1414638 . ПМИД 16567621 .
- ^ Гутьеррес С., Михалакис Ю., Блан С. (октябрь 2012 г.). «Узкие места популяции вируса во время развития внутри хозяина и передачи от хозяина к хозяину» . Современное мнение в вирусологии . 2 (5): 546–55. дои : 10.1016/j.coviro.2012.08.001 . ПМИД 22921636 .
- ^ Булл Р.А., Лучани Ф., МакЭлрой К., Гаудиери С., Фам С.Т., Чопра А. и др. (сентябрь 2011 г.). «Последовательные узкие места стимулируют эволюцию вируса на ранней стадии острой инфекции вируса гепатита С» . ПЛОС Патогены . 7 (9): e1002243. дои : 10.1371/journal.ppat.1002243 . ПМК 3164670 . ПМИД 21912520 .
- ^ Чао Л. (ноябрь 1990 г.). «Пригодность РНК-вируса снижается с помощью храповика Мюллера». Природа . 348 (6300): 454–5. Бибкод : 1990Natur.348..454C . дои : 10.1038/348454a0 . ПМИД 2247152 . S2CID 4235839 .
- ^ Дуарте Э., Кларк Д., Мойя А., Доминго Э., Холланд Дж. (июль 1992 г.). «Быстрая потеря приспособленности клонов РНК-вирусов млекопитающих из-за храпового механизма Мюллера» . Труды Национальной академии наук Соединенных Штатов Америки . 89 (13): 6015–9. Бибкод : 1992PNAS...89.6015D . дои : 10.1073/pnas.89.13.6015 . ПМК 402129 . ПМИД 1321432 .
- ^ Мюллер HJ (май 1964 г.). «Отношение рекомбинации к мутационному прогрессу». Мутационные исследования . 106 (1): 2–9. дои : 10.1016/0027-5107(64)90047-8 . ПМИД 14195748 .
- ^ Эскамис К., Давила М., Шарпантье Н., Брачо А., Мойя А., Доминго Э. (ноябрь 1996 г.). «Генетические поражения, связанные с храповиком Мюллера в РНК-вирусе». Журнал молекулярной биологии . 264 (2): 255–67. дои : 10.1006/jmbi.1996.0639 . ПМИД 8951375 .
- ^ Эскармис К., Давила М., Доминго Э. (январь 1999 г.). «Множественные молекулярные пути восстановления пригодности РНК-вируса, ослабленного в результате действия храпового механизма Мюллера». Журнал молекулярной биологии . 285 (2): 495–505. дои : 10.1006/jmbi.1998.2366 . ПМИД 9878424 .
- ^ Руис-Харабо СМ, Парьенте Н, Барановский Э, Давила М, Гомес-Мариано Г, Доминго Э (август 2004 г.). «Расширение тропизма клетки-хозяина вируса ящура несмотря на репликацию в постоянной среде» . Журнал общей вирусологии . 85 (Часть 8): 2289–97. дои : 10.1099/vir.0.80126-0 . ПМИД 15269370 .
- ^ Мартинес М.А., Допасо Дж., Эрнандес Дж., Матеу М.Г., Собрино Ф., Доминго Э., Ноулз, Нью-Джерси (июнь 1992 г.). «Эволюция генов капсидного белка вируса ящура: антигенная вариация без накопления аминокислотных замен за шесть десятилетий» . Журнал вирусологии . 66 (6): 3557–65. doi : 10.1128/JVI.66.6.3557-3565.1992 . ПМК 241137 . ПМИД 1316467 .
- ^ Хо С.Ю., Дюшен С., Молак М., Шапиро Б. (декабрь 2015 г.). «Зависящие от времени оценки скорости молекулярной эволюции: доказательства и причины» . Молекулярная экология . 24 (24): 6007–12. Бибкод : 2015MolEc..24.6007H . дои : 10.1111/mec.13450 . ПМИД 26769402 . S2CID 14433111 .
- ^ Доминго Э (1989). «Эволюция РНК-вируса и борьба с вирусными заболеваниями». Прогресс в исследованиях лекарств . Том. 33. Биркхойзер Базель. стр. 93–133. дои : 10.1007/978-3-0348-9146-2_5 . ISBN 9783034899253 . ПМИД 2687948 .
{{cite book}}:|journal=игнорируется ( помогите ) - ^ Уильямс П.Д. (февраль 2010 г.). «Дарвиновские вмешательства: укрощение патогенов посредством эволюционной экологии». Тенденции в паразитологии . 26 (2): 83–92. дои : 10.1016/j.pt.2009.11.009 . ПМИД 20036799 .
- ^ Jump up to: а б Пералес С., Ортега-Прието А.М., Бич Н.М., Шелдон Дж., Менендес-Ариас Л., Доминго Э. (2017). «Квазивиды и лекарственная устойчивость». Справочник по устойчивости к противомикробным препаратам . Спрингер Нью-Йорк. стр. 123–147. дои : 10.1007/978-1-4939-0694-9_1 . ISBN 9781493906932 .
- ^ Jump up to: а б Леб Л.А., Эссигманн Дж.М., Казази Ф., Чжан Дж., Роуз К.Д., Маллинз Дж.И. (февраль 1999 г.). «Летальный мутагенез ВИЧ мутагенными аналогами нуклеозидов» . Труды Национальной академии наук Соединенных Штатов Америки . 96 (4): 1492–7. Бибкод : 1999PNAS...96.1492L . дои : 10.1073/pnas.96.4.1492 . ПМК 15492 . ПМИД 9990051 .
- ^ Jump up to: а б с Пералес К., Гальего И., де Авила А.И., Сориа М.Э., Грегори Дж., Кер Дж., Доминго Э. (июль 2019 г.). «Усиливающееся воздействие летального мутагенеза вирусов». Будущая медицинская химия . 11 (13): 1645–1657. дои : 10.4155/fmc-2018-0457 . hdl : 10261/216260 . ПМИД 31469331 . S2CID 201673871 .
- ^ Эйген М. (октябрь 2002 г.). «Катастрофа ошибок и антивирусная стратегия» . Труды Национальной академии наук Соединенных Штатов Америки . 99 (21): 13374–6. Бибкод : 2002PNAS...9913374E . дои : 10.1073/pnas.212514799 . ПМК 129678 . ПМИД 12370416 .
- ^ Венкатесан С., Розенталь Р., Кану Н., МакГранахан Н., Бартек Дж., Кесада С.А. и др. (март 2018 г.). «Перспектива: мутагенез APOBEC при лекарственной устойчивости и ускользании от иммунитета при эволюции ВИЧ и рака» . Анналы онкологии . 29 (3): 563–572. дои : 10.1093/annonc/mdy003 . ПМЦ 5888943 . ПМИД 29324969 .
- ^ Фокс Э.Дж., Леб Л.А. (октябрь 2010 г.). «Летальный мутагенез: воздействие на мутаторный фенотип при раке» . Семинары по биологии рака . 20 (5): 353–9. дои : 10.1016/j.semcancer.2010.10.005 . ПМК 3256989 . ПМИД 20934515 .
- ^ Леб Л.А. (июнь 2011 г.). «Рак человека экспрессирует мутаторные фенотипы: происхождение, последствия и направление» . Обзоры природы. Рак . 11 (6): 450–7. дои : 10.1038/nrc3063 . ПМК 4007007 . ПМИД 21593786 .
- ^ Jump up to: а б Саммерс Дж., Литвин С. (январь 2006 г.). «Изучение теории катастроф ошибок» . Журнал вирусологии . 80 (1): 20–6. doi : 10.1128/JVI.80.1.20-26.2006 . ПМЦ 1317512 . ПМИД 16352527 .
- ^ Кротти С., Кэмерон С.Э., Андино Р. (июнь 2001 г.). «Катастрофа ошибки РНК-вируса: прямой молекулярный тест с использованием рибавирина» . Труды Национальной академии наук Соединенных Штатов Америки . 98 (12): 6895–900. Бибкод : 2001PNAS...98.6895C . дои : 10.1073/pnas.111085598 . ПМЦ 34449 . ПМИД 11371613 .
- ^ Уилке СО (август 2005 г.). «Теория квазивидов в контексте популяционной генетики» . Эволюционная биология BMC . 5 (1): 44. Бибкод : 2005BMCEE...5...44W . дои : 10.1186/1471-2148-5-44 . ПМК 1208876 . ПМИД 16107214 .
- ^ Вагнер Г.П., Кралл П. (ноябрь 1993 г.). «В чем разница между моделями порогов ошибок и храповиком Мюллера?». Журнал математической биологии . 32 (1): 33–44. дои : 10.1007/BF00160372 . S2CID 122142345 .
- ^ Санхуан Р., Моя А., Елена С.Ф. (июнь 2004 г.). «Распределение эффектов приспособленности, вызванных однонуклеотидными заменами в РНК-вирусе» . Труды Национальной академии наук Соединенных Штатов Америки . 101 (22): 8396–401. Бибкод : 2004PNAS..101.8396S . дои : 10.1073/pnas.0400146101 . ПМК 420405 . ПМИД 15159545 .
- ^ Использование фитнес-ландшафтов для визуализации эволюции в действии , получено 22 октября 2019 г.
Внешние ссылки
[ редактировать ]- Видео: Использование фитнес-ландшафтов для визуализации эволюции в действии — содержит пример «выживания самых плоских».