Нигростриатальный путь
| Нигростриатальный путь | |
|---|---|
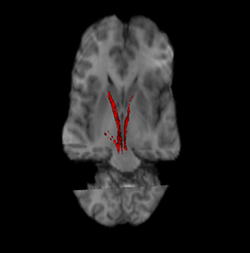 Нигростриатальный путь (слева и справа в красном). | |
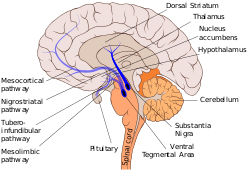 Нигростриатальный путь показан здесь в твердом синем, соединяющем черту субстанции с дорсальным стриатумом. | |
| Анатомическая терминология |
Нигростриатальный путь представляет собой двусторонний дофаминергический путь в мозге, который соединяет субстанцию nigra pars compacta (SNC) в среднем мозге с дорсальным стриатумом (то есть хвостовым ядром и путаменом ) в переднем мозге. Это один из четырех основных дофаминовых путей в мозге и имеет решающее значение для производства движения как части системы, называемой базальной ганглийской моторной петлей . Дофаминергические нейроны этого пути высвобождают дофамин из терминалов аксона, которые синаптируются на колючие нейроны ГАМКергической среды (MSN), также известные как колючие проекционные нейроны (SPNS), [ 1 ] [ 2 ] расположен в стриатуме.
Дегенерация дофаминергических нейронов в SNC является одной из основных патологических особенностей болезни Паркинсона , [ 3 ] приводя к заметному снижению функции дофамина и симптоматическому моторному дефициту болезни Паркинсона, включая гипокинезию , тремор , жесткость и постуральный дисбаланс .
Анатомия
[ редактировать ]Связь между субстанцией nigra pars compacta и дорсальным стриатумом опосредуется через дофаминергические аксоны.
Черная вечеринка компакт (SNC)
[ редактировать ]Субъективная привязка расположена в вентральном среднем мозге каждого полушария. Он имеет две отдельные части: PARS Compacta (SNC) и PARS Reticulata (SNR). PARS Compacta содержит дофаминергические нейроны из клеточной группы A9 , которые образуют нигростриатальный путь, который, поставляя дофамин в стриатум , передает информацию в базальные ганглии . Напротив, Pars reticulata содержит в основном ГАМКергические нейроны.
SNC состоит из тонкой полосы клеток, которые перекрывают SNR и расположены в боковом направлении к группе A10 дофаминергических нейронов в вентральной области сегментарной (VTA), которая образует мезолимбический путь дофаминового пути . SNC легко визуализируется в разделах мозга человека, потому что нейроны дофамина содержат черный пигмент, называемый нейромеланином , который, как известно, накапливается с возрастом. [ 4 ] Тела дофаминергических клеток в SNC плотно упакованы с примерно от 200 000 до 420 000 дофаминовых клеток в SNC человека и от 8000 до 12000 дофаминовых клеток в SNC мыши. [ 5 ] Эти дофаминовые клеточные тела локализованы в одном из двух химически определенных слоев. [ 6 ] Те, кто в верхнем слое (или дорсальном уровне ) содержат связывающий белок, называемый кальбиндином -D28K , который может буферировать уровни кальция внутри клетки, когда он становится слишком высоким или токсичным. Дофаминовые клетки в нижнем слое (или вентральном уровне ) отсутствуют этот белок и более уязвимы к эффектам нейротоксинов (например, MPTP ), которые могут вызвать симптомы, подобные болезни Паркинсона. [ 7 ] [ 8 ] Добальные дофаминовые клетки имеют дендриты , которые излучают горизонтально через PARS Compacta, тогда как дофаминовые клетки вентрального уровня имеют дендриты, которые простираются вентрально в ретикулаты PARS. [ 6 ] [ 9 ]
Дофаминергические аксоны
[ редактировать ]Аксоны (на одной и той из дофаминовых нейронов исходят из первичного дендрита и проецируют ипсилатерально же стороне) через пакет медиального переднего мозга до дорсального стриатума. Существует грубая топографическая корреляция между анатомической локализацией тела дофаминовых клеток в SNC и площадью прекращения в дорсальном стриатуме. Дофаминергические клетки в боковых частях проекта SNC в основном в боковых и каудальных (задних) частях стриатума, тогда как дофаминовые клетки в медиальном SNC проецируют в медиальный стриатум. [ 10 ] [ 9 ] Кроме того, дофаминовые клетки в проекте дорсального уровня к вентромедиальному стриатуму, тогда как нейроны вентрального уровня проецируются на дорсальное хвостовое ядро и путамен. [ 6 ] [ 9 ] В целом, существует большая плотность дофаминергического ввода в дорсолатеральный стриатум. [ 9 ]
Каждый дофаминовый нейрон имеет чрезвычайно большую немиелинизированную аксональную арборизацию, которая может иннервировать до 6% полосатого объема у крысы. [ 11 ] Хотя все дофаминовые клетки SNC проецируют как на стрисомом (или пластырь), так и на матриксные нейрохимические компартменты стриатума, большая часть аксонов территории нейрона дорсального уровня находится в матричном компартменте, в то время как большинство аксонов нейронов вентрального уровня. Стриосомы. [ 6 ] [ 10 ] [ 11 ] Нигростриатальные дофаминовые аксоны также могут привести к коллатералам аксонов, которые проецируются в другие области мозга. Например, некоторые аксоны SNC Нигростриатальные дофамин посылают коллатерали аксонов в педункулопонтиновое ядро , вентральное паллидум , субталамическое ядро , Globus pallidus , миндалина и таламус . [ 6 ] [ 9 ] [ 12 ]
Небольшое количество нейронов дофамина SNC дофамина также проецируется непосредственно в кору, хотя большая часть дофаминергической иннервации коры поступает из соседних нейронов дофамина VTA. [ 9 ]
Дорсальный стриатум
[ редактировать ]Спинной стриатум расположен в подкорковой области переднего мозга . У приматов и других млекопитающих он разделен на переднюю конечность тракта белого вещества , называемого внутренней капсулой [ 13 ] в две части: хвостовое ядро и путамен . [ 14 ] У грызунов внутренняя капсула плохо развита, так что хвостат и путамен не разделены, а образуют одну большую сущность, называемую хвостатным путаменом (ЦП). [ 15 ] [ 16 ] Большинство (около 95%) клеток в дорсальном стриатуме - ГАМКергические средние колючие нейроны (MSN), также известные как колючие проекционные нейроны (SPN). Приблизительно половина из этих MSN содержат рецепторы дофамина D1 и проецируются непосредственно на черту субстанции, чтобы сформировать прямой путь базальных ганглиев, тогда как другая половина экспрессирует рецепторы дофамина D2 , которые косвенно выступают в субстанцию через Nigra через глобус паллидус и ядра субтамика для формирования субстанции через глобус Pallidus и ядра субтамика, которые проецируются в форме субстанции. Косвенный путь базальных ганглиев. [ 17 ] Остальные 5% клеток являются интернейронами , которые являются либо холинергическими нейронами [ 18 ] или один из нескольких типов ГАМКергических нейронов. [ 19 ] Аксоны и дендриты этих интернейронов остаются в стриатуме.
Хвостовое ядро и путамен получают возбуждающую информацию со всех областей коры головного мозга . [ 20 ] Эти глутаматергические входные данные, как правило, расположены топографически так, что путамен в основном получает информацию из сенсомоторной коры, тогда как хвостовое ядро получает информацию в основном из коры ассоциации. [ 20 ] Кроме того, дорсальный стриатум получает возбуждающие входы от других структур мозга, таких как таламус, [ 21 ] и незначительные возбуждающие входные данные из гиппокампа и миндалины .
Дорсальный стриатум содержит нейрохимически определенные компартменты, называемые стриосомами (также известными как пластыри), которые демонстрируют плотное окрашивание μ-опиоидным рецептором, встроенным в матричный компартмент, который содержит более высокую ацетилхолинэстеразу и кальбиндин-D28K. [ 22 ]
Дофаминергические аксонные терминалы синапса нигростриатального пути на GABAergic MSN в дорсальном стриатуме. Они формируют синапсы на корпусе клеточного тела и областях дендритного вала, но в основном на шеях дендритных шипов , которые также получают глутаматергический вход в головы тех же дендритных шипов. [ 1 ]
Функция
[ редактировать ]Основная функция нигростриатального пути состоит в том, чтобы влиять на добровольное движение через базальные моторные петли базальных ганглиев. Наряду с мезолимбическими и мезокортическими дофаминергическими путями, нигростриатальный путь дофамина может также влиять на другие функции мозга, включая познание , [ 23 ] награда и зависимость . [ 24 ] Нигростриатальные дофаминергические нейроны демонстрируют тонизированные и фазовые паттерны активности стрельбы нейрона. Это может привести к различным моделям высвобождения дофамина из терминалов аксона в дорсальном стриатуме, а также от тела клеток (SOMA) и дендритов в SNC и SNR. [ 25 ] [ 26 ] Помимо выпуска дофамина, некоторые аксоны в нигростриатальном пути также могут совместно сдать ГАМК. [ 27 ] [ 28 ]

Нигростриатальный путь влияет на движение через два пути, прямой путь движения и косвенный путь движения . [ 29 ] [ 30 ]
Прямой путь движения
[ редактировать ]Прямой путь участвует в облегчении разыскиваемых движений . Проекции от рецепторов дофамина D1, содержащих средние колючих нейронов в хвостатском ядре и синапсе путаменов на тонически активных GABAergic Cells в субстанции Nigra pars reticulata и внутренний сегмент Globus pallidus (GPI), которые затем проецируют таламус. Поскольку пути стьятотониграла / стриатенопедонкулярного и нигроталамуса являются ингибирующими, активация прямого пути создает общий чистый возбуждающий эффект на таламус и на движение, генерируемое моторной корой.
Непрямой путь движения
[ редактировать ]Косвенный путь участвует в подавлении нежелательного движения . Проекции от рецепторов дофамина D2, содержащих средние колючих нейронов в хвостатском ядре и синапсе путаменов на тонически активных GABAergic Clts во внешнем сегменте Globus pallidus (GPE), который затем проецируется на субстанцию Nigra pars reticulata через возбуждающее подбодное ядро (STN. ) Поскольку пути стриатопаллидного и нигроталамового являются ингибирующими, но путь к субталамусу к нигре является возбуждающим, активация косвенного пути создает общий ингибирующий эффект чистого на таламусе и на движение моторной корой.
Клиническое значение
[ редактировать ]Болезнь Паркинсона
[ редактировать ]Болезнь Паркинсона характеризуется тяжелыми моторными проблемами, в основном гипокинезией , жесткостью, тремор и постуральным дисбалансом. [ 31 ] Потеря дофаминовых нейронов в нигростриатальном пути является одной из основных патологических особенностей болезни Паркинсона. [ 32 ] Дегенерация дофамина, продуцирующих нейроны, в субстанции Nigra pars compacta и комплекс-путамен, приводит к снижению концентрации дофамина в нигростриатальном пути, что приводит к снижению функции и характерным симптомам. [ 33 ] Симптомы заболевания обычно не проявляются до тех пор, пока не будут потеряны 80-90% функции дофамина.
Другая гипотеза предполагает, что болезнь Паркинсона - это дисбаланс между дофамином (DA) и ацетилхолином (ACH) в дорсальном стриатуме, а не только дефицитом дофамина. [ 34 ]
Индуцированная леводопа дискинезия
[ редактировать ]Дискинезии, вызванные леводопой (LID), представляет собой осложнение, связанное с долгосрочным использованием лечения Parkinson L-DOPA , характеризующегося непроизвольным движением и сокращениями мышц. Это расстройство происходит у 90% пациентов после 9 лет лечения. Использование L-DOPA у пациентов может привести к прерыванию нигростриатальных проекций дофамина, а также изменениям в постсинаптических нейронах в базальных ганглиях. [ 35 ]
Шизофрения
[ редактировать ]Преснаптический метаболизм дофамина изменяется при шизофрении . [ 36 ] [ 37 ]
Другие пути дофамина
[ редактировать ]Другие основные пути дофамина включают:
Смотрите также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а беременный Дэвид Смит, А.; Пол Болам, Дж. (1990-07-01). «Нейронная сеть базальных ганглиев, как выявило изучение синаптических связей идентифицированных нейронов». Тенденции в нейронауках . 13 (7): 259–265. doi : 10.1016/0166-2236 (90) 90106-K . ISSN 0166-2236 . PMID 1695400 . S2CID 4018397 .
- ^ Thritsch, NX; Ding, JB; Sabatini, BL (октябрь 2012 г.). «Дофаминергические нейроны ингибируют стриатальный выход путем неканонического высвобождения ГАМК» . Природа . 490 (7419): 262–6. Bibcode : 2012natur.490..262t . doi : 10.1038/nature11466 . PMC 3944587 . PMID 23034651 .
- ^ Диас, Хайме. Как наркотики влияют на поведение. Englewood Cliffs: Prentice Hall, 1996.
- ^ Тыква, Фабио А.; Бас, Эми; Cupaioli, Francesca A.; Ferrari, Emanuele; Зульцер, Дэвид; Казелла, Луиджи; Монетный двор, Луиджи (Janogy 2014). «Нейромеланин человеческой субстанции Nigra: обновление». Исследование нейротоксичности . 25 (1): 13–23. Doi : 10,1007/s12640-013-9435-y . ISSN 1476-3524 . PMID 24155156 . S2CID 8372724 .
- ^ Брихта, Ларс; Грингард, Пол (2014). «Молекулярные детерминанты селективной дофаминергической уязвимости при болезни Паркинсона: обновление» . Границы в нейроанатомии . 8 : 152. DOI : 10.3389/fnana.2014.00152 . ISSN 1662-5129 . PMC 4266033 . PMID 25565977 .
- ^ Jump up to: а беременный в дюймовый и Prensa, L.; Giménez-Amaya, JM; Родитель, а.; Bernácer, J.; Cebrián, C. (2009). «Нигростриатальный путь: аксональная коллатерализация и специфичность компартмента». Рождение, жизнь и смерть дофаминергических нейронов в черной субстанции . С. 49–58. doi : 10.1007/978-3-2111-92660-4_4 . ISBN 978-3-211-92659-8 Полем ISSN 0303-6995 . PMID 20411767 .
{{cite book}}:|journal=игнорируется ( помощь ) - ^ Nemoto, C.; Хида, Т.; Arai, R. (1999-10-30). «Кальретинин и кальбиндин-D28K в дофаминергических нейронах среднего мозга крысы: иммуногистохимическое исследование с тройной маркировкой». Исследование мозга . 846 (1): 129–136. doi : 10.1016/s0006-8993 (99) 01950-2 . ISSN 0006-8993 . PMID 10536220 . S2CID 26684957 .
- ^ Допес-Рейес, Ирия Г.; Рико, Альберто Дж.; Рода, Эльвира; Сьерра, Сальвадор; Пиньятаро, Диего; Ланц, Мария; Суси, Диего; Чанг-Азанкот, Луис; Lanciego, Jose L. (2014). «Содержание кальбиндина и дифференциальная уязвимость эфферентных дофаминергических нейронов среднего мозга в макаках» . Границы в нейроанатомии . 8 : 146. doi : 10.3389/fnana.2014.00146 . ISSN 1662-5129 . PMC 4253956 . PMID 25520629 .
- ^ Jump up to: а беременный в дюймовый и фон Haber, SN (2014-12-12). «Место дофамина в цепи кортико-базальной ганглии» . Нейробиология . 282 : 248–257. doi : 10.1016/j.neuroscience.2014.10.008 . ISSN 1873-7544 . PMC 5484174 . PMID 25445194 .
- ^ Jump up to: а беременный Герфен, кр; Herkenham, M.; Thibault, J. (декабрь 1987 г.). «Неостриатальная мозаика: II. Патч-режиссер мезостриатальные дофаминергические и непаминергические системы» . Журнал нейробиологии . 7 (12): 3915–3934. doi : 10.1523/jneurosci.07-12-03915.1987 . ISSN 0270-6474 . PMC 6569093 . PMID 2891799 .
- ^ Jump up to: а беременный Мацуда, Вакото; Фурута, Такахиро; Накамура, Куичи С.; Хики, Хироюки; Фудзияма, Фумино; Арай, Рёхачи; Канеко, Такеши (2009-01-14). «Одиночные нигростриатальные дофаминергические нейроны образуют широко распространенные и очень плотные аксональные беседы в неостриатуме» . Журнал нейробиологии . 29 (2): 444–453. doi : 10.1523/jneurosci.4029-08.2009 . ISSN 1529-2401 . PMC 6664950 . PMID 19144844 .
- ^ Prensa, L.; Parent, A. (2001-09-15). «Нигростриатальный путь у крысы: одноаксонское исследование взаимосвязи между дорсальными и вентральными нитяльными нейронами и стриатальными компартментами стриата/матрицы» . Журнал нейробиологии . 21 (18): 7247–7260. doi : 10.1523/jneurosci.21-18-07247.2001 . ISSN 1529-2401 . PMC 6762986 . PMID 11549735 .
- ^ Эмос, Марк Кристофер; Agarwal, Sanjeev (2019), «Нейроанатомия, внутренняя капсула» , StatePearls , Statpearls Publishing, PMID 31194338 , получен 2019-10-06
- ^ Май, Юрген К. (14 декабря 2015 г.). Атлас человеческого мозга . Majtanik, Milan ,, Paxinos, George, 1944- (4-е изд.). Амстердам. ISBN 9780128028001 Полем OCLC 934406284 .
{{cite book}}: CS1 Maint: местоположение отсутствует издатель ( ссылка ) - ^ Coizet, Вероник; Хейлброннер, Сара Р.; Карнац, Кэрол; Мейли, Филипп; Lehman, Julia F.; Саваста, Марк; Дэвид, Оивье; Дениау, Жан-Мишель; Groenewegen, Henk J.; Хабер, Сюзанна Н. (8 марта 2017 г.). «Организация передней конечности внутренней капсулы у крысы» . Журнал нейробиологии . 37 (10): 2539–2554. doi : 10.1523/jneurosci.3304-16.2017 . ISSN 1529-2401 . PMC 5354315 . PMID 28159909 .
- ^ Paxinos, George, 1944- (2013-11-07). Мозг крысы в стереотаксических координатах . Уотсон, Чарльз, 1943- (седьмое изд.). Амстердам. ISBN 9780123919496 Полем OCLC 859555862 .
{{cite book}}: CS1 Maint: местоположение отсутствует издатель ( ссылка ) CS1 Maint: Несколько имен: список авторов ( ссылка ) CS1 Maint: числовые имена: список авторов ( ссылка ) - ^ Герфен, Чарльз Р.; Surmeier, D. James (2011). «Модуляция стриатальных проекционных систем с помощью дофамина» . Ежегодный обзор нейробиологии . 34 : 441–466. doi : 10.1146/annurev-neuro-061010113641 . ISSN 1545-4126 . PMC 3487690 . PMID 21469956 .
- ^ Гонсалес, Калинда К.; Смит, Иоланд (сентябрь 2015 г.). «Холинергические интернейроны в дорсальном и вентральном стриатуме: анатомические и функциональные соображения в нормальных и больных состояниях» . Анналы нью -йоркской академии наук . 1349 (1): 1–45. BIBCODE : 2015NYASA1349 .... 1G . doi : 10.1111/nyas.12762 . ISSN 1749-6632 . PMC 4564338 . PMID 25876458 .
- ^ Теппер, Джеймс М.; Коус, Тибор; Ибанез-Сандовал, Освальдо; Tecuapetla, Fatuel; Фауст, Томас У.; Assous, Maxime (2018). «Гетерогенность и разнообразие стриатальных ГАМКергических интернейронов: обновление 2018» . Границы в нейроанатомии . 12 : 91. doi : 10.3389/fnana.2018.00091 . ISSN 1662-5129 . PMC 6235948 . PMID 30467465 .
- ^ Jump up to: а беременный Хабер, Сюзанна Н. (март 2016 г.). «Кортикостриатальная схема» . Диалоги в клинической нейробиологии . 18 (1): 7–21. doi : 10.31887/dcns.2016.18.1/shaber . ISSN 1958-5969 . PMC 4826773 . PMID 27069376 .
- ^ Смит, Иоланд; Гальван, Адриана; Ellender, Tommas J.; Дойг, Натали; Villalba, Rosa M.; Уэрта-Окампо, Icnelia; Вичманн, Томас; Болам, Дж. Пол (2014). «Таламостриатальная система в нормальных и больных состояниях» . Границы в системах нейробиологии . 8 : 5. DOI : 10.3389/fnsys.2014.00005 . ISSN 1662-5137 . PMC 3906602 . PMID 24523677 .
- ^ Brimblecombe, Katherine R.; Крэгг, Стефани Дж. (15 февраля 2017 г.). «Стрисомы и матричные отсеки стриатума: путь через лабиринт от нейрохимии к функционированию» . ACS Химическая нейробиология . 8 (2): 235–242. doi : 10.1021/acschemneuro.6b00333 . ISSN 1948-7193 . PMID 27977131 .
- ^ Ботинок, Натали; Баас, Маттиджс; Ван Гаал, Саймон; Охладно, Рошан; Де Дре, Карстен КВ (июль 2017 г.). «Творческое познание и дофаминергическая модуляция фронто-стриатальных сетей: интегративный обзор и программа исследований». Нейробиологии и биобиоэвиральные обзоры . 78 : 13–23. doi : 10.1016/j.neubiorev.2017.04.007 . ISSN 1873-7528 . PMID 28419830 . S2CID 21315163 .
- ^ Мудрый, RA (октябрь 2009 г.). «Роли нигростриатального-не просто мезокортиколимбика-дофамин в награде и зависимости» . Тенденции в нейронауках . 32 (10): 517–524. doi : 10.1016/j.tins.2009.06.004 . PMC 2755633 . PMID 19758714 .
- ^ Райс, я; Патель, JC; Cragg, SJ (2011-12-15). «Выпуск дофамина в базальных ганглиях» . Нейробиология . 198 : 112–137. doi : 10.1016/j.neuroscience.2011.08.066 . ISSN 1873-7544 . PMC 3357127 . PMID 21939738 .
- ^ Райс, Маргарет Э.; Патель, Джиоти С. (2015-07-05). «Соматодендритный высвобождение дофамина: недавние механистические идеи» . Философские транзакции Королевского общества Лондона. Серия B, биологические науки . 370 (1672): 20140185. DOI : 10.1098/rstb.2014.0185 . ISSN 1471-2970 . PMC 4455754 . PMID 26009764 .
- ^ Трич, Николас Х.; Грейнджер, Адам Дж.; Сабатини, Бернардо Л. (март 2016 г.). «Механизмы и функции совместного высвобождения ГАМК» . Природные обзоры. Нейробиология . 17 (3): 139–145. doi : 10.1038/nrn.2015.21 . ISSN 1471-0048 . PMC 6980171 . PMID 26865019 .
- ^ Трюдо, Луи-Эрик; Хнаско, Томас С.; Уолз-Маккензи, Аса; Моралес, Марисела; Рэйпорт, Стивен; Sulzer, David (2014). «Многоязычная природа дофаминовых нейронов». Дофамин . Прогресс в исследовании мозга. Тол. 211. С. 141–164. doi : 10.1016/b978-0-444-63425-2.00006-4 . ISBN 9780444634252 Полем ISSN 1875-7855 . PMC 4565795 . PMID 24968779 .
- ^ Кравитц, Алексай против.; Крейцер, Анатол С. (июнь 2012 г.). «Стриатальные механизмы, лежащие в основе движения, подкрепления и наказания» . Физиология . 27 (3): 167–177. doi : 10.1152/physiol.00004.2012 . ISSN 1548-9221 . PMC 3880226 . PMID 22689792 .
- ^ Кравитц, Алексай против.; Freeze, Benjamin S.; Паркер, Филип Р.Л.; Кей, Кеннет; Thwin, Myo T.; Deisseroth, Карл; Kreitzer, Anatol C. (2010-07-29). «Регуляция паркинсонского моторного поведения путем оптогенетического контроля схемы базальных ганглиев» . Природа . 466 (7306): 622–626. Bibcode : 2010natur.466..622K . doi : 10.1038/nature09159 . ISSN 1476-4687 . PMC 3552484 . PMID 20613723 .
- ^ Cenci, Angela M (2006). «Пост- против пресинаптического пластика в дискинезии, вызванной L-допа» (PDF) . Журнал нейрохимии . 99 (2): 381–92. doi : 10.1111/j.1471-4159.2006.04124.x . PMID 16942598 . S2CID 9649270 .
- ^ Deumens, Ronald (21 июня 2002 г.). «Моделирование болезни Паркинсона у крыс: оценка поражений 6-OHDA нигростриатального пути». Экспериментальная неврология . 175 (2): 303–17. doi : 10.1006/exnr.2002.7891 . PMID 12061862 . S2CID 2770493 .
- ^ Грогер, Адрейн (8 января 2014 г.). «Снижение дофамина в черной субстанции у пациентов с болезнью Паркинсона, подтвержденного магнитно -резонансной визуализацией in vivo» . Plos один . 9 (1): E84081. BIBCODE : 2014PLOSO ... 984081G . doi : 10.1371/journal.pone.0084081 . PMC 3885536 . PMID 24416192 .
- ^ Спелманн, Рейнер; Шталь, Стивенм. (1976-04-03). «Дисбаланс ацетилхолина дофамина при болезни Паркинсона: возможный регенеративный разрастание терминалов холинергических аксонов» . Lancet . Первоначально опубликовано как том 1, выпуск 7962. 307 (7962): 724–726. doi : 10.1016/s0140-6736 (76) 93095-6 . ISSN 0140-6736 . PMID 56538 . S2CID 26024410 .
- ^ Niethammer, Martin (май 2012 г.). «Функциональное нейровизуализацию при болезни Паркинсона» . Перспективы Cold Spring Harbor в медицине . 2 (5): A009274. doi : 10.1101/cshperspect.a009274 . PMC 3331691 . PMID 22553499 .
- ^ Фусар-Поли, Паоло; Мейер-Линденберг, Андреас (1 января 2013 г.). «Стриатальный пресинаптический дофамин при шизофрении, часть II: Мета-анализ [(18) F/(11) C] -допа ПЭТ-исследования» . Бюллетень шизофрении . 39 (1): 33–42. doi : 10.1093/schbul/sbr180 . ISSN 1745-1701 . PMC 3523905 . PMID 22282454 .
- ^ Вайнштейн, Джоди Дж.; Чохан, Мухаммед О.; Слифштейн, Марк; Кегелес, Лоуренс С.; Мур, Холли; Аби-Даргхам, Анисса (1 января 2017 г.). «Специфичные для пути дофаминовые аномалии при шизофрении» . Биологическая психиатрия . 81 (1): 31–42. doi : 10.1016/j.biopsych.2016.03.2104 . ISSN 1873-2402 . PMC 5177794 . PMID 27206569 .