Рибонуклеотиды
В биохимии рибонуклеотид — это нуклеотид, содержащий рибозу в качестве пентозного компонента. Его считают молекулярным предшественником нуклеиновых кислот . Нуклеотиды являются основными строительными блоками ДНК и РНК . Рибонуклеотиды сами по себе являются основными мономерными строительными блоками РНК. Дезоксирибонуклеотиды , образующиеся путем восстановления рибонуклеотидов с помощью фермента рибонуклеотидредуктазы (RNR), являются важными строительными блоками ДНК. [ 1 ] Между дезоксирибонуклеотидами ДНК и рибонуклеотидами РНК есть несколько различий. Последовательные нуклеотиды связаны между собой фосфодиэфирными связями.
Рибонуклеотиды также используются в других клеточных функциях. Эти специальные мономеры используются как в регуляции клеток, так и в передаче сигналов клеткам , как это видно в аденозинмонофосфате ( АМФ ). Кроме того, рибонуклеотиды могут превращаться в аденозинтрифосфат ( АТФ ), энергетическую валюту в организмах. могут превращаться в циклический аденозинмонофосфат ( циклический АМФ ) для регулирования гормонов в организме. Рибонуклеотиды также [ 1 ] В живых организмах наиболее распространенными основаниями рибонуклеотидов являются аденин (А), гуанин (G), цитозин (С) или урацил (U). Азотистые основания подразделяются на два исходных соединения: пуриновые и пиримидиновые .

Структура
[ редактировать ]Общая структура
[ редактировать ]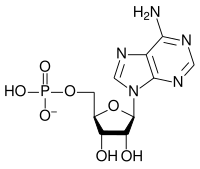
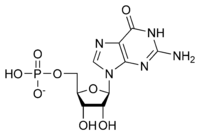


Общая структура рибонуклеотида состоит из фосфатной группы, группы сахара рибозы и нуклеинового основания, в котором азотистое основание может представлять собой аденин, гуанин, цитозин или урацил. Без фосфатной группы состав азотистого основания и сахара известен как нуклеозид. Взаимозаменяемые азотистые азотистые основания происходят от двух исходных соединений: пурина и пиримидина. Нуклеотиды являются гетероциклическими соединениями , то есть содержат в качестве членов своих колец как минимум два разных химических элемента. [ нужна ссылка ]
И РНК, и ДНК содержат два основных пуриновых основания: аденин (А) и гуанин (G), а также два основных пиримидина. И в ДНК, и в РНК одним из пиримидинов является цитозин (С). Однако ДНК и РНК различаются по второму основному пиримидину. ДНК содержит тимин (Т), а РНК — урацил (U). Есть несколько редких случаев, когда тимин действительно встречается в РНК, а урацил - в ДНК. [ 1 ]
Вот 4 основных рибонуклеотида (рибонуклеозид-5'-монофосфат), которые являются структурными единицами РНК.
| Нуклеотид | Символы | Нуклеозид |
|---|---|---|
| Аденилат (аденозин-5'-монофосфат) | А, АМФ | Аденозин |
| Гуанилат (гуанозин-5'-монофосфат) | Г, ГМП | Гуанозин |
| Уридилат (уридин-5'-монофосфат) | У, УМП | Уридин |
| Цитидилат (цитидин-5'-монофосфат) | С, КМП | Цитидин |
ДНК-дезоксирибонуклеотиды в сравнении с РНК-рибонуклеотидами
[ редактировать ]В рибонуклеотидах сахарным компонентом является рибоза, а в дезоксирибонуклеотидах сахарным компонентом является дезоксирибоза. Вместо гидроксильной группы у второго углерода в кольце рибозы она заменена атомом водорода. [ 2 ]
Оба типа пентоз в ДНК и РНК находятся в форме β-фуранозы (замкнутое пятичленное кольцо) и определяют идентичность нуклеиновой кислоты. ДНК определяется как содержащая нуклеиновую кислоту 2'-дезоксирибозы, тогда как РНК определяется как содержащая нуклеиновую кислоту рибозы. [ 1 ]
В некоторых случаях ДНК и РНК могут содержать некоторые второстепенные основания. Метилированные формы основных оснований наиболее распространены в ДНК. В вирусной ДНК некоторые основания могут быть гидроксиметилированными или глюкозилированными. В РНК чаще встречаются минорные или модифицированные основания. Некоторые примеры включают гипоксантин, дигидроурацил, метилированные формы урацила, цитозин и гуанин, а также модифицированный нуклеозид псевдоуридин. [ 3 ] Также наблюдались нуклеотиды с фосфатными группами в положениях, отличных от 5'-углерода. Примеры включают рибонуклеозид-2',3'-циклические монофосфаты, которые являются изолируемыми промежуточными соединениями, и рибонуклеозид-3'-монофосфаты, которые являются конечными продуктами гидролиза РНК определенными рибонуклеазами. Другие варианты включают аденозин-3',5'-циклический монофосфат (цАМФ) и гуанозин-3',5'-циклический монофосфат (цГМФ). [ 4 ]
Связывание последовательных нуклеотидов
[ редактировать ]Рибонуклеотиды соединяются вместе, образуя цепи РНК посредством фосфодиэфирных связей . 5'-фосфатная группа одного нуклеотида связана с 3'-гидроксильной группой следующего нуклеотида, образуя основу из чередующихся фосфатных и пентозных остатков. На каждом конце полинуклеотида нет фосфодиэфирной связи. [ 5 ] Фосфодиэфирные связи образуются между рибонуклеотидами под действием фермента РНК-полимеразы . Цепь РНК синтезируется от 5'-конца к 3'-концу, поскольку 3'-гидроксильная группа последнего рибонуклеотида в цепи действует как нуклеофил и начинает гидрофильную атаку на 5'-трифосфат входящего рибонуклеотида, высвобождая пирофосфат как побочный продукт [ 6 ] продукт. Из-за физических свойств нуклеотидов основа РНК очень гидрофильна и полярна. При нейтральном pH нуклеиновые кислоты имеют высокий заряд, поскольку каждая фосфатная группа несет отрицательный заряд. [ 7 ]
И ДНК, и РНК построены из нуклеозидфосфатов, также известных как мононуклеотидные мономеры, которые термодинамически менее склонны к объединению, чем аминокислоты. Фосфодиэфирные связи при гидролизе выделяют значительное количество свободной энергии. Следовательно, нуклеиновые кислоты имеют тенденцию спонтанно гидролизоваться в мононуклеотиды. Предшественниками РНК являются ГТФ, ЦТФ, УТФ и АТФ, который является основным источником энергии в реакциях группового переноса. [ 8 ]
Функция
[ редактировать ]Предшественники дезоксирибонуклеотидов
[ редактировать ]Ученые полагают, что РНК возникла раньше ДНК. [ 9 ]
Восстановление рибонуклеотидов до дезоксирибонуклеотидов катализируется рибонуклеотидредуктазой . Рибонуклеотидредуктаза (РНР) является важным ферментом для всех живых организмов, поскольку она отвечает за последний этап синтеза четырех дезоксирибонуклеотидов (дНТФ), необходимых для репликации и восстановления ДНК. [ 10 ] Для реакции также необходимы два других белка: тиоредоксин и тиоредоксинредуктаза . Рибонуклеозиддифосфат (НДФ) восстанавливается тиоредоксином до дезоксирибонуклеозиддифосфата (дНТФ).
Общая реакция такая:
Рибонуклеозиддифосфат + НАДФН + ЧАС + → Дезоксирибонуклеозиддифосфат + НАДП + + Н 2 О
[ 11 ]
Чтобы проиллюстрировать это уравнение, dATP и dGTP синтезируются из ADP и GDP соответственно. Сначала они восстанавливаются с помощью RNR, а затем фосфорилируются нуклеозиддифосфаткиназами до dATP и dGTP. Рибонуклеотидредуктаза контролируется аллостерическими взаимодействиями. Как только dATP связывается с рибонуклеотидредуктазой, общая каталитическая активность фермента снижается, поскольку это означает избыток дезоксирибонуклеотидов. Это ингибирование по принципу обратной связи прекращается после связывания АТФ. [ 12 ]
Дискриминация рибонуклеотидов
[ редактировать ]Во время синтеза ДНК ДНК-полимеразы должны отбирать рибонуклеотиды, присутствующие на гораздо более высоких уровнях по сравнению с дезоксирибонуклеотидами. Крайне важно обеспечить селективность, поскольку репликация ДНК должна быть точной для поддержания генома организма. Показано, что активные центры ДНК-полимераз Y-семейства отвечают за поддержание высокой селективности в отношении рибонуклеотидов. [ 13 ] Большинство ДНК-полимераз также способны исключать рибонуклеотиды из их активного сайта посредством объемистого остатка боковой цепи, который может стерически блокировать 2'-гидроксильную группу рибозного кольца. Однако многие ядерные репликативные и репарационные ДНК-полимеразы включают в ДНК рибонуклеотиды. [ 14 ] [ 15 ] предполагая, что механизм исключения не идеален. [ 16 ]
Синтез
[ редактировать ]Синтез рибонуклеотидов
[ редактировать ]Рибонуклеотиды могут синтезироваться в организмах из более мелких молекул по пути de novo или перерабатываться по пути утилизации. В случае пути de novo как пурины, так и пиримидины синтезируются из компонентов, полученных из предшественников аминокислот, рибозо-5-фосфатов, CO 2 и НХ 3 . [ 17 ] [ 12 ]

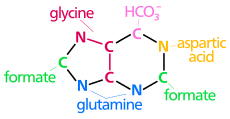 |
Биосинтетическое пуринового кольца происхождение атомов N 1 возникает из аминной группы Asp С 2 и C 8 происходят из формиата № 3 и N 9 вносят амидная группа Gln. С 4 , С 5 и N 7 происходят от Gly C 6 происходит от HCO − 3 (CO 2 ) |
Биосинтез пуриновых нуклеотидов de novo довольно сложен и состоит из нескольких ферментативных реакций. Используя пятикольцевую структуру сахара в качестве основы, пуриновое кольцо строится по несколько атомов за один раз в ходе одиннадцатиэтапного процесса, который приводит к образованию инозината (ИМФ). По сути, ИМФ превращается в пуриновые нуклеотиды, необходимые для синтеза нуклеиновых кислот. [ 1 ]
Путь начинается с превращения рибозо-5-фосфата (R5P) в фосфорибозилпирофосфат (PRPP) под действием фермента рибозо-фосфатдифосфокиназы (PRPS1). PRPP затем превращается в 5-фосфорибозиламин (5-PRA), поскольку глутамин отдает аминогруппу C-1 PRPP. В реакции конденсации фермент GAR-синтетаза вместе с глицином и АТФ активирует глицинкарбоксилазную группу 5-PRA с образованием глицинамидрибонуклеотида (GAR). Кофермент N10-формил-ТГФ вместе с ферментом GAR-трансформилазой затем отдает одноуглеродную единицу аминогруппе глицину GAR с последующим добавлением глутамина ферментом FGAR-амидотрансферазой, что приводит к образованию формилглицинамидинрибонуклеотида (FGAM). ). Дегидратация FGAM ферментом FGAM циклазой приводит к замыканию имидазольного кольца в виде 5-аминоимидазолрибонуклеотида (AIR). Карбоксильная группа присоединяется к AIR с помощью N5-CAIR-синтетазы с образованием N5-карбоксиминоимидазолрибонуклеотида (N5-CAIR), который затем превращается в карбоксиминоимидазолрибонуклеотид (CAIR) с помощью фермента N5-CAIR мутазы. Фермент SAICAR-синтетаза вместе с аминогруппой аспартата образует амидную связь с образованием N-сукцинил-5-аминоимидазол-4-карбоксамид рибонуклеотида (SAICAR). Продолжая этот путь, удаление углеродного скелета аспартата лиазой SAICAR приводит к образованию 5-аминоимидазол-4-карбоксамид рибонуклеотида (AICAR). Фермент трансформилаза AICAR способствует окончательному переносу углерода от N10-формилтетрагидрофолата с образованием N-формиламиноимидазол-4-карбоксамид рибонуклеотида (FAICAR). Наконец, закрытие второй кольцевой структуры осуществляется с помощью IMP-синтазы с образованием IMP, где судьба IMP приведет к образованию пуринового нуклеотида. [ 1 ]

Синтез пиримидиновых нуклеотидов — гораздо более простой процесс. Образование пиримидинового кольца начинается с превращения аспартата в N-карбамоиласпартат путем реакции конденсации с карбамоилфосфатом. Дигидрооротаза и дигидрооротаза-дегидрогеназа затем превращают N-карбамоиласпартат в оротат. Оротат ковалентно связан с фосфорибозилпирофосфатом (PRPP) с помощью оротатфосфорибизол-трансферазы, образуя оротидинмонофосфат (OMP). За OMP следует декарбоксилирование оротидилдекарбоксилазой с образованием рибонуклеотидной структуры уридилата (UMP). UMP затем может быть преобразован в уридин-5'-трифосфат (UTP) с помощью реакции двух киназ. Образование цитидин-5'-трифосфата (CTP) из UTP может быть достигнуто с помощью цитидилатсинтетазы с помощью промежуточного ацилфосфата. [ 1 ]
Пребиотический синтез рибонуклеотидов
[ редактировать ]Чтобы понять, как возникла жизнь , необходимы знания о химических путях, которые позволяют формировать ключевые строительные блоки жизни в вероятных пребиотических условиях . Согласно гипотезе мира РНК, в примитивном супе присутствовали свободно плавающие рибонуклеотиды. Это были фундаментальные молекулы, которые последовательно соединялись, образуя РНК . Молекулы, столь сложные, как РНК, должны были возникнуть из небольших молекул, реакционная способность которых определялась физико-химическими процессами. РНК состоит из пуриновых и пиримидиновых нуклеотидов, оба из которых необходимы для надежной передачи информации и, следовательно, для дарвиновского естественного отбора и эволюции . Синтез активированных пиримидинрибонуклеотидов был продемонстрирован в вероятных пребиотических условиях. [ 18 ] Исходными материалами для синтеза ( цианамид , цианоацетилен , гликольальдегид , глицеральдегид и неорганический фосфат ) считались вероятными молекулами пребиотического сырья. [ 18 ] Нам и др. продемонстрировали прямую конденсацию нуклеиновых оснований с рибозой с образованием рибонуклеозидов в водных микрокапельках, что является ключевым этапом, ведущим к образованию РНК. [ 19 ] Кроме того, Becker et al. представили возможный пребиотический процесс синтеза пиримидиновых и пуриновых рибонуклеотидов с использованием циклов влажно-сухой. [ 20 ]
История
[ редактировать ]
До появления знаковой статьи Джеймса Уотсона и Фрэнсиса Крика , в которой подробно описывалась структура ДНК по изображению Розалинды Франклин , рентгеновскому кристаллографическому в ее открытие также внесли свой вклад несколько ученых-историков. [ 21 ] Фридрих Мишер , швейцарский врач, который в 1869 году первым выделил и идентифицировал нуклеиновое вещество из ядер лейкоцитов, которое он позже назвал «нуклеином», проложив путь к открытию ДНК. [ 22 ] После работы Мишера немецкий биохимик Альбрехт Коссель в 1878 году выделил небелковые компоненты «нуклеина» и открыл пять нуклеиновых оснований, присутствующих в нуклеиновых кислотах: аденин, цитозин, гуанин, тимин и урацил. [ 23 ] Хотя благодаря этим ранним открытиям о нуклеиновых кислотах стали известны некоторые фундаментальные факты, их структура и функция оставались загадкой.
Лишь открытие нуклеотидов в 1919 году Фебусом Левеном , русско-литовским биохимиком, вновь открыло врата открытия ДНК. Левен впервые определил, что углеводный компонент, присутствующий в дрожжевой РНК , на самом деле представляет собой рибозу . Однако только после его открытия того, что углеводный компонент нуклеиновой кислоты тимуса также представляет собой сахар, но не имеет одного атома кислорода, называемого дезоксирибозой , его открытие получило широкую оценку научного сообщества. В конце концов Левен смог определить правильный порядок соединения компонентов РНК и ДНК, фосфатно-сахарную единицу, которую он позже назвал нуклеотидом . Хотя Левен хорошо понимал порядок расположения нуклеотидных компонентов, структура расположения нуклеотидов в пространстве и их генетический код в первые годы его карьеры все еще оставались загадкой. [ 24 ]
См. также
[ редактировать ]- Рибонуклеозиды или рибозиды
Ссылки
[ редактировать ]- ^ Jump up to: а б с д и ж г Нельсон, Дэвид Л.; Ленинджер, Альберт Л.; Кокс, Майкл М. (2008). Ленингерские принципы биохимии (5-е изд.). У. Х. Фриман. стр. 272–3. ISBN 978-0-7167-7108-1 .
- ^ Ньюхолм, Эрик А.; Лич, Энтони Р.; Совет, Мэри (2008). Функциональная биохимия в здоровье и болезни: метаболическая регуляция в здоровье и болезни (2-е изд.). Хобокен, Нью-Джерси: Уайли. ISBN 978-0-471-98820-5 .
- ^ Дас, Дебаджьоти (2010). Биохимия . Бимал Кумар Дхур из Academic Publishers.
- ^ Кокс, Майкл М.; Нельсон, Дэвид Л. (2008). Принципы биохимии . У. Х. Фриман. ISBN 978-1-4292-2263-1 . OCLC 216940502 .
- ^ Раймонд, Кеннет В. (2010). Общая, органическая и биологическая химия: комплексный подход (3-е изд.). Уайли. ISBN 978-0-470-55124-0 . ОСЛК 699600111 .
- ^ Шехтер, Моселио; Ледерберг, Джошуа, ред. (2004). Настольная энциклопедия микробиологии (1-е изд.). Амстердам: Эльзевир. ISBN 0-12-621361-5 . OCLC 1055874153 .
- ^ Тернер, Фил; и др. (2005). Молекулярная биология . Мгновенные заметки (3-е изд.). CRC, Тейлор и Фрэнсис. ISBN 0-415-35167-7 . OCLC 61745541 .
- ^ Нельсон, Дэвид (2008). Ленингерские принципы биохимии . WH Freeman and Co., стр. 274–275.
- ^ Чаухан, Ашок К.; Варма, Аджит, ред. (2009). Учебник молекулярной биотехнологии . Нью-Дели: Международный паб IK. Дом. ISBN 978-93-80026-37-4 .
- ^ Сендра Мдел, М; Хуарес, А; Торрентс, Э (2012). «Биопленка изменяет экспрессию генов рибонуклеотидредуктазы в Escherichia coli» . ПЛОС ОДИН . 7 (9): е46350. Бибкод : 2012PLoSO...746350C . дои : 10.1371/journal.pone.0046350 . ПМЦ 3458845 . ПМИД 23050019 .
- ^ Кэмпбелл, Мэри К.; Фаррелл, Шон О. (2009). Биохимия (7-е изд.). Бельмонт, Калифорния: Обучение Брукса/Коула Сенгеджа. ISBN 978-0-8400-6858-3 .
- ^ Jump up to: а б Берг, Дж. М.; Тимочко, Дж.Л.; Страйер, Л. (2002). «§25.2 Пуриновые основания могут быть синтезированы компанией de Novo или переработаны с помощью путей утилизации». Биохимия . У. Х. Фриман. ISBN 9780716730514 . OCLC 48055706 .
- ^ Кируак, Кевин Н.; Суо, Зукай; Линг, Хонг (1 апреля 2011 г.). «Структурный механизм дискриминации рибонуклеотидов ДНК-полимеразой Y-семейства». Журнал молекулярной биологии . 407 (3): 382–390. дои : 10.1016/j.jmb.2011.01.037 . ПМИД 21295588 .
- ^ Ник МакЭлхинни, ЮАР; Кумар, Д; Кларк, AB; Ватт, Д.Л.; Уоттс, Британская Колумбия; Лундстрём, Е.Б.; Йоханссон, Э; Чабес, А; Кункель, Т.А. (октябрь 2010 г.). «Нестабильность генома из-за включения рибонуклеотидов в ДНК» . Химическая биология природы . 6 (10): 774–81. дои : 10.1038/nchembio.424 . ПМЦ 2942972 . ПМИД 20729855 .
- ^ Ник МакЭлхинни, ЮАР; Уоттс, Британская Колумбия; Кумар, Д; Ватт, Д.Л.; Лундстрём, Е.Б.; Бургеры, премьер-министр; Йоханссон, Э; Чабес, А; Кункель, Т.А. (16 марта 2010 г.). «Обильное включение рибонуклеотидов в ДНК дрожжевыми репликативными полимеразами» . Труды Национальной академии наук Соединенных Штатов Америки . 107 (11): 4949–54. Бибкод : 2010PNAS..107.4949N . дои : 10.1073/pnas.0914857107 . ПМК 2841928 . ПМИД 20194773 .
- ^ Касивисванатан, Р; Коупленд, WC (9 сентября 2011 г.). «Дискриминация рибонуклеотидов и обратная транскрипция митохондриальной ДНК-полимеразой человека» . Журнал биологической химии . 286 (36): 31490–500. дои : 10.1074/jbc.M111.252460 . ПМЦ 3173122 . ПМИД 21778232 .
- ^ Нельсон, Ленинджер и Кокс, 2008 , стр. 881–894.
- ^ Jump up to: а б Владелец М.В., Герланд Б., Сазерленд Дж.Д. (май 2009 г.). «Синтез активированных пиримидинрибонуклеотидов в пребиотически приемлемых условиях». Природа . 459 (7244): 239–42. дои : 10.1038/nature08013 . ПМИД 19444213 .
- ^ Нам И, Нам Х.Г., Заре Р.Н. (январь 2018 г.). «Абиотический синтез пуриновых и пиримидиновых рибонуклеозидов в водных микрокапельках» . Proc Natl Acad Sci США . 115 (1): 36–40. дои : 10.1073/pnas.1718559115 . ПМЦ 5776833 . ПМИД 29255025 .
- ^ Беккер С., Фельдманн Дж., Видеманн С., Окамура Х., Шнайдер С., Иван К., Крисп А., Росса М., Аматов Т., Карелл Т. (октябрь 2019 г.). «Единый пребиотически возможный синтез пиримидиновых и пуриновых РНК-рибонуклеотидов». Наука . 366 (6461): 76–82. дои : 10.1126/science.aax2747 . ПМИД 31604305 .
- ^ Уотсон, доктор медицинских наук; Крик, FH (25 апреля 1953 г.). «Молекулярная структура нуклеиновых кислот; структура нуклеиновой кислоты дезоксирибозы». Природа . 171 (4356): 737–8. Бибкод : 1953Natur.171..737W . дои : 10.1038/171737a0 . ПМИД 13054692 . S2CID 4253007 .
- ^ Дам, Р. (январь 2008 г.). «Открытие ДНК: Фридрих Мишер и первые годы исследований нуклеиновых кислот». Генетика человека . 122 (6): 565–81. дои : 10.1007/s00439-007-0433-0 . ПМИД 17901982 . S2CID 915930 .
- ^ Джонс, Мэн (сентябрь 1953 г.). «Альбрехт Коссель, биографический очерк» . Йельский журнал биологии и медицины . 26 (1): 80–97. ПМК 2599350 . ПМИД 13103145 .
- ^ Левен, Феб (1919). «Строение нуклеиновой кислоты дрожжей IV. Гидролиз аммиака». Журнал биологической химии . 40 (2): 415–424. дои : 10.1016/S0021-9258(18)87254-4 .