Ауреузидинсинтаза
| Ауреузидинсинтаза | |||
|---|---|---|---|
| Идентификаторы | |||
| Номер ЕС. | 1.21.3.6 | ||
| Номер CAS. | 320784-48-3 | ||
| Базы данных | |||
| ИнтЭнк | вид IntEnz | ||
| БРЕНДА | БРЕНДА запись | ||
| ЭксПАСи | Просмотр NiceZyme | ||
| КЕГГ | КЕГГ запись | ||
| МетаЦик | метаболический путь | ||
| ПРЯМОЙ | профиль | ||
| PDB Структуры | RCSB PDB PDBe PDBsum | ||
| |||
Ауреусидинсинтаза ( EC 1.21.3.6 , AmAS1 ) представляет собой фермент с систематическим названием 2',4,4',6'-тетрагидроксихалкон 4'-O-бета-D-глюкозид:кислород оксидоредуктаза . [ 1 ] [ 2 ] [ 3 ] [ 4 ]
Ауреузидинсинтаза выполняет две основные ферментативные задачи: гидроксилирование в положении 3 B-кольца халконов и окислительную циклизацию халконов с образованием ауронов . [ 2 ] Модифицированные халконы обычно представляют собой глюкозилированные 2',4,4',6'-тетрагидроксихалкон (THC) и 2',3,4,4',6'-пентагидроксихалкон (PHC). [ 2 ] Эти ауроны, особенно аурезидин, образуют пигменты, отвечающие за окраску цветов. [ 1 ] Эти пигменты, возможно, были разработаны для привлечения и направления пчел к опылению . [ 5 ] но они также обеспечивают защиту от вирусов , вредителей и грибков . [ 6 ]
Структура фермента
[ редактировать ]Ауреусидинсинтаза представляет собой мономерный гликопротеин массой 39 кДа, содержащий биядерную медь . [ 1 ] Добавление фенилтиомочевины , которая конкурентно связывается с биядерной медью, [ 7 ] подавляет продуктивность фермента в целом. [ 2 ] Поэтому вполне вероятно, что активный центр содержит биядерную медь.
Ауреузидинсинтаза гомологична растений полифенолоксидазе (PPO). [ 1 ] но содержит некоторые существенные изменения. В то время как ППО имеет высококонсервативную N-концевую аминокислотную последовательность, облегчающую транспортировку в просвет пластиды, у ауреузидинсинтазы эта последовательность отсутствует. [ 1 ] и, таким образом, не локализован в плазмиде. Подобно PPO, [ 8 ] ауреусидинсинтаза, вероятно, сначала синтезируется в виде более крупного белка размером ~60 кДа, а затем подвергается протеолитическому расщеплению для удаления транспортных групп. [ 1 ]
Ферментативный механизм
[ редактировать ]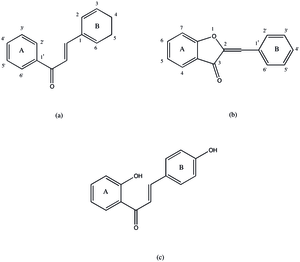
Ауреузидинсинтаза катализирует образование ауронов из халконов посредством гидроксилирования и окислительной циклизации. К этому классу реакций относятся:
- (1) 2',4,4',6'-тетрагидроксихалкон 4'-О-бета-D-глюкозид + O 2 ауреусидин 6-О-бета-D-глюкозид + H 2 O
- (2) 2',3,4,4',6'-пентагидроксихалкон 4'-O-бета-D-глюкозид + 1/2 O 2 ауреусидин 6-О-бета-D-глюкозид + H 2 O
- (3) 2',3,4,4',6'-пентагидроксихалкон 4'-О-бета-D-глюкозид + O 2 брактеатин 6-О-бета-D-глюкозид + H 2 O
Хотя белок назван в честь желтого пигмента ауреусидина, который он часто производит, он может продуцировать ряд аналогичных ауронов, включая сульфуретин, брактеатин и 3',4',5',6-тетрагидроксиаурон. Чтобы модифицировать халкон в аурон, халкон должен подвергнуться окислительной циклизации с образованием пятичленного гетероцикла , конденсированного с a-кольцом аурона. Этот этап может не продолжаться, если 3-я позиция B-кольца халкона не насыщена кислородом. Исходя из этого, а также из гомологии белка с PPO, предлагаемый в настоящее время механизм ауреузидинсинтазы показан на рис. 2. Первый этап процесса приводит к гидроксилированию в положении 3 (для ТГК) и окислению до дикетонового кольца. Обычно считается, что этот механизм такой же, как и у тирозиназы . [ 9 ] Это предположение основано на гомологии двух структур и схожей функциональности. Затем этот продукт подвергается окислительной циклизации, а затем изомеризации с образованием конечного продукта, но возможно, что эти этапы происходят вне фермента . [ 2 ] Этот механизм может производить ауроны только с 3',4'-дигидрокси- или 3',4',5'-тригидрокси-функционализацией, но сообщалось об ауронах с одной гидроксильной группой или без нее в B-кольце. Неясно, связано ли образование ауронов с альтернативным механизмом или с другим белком. [ 10 ]

Биологическая функция
[ редактировать ]Ауреусидин — это растительный флавоноид , который обеспечивает желтую окраску у некоторых растений, включая львиный зев и космос. [ 1 ] Он также обеспечивает различные защитные свойства от болезней и паразитов. [ 6 ] Аурезидинсинтаза активна только в вакуоли и транспортируется непосредственно из эндоплазматического ретикулума в вакуоль через тельца Гольджи. [ 4 ] Исследования in vitro показали, что синтез ауронов происходит гораздо быстрее, когда халкон сначала глюкозилируется, [ 2 ] показали исследования in vivo , что желтая окраска не проявляется без совместной экспрессии УДФ-глюкуронозилтрансферазы UGT88D3, которая сначала глюкозилирует халкон. [ 4 ] Это глюкозилирование способствует выработке ауронов путем метаболического направления модифицированных халконов в вакуоль. [ 11 ]
Промышленная значимость
[ редактировать ]Генетическая модификация цветковых растений для придания окраски, невозможной при естественной селекции, была одной из главных целей цветочной индустрии . [ 12 ] Ауреузидинсинтаза была введена в растения с естественными синими цветками для образования новых трансгенных желтых цветков у Torenia . видов [ 4 ] Это достигается за счет совместной экспрессии ауреузидинсинтазы и УДФ-глюкозо:халкон-4'-О-глюкозилтрансферазы в цветах и использования РНК-интерференции для блокирования экспрессии продукции естественного пигмента . [ 4 ]
Помимо своей важности для цветоводческой промышленности, ауреузидинсинтаза является относительно новой целью для биомедицинских исследований. [ 13 ] Было обнаружено, что ауроны обладают антиоксидантным , антибактериальным и противораковым действием. [ 14 ] создание трансгенных листьев салата и табака с улучшенными антиоксидантными свойствами. Ауреузидинсинтаза представляет особую привлекательность при создании генетически модифицированных растений, которые могут придавать лечебные свойства, и уже продемонстрировано [ 15 ]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с д и ж г Накаяма Т., Ёнекура-Сакакибара К., Сато Т., Кикучи С., Фукуи Ю., Фукучи-Мизутани М., Уэда Т., Накао М., Танака Ю., Кусуми Т., Нишино Т. (ноябрь 2000 г.). «Ауреусидинсинтаза: гомолог полифенолоксидазы, ответственный за окраску цветов». Наука . 290 (5494): 1163–6. Бибкод : 2000Sci...290.1163N . дои : 10.1126/science.290.5494.1163 . ПМИД 11073455 .
- ^ Перейти обратно: а б с д и ж Накаяма Т., Сато Т., Фукуи Ю., Ёнекура-Сакакибара К., Хаяси Х., Танака Ю., Кусуми Т., Нишино Т. (июнь 2001 г.). «Анализ специфичности и механизм синтеза ауронов, катализируемый ауреузидинсинтазой, гомологом полифенолоксидазы, ответственным за окраску цветов» . Письма ФЭБС . 499 (1–2): 107–11. дои : 10.1016/S0014-5793(01)02529-7 . ПМИД 11418122 .
- ^ Сато Т., Накаяма Т., Кикучи С., Фукуи Ю., Ёнекура-Сакакибара К., Уэда Т., Нишино Т., Танака Ю., Кусуми Т. (январь 2001 г.). «Ферментативное образование ауронов в экстрактах цветков львиного зева желтого». Наука о растениях . 160 (2): 229–236. дои : 10.1016/s0168-9452(00)00385-x . ПМИД 11164594 .
- ^ Перейти обратно: а б с д и Оно Э, Фукучи-Мизутани М, Накамура Н, Фукуи Ю, Ёнекура-Сакакибара К, Ямагути М, Накаяма Т, Танака Т, Кусуми Т, Танака Ю (июль 2006 г.). «Желтые цветы, возникающие в результате экспрессии пути биосинтеза аурона» . Труды Национальной академии наук Соединенных Штатов Америки . 103 (29): 11075–80. Бибкод : 2006PNAS..10311075O . дои : 10.1073/pnas.0604246103 . ПМК 1544175 . ПМИД 16832053 .
- ^ Лунау К., Вахт С., Читтка Л. (1996). «Выбор цвета наивных шмелей и его значение для восприятия цвета». Журнал сравнительной физиологии А. 178 (4). дои : 10.1007/BF00190178 . S2CID 21435915 .
- ^ Перейти обратно: а б Буменджель А. (декабрь 2003 г.). «Ауроны: подкласс флавонов с многообещающим биологическим потенциалом». Современная медицинская химия . 10 (23): 2621–30. дои : 10.2174/0929867033456468 . ПМИД 14529476 .
- ^ Клабунде Т., Эйкен С., Саккеттини Дж. К., Кребс Б. (декабрь 1998 г.). «Кристаллическая структура растительной катехолоксидазы, содержащей димедный центр». Структурная биология природы . 5 (12): 1084–90. дои : 10.1038/4193 . ПМИД 9846879 . S2CID 29946865 .
- ^ Робинсон С.П., Сухой I (май 1992 г.). «Полифенолоксидаза листьев широкой фасоли представляет собой белок массой 60 килодальтон, чувствительный к протеолитическому расщеплению» . Физиология растений . 99 (1): 317–323. дои : 10.1104/стр.99.1.317 . ПМЦ 1080442 . ПМИД 16668868 .
- ^ Санчес-Феррер А., Родригес-Лопес Х.Н., Гарсия-Канос Ф., Гарсия-Кармона Ф. (февраль 1995 г.). «Тирозиназа: всесторонний обзор ее механизма». Biochimica et Biophysical Acta (BBA) - Структура белка и молекулярная энзимология . 1247 (1): 1–11. дои : 10.1016/0167-4838(94)00204-т . ПМИД 7873577 .
- ^ Ратмелл В.Г., Бендалл Д.С. (март 1972 г.). «Катализируемое пероксидазой окисление халкона и его возможное физиологическое значение» . Биохимический журнал . 127 (1): 125–32. дои : 10.1042/bj1270125 . ПМЦ 1178567 . ПМИД 5073737 .
- ^ Йоргенсен К., Расмуссен А.В., Морант М., Нильсен А.Х., Бьярнхольт Н., Загробельный М., Бак С., Мёллер Б.Л. (июнь 2005 г.). «Образование метаболонов и метаболические каналы в биосинтезе растительных натуральных продуктов». Современное мнение в области биологии растений . 8 (3): 280–91. дои : 10.1016/j.pbi.2005.03.014 . ПМИД 15860425 .
- ^ Мол Дж., Корниш Э., Мейсон Дж., Коес Р. (1999). «Новые цветные цветы». Современное мнение в области биотехнологии . 10 (2): 198–201. дои : 10.1016/S0958-1669(99)80035-4 . ПМИД 10209139 .
- ^ Одекер Р., Буменджель А. (2012). «Последние достижения в медицинской химии ауронов». Современная медицинская химия . 19 (18): 2861–75. дои : 10.2174/092986712800672085 . ПМИД 22519399 .
- ^ Деци А., Маждалани М., Контогиоргис К.А., Хаджипавлу-Литина Д., Кефалас П. (декабрь 2009 г.). «Природные и синтетические 2'-гидроксихалконы и ауроны: синтез, характеристика и оценка антиоксидантной и ингибирующей активности липоксигеназы сои». Биоорганическая и медицинская химия . 17 (23): 8073–85. дои : 10.1016/j.bmc.2009.10.002 . ПМИД 19853459 .
- ^ Шакья Р., Йе Дж., Ромменс К.М. (декабрь 2012 г.). «Измененный цвет листьев связан с повышенной активностью по удалению супероксида у трансгенных растений, продуцирующих ауреусидин» . Журнал биотехнологии растений . 10 (9): 1046–55. дои : 10.1111/j.1467-7652.2012.00732.x . ПМИД 22924954 .
Внешние ссылки
[ редактировать ]- Ауреусидин + синтаза в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)
