V(D)J рекомбинация
Рекомбинация V(D)J (перестройка вариабельного разнообразия-соединения) представляет собой механизм соматической рекомбинации , который происходит только в развивающихся лимфоцитах на ранних стадиях созревания Т- и В-клеток. Это приводит к весьма разнообразному репертуару антител/иммуноглобулинов и рецепторов Т-клеток (TCR), обнаруживаемых в В-клетках и Т-клетках соответственно. Этот процесс является определяющей особенностью адаптивной иммунной системы .
Рекомбинация V(D)J у млекопитающих происходит в первичных лимфоидных органах ( костном мозге для В-клеток и тимусе для Т-клеток) и почти случайным образом перестраивает переменную (V), соединение (J), а в некоторых случаях и разнообразие ( Г) сегменты гена. В конечном итоге этот процесс приводит к появлению новых аминокислотных последовательностей в антигенсвязывающих областях иммуноглобулинов и TCR, которые позволяют распознавать антигены практически всех патогенов, включая бактерии , вирусы , паразиты и черви , а также «измененные собственные клетки», как показано на рак . Распознавание также может носить аллергический характер ( например , на пыльцу или другие аллергены ) или может совпадать с тканями хозяина и приводить к аутоиммунитету .
В 1987 году Сусуму Тонегава был удостоен Нобелевской премии по физиологии и медицине «за открытие генетического принципа создания разнообразия антител». [ 1 ]
Фон
[ редактировать ]человека Молекулы антител (включая рецепторы В-клеток ) состоят из тяжелых и легких цепей, каждая из которых содержит как константные (С), так и вариабельные (V) области, генетически кодируемые тремя локусами :
- Локус тяжелой цепи иммуноглобулина ( IGH@ ) на хромосоме 14, содержащий сегменты гена тяжелой цепи иммуноглобулина .
- Локус каппа (κ) иммуноглобулина ( IGK@ ) на хромосоме 2, содержащий сегменты гена одного типа (κ) легкой цепи иммуноглобулина .
- Локус лямбда (λ) иммуноглобулина ( IGL@ ) на хромосоме 22, содержащий сегменты гена другого типа (λ) легкой цепи иммуноглобулина.
Каждый ген тяжелой цепи или легкой цепи содержит множество копий трех различных типов генных сегментов вариабельных областей белков антител. Например, область тяжелой цепи иммуноглобулина человека содержит 2 константных генных сегмента (Cμ и Cδ) и 44 вариабельных генных сегмента (V), а также 27 генных сегментов разнообразия (D) и 6 соединительных генных сегментов (J). [ 2 ] Гены легкой цепи содержат либо один (Cκ), либо четыре (Cλ) константных генных сегмента с многочисленными генными сегментами V и J, но не имеют генных сегментов D. [ 3 ] Перестройка ДНК приводит к тому, что одна копия каждого типа генного сегмента попадает в любой данный лимфоцит, создавая огромный репертуар антител; примерно 3×10 11 возможны комбинации, хотя некоторые из них удаляются из-за собственной реактивности.
Большинство рецепторов Т-клеток состоят из вариабельной альфа-цепи и бета-цепи. Гены Т-клеточных рецепторов подобны генам иммуноглобулинов тем, что они также содержат множество генных сегментов V, D и J в своих бета-цепях (а также генные сегменты V и J в их альфа-цепях), которые перестраиваются во время развития лимфоцита в снабдить эту клетку уникальным рецептором антигена. В этом смысле Т-клеточный рецептор является топологическим эквивалентом антигенсвязывающего фрагмента антитела, поскольку оба они являются частью суперсемейства иммуноглобулинов.
Аутоиммунный ответ предотвращается путем устранения самореагирующих клеток. Это происходит в тимусе путем тестирования клетки на наличие множества аутоантигенов, экспрессируемых посредством функции аутоиммунного регулятора (AIRE). Локус легкой цепи лямбда иммуноглобулина содержит гены, кодирующие белок, которые могут быть потеряны в результате его реаранжировки. Это основано на физиологическом механизме и не является патогенетическим для лейкозов или лимфом. Клетка сохраняется, если она создает успешный продукт, который не реагирует самостоятельно, в противном случае она удаляется посредством апоптоза .
Иммуноглобулины
[ редактировать ]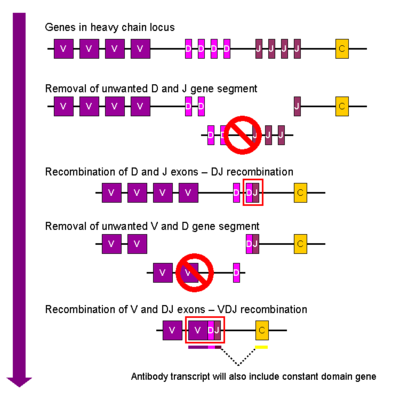
Тяжелая цепь
[ редактировать ]В развивающейся В-клетке первое событие рекомбинации происходит между одним генным сегментом D и одним J-сегментом локуса тяжелой цепи. Любая ДНК между этими двумя сегментами гена удаляется. За этой рекомбинацией DJ следует присоединение одного сегмента гена V из области выше вновь образованного комплекса DJ, образуя реаранжированный сегмент гена VDJ. Все остальные сегменты гена между сегментами V и D теперь удалены из генома клетки. первичный транскрипт Генерируется (несплайсированная РНК), содержащий область VDJ тяжелой цепи, а также константные мю- и дельта- цепи (Cμ и Cδ ) . (т.е. первичный транскрипт содержит сегменты: VDJC μ -C δ ). Первичная РНК обрабатывается для добавления полиаденилированного (поли-А) хвоста после C - цепи и удаления последовательности между сегментом VDJ и этим константным сегментом гена. Трансляция этой мРНК приводит к образованию белка тяжелой цепи IgM .
Легкая цепь
[ редактировать ]Каппа (κ) и лямбда (λ) цепи локусов легкой цепи иммуноглобулина перестраиваются очень похожим образом, за исключением того, что в легких цепях отсутствует сегмент D. Другими словами, первый этап рекомбинации легких цепей включает соединение цепей V и J с образованием комплекса VJ перед добавлением гена константной цепи во время первичной транскрипции. Трансляция сплайсированной мРНК каппа- или лямбда-цепей приводит к образованию белка легкой цепи Ig κ или Ig λ.
Сборка тяжелой цепи Igμ и одной из легких цепей приводит к образованию мембраносвязанной формы иммуноглобулина IgM, которая экспрессируется на поверхности незрелой В-клетки.
Т-клеточные рецепторы
[ редактировать ]Во время тимоцитов развития цепи рецепторов Т-клеток (TCR) подвергаются по существу той же самой последовательности событий упорядоченной рекомбинации, что и описанная для иммуноглобулинов. Рекомбинация D-to-J сначала происходит в β-цепи TCR. Этот процесс может включать либо присоединение сегмента гена Dβ1 к одному из шести сегментов Jβ1 , либо присоединение сегмента гена Dβ2 к одному из шести сегментов Jβ2 . [ 3 ] За рекомбинацией DJ (как указано выше) следуют перегруппировки V β - в D β J β . Все генные сегменты между генными сегментами V β -D β -J β во вновь образованном комплексе удаляются и синтезируется первичный транскрипт, включающий ген константного домена (V β -D β -J β -C β ). Транскрипция мРНК расщепляет любую промежуточную последовательность и обеспечивает трансляцию полноразмерного белка для β-цепи TCR.
Перегруппировка альфа-(α)-цепи TCR следует за перегруппировкой β-цепи и напоминает перегруппировку V-to-J, описанную для легких цепей Ig (см. выше). Сборка β- и α-цепей приводит к образованию αβ-TCR, который экспрессируется на большинстве Т-клеток .
Механизм
[ редактировать ]Ключевые ферменты и компоненты
[ редактировать ]Процесс рекомбинации V(D)J опосредуется рекомбиназой VDJ, которая представляет собой разнообразную совокупность ферментов. Ключевыми участвующими ферментами являются гены 1 и 2, активирующие рекомбинацию (RAG), терминальная дезоксинуклеотидилтрансфераза (TdT) и нуклеаза Artemis , участник повсеместного пути негомологичного соединения концов (NHEJ) для репарации ДНК. [ 4 ] Известно, что в этом процессе участвуют несколько других ферментов, в том числе ДНК-зависимая протеинкиназа (DNA-PK), перекрестно-комплементирующий белок 4 рентгеновской репарации (XRCC4), ДНК-лигаза IV , негомологичный фактор соединения концов 1 ( NHEJ1, также известный как Cernunnos или XRCC4-подобный фактор [XLF]), недавно открытый паралог XRCC4 и XLF (PAXX) и ДНК; полимеразы λ и μ. [ 5 ] Некоторые участвующие ферменты специфичны для лимфоцитов ( например , RAG, TdT), тогда как другие обнаруживаются в других типах клеток и даже повсеместно ( например , компоненты NHEJ).
Чтобы поддерживать специфичность рекомбинации, рекомбиназа V(D)J распознает и связывается с сигнальными последовательностями рекомбинации (RSS), фланкирующими сегменты генов вариабельности (V), разнообразия (D) и соединения (J). RSS состоят из трех элементов: гептамера из семи консервативных нуклеотидов, спейсерной области длиной 12 или 23 пары оснований и нонамера из девяти консервативных нуклеотидов. Хотя большинство RSS различаются по последовательности, консенсусными гептамерными и нонамерными последовательностями являются CACAGTG и ACAAAAACC соответственно; и хотя последовательность спейсерной области плохо консервативна, ее длина высоко консервативна. [ 6 ] [ 7 ] Длина спейсерной области соответствует примерно одному (12 пар оснований) или двум виткам (23 пары оснований) спирали ДНК. Следуя так называемому правилу 12/23, сегменты гена, подлежащие рекомбинации, обычно соседствуют с RSS с разной длиной спейсера ( т.е. один имеет «12RSS», а другой — «23RSS»). [ 8 ] Это важная особенность регуляции рекомбинации V(D)J. [ 9 ]
Процесс
[ редактировать ]Рекомбинация V(D)J начинается, когда рекомбиназа V(D)J (за счет активности RAG1) связывает RSS, фланкирующий сегмент кодирующего гена (V, D или J), и создает одноцепочечный разрыв в ДНК между первыми основание RSS (непосредственно перед гептамером) и сегмент кодирования. Это по существу энергетически нейтрально (нет необходимости гидролиза АТФ ) и приводит к образованию свободной 3'- гидроксильной группы и 5'- фосфатной группы на одной и той же цепи. Реактивная гидроксильная группа позиционируется рекомбиназой для атаки фосфодиэфирной связи противоположной цепи, образуя два конца ДНК: шпильку (стебель-петля) на кодирующем сегменте и тупой конец на сигнальном сегменте. [ 10 ] Текущая модель состоит в том, что разрыв ДНК и образование шпильки происходят на обеих цепях одновременно (или почти) в комплексе, известном как центр рекомбинации . [ 11 ] [ 12 ] [ 13 ] [ 14 ]
Тупые сигнальные концы лигируются заподлицо, образуя кольцевой участок ДНК, содержащий все промежуточные последовательности между кодирующими сегментами, известный как сигнальный сустав (хотя по своей природе он кольцевой, его не следует путать с плазмидой ) . Первоначально считалось, что сигнальные соединения теряются во время последовательных делений клеток, но есть свидетельства того, что сигнальные соединения могут повторно проникать в геном и приводить к патологиям за счет активации онкогенов или прерывания функции(й) генов-супрессоров опухолей [Ссылка].
Кодирующие концы обрабатываются далее перед их лигированием с помощью нескольких событий, которые в конечном итоге приводят к разнообразию соединений. [ 15 ] Процессинг начинается, когда DNA-PK связывается с каждым разорванным концом ДНК и привлекает несколько других белков, включая Artemis, XRCC4, ДНК-лигазу IV, Cernunnos и несколько ДНК-полимераз. [ 16 ] ДНК-ПК образует комплекс, который приводит к ее аутофосфорилированию , что приводит к активации Артемиды. Кодирующие концевые шпильки открываются деятельностью Артемиды. [ 17 ] Если их открыть в центре, образуется тупой конец ДНК; однако во многих случаях отверстие находится «не от центра», что приводит к тому, что на одной нити остаются дополнительные основания (выступ). Они известны как палиндромные (P) нуклеотиды из-за палиндромной природы последовательности, образующейся, когда ферменты репарации ДНК устраняют выступающий конец. [ 18 ] Процесс открытия шпильки с помощью Artemis является решающим этапом рекомбинации V(D)J и является дефектным в мышиной модели тяжелого комбинированного иммунодефицита (scid) .
Затем XRCC4, Cernunnos и DNA-PK выравнивают концы ДНК и привлекают терминальную дезоксинуклеотидилтрансферазу (TdT), независимую от матрицы ДНК-полимеразу, которая добавляет нематрицированные (N) нуклеотиды к кодирующему концу. Добавление в основном случайное, но TdT действительно отдает предпочтение нуклеотидам G/C. [ 19 ] Как и все известные ДНК-полимеразы, TdT добавляет нуклеотиды к одной цепи в направлении от 5’ к 3’. [ 20 ]
Наконец, экзонуклеазы могут удалять основания с кодирующих концов (включая любые образовавшиеся P или N нуклеотиды). Затем ДНК-полимеразы λ и μ вставляют дополнительные нуклеотиды по мере необходимости, чтобы сделать два конца совместимыми для соединения. Это стохастический процесс, поэтому может произойти любая комбинация добавления нуклеотидов P и N и экзонуклеолитического удаления (или вообще не произойти). Наконец, обработанные кодирующие концы связываются вместе ДНК-лигазой IV. [ 21 ]
Все эти события обработки приводят к образованию очень изменчивого паратопа , даже когда рекомбинируются одни и те же генные сегменты. Рекомбинация V(D)J позволяет генерировать иммуноглобулины и Т-клеточные рецепторы к антигенам, с которыми ни организм, ни его предки не должны были ранее сталкиваться, что обеспечивает адаптивный иммунный ответ на новые развивающиеся патогены или на те, которые часто изменения ( например , сезонный грипп ). Однако основным предостережением в этом процессе является то, что последовательность ДНК должна оставаться в рамке считывания , чтобы сохранить правильную аминокислотную последовательность в конечном белковом продукте. Если полученная последовательность окажется вне кадра, развитие клетки будет остановлено, и клетка не доживет до зрелости. Таким образом, рекомбинация V(D)J представляет собой очень дорогостоящий процесс, который должен строго регулироваться и контролироваться.
См. также
[ редактировать ]- В-клеточный рецептор
- Т-клеточный рецептор
- Базельский институт иммунологии
- Чарльз М. Стейнберг
- NKT-клетка
- Ген, активирующий рекомбинацию
Ссылки
[ редактировать ]- ^ «Нобелевская премия по физиологии и медицине 1987 года» . nobelprize.org . Архивировано из оригинала 13 февраля 2021 года . Проверено 26 декабря 2014 г.
- ^ Ли А., Рю М., Чжоу Дж. и др. (июнь 2004 г.). «Использование переменной тяжелой цепи Ig, разнообразия и соединения сегментов гена у детей с острым лимфобластным лейкозом B-линии: значение для механизмов рекомбинации VDJ и патогенеза» . Кровь . 103 (12): 4602–9. дои : 10.1182/кровь-2003-11-3857 . ПМИД 15010366 .
- ^ Перейти обратно: а б Аббас, Абул К. (2018). «Развитие лимфоцитов и перестройка генов антигенных рецепторов». Клеточная и молекулярная иммунология (9-е изд.). Филадельфия, Пенсильвания: Эльзевир. ISBN 978-0-323-47978-3 .
- ^ Ма, Юнмей; Лу, Хайхуэй; Шварц, Клаус; Либер, Майкл (сентябрь 2005 г.). «Восстановление разрывов двухцепочечной ДНК с помощью пути соединения концов негомологичной ДНК человека: модель итеративной обработки» . Клеточный цикл . 4 (9): 1193–1200. дои : 10.4161/cc.4.9.1977 . ПМИД 16082219 .
- ^ Малу, Шрути; Малшетти, Видьясагар; Фрэнсис, Дайлия; Кортес, Патрисия (2012). «Роль негомологичного соединения концов в рекомбинации V (D) J». Иммунологические исследования . 54 (1–3): 233–246. дои : 10.1007/s12026-012-8329-z . ПМИД 22569912 . S2CID 45771818 .
- ^ Рамсден, Дейл; Баец, Кристин; Ву, Джиллиан (1994). «Сохранение последовательности в спейсерах последовательности рекомбинационных сигналов» . Исследования нуклеиновых кислот . 22 (10): 1785–1796. дои : 10.1093/нар/22.10.1785 . ПМК 308075 . ПМИД 8208601 .
- ^ Коуэлл, Линдси; Давила, Марко; Рамсден, Дейл; Келсо, Гарнетт (2004). «Вычислительные инструменты для понимания изменчивости последовательностей в сигналах рекомбинации». Иммунологические обзоры . 200 : 57–69. дои : 10.1111/j.0105-2896.2004.00171.x . ПМИД 15242396 . S2CID 40771963 .
- ^ ван Гент, Дик; Рамсден, Дейл; Геллерт, Мартин (1996). «Белки RAG1 и RAG2 устанавливают правило 12/23 в рекомбинации V(D)J» . Клетка . 85 (1): 107–13. дои : 10.1016/s0092-8674(00)81086-7 . ПМИД 8620529 .
- ^ Хиом, Кевин; Геллерт, Мартин (1998). «Сборка парного сигнального комплекса 12/23: критическая контрольная точка в рекомбинации V (D) J» . Молекулярная клетка . 1 (7): 1011–1019. дои : 10.1016/s1097-2765(00)80101-x . ПМИД 9651584 .
- ^ Шац, Дэвид; Суонсон, Патрик (2011). «Рекомбинация V (D) J: механизмы инициации». Ежегодный обзор генетики . 45 : 167–202. doi : 10.1146/annurev-genet-110410-132552 . ПМИД 21854230 .
- ^ Шац, Дэвид; Цзи, Яньхун (2011). «Центры рекомбинации и организация рекомбинации V (D) J». Обзоры природы Иммунология . 11 (4): 251–263. дои : 10.1038/nri2941 . ПМИД 21394103 . S2CID 33489235 .
- ^ Карри, Джон; Гейер, Джейми; Шлиссель, Марк (2005). «Ники последовательности сигналов одноцепочечной рекомбинации in vivo: данные в пользу модели захвата Synapsis». Природная иммунология . 6 (12): 1272–1279. дои : 10.1038/ni1270 . ПМИД 16286921 . S2CID 10975251 .
- ^ Агравал, Алка; Шац, Дэвид (1997). «RAG1 и RAG2 образуют стабильный синаптический комплекс после расщепления с ДНК, содержащей сигнальные концы, при рекомбинации V (D) J» . Клетка . 89 (1): 43–53. дои : 10.1016/s0092-8674(00)80181-6 . ПМИД 9094713 .
- ^ Фугманн, Себастьян; Ли, АИфред; Шокетт, Пенни; Вилли, Изабель; Шац, Дэвид (2000). «Белки RAG и рекомбинация V (D) J: комплексы, концы и транспозиция». Ежегодный обзор иммунологии . 18 : 495–527. doi : 10.1146/annurev.immunol.18.1.495 . ПМИД 10837067 .
- ^ Льюис, Сюзанна (1994). «Механизм присоединения V (D) J: уроки молекулярного, иммунологического и сравнительного анализа». Достижения иммунологии, том 56 . Достижения иммунологии. Том. 56. стр. 27–150. дои : 10.1016/s0065-2776(08)60450-2 . ISBN 9780120224562 . ПМИД 8073949 .
- ^ Хелминк, Бет; Слекман, Барри (2012). «Реакция на двухцепочечные разрывы ДНК, опосредованные RAG, и их восстановление» . Ежегодный обзор иммунологии . 30 : 175–202. doi : 10.1146/annurev-immunol-030409-101320 . ПМК 4038028 . ПМИД 22224778 .
- ^ Ма, Юнмей; Шварц, Клаус; Либер, Майкл (2005). «Артемида: эндонуклеаза DNA-PKcs расщепляет петли, лоскуты и пробелы ДНК». Восстановление ДНК . 4 (7): 845–851. дои : 10.1016/j.dnarep.2005.04.013 . ПМИД 15936993 .
- ^ Лу, Хайхуэй; Шварц, Клаус; Либер, Майкл (2007). «Степень, в которой открытие шпильки комплексом Артемида: ДНК-PKcs может способствовать разнообразию соединений при рекомбинации V (D) J» . Исследования нуклеиновых кислот . 35 (20): 6917–6923. дои : 10.1093/нар/gkm823 . ПМК 2175297 . ПМИД 17932067 .
- ^ Гаусс, Джордж; Либер, Майкл (1996). «Механистические ограничения разнообразия в рекомбинации V(D)J человека» . Молекулярная и клеточная биология . 16 (1): 258–269. дои : 10.1128/MCB.16.1.258 . ПМК 230999 . ПМИД 8524303 .
- ^ Бенедикт, Синди; Гилфиллан, Сьюзен; Тайский, То-Ха; Кирни, Джон (2000). «Терминальная дезоксинуклеотидилтрансфераза и развитие репертуара». Иммунологические обзоры . 175 : 150–157. дои : 10.1111/j.1600-065x.2000.imr017518.x . ПМИД 10933600 . S2CID 20634390 .
- ^ ван Гент, округ Колумбия; ван дер Бург, М (10 декабря 2007 г.). «Номологическое соединение концов, трудный вопрос». Онкоген . 26 (56): 7731–40. дои : 10.1038/sj.onc.1210871 . ПМИД 18066085 .
Дальнейшее чтение
[ редактировать ]- Хартвелл Л.Х., Худ Л., Голдберг М.Л., Рейнольдс А.Е., Сильвер Л.М., Верес Р.К. (2000). Глава 24. Эволюция на молекулярном уровне. В: Генетика . Нью-Йорк: МакГроу-Хилл. стр. 805–807. ISBN 978-0-07-299587-9 .
- V(D)J-рекомбинация. Серия: Достижения экспериментальной медицины и биологии, Том. 650 Ферье, Пьер (ред.) Landes Bioscience 2009, XII, 199 стр. ISBN 978-1-4419-0295-5