Глиоксиловая кислота

| |

| |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК
Оксоуксусная кислота [ 1 ] | |
| Систематическое название ИЮПАК
Оксоэтановая кислота | |
| Другие имена | |
| Идентификаторы | |
3D model ( JSmol )
|
|
| 741891 | |
| КЭБ | |
| ХЭМБЛ | |
| ХимическийПаук | |
| Лекарственный Банк | |
| Информационная карта ECHA | 100.005.508 |
| Номер ЕС |
|
| 25752 | |
| КЕГГ | |
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 2 Н 2 О 3 | |
| Молярная масса | 74.035 g·mol −1 |
| Плотность | 1,384 г/мл |
| Температура плавления | 80 ° С (176 ° F; 353 К) [ 4 ] |
| Точка кипения | 111 ° С (232 ° F; 384 К) |
| Кислотность ( pKa ) | 3.18, [ 2 ] 3.32 [ 3 ] |
| Родственные соединения | |
Другие анионы
|
глиоксилат |
Родственные карбоновые кислоты
|
муравьиная кислота уксусная кислота гликолевая кислота щавелевая кислота пропионовая кислота пировиноградная кислота |
Родственные соединения
|
ацетальдегид глиоксаль гликольальдегид |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Глиоксиловая кислота или оксоуксусная кислота является органическим соединением . Глиоксиловая кислота вместе с уксусной , гликолевой и щавелевой кислотами относится к группе С 2 -карбоновых кислот . Это бесцветное твердое вещество, встречающееся в природе и используемое в промышленности.
Структура и номенклатура
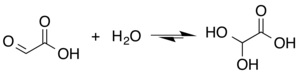
[ редактировать ]Показано, что структура глиоксиловой кислоты имеет альдегидную функциональную группу . Альдегид является лишь второстепенным компонентом формы, наиболее распространенной в некоторых ситуациях. Вместо этого глиоксалевая кислота часто существует в виде гидрата или циклического димера . Например, в присутствии воды карбонил быстро превращается в геминальный диол (описываемый как «моногидрат»). Константа равновесия ( К ) равна 300 для образования дигидроксиуксусной кислоты при комнатной температуре: [ 5 ] Дигидроксиуксусная кислота охарактеризована методом рентгеновской кристаллографии . [ 6 ]
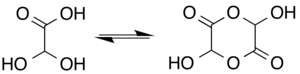
В водном растворе этот моногидрат существует в равновесии с формой полуацилального димера: [ 7 ]
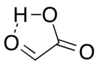
Изолированно, альдегидная структура имеет в качестве основного конформера циклическую структуру с водородными связями , в которой карбонил альдегида находится в непосредственной близости от карбоксильного водорода: [ 8 ]
глиоксиловой Константа закона Генри кислоты равна K H = 1,09 × 10. 4 × exp[(40,0 × 10 3 /R) × (1/T − 1/298)]. [ 9 ]
Препараты
[ редактировать ]Сопряженное основание глиоксиловой кислоты известно как глиоксилат и представляет собой форму, в которой соединение существует в растворе при нейтральном pH. Глиоксилат является побочным продуктом процесса амидирования при биосинтезе нескольких амидированных пептидов .
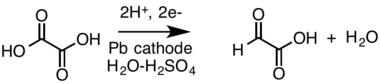
Для справки: глиоксиловую кислоту получали из щавелевой кислоты электросинтетически : [ 10 ] [ 11 ] в органическом синтезе катоды из диоксида свинца нашли применение для получения глиоксиловой кислоты из щавелевой кислоты в сернокислом электролите. [ 12 ]
Горячая азотная кислота может окислить глиоксаль до глиоксиловой кислоты; однако эта реакция сильно экзотермична и склонна к выходу из-под контроля. Кроме того, щавелевая кислота является основным побочным продуктом.
Также озонолиз малеиновой кислоты . эффективен [ 7 ]
Биологическая роль
[ редактировать ]Глиоксилат является промежуточным продуктом глиоксилатного цикла , который позволяет организмам , таким как бактерии, [ 13 ] грибы и растения [ 14 ] превращать жирные кислоты в углеводы . Глиоксилатный цикл также важен для индукции защитных механизмов растений в ответ на грибки. [ 15 ] Глиоксилатный цикл инициируется активностью изоцитратлиазы, которая превращает изоцитрат в глиоксилат и сукцинат. Проводятся исследования, чтобы использовать этот путь для различных целей, таких как биосинтез сукцината. [ 16 ]
У людей
[ редактировать ]Глиоксилат образуется двумя путями: окислением гликолята в пероксисомах или катаболизмом гидроксипролина в митохондриях. [ 17 ] В пероксисомах глиоксилат превращается в глицин под действием AGT1 или в оксалат под действием гликолатоксидазы. В митохондриях глиоксилат превращается в глицин под действием AGT2 или в гликолат под действием глиоксилатредуктазы. Небольшое количество глиоксилата превращается в оксалат под действием цитоплазматической лактатдегидрогеназы. [ 18 ]

В растениях
[ редактировать ]Помимо того, что глиоксилат является промежуточным продуктом глиоксилатного цикла , он также является важным промежуточным продуктом в пути фотодыхания . Фотодыхание является результатом побочной реакции RuBisCO с O 2 вместо CO 2 . Хотя фотодыхание сначала считалось пустой тратой энергии и ресурсов, оно оказалось важным методом регенерации углерода и CO 2 , удаления токсичного фосфогликолата и запуска защитных механизмов. [ 19 ] [ 20 ] При фотодыхании глиоксилат превращается из гликолата за счет активности гликолатоксидазы в пероксисоме. Затем он превращается в глицин посредством параллельного действия SGAT и GGAT, который затем транспортируется в митохондрии. [ 21 ] [ 20 ] Также сообщалось, что комплекс пируватдегидрогеназы может играть роль в метаболизме гликолатов и глиоксилатов. [ 22 ]

Актуальность заболевания
[ редактировать ]Диабет
[ редактировать ]Считается, что глиоксилат является потенциальным ранним маркером диабета II типа . [ 23 ] Одним из ключевых состояний патологии диабета является выработка конечных продуктов гликирования (AGE), вызванная гипергликемией . [ 24 ] КПГ могут привести к дальнейшим осложнениям диабета, таким как повреждение тканей и сердечно-сосудистые заболевания. [ 25 ] Обычно они образуются из реактивных альдегидов, например, присутствующих в редуцирующих сахарах и альфа-оксоальдегидах . В исследовании было обнаружено, что уровни глиоксилата значительно повышаются у пациентов, у которых позже был диагностирован диабет II типа. [ 23 ] Повышенные уровни иногда обнаруживались за три года до постановки диагноза, что демонстрирует потенциальную роль глиоксилата в качестве раннего прогностического маркера.
Нефролитиаз
[ редактировать ]Глиоксилат участвует в развитии гипероксалурии , ключевой причины нефролитиаза (широко известного как камни в почках). Глиоксилат является одновременно субстратом и индуктором переносчика сульфат-анионов-1 (sat-1), гена, ответственного за транспортировку оксалатов, что позволяет ему увеличивать экспрессию мРНК sat-1 и, как следствие, отток оксалатов из клетки. Повышенное высвобождение оксалатов приводит к накоплению оксалата кальция в моче и, следовательно, к возможному образованию камней в почках. [ 18 ]
Нарушение обмена глиоксилатов является дополнительным механизмом развития гипероксалурии. Мутации потери функции в гене HOGA1 приводят к потере 4-гидрокси-2-оксоглутаратальдолазы, фермента пути превращения гидроксипролина в глиоксилат. Глиоксилат, образующийся в результате этого пути, обычно хранится, чтобы предотвратить окисление до оксалата в цитозоле. Однако нарушенный путь вызывает накопление 4-гидрокси-2-оксоглутарата, который также может транспортироваться в цитозоль и превращаться в глиоксилат с помощью другой альдолазы. Эти молекулы глиоксилата могут окисляться в оксалат, увеличивая его концентрацию и вызывая гипероксалурию. [ 17 ]
Реакции и использование
[ редактировать ]Глиоксиловая кислота примерно в десять раз сильнее кислоты, чем уксусная , с константой диссоциации кислоты 4,7 × 10. −4 (р К а = 3,32):
- ОЧКО 2 H ⇌ ОЧКО −
2 + Ч +
С концентрированным основанием глиоксиловая кислота диспропорционируется посредством реакции Канниццаро , образуя гидроксиуксусную кислоту и щавелевую кислоту : [ нужна ссылка ]
- 2 OCHCO 2 H + H 2 O → HOCH 2 CO 2 H + HO 2 CCO 2 H
Глиоксиловая кислота при конденсации с мочевиной и 1,2-диаминобензолом дает гетероциклы .
Производные фенола
[ редактировать ]В общем, глиоксиловая кислота подвергается электрофильного ароматического замещения реакции фенолами , что является универсальной стадией в синтезе ряда других соединений.
Непосредственным продуктом фенола является 4-гидроксиминдальная кислота . Этот вид реагирует с аммиаком с образованием гидроксифенилглицина, предшественника препарата амоксициллин . Восстановление 4-гидроксиминдальной кислоты дает 4-гидроксифенилуксусную кислоту , предшественник препарата атенолол .
Последовательность реакций, в которых глиоксиловая кислота реагирует с гваяколом (фенольным компонентом) с последующим окислением и декарбоксилированием , открывает путь к получению ванилина как чистого процесса формилирования . [ 7 ] [ 26 ] [ 27 ]
Реакция Хопкинса Коула
[ редактировать ]Глиоксиловая кислота является компонентом реакции Хопкинса-Коула , используемой для проверки наличия триптофана в белках. [ 28 ]
Экологическая химия
[ редактировать ]Глиоксиловая кислота — одна из нескольких кетон- и альдегидсодержащих карбоновых кислот, которые вместе широко распространены во вторичных органических аэрозолях . В присутствии воды и солнечного света глиоксиловая кислота может подвергаться фотохимическому окислению. Может произойти несколько различных путей реакции, приводящих к образованию различных других карбоновых кислот и альдегидных продуктов. [ 29 ]
Безопасность
[ редактировать ]Соединение не очень токсично: ЛД 50 для крыс составляет 2500 мг/кг.
Но недавний эксперимент показывает, что он токсичен. См . https://karger.com/cnd/article/12/2/112/827730/Acute-Kidney-Injury-following-Exposure-to .
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Перейти обратно: а б «Фронт материи». Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга) . Кембридж: Королевское химическое общество . 2014. с. 748. дои : 10.1039/9781849733069-FP001 . ISBN 978-0-85404-182-4 .
- ^ Константы диссоциации органических кислот и оснований (600 соединений), http://zirchrom.com/organic.htm .
- ^ Данные pKa, составленные Р. Уильямсом, «Архивная копия» (PDF) . Архивировано из оригинала (PDF) 2 июня 2010 г. Проверено 2 июня 2010 г.
{{cite web}}: CS1 maint: архивная копия в заголовке ( ссылка ) . - ^ Индекс Merck , 11-е издание, 4394.
- ^ Соренсен, ЧП; Брюн, К.; Линделёв, Ф. (1974). «Кинетика и равновесия обратимой гидратации альдегидной группы в глиоксиловой кислоте» . Акта Хим. Скан . 28 : 162–168. doi : 10.3891/acta.chem.scand.28a-0162 .
- ^ Чапик, Агнешка; Гданец, Мария (2007). «Хиноксалин-дигидроксиуксусная кислота (1/1)». Acta Crystallographica Раздел E: Онлайн-отчеты о структуре . 63 (7): о3081. дои : 10.1107/S1600536807025792 .
- ^ Перейти обратно: а б с Жорж Маттиода и Яни Кристидис «Глиоксиловая кислота», Энциклопедия промышленной химии Ульмана, 2002, Wiley-VCH, Вайнхайм. два : 10.1002/14356007.a12_495
- ^ Редингтон, Ричард Л.; Лян, Чин-Кан Джим (1984). «Колебательные спектры мономеров глиоксиловой кислоты». Журнал молекулярной спектроскопии . 104 (1): 25–39. Бибкод : 1984JMoSp.104...25R . дои : 10.1016/0022-2852(84)90242-X .
- ^ ИП, Х.С. Саймон; Хуанг, XH Хильда; Ю, Цзянь Чжэнь (2009). «Эффективные константы закона Генри для глиоксаля, глиоксиловой кислоты и гликолевой кислоты» (PDF) . Письма о геофизических исследованиях . 36 (1): L01802. Бибкод : 2009GeoRL..36.1802I . дои : 10.1029/2008GL036212 . S2CID 129747490 .
- ^ Тафель, Юлиус; Фридрихс, Густав (1904). «Электролитическое восстановление карбоновых кислот и эфиров карбоновых кислот в растворе серной кислоты» . Отчеты Немецкого химического общества . 37 (3): 3187–3191. дои : 10.1002/cber.190403703116 .
- ^ Коэн, Юлиус (1920). Практическая органическая химия, 2-е изд. (PDF) . Лондон: Macmillan and Co. Limited. стр. 102–104.
- ^ Франсуа Кардарелли (2008). Справочник материалов: краткий настольный справочник . Спрингер. п. 574. ИСБН 978-1-84628-668-1 .
- ^ Холмс WH (1987). «Контроль потока через цикл лимонной кислоты и обход глиоксилата в Escherichia coli». Biochem Soc Symp . 54 : 17–31. ПМИД 3332993 .
- ^ Эшер КЛ, Видмер Ф (1997). «Мобилизация липидов и глюконеогенез в растениях: представляет ли активность ферментов глиоксилатного цикла настоящий цикл? Гипотеза». Биол. Хим . 378 (8): 803–813. ПМИД 9377475 .
- ^ Дубей, Мукеш К.; Броберг, Андерс; Сурияараччи, Сандживани; Убхаясекера, Вимал; Дженсен, Дэн Фанк; Карлссон, Магнус (сентябрь 2013 г.). «Глиоксилатный цикл участвует в плеотропных фенотипах, антагонизме и индукции защитных реакций растений в средстве биоконтроля грибков Trichoderma atroviride». Грибковая генетика и биология . 58–59: 33–41. дои : 10.1016/j.fgb.2013.06.008 . ISSN 1087-1845 . ПМИД 23850601 .
- ^ Чжу, Ли-Вэнь; Ли, Сяо-Хун; Чжан, Лей; Ли, Хун-Мэй; Лю, Цзянь-Хуа; Юань, Чжан-Пэн; Чен, Тао; Тан, Я-Цзе (ноябрь 2013 г.). «Активация глиоксилатного пути без активации родственного ему гена в сконструированной Escherichia coli, продуцирующей сукцинат». Метаболическая инженерия . 20 :9–19. дои : 10.1016/j.ymben.2013.07.004 . ISSN 1096-7176 . ПМИД 23876414 .
- ^ Перейти обратно: а б Белостоцкий, Рут; Питт, Джеймс Джонатон; Фришберг, Яаков (1 декабря 2012 г.). «Первичная гипероксалурия III типа — модель для изучения нарушений метаболизма глиоксилатов». Журнал молекулярной медицины . 90 (12): 1497–1504. дои : 10.1007/s00109-012-0930-z . hdl : 11343/220107 . ISSN 0946-2716 . ПМИД 22729392 . S2CID 11549218 .
- ^ Перейти обратно: а б Шнедлер, Нина; Буркхардт, Герхард; Буркхардт, Биргитта К. (март 2011 г.). «Глиоксилат является субстратом сульфат-оксалатного обменника sat-1 и увеличивает его экспрессию в клетках HepG2». Журнал гепатологии . 54 (3): 513–520. дои : 10.1016/j.jhep.2010.07.036 . ISSN 0168-8278 . ПМИД 21093948 .
- ^ «фотодыхание» . Архивировано из оригинала 11 декабря 2006 г. Проверено 9 марта 2017 г.
- ^ Перейти обратно: а б Петерансель, Кристоф; Хорст, Ина; Ниссен, Маркус; Блюм, Кристиан; Кебейш, Рашад; Кюркчуоглу, София; Кройзалер, Фриц (23 марта 2010 г.). «Фотодыхание» . Книга «Арабидопсис» . 8 : e0130. дои : 10.1199/tab.0130 . ISSN 1543-8120 . ПМК 3244903 . ПМИД 22303256 .
- ^ Чжан, Чжишэн; Мао, Синсюэ; Оу, Хуаньин; Да, Нэнхуэй; Чжан, Цзяньхуа; Пэн, Синьсян (январь 2015 г.). «Отличные фотодыхательные реакции преимущественно катализируются глутамат:глиоксилатными и серин:глиоксилатаминотрансферазами в рисе». Журнал фотохимии и фотобиологии B: Биология . 142 : 110–117. doi : 10.1016/j.jphotobiol.2014.11.009 . ISSN 1011-1344 . ПМИД 25528301 .
- ^ Блюм, Кристиан; Беренс, Кристоф; Эйбель, Хольгер; Браун, Ханс-Петер; Петерансель, Кристоф (ноябрь 2013 г.). «Возможная роль комплекса пируватдегидрогеназы хлоропластов в метаболизме гликолатов и глиоксилатов растений». Фитохимия . 95 : 168–176. Бибкод : 2013PChem..95..168B . doi : 10.1016/j.phytochem.2013.07.009 . ISSN 0031-9422 . ПМИД 23916564 .
- ^ Перейти обратно: а б Никифорова Виктория Дж.; Гисбертц, Питер; Вимер, Ян; Бетан, Бьянка; Лузер, Ральф; Либенберг, Волкер; Руис Ноппингер, Патрисия; Дэниел, Ханнелор; Рейн, Дитрих (2014). «Глиоксилат, новый метаболит-маркер диабета 2 типа» . Журнал исследований диабета . 2014 : 685204. doi : 10.1155/2014/685204 . ISSN 2314-6745 . ПМК 4265698 . ПМИД 25525609 .
- ^ Нгуен, Дунг В.; Шоу, Линн С.; Грант, Мария Б. (21 декабря 2012 г.). «Воспаление в патогенезе микрососудистых осложнений при сахарном диабете» . Границы эндокринологии . 3 : 170. дои : 10.3389/fendo.2012.00170 . ISSN 1664-2392 . ПМЦ 3527746 . ПМИД 23267348 .
- ^ Пиарулли, Франческо; Сарторе, Джованни; Лаполла, Аннунциата (апрель 2013 г.). «Гликоокисление и сердечно-сосудистые осложнения при диабете 2 типа: обновленная клиническая информация» . Акта Диабетологика . 50 (2): 101–110. дои : 10.1007/s00592-012-0412-3 . ISSN 0940-5429 . ПМЦ 3634985 . ПМИД 22763581 .
- ^ Фатиади, Александр; Шаффер, Роберт (1974). «Улучшенная процедура синтеза DL -4-гидрокси-3-метоксиминдальной кислоты ( DL- «ванилил»-миндальная кислота, VMA)» . Журнал исследований Национального бюро стандартов . Раздел A. 78А (3): 411–412. дои : 10.6028/jres.078A.024 . ПМК 6742820 . ПМИД 32189791 .
- ^ Камлет, Йонас ; Мэтисон, Олин (1953). Производство ванилина и его гомологов. Патент США 2 640 083 (PDF) . Патентное ведомство США.
- ^ Р.А. Джоши (2006). Вопрос Банка Биохимии . Нью Эйдж Интернэшнл. п. 64. ИСБН 978-81-224-1736-4 .
- ^ Юджин, Алексис Дж.; Ся, Ша-Ша; Гусман, Марсело И. (2016). «Водная фотохимия глиоксиловой кислоты» . Дж. Физ. хим. А. 120 (21): 3817–3826. Бибкод : 2016JPCA..120.3817E . дои : 10.1021/acs.jpca.6b00225 . ПМИД 27192089 .