Укладка (химия)

В химии укладка пи (также называемая укладкой π – π ) относится к предполагаемым притягивающим взаимодействиям пи ( перекрытие орбиталей ) между пи-связями ароматических нековалентным колец. [1] По мнению некоторых авторов, прямая укладка ароматических колец («сэндвич-взаимодействие») является электростатически отталкивающей.
Чаще всего наблюдается (см. рисунок справа) либо шахматное штабелирование (параллельно смещенное), либо тройчатое (перпендикулярное Т-образное) взаимодействие, оба из которых являются электростатическими притяжениями. [2] [3] Например, наиболее часто наблюдаемое взаимодействие между ароматическими кольцами аминокислотных остатков в белках представляет собой шахматное расположение, за которым следует перпендикулярная ориентация. Сэндвич-ориентации встречаются относительно редко. [4]
Укладка Pi является отталкивающей, поскольку она помещает атомы углерода с частичными отрицательными зарядами из одного кольца поверх других частично отрицательно заряженных атомов углерода из второго кольца, а атомы водорода с частичными положительными зарядами поверх других атомов водорода, которые также несут частичные положительные заряды. [2] При шахматной укладке одно из двух ароматических колец смещено вбок, так что атомы углерода с частичным отрицательным зарядом в первом кольце располагаются над атомами водорода с частичным положительным зарядом во втором кольце, так что электростатические взаимодействия становятся притягивающими. Аналогичным образом, взаимодействия с тройником, при которых два кольца ориентированы перпендикулярно друг другу, являются электростатически привлекательными, поскольку они помещают частичные положительно заряженные атомы водорода в непосредственной близости от частично отрицательно заряженных атомов углерода. Альтернативное объяснение предпочтения шахматной упаковки связано с балансом между взаимодействиями Ван-дер-Ваальса (притягивающая дисперсия плюс отталкивание Паули ). [5]
Эти шахматные взаимодействия и π-образные взаимодействия между ароматическими кольцами важны для нуклеиновых оснований укладки в молекулах ДНК и РНК , сворачивания белков , синтеза, управляемого матрицей , материаловедения и молекулярного распознавания . Несмотря на широкое использование термина «наложение пи» в научной литературе, теоретического обоснования его использования нет. [2]
Доказательства против сложения числа Пи
[ редактировать ]Димер бензола является прототипом системы для изучения упаковки пи и экспериментально связывается со скоростью 8–12 кДж/моль (2–3 ккал/моль) в газовой фазе с расстоянием 4,96 Å между центрами масс для Т-образный димер. Небольшая энергия связи затрудняет экспериментальное исследование димера бензола, а сам димер стабилен только при низких температурах и склонен к кластеризации. [6]
Другое свидетельство против укладки чисел «пи» получено из рентгеновской кристаллографии . Перпендикулярные и смещенно-параллельные конфигурации можно наблюдать в кристаллических структурах многих простых ароматических соединений. [6] Аналогичная смещенная параллельная или перпендикулярная геометрия наблюдалась при исследовании рентгеновских кристаллических структур белков с высоким разрешением в Банке данных белков . [7] Анализ ароматических аминокислот фенилаланина, тирозина, гистидина и триптофана показывает, что димеры этих боковых цепей имеют множество возможных стабилизирующих взаимодействий на расстояниях, превышающих средний радиус Ван-дер-Ваальса. [4]
Димеры бензола и родственные виды
[ редактировать ]Предпочтительная геометрия димера бензола была смоделирована на высоком уровне теории с помощью вычислений MP2-R12/A и очень больших базисных наборов aug-cc-PVTZ с поправкой на противовес. [6] Двумя наиболее стабильными конформациями являются параллельно-смещенная и Т-образная, которые по существу изоэнергетические. Напротив, сэндвич-конфигурация максимизирует перекрытие пи-системы, что дестабилизирует взаимодействие. Сэндвич-конфигурация представляет собой энергетическую седловую точку, что соответствует относительной редкости этой конфигурации в данных рентгеновского кристалла. [ нужна ссылка ]

Относительные энергии связи этих трех геометрических конфигураций димера бензола можно объяснить балансом квадрупольных/квадрупольных и лондоновских дисперсионных сил . Хотя бензол не имеет дипольного момента, он обладает сильным квадрупольным моментом . [8] Локальный диполь C–H означает, что атомы в кольце имеют положительный заряд и, соответственно, отрицательный заряд, представляющий электронное облако выше и ниже кольца. Квадрупольный момент обращен к гексафторбензолу из-за электроотрицательности фтора. Димер бензола в сэндвич-конфигурации стабилизируется дисперсионными силами Лондона, но дестабилизируется отталкивающими квадруполь/квадрупольными взаимодействиями. Смещая одно из бензольных колец, параллельная смещенная конфигурация уменьшает эти отталкивающие взаимодействия и стабилизируется. Большая поляризуемость ароматических колец приводит к дисперсионным взаимодействиям, которые являются основным вкладом в эффекты пакетирования. Они играют важную роль во взаимодействиях нуклеиновых оснований, например, в ДНК . [9] Т-образная конфигурация обладает благоприятными квадрупольными/квадрупольными взаимодействиями, поскольку положительный квадруполь одного бензольного кольца взаимодействует с отрицательным квадруполем другого. Бензольные кольца в этой конфигурации расположены дальше всего друг от друга, поэтому благоприятные квадруполь-квадрупольные взаимодействия, очевидно, компенсируют уменьшение дисперсионных сил.
Эффекты заместителя
[ редактировать ]Возможность точной настройки взаимодействия сложения чисел пи была бы полезна в многочисленных синтетических усилиях. Одним из примеров может быть увеличение аффинности связывания низкомолекулярного ингибитора с ферментным карманом, содержащим ароматические остатки. Эффекты гетероатомов [7] Взаимодействия при укладке пи и заместителей трудно смоделировать и являются предметом дискуссий.
Электростатическая модель
[ редактировать ]Ранняя модель роли заместителей во взаимодействиях стэкинга пи была предложена Хантером и Сандерсом. [10] Они использовали простую математическую модель, основанную на зарядах атомов сигма и пи, относительной ориентации и взаимодействиях Ван-дер-Ваальса, чтобы качественно определить, что электростатика доминирует в эффектах заместителей. Согласно их модели, электроноакцепторные группы восстанавливают отрицательный квадруполь ароматического кольца и тем самым способствуют параллельным смещенным и сэндвич-конформациям. Напротив, электронодонорные группы увеличивают отрицательный квадруполь, что может увеличить силу взаимодействия в Т-образной конфигурации с правильной геометрией. Основываясь на этой модели, авторы предложили набор правил, управляющих взаимодействиями суммирования пи, которые преобладали до тех пор, пока не были применены более сложные вычисления. [ нужна ссылка ]
Экспериментальные доказательства модели Хантера-Сандерса были предоставлены Сигелом и др. с использованием ряда замещенных син- и анти-1,8-ди- о -толилнафталинов. [11] В этих соединениях арильные группы «вталкиваются» в многоуровневую геометрию из-за стерического скученности, а барьер эпимеризации измерялся с помощью спектроскопии ядерного магнитного резонанса . Авторы сообщили, что арильные кольца с электроноакцепторными заместителями обладают более высокими барьерами вращения. Интерпретация этого результата заключалась в том, что эти группы уменьшали электронную плотность ароматических колец, обеспечивая более благоприятные сэндвич-пи-стекинговые взаимодействия и, следовательно, более высокий барьер. Другими словами, электроноакцепторные группы приводили к «менее неблагоприятным» электростатическим взаимодействиям в основном состоянии. [ нужна ссылка ]

Хантер и др. применил более сложный химический двойной мутантный цикл с «застежкой-молнией» с водородными связями для решения проблемы эффектов заместителей во взаимодействиях стэкинга пи. [12] Этот метод использовался для изучения множества нековалентных взаимодействий. Одиночная мутация, в данном случае изменяющая заместитель в ароматическом кольце, приводит к вторичным эффектам, таким как изменение прочности водородной связи . Двойная мутация дает количественную оценку этих вторичных взаимодействий, так что даже слабое интересующее взаимодействие можно выделить из массива. Их результаты показывают, что более электроноакцепторные заместители имеют менее отталкивающие пи-стакинг-взаимодействия. Соответственно, эта тенденция была именно обратной для взаимодействий с пентафторфенилбензолом, который имеет квадрупольный момент, равный по величине, но противоположный по знаку, что и бензол. [8] Полученные результаты являются прямым доказательством модели Хантера-Сандерса. Однако стекинг-взаимодействия, измеренные с использованием метода двойных мутантов, были на удивление малы, и авторы отмечают, что эти значения не могут быть перенесены в другие системы.
В последующем исследовании Hunter et al. в первом приближении подтверждено, что в энергиях взаимодействия взаимодействующих ароматических колец в двойном мутантном цикле преобладают электростатические эффекты. [13] Однако авторы отмечают, что важный вклад также вносят прямые взаимодействия с заместителями в кольце, обсуждаемые ниже. Действительно, взаимодействие этих двух факторов может привести к сложному поведению стекинг-взаимодействий пи, зависящему от заместителя и геометрии.
Модель прямого взаимодействия
[ редактировать ]Модель Хантера-Сандерса подверглась критике со стороны многочисленных исследовательских групп, предлагающих противоречивые экспериментальные и вычислительные доказательства взаимодействий суммирования пи, которые не определяются в первую очередь электростатическими эффектами. [14]
Наиболее четкие экспериментальные доказательства против эффектов электростатических заместителей были получены Рашкиным и Уотерсом. [15] В качестве модельной системы для пи-взаимодействий стэкинга они использовали мета- и паразамещенные бромиды N-бензил-2-(2-фторфенил)пиридиния, которые укладываются в параллельную смещенную конформацию. В их системе метиленовый линкер препятствует благоприятным Т-образным взаимодействиям. Как и в предыдущих моделях, относительная сила стэкинг-взаимодействий пи измерялась с помощью ЯМР как скорость вращения вокруг биарильной связи, поскольку стэкинг-взаимодействия пи разрушаются в переходном состоянии . Паразамещенные кольца имели небольшие вращательные барьеры, которые увеличивались по мере увеличения электроноакцепторных групп, что согласуется с предыдущими результатами. Однако метазамещенные кольца имели гораздо большие барьеры вращения, несмотря на почти одинаковую электронную плотность в ароматическом кольце. Авторы объясняют это несоответствие прямым взаимодействием края атомов водорода одного кольца с электроотрицательными заместителями другого кольца. Это утверждение подтверждается данными о химическом сдвиге рассматриваемого протона. [ нужна ссылка ]
Большая часть подробного анализа относительного вклада факторов в суммирование чисел «пи» была подтверждена расчетами. Шерилл и Синнокрот сообщили об удивительном открытии, сделанном с использованием теории высокого уровня, что все замещенные димеры бензола имеют более благоприятные взаимодействия связывания, чем димер бензола в сэндвич-конфигурации. [16] Более поздние вычислительные работы группы Шерилла показали, что эффекты заместителей в сэндвич-конфигурации аддитивны, что указывает на сильное влияние дисперсионных сил и прямых взаимодействий между заместителями. [17] Отмечено, что взаимодействия между замещенными бензолами в Т-образной конфигурации имеют более сложный характер. Наконец, Шерилл и Синнокрот в своей обзорной статье утверждают, что любое подобие тенденции, основанной на донорстве или отводе электронов заместителей, можно объяснить условиями обменного отталкивания и дисперсии. [18]

Хоук и Уилер также предоставили убедительные вычислительные доказательства важности прямого взаимодействия при складывании чисел Пи. [19] В своем анализе замещенных димеров бензола в сэндвич-конформации они смогли обобщить свои результаты, используя чрезвычайно простую модель, в которой замещенный бензол Ph–X был заменен на H–X. Примечательно, что эта грубая модель привела к той же тенденции в относительных энергиях взаимодействия и сильно коррелировала со значениями, рассчитанными для Ph – X. Это открытие позволяет предположить, что эффекты заместителя в димере бензола обусловлены прямым взаимодействием заместителя с ароматическим кольцом и что пи-система замещенного бензола не участвует. Этот последний пункт более подробно рассматривается ниже.
Подводя итог, можно сказать, что относительный вклад электростатики, дисперсии и прямых взаимодействий в эффекты заместителей, наблюдаемые при стэкинг-взаимодействиях пи, сильно зависят от геометрии и плана эксперимента. Отсутствие консенсуса по этому вопросу может просто отражать сложность проблемы.
Требование ароматичности
[ редактировать ]Традиционное понимание укладки пи включает квадрупольные взаимодействия между делокализованными электронами на p-орбиталях. Другими словами, для того, чтобы это взаимодействие произошло, должна быть необходима ароматичность. Однако несколько групп представили противоположные доказательства, поставив под сомнение, является ли укладка пи уникальным явлением или оно распространяется и на другие нейтральные молекулы с закрытой оболочкой.
В эксперименте, мало чем отличающемся от других, упомянутых выше, Паливал и соавторы построили молекулярный торсионный баланс из арилового эфира с двумя конформационными состояниями. [20] Свернутое состояние имело четко выраженное пи-стакинг-взаимодействие с Т-образной геометрией, тогда как развернутое состояние не имело арил-арильных взаимодействий. Химические сдвиги ЯМР двух конформаций были различны и могли быть использованы для определения соотношения двух состояний, которое интерпретировалось как мера внутримолекулярных сил. Авторы сообщают, что предпочтение свернутого состояния характерно не только для ариловых эфиров. Например, циклогексиловый эфир больше благоприятствует свернутому состоянию, чем фениловый эфир, а трет-бутиловый эфир благоприятствует свернутому состоянию с большей предпочтительностью, чем тот, который демонстрирует любой ариловый эфир. Это говорит о том, что ароматичность не является строгим требованием для благоприятного взаимодействия с ароматическим кольцом.
Другие доказательства результатов неароматических взаимодействий стэкинга пи включают критические исследования в области теоретической химии, объясняющие основные механизмы эмпирических наблюдений. Гримме сообщил, что энергии взаимодействия более мелких димеров, состоящих из одного или двух колец, очень схожи как для ароматических, так и для насыщенных соединений. [21] Это открытие имеет особое значение для биологии и предполагает, что вклад пи-систем в такие явления, как сложенные нуклеиновые основания, может быть переоценен. Однако было показано, что повышенное стабилизирующее взаимодействие наблюдается для крупных ароматических димеров. Как отмечалось ранее, эта энергия взаимодействия сильно зависит от геометрии. Действительно, большие ароматические димеры стабилизируются относительно своих насыщенных аналогов только в сэндвич-геометрии, тогда как их энергии аналогичны при Т-образном взаимодействии.
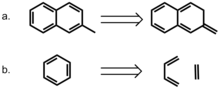
Более прямой подход к моделированию роли ароматичности был использован Блумом и Уилером. [22] Авторы сравнили взаимодействие бензола либо с 2-метилнафталином, либо с его неароматическим изомером 2-метилен-2,3-дигидронафталином. Последнее соединение позволяет сохранить количество p-электронов, однако устраняя эффекты делокализации. Удивительно, но энергии взаимодействия с бензолом выше для неароматического соединения, что позволяет предположить, что локализация пи-связи благоприятна при взаимодействиях стэкинга пи. Авторы также рассмотрели гомодесмотическое расслоение бензола на этилен и 1,3-бутадиен и сравнили эти взаимодействия в сэндвиче с бензолом. Их расчет показывает, что энергия взаимодействия между бензолом и гомодесмотическим бензолом выше, чем у димера бензола как в сэндвич-, так и в параллельно-смещенных конформациях, что еще раз подчеркивает благоприятность локализованных взаимодействий пи-связей. Эти результаты убедительно свидетельствуют о том, что ароматичность не требуется для стекинг-взаимодействий в этой модели.
Даже в свете этих доказательств Гримме приходит к выводу, что сложение чисел действительно существует. [21] Однако он предупреждает, что меньшие кольца, особенно в Т-образных конформациях, ведут себя существенно не иначе, чем их насыщенные аналоги, и что этот термин следует указывать для более крупных колец в сложенных конформациях, которые, по-видимому, действительно демонстрируют кооперативный пи-электронный эффект.
Примеры
[ редактировать ]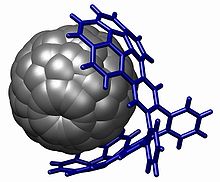
Одна демонстрация укладки находится в buckycatcher . [23] Этот молекулярный пинцет основан на двух вогнутых чашах , которые идеально подходят для одной выпуклой фуллерена молекулы . Комплексообразование происходит просто путем выпаривания раствора в толуоле, содержащего оба соединения. В растворе константа ассоциации 8600 М. −1 измеряется на основе изменений химических сдвигов ЯМР . [ нужна ссылка ]

Укладка Pi преобладает в кристаллических структурах белков, а также способствует взаимодействиям между небольшими молекулами и белками. В результате взаимодействия пи-пи и катион-пи являются важными факторами в рациональном дизайне лекарств. [24] Одним из примеров является одобренный FDA ингибитор ацетилхолинэстеразы (АХЭ) такрин , который используется при лечении болезни Альцгеймера . Предполагается, что такрин взаимодействует с индольным кольцом Trp84 посредством пи-стэкинга, и это взаимодействие было использовано при рациональном создании новых ингибиторов AChE. [25]
Добавление фармакологических активных соединений
[ редактировать ]
Несколько вариантов пи-координированных фенилов даже были протестированы с использованием переходных металлов для укладки η. 6 -фенилтропаны с использованием циклопентадиенила и трикарбонила вместо бензола. Что в случае с трикарбонилом удвоило сродство соединения к предполагаемому участку лиганда (предполагается, что возникающие в результате электростатические воздействия более способствуют достижению цели). [26]
Супрамолекулярная сборка
[ редактировать ]
π-системы являются строительными блоками супрамолекулярной сборки , поскольку они часто участвуют в нековалентных взаимодействиях. Примером π–π-взаимодействий в супрамолекулярной сборке является синтез катенана . Основная задача синтеза катенана — контролируемое соединение молекул. Стоддарт и его коллеги разработали серию систем, использующих сильные π – π-взаимодействия между богатыми электронами производными бензола и бедными электронами пиридиниевыми кольцами. [27] [2]Катанен был синтезирован реакцией бис(пиридиния) ( А ), биспарафенилен-34-краун-10 ( Б ) и 1,4-бис(бромметил)бензола ( С ) (рис. 2). π–π-взаимодействие между A и B привело к образованию взаимосвязанного матричного промежуточного соединения, которое далее циклизовалось в результате реакции замещения соединением C с образованием продукта [2] катенана.
См. также
[ редактировать ]- Нековалентное взаимодействие
- Дисперсия (химия)
- Взаимодействие катион-пи
- Интеркаляция (биохимия)
- Интеркаляция (химия)
Ссылки
[ редактировать ]- ^ Смит, Майкл Б.; Марч, Джерри (2007), Продвинутая органическая химия: реакции, механизмы и структура (6-е изд.), Нью-Йорк: Wiley-Interscience, стр. 114, ISBN 978-0-471-72091-1
- ^ Jump up to: а б с Мартинес CR, Айверсон Б.Л. (2012). «Переосмысление термина «пи-стекинг» » . Химическая наука . 3 (7): 2191. doi : 10.1039/c2sc20045g . hdl : 2152/41033 . ISSN 2041-6520 . S2CID 95789541 .
- ^ Льюис М., Бэгвилл С., Хардебек Л., Wireduaah S (2016). «Современные вычислительные подходы к пониманию взаимодействий ароматических соединений» . В Джонсон Д.В., Хоф Ф. (ред.). Ароматические взаимодействия: границы знаний и применения . Англия: Королевское химическое общество. стр. 1–17. ISBN 978-1-78262-662-6 .
- ^ Jump up to: а б Макгои ГБ, Ганье М, Раппе А.К. (июнь 1998 г.). «Взаимодействия пи-стекинга. Живы и здоровы в белках» . Журнал биологической химии . 273 (25): 15458–63. дои : 10.1074/jbc.273.25.15458 . ПМИД 9624131 .
- ^ Картер-Фенк К., Герберт Дж. М. (ноябрь 2020 г.). «Переосмысление π-стекинга». Физическая химия Химическая физика . 22 (43): 24870–24886. дои : 10.1039/d0cp05039c . ПМИД 33107520 . S2CID 225083299 .
- ^ Jump up to: а б с Синнокрот М.О., Валеев Э.Ф., Шерил К.Д. (сентябрь 2002 г.). «Оценки ab initio предела для пи-пи-взаимодействий: димер бензола». Журнал Американского химического общества . 124 (36): 10887–10893. дои : 10.1021/ja025896h . ПМИД 12207544 .
- ^ Jump up to: а б Хубер Р.Г., Маргрейтер М.А., Фукс Дж.Е., фон Графенштайн С., Таутерманн К.С., Лидл К.Р., Фокс Т. (май 2014 г.). «Гетероароматические энергетические ландшафты с π-складкой» . Журнал химической информации и моделирования . 54 (5): 1371–1379. дои : 10.1021/ci500183u . ПМК 4037317 . ПМИД 24773380 .
- ^ Jump up to: а б Батталья М.Р., Букингем А.Д., Уильямс Дж.Х. (1981). «Электрические квадрупольные моменты бензола и гексафторбензола». хим. Физ. Летт . 78 (3): 421–423. Бибкод : 1981CPL....78..421B . дои : 10.1016/0009-2614(81)85228-1 .
- ^ Райли К.Э., Хобза П. (апрель 2013 г.). «О значении и происхождении ароматических взаимодействий в химии и биодисциплинах». Отчеты о химических исследованиях . 46 (4): 927–936. дои : 10.1021/ar300083h . ПМИД 22872015 .
- ^ Хантер Калифорния, Сандерс Дж. К. (1990). «Природа π – π-взаимодействий». Дж. Ам. хим. Соц . 112 (14): 5525–5534. дои : 10.1021/ja00170a016 .
- ^ Коцци Ф., Чинквини М., Аннузиата Р., Сигел Дж.С. (1993). «Доминирование полярного / .pi. над эффектами переноса заряда в многоуровневых взаимодействиях фенила». Дж. Ам. хим. Соц . 115 (12): 5330–5331. дои : 10.1021/ja00065a069 .
- ^ Jump up to: а б Кокрофт С.Л., Хантер К.А., Лоусон К.Р., Перкинс Дж., Урч С.Дж. (июнь 2005 г.). «Электростатический контроль ароматических взаимодействий при штабелировании». Журнал Американского химического общества . 127 (24): 8594–8595. дои : 10.1021/ja050880n . ПМИД 15954755 .
- ^ Кокрофт С.Л., Перкинс Дж., Зонта С., Адамс Х., Спей С.Э., Лоу СМ и др. (апрель 2007 г.). «Влияние заместителей на ароматические взаимодействия». Органическая и биомолекулярная химия . 5 (7): 1062–1080. дои : 10.1039/b617576g . ПМИД 17377660 . S2CID 37409177 .
- ^ Мартинес, Челси Р.; Айверсон, Брент Л. (2012). «Переосмысление термина «пи-стекинг» ». Химическая наука . 3 (7): 2191. дои : 10.1039/C2SC20045G . hdl : 2152/41033 .
- ^ Рашкин М.Дж., Уотерс М.Л. (март 2002 г.). «Неожиданные эффекты заместителей в смещенных взаимодействиях пи-пи в воде». Журнал Американского химического общества . 124 (9): 1860–1861. дои : 10.1021/ja016508z . ПМИД 11866592 .
- ^ Синнокрот М.О., Шерил КД (2003). «Неожиданные эффекты заместителей при взаимодействии π-стекинга лицом к лицу». Дж. Физ. хим. А. 107 (41): 8377–8379. Бибкод : 2003JPCA..107.8377S . дои : 10.1021/jp030880e .
- ^ Рингер А.Л., Синнокрот М.О., Lively RP, Sherrill CD (май 2006 г.). «Влияние нескольких заместителей на сэндвич- и Т-образные пи-пи-взаимодействия». Химия: Европейский журнал . 12 (14): 3821–3828. дои : 10.1002/chem.200501316 . ПМИД 16514687 .
- ^ Синнокрот М.О., Шерил CD (сентябрь 2006 г.). «Высокоточные квантово-механические исследования пи-пи-взаимодействий в димерах бензола». Журнал физической химии А. 110 (37): 10656–10668. Бибкод : 2006JPCA..11010656S . дои : 10.1021/jp0610416 . ПМИД 16970354 .
- ^ Jump up to: а б Уилер С.Е., Хоук К.Н. (август 2008 г.). «Эффекты заместителей в димере бензола обусловлены прямым взаимодействием заместителей с незамещенным бензолом» . Журнал Американского химического общества . 130 (33): 10854–10855. дои : 10.1021/ja802849j . ПМЦ 2655233 . ПМИД 18652453 .
- ^ Паливал С., Гейб С., Уилкокс К.С. (1994). «Молекулярный торсионный баланс для слабых сил молекулярного распознавания. Влияние ароматических взаимодействий между краями и гранями «наклоненной Т» на конформационный отбор и структуру твердого тела». Дж. Ам. хим. Соц . 116 (10): 4497–4498. дои : 10.1021/ja00089a057 .
- ^ Jump up to: а б Гримме С (2008). «Действительно ли существуют особые нековалентные стекирующие взаимодействия пи-пи?» . Ангеванде Хеми . 47 (18): 3430–3434. дои : 10.1002/anie.200705157 . ПМИД 18350534 .
- ^ Jump up to: а б Блум Дж.В., Уилер С.Е. (2011). «Устранение ароматичности ароматических взаимодействий». Энджью. Хим . 123 (34): 7993–7995. Бибкод : 2011АнгЧ.123.7993Б . дои : 10.1002/ange.201102982 .
- ^ Jump up to: а б Сигула А., Фрончек Ф.Р., Сигула Р., Рабидо П.В., Олмстед М.М. (апрель 2007 г.). «Двойной вогнутый ловец углеводородов». Журнал Американского химического общества . 129 (13): 3842–3843. дои : 10.1021/ja070616p . ПМИД 17348661 . S2CID 25154754 .
- ^ Бабина Р.Э., Бендер С.Л. (август 1997 г.). «Молекулярное распознавание комплексов белок-минус-лиганд: применение к разработке лекарств». Химические обзоры . 97 (5): 1359–1472. дои : 10.1021/cr960370z . ПМИД 11851455 .
- ^ да Силва CH, Кампо ВЛ, Карвальо I, Тафт Калифорния (октябрь 2006 г.). «Молекулярное моделирование, докинг и исследования ADMET применительно к созданию нового гибрида для лечения болезни Альцгеймера». Журнал молекулярной графики и моделирования . 25 (2): 169–175. дои : 10.1016/j.jmgm.2005.12.002 . ПМИД 16413803 .
- ^ Сингх С. (март 2000 г.). «Химия, дизайн и взаимосвязь структура-активность антагонистов кокаина». Химические обзоры . 100 (3): 925–1024. дои : 10.1021/cr9700538 . ПМИД 11749256 .
- ^ Эштон П.Р., Гуднау Т.Т., Кайфер А.Е., Реддингтон М.В., Славин А.М., Спенсер Н. и др. (1989). «А [2] Катенан на заказ». Дж. Энджью. хим. Межд. Эд . 28 (10): 1396–1399. дои : 10.1002/anie.198913961 .
Внешние ссылки
[ редактировать ]- Луо Р., Гилсон Х.С., Поттер М.Дж., Гилсон М.К. (январь 2001 г.). «Физическая основа укладки оснований нуклеиновых кислот в воде» . Биофизический журнал . 80 (1): 140–148. Бибкод : 2001BpJ....80..140L . дои : 10.1016/S0006-3495(01)76001-8 . ПМК 1301220 . ПМИД 11159389 .
- Ларри Вольф (2011): π-π (π-стекинг) взаимодействия: происхождение и модуляция


