Кораннулен

| |

| |
| Имена | |
|---|---|
| Имя IUPAC
Dibenzo [ Ghi , Me ] Fluorentaune [ 1 ]
| |
| Другие имена
[5] Цирлен
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| Chemspider | |
PubChem CID
|
|
| НЕКОТОРЫЙ | |
Comptox Dashboard ( EPA )
|
|
| Характеристики | |
| C 20 H 10 | |
| Молярная масса | 250.29 g/mol |
За исключением случаев, когда отмечены, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа).
| |
Кораннулен является полициклическим ароматическим углеводородом с химической формулой C 20 H 10 . [ 2 ] Молекула слитого состоит из циклопентанового кольца, с 5 бензольными кольцами, поэтому другое название для него - [5] Circulene . Это представляет научный интерес, потому что это геодезический полиарен и может считаться фрагментом Buckminsterfullerene . Из -за этого соединения, а также формы чаши, Кораннулен также известен как Buckybowl. Buckybowls - это фрагменты Buckyballs. Кораннулена демонстрирует инверсию чаши к кусочке с инверсионным барьером 10,2 ккал / моль (42,7 кДж / моль) при -64 ° C. [ 3 ]
Синтез
[ редактировать ]Несколько синтетических маршрутов существуют в Кораннулене. Методы флэш-вакуумного пиролиза, как правило, имеют более низкую химическую доходность , чем синтез-химии раствора, но предлагают маршруты для большего количества производных. Кораннулен был впервые изолирован в 1966 году с помощью многоэтажного органического синтеза. [ 4 ] В 1971 году сообщалось о синтезе и свойствах Кораннулана. [ 5 ] Метод флэш -вакуумного пиролиза следовал в 1991 году. [ 6 ] Один синтез, основанный на химии растворов [ 7 ] состоит из нуклеофильного смещения - реакция элиминации октабромида с гидроксидом натрия :
Заместители брома удаляются с избытком n -бутиллита .
Синтез коранулена шкалы килограмма был достигнут. [ 8 ]
Много усилий направлено на функционализацию коранта коранулена с помощью новых функциональных групп, таких как группы Ethynyl, [ 3 ] [ 9 ] [ 10 ] эфирные группы, [ 11 ] Thioether Groups, [ 12 ] платиновые функциональные группы, [ 13 ] арильные группы, [ 14 ] Феналенил слился [ 15 ] и расширения Индено. [ 16 ] и ферроценовые группы. [ 17 ]
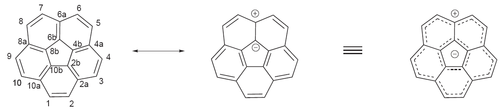
Ароматичность
[ редактировать ]Наблюдаемая ароматичность для этого соединения объясняется так называемой моделью аннулен-ватин-аннулен . Согласно этой модели, Кораннулен состоит из ароматического 6 -я циклопентадиенилового аниона, окруженного ароматическим 14 электронным аннуленильным катионом . Эта модель была предложена Бартом и Лоутоном в первом синтезе Кораннулена в 1966 году. [ 4 ] Они также предложили тривиальное название «Кораннулен», которое получено из модели аннулен-ватин-аннулен: Core + Annulene.
Однако более поздние теоретические расчеты оспорили обоснованность этого приближения. [ 18 ] [ 19 ]
Реакция
[ редактировать ]Снижение
[ редактировать ]Кораннулен может быть уменьшена до тетрааниона в серии одноэлектронных сокращений . Это было выполнено с щелочными металлами , электрохимически и с основаниями. Кораннулена Дианион является антиароматическим , а тетраанион снова аромат . С литием в качестве восстановительного агента два тетраанионы образуют супрамолекулярный димер с двумя чашами, сложенными друг в друга с 4 литийными ионами между и 2 парами выше и ниже стека. [ 20 ] Этот мотив самосборки был применен в организации фуллерена. Пента-замещенные фуллерены (с метил или фенильные группы), заряженные пятью электронами, образуют супрамолекулярные димеры с помощью комплементарной чаши с тетраанионом коранулена, «сшитые» интерстициальными литийными катионами. [ 21 ] В связанной системе 5 литий -ионы зажаты между двумя чашами Кораннулена [ 22 ]
В одном циклопенте [BC] Кораннулена вогнутая вогнутая агрегат наблюдается с помощью ЯМР -спектроскопии с 2 C -Li -C -связующими связями, соединяющими тетраанионы. [ 23 ]
Металлы имеют тенденцию связываться с выпуклой поверхностью аннулен. Вогнутое связывание было сообщено для системы эфира цезиума / короны [ 24 ]
Окисление
[ редактировать ]УФ-193-нм фотоионизация эффективно удаляет π-электрон из двойного вырожденного e 1 -homo, расположенного в ароматической сети электронов, дающих катион радикала коранулентного радикала. [ 25 ] Благодаря вырождению в орбитале гомо, катион радикалов кораннулена нестабильна в его первоначальном молекулярном расположении C 5V и, следовательно, зависит от виброконного искажения Jahn-Teller (JT).
Используя электрораспылительную ионизация, была получена протонированный катион коранулена, в котором, как наблюдалось сайт протонации, находится на периферийном SP 2 -Коглельный атом. [ 25 ]
Реакция с электрофилами
[ редактировать ]Кораннулен может реагировать с электрофилами, образуя карбокацию кораннулена . Реакция с хлорметаном и хлоридом алюминия приводит к образованию ALCL 4 − соль с метильной группой, расположенной в центре с катионным центром на ободе. Анализ дифракции рентгеновского излучения показывает, что новая углерод-углеродная связь удлинена (157 вечера) [ 26 ]
Bicorannulenyl
[ редактировать ]Бикораннуленил является продуктом дегидрогенической связи кораннулена. С формулой C 20 H 9 -C 20 H 9 она состоит из двух единиц коранулена, соединенных через одну связь CC. Стереохимия молекулы состоит из двух хиральных элементов: асимметрии отдельно замещенного корануленила и спирального поворота о центральной связи. В нейтральном состоянии бикораннуленил существует как 12 конформеров, которые взаимодействуют через множественные инверсии чаши и обстреливания. [ 27 ] Когда бикораннуленил сводится к дианиону с металлом калия, центральная связь предполагает значительный характер с двойным связью. Это изменение объясняется орбитальной структурой, которая имеет орбитализированную ламо, локализованную на центральной связи. [ 28 ] Когда бикораннуленил сводится к октааниону с литием-металлом, он сами входит в супрамолекулярные олигомеры. [ 29 ] Этот мотив иллюстрирует «заряженную полиаренную укладку».
Исследовать
[ редактировать ]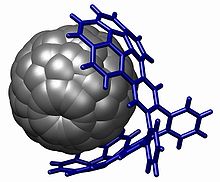
Группа Corannulene используется в химии хозяина - Guest с взаимодействиями на основе укладки PI , особенно с Fullerenes (The Burcycatcher) [ 30 ] [ 31 ] но также с нитробензолом [ 32 ]
Алкилзамещенные корануленты образуют термотропную шестиугольную столбчатую жидкокристаллическую мезофазу . [ 33 ] Кораннулен также использовалась в качестве основной группы в дендримере . [ 14 ] Как и другие ПАУ, Кораннулена связывает металлы. [ 34 ] [ 35 ] [ 36 ] [ 37 ] [ 38 ] [ 39 ] [ 40 ] Кораннульены с группами этиньяна исследуются на предмет их потенциального использования в качестве синих излучателей. [ 10 ] Структура анализировали с помощью инфракрасной спектроскопии, спектроскопии комбинационного рама и рентгеновской фотоэлектронной спектроскопии. [ 41 ]
Смотрите также
[ редактировать ]Ссылки
[ редактировать ]- ^ Флуорантен так назван в честь его флуоресцентного свойства. Это не фториновое соединение.
- ^ Скотт, LT; Бронштейн, он; Preda, DV; Ansems, RBM; Bratcher, MS; Хаген С. (1999). «Геодезические полиарены с открытыми вогнутыми поверхностями» . Чистая и прикладная химия . 71 (2): 209. doi : 10.1351/pac199971020209 . S2CID 37901191 .
- ^ Jump up to: а беременный Скотт, LT; Hashemi, MM; Bratcher, MS (1992). «Инверсия коранулена к чаше-чаше-чаше-чаше-чаше-чаше-чаше-чашу быстрая при комнатной температуре». Журнал Американского химического общества . 114 (5): 1920–1921. doi : 10.1021/ja00031a079 .
- ^ Jump up to: а беременный Барт, мы; Перевод, RG (1966). Девенцо. общество Американское 88 (2): 380–381. doi : 10.1021/ja .
- ^ Лоутон, Ричард Дж.; Барт, Уэйн Э. (апрель 1971 г.). «Синтез кораннулена». Журнал Американского химического общества . 93 (7): 1730–1745. doi : 10.1021/ja00736a028 . S2CID 94872875 .
- ^ Скотт, LT; Hashemi, MM; Мейер, DT; Уоррен, HB (1991). «Кораннулен. Удобный новый синтез». Журнал Американского химического общества . 113 (18): 7082–7084. doi : 10.1021/ja00018a082 .
- ^ Sygula, A.; Rabideau, PW (2000). «Практический, крупномасштабный синтез системы кораннулена». Журнал Американского химического общества . 122 (26): 6323–6324. doi : 10.1021/ja0011461 .
- ^ Баттерфилд, А.; Гиломен, б.; Siegel, J. (2012). «Производство в масштабе килограмма Кораннулена». Органические процессы исследования и разработки . 16 (4): 664–676. doi : 10.1021/op200387s .
- ^ Wu, y.; Бандера, Д.; Maag, R.; Линден, А.; Baldridge, K.; Siegel, J. (2008). «Multiethynyl Corannulenes: синтез, структура и свойства». Журнал Американского химического общества . 130 (32): 10729–10739. doi : 10.1021/ja802334n . PMID 18642812 .
- ^ Jump up to: а беременный Mack, J.; Фогель, П.; Джонс, Д.; Кавал, Н.; Саттон А. (2007). «Разработка синих излучателей на основе Кораннулена». Органическая и биомолекулярная химия . 5 (15): 2448–2452. doi : 10.1039/b705621d . PMID 17637965 .
- ^ Gershoni-Poranne, R.; Pappo, D.; Solel, E.; Кейнан, Э. (2009). «Коранулентные эфиры через конденсацию Ullmann». Органические буквы . 11 (22): 5146–5149. Doi : 10.1021/ol902352k . PMID 19905024 .
- ^ Baldridge, K.; Hardcastle, K.; Seiders, T.; Siegel, J. (2010). «Синтез, структура и свойства Decakis (фенилтио) кораннулена». Органическая и биомолекулярная химия . 8 (1): 53–55. doi : 10.1039/b919616a . PMID 20024131 .
- ^ Choi, H.; Ким, C.; Парк, KM; Ким, Дж.; Kang, Y.; KO, J. (2009). «Синтез и структура пента-платиновых σ-связанных производных коранулена». Журнал органометаллической химии . 694 (22): 3529–3532. doi : 10.1016/j.jorganchem.2009.07.015 .
- ^ Jump up to: а беременный Pappo, D.; Mejuch, T.; Reany, o.; Solel, E.; Gurram, M.; Кейнан, Э. (2009). «Разнообразная функционализация кораннулена: легкий доступ к пентагональной суперструктуре». Органические буквы . 11 (5): 1063–1066. doi : 10.1021/ol8028127 . PMID 19193048 .
- ^ Nishida, S.; Morita, Y.; Уэда, а.; Kobayashi, T.; Fukui, K.; Огасавара, К.; Сато, К.; Takui, T.; Накасуджи, К. (2008). «Кривая структурированная феналениловая химия: синтез, электронная структура и барьер инверсии чаши в анионе коранулена феналенилового коранулина». Журнал Американского химического общества . 130 (45): 14954–14955. doi : 10.1021/ja806708j . PMID 18937470 .
- ^ Steinberg, B.; Джексон, E.; Филатов, а.; Wakamiya, A.; Петрухина, М.; Скотт Л. (2009). «Ароматические PI-системы более изогнуты, чем C (60). Полное семейство всех инденокраннуленов, синтезируемых итеративными микроволновыми внутримолекулярными арилированиями». Журнал Американского химического общества . 131 (30): 10537–10545. doi : 10.1021/ja9031852 . PMID 19722628 .
- ^ Тополински, Берит; Шмидт, Бернд М.; Катан, Майкл; Троянов, Сержж I.; Ленц, Дитер (2012). «Корануленилферроценов: к 1D нековалентному металлическому нанопроволосу». Химический Общение 48 (50): 6298–6300. doi : 10.1039/c2cc32275g . PMID 22595996 .
- ^ Sygula, A.; Rabideau, PW (1995). «Структурные и инверсионные барьеры Кораннулена, его Дианиона и Тетрааниона. Исследование AB initio». Журнал молекулярной структуры: Теохем . 333 (3): 215–226. doi : 10.1016/0166-1280 (94) 03961-J .
- ^ Монако, Г.; Скотт, Л.; Занаси Р. (2008). «Магнитный Еврипи в Кораннулине». Журнал физической химии а . 112 (35): 8136–8147. Bibcode : 2008jpca..112.8136m . doi : 10.1021/jp8038779 . PMID 18693706 .
- ^ Айалон, а.; Sygula, A.; Ченг, П.; Рабиновиц, М.; Rabideau, P.; Скотт Л. (1994). «Стабильные молекулярные бутерброды высокого порядка: углеводородные полианионные пары с множественными ионами лития внутри и снаружи». Наука . 265 (5175): 1065–1067. Bibcode : 1994sci ... 265.1065a . doi : 10.1126/science.265.5175.1065 . PMID 17832895 . S2CID 4979579 .
- ^ Апрахамский, я.; Эйзенберг, Д.; Хоффман, Р.; Sternfeld, T.; Matsuo, y.; Джексон, E.; Накамура, E.; Скотт, Л.; Sheradsky, T.; Рабиновиц М. (2005). «Упаковка с шариковыми геодезическими полиаренами с наддувом: связывание с помощью ионов интерстициального лития». Журнал Американского химического общества . 127 (26): 9581–9587. doi : 10.1021/ja0515102 . PMID 15984885 .
- ^ Забула, AV (2011). «Основной групповой металлический бутерброд: пять литий -катионов застряли между двумя коранулентными тетраанионными палубами». Наука . 333 (6045): 1008–1011. Bibcode : 2011sci ... 333.1008Z . doi : 10.1126/science.1208686 . PMID 21852497 . S2CID 1125747 .
- ^ Апрахамский, я.; Preda, D.; Bancu, M.; Белангер, А.; Sheradsky, T.; Скотт, Л.; Рабиновиц М. (2006). «Сокращение углеводородов в форме чаши: дианионы и тетраанионы аннулированных корануленов». Журнал органической химии . 71 (1): 290–298. doi : 10.1021/jo051949c . PMID 16388648 .
- ^ Spisak, sn; Забула, AV; Филатов, как; Рогачев, да; Петрухина, Массачусетс (2011). «Селективное эндо и EXO -связывание щелочных металлов с Coranuale». Angewandte Chemie International Edition . 50 (35): 8090–8094. Doi : 10.1002/anie 201103028 . PMID 21748832 .
- ^ Jump up to: а беременный Галуэ, Эктор Альваро; Райс, Кори А.; Steill, Jeffrey D.; Oomens, JOS (1 января 2011 г.). «Инфракрасная спектроскопия ионизированного коранолина в газовой фазе» (PDF) . Журнал химической физики . 134 (5): 054310. Bibcode : 2011JCHPH.134E4310G . doi : 10.1063/1,3540661 . PMID 21303123 .
- ^ Забула, AV; Spisak, sn; Филатов, как; Рогачев, да; Петрухина, Массачусетс (2011). «Деформационная ловушка для высокореактивных электрофилов: структурная характеристика карбокаций в форме миски». Angewandte Chemie International Edition . 50 (13): 2971–2974. doi : 10.1002/anie.201007762 . PMID 21404379 .
- ^ Эйзенберг, Д.; Филатов, а.; Джексон, E.; Рабиновиц, М.; Петрухина, М.; Скотт, Л.; Шенхар Р. (2008). «Bicorannulenyl: стереохимия Biaryl C40H18, состоящий из двух хиральных чаш». Журнал органической химии . 73 (16): 6073–6078. doi : 10.1021/jo800359z . PMID 18505292 .
- ^ Эйзенберг, Д.; Quimby, JM; Джексон, EA; Скотт, LT; Шенхар Р. (2010). «Бикораннуленил Дианион: заряженный переполненный этилен». Angewandte Chemie International Edition . 49 (41): 7538–7542. doi : 10.1002/anie.201002515 . PMID 20814993 .
- ^ Эйзенберг, Д.; Quimby, JM; Джексон, EA; Скотт, LT; Шенхар Р. (2010). «Высокоряженные супрамолекулярные олигомеры на основе димеризации кораннулентного тетрааниона». Химическая связь . 46 (47): 9010–9012. doi : 10.1039/c0cc03965a . PMID 21057679 .
- ^ Sygula, A.; Fronczek, F.; Sygula, R.; Rabideau, P.; Olmstead, M. (2007). «Двойной вогнутый гидроуглельный шкафчик». Журнал Американского химического общества . 129 (13): 3842–3843. doi : 10.1021/ja070616p . PMID 17348661 . S2CID 25154754 .
- ^ Вонг, Б.М. (2009). «Нековалентные взаимодействия в супрамолекулярных комплексах: исследование по кораннулину и двойному вогнутому ведению шкафы». Журнал вычислительной химии . 30 (1): 51–56. Arxiv : 1004,4243 . doi : 10.1002/jcc.21022 . PMID 18504779 . S2CID 18247078 .
- ^ Kobryn, L.; Генри, WP; Fronczek, FR; Sygula, R.; Sygula, A. (2009). «Молекулярные зажимы и пинцет с кораннулентными клещами». Тетраэдр буквы . 50 (51): 7124–7127. doi : 10.1016/j.tetlet.2009.09.177 .
- ^ Miyajima, D.; Таширо, К.; Araoka, F.; Taftzoe, H.; Ким, Дж.; Като, К.; Таката, М.; Аида, Т. (2009). «Жидкий кристаллический коранулен, реагирующий на электрическое поле». Журнал Американского химического общества . 131 (1): 44–45. doi : 10.1021/ja808396b . PMID 19128171 .
- ^ Seiders, T. Jon; Baldridge, Kim K.; О'Коннор, Джозеф М.; Зигель, Джей С. (1997). «Координация металла гексахапто с изогнутыми полиароматическими углеводородными поверхностями: первый переходной металл коранно -комплекс». J. Am. Химический Соц 119 (20): 4781–4782. doi : 10.1021/ja964380t .
- ^ Зигель, Джей С.; Baldridge, Kim K.; Линден, Энтони; Дорта, Рето (2006). «D8 Rhodium и Iridium Complexes of Corannulene». J. Am. Химический Соц 128 (33): 10644–10645. doi : 10.1021/ja062110x . PMID 16910635 .
- ^ Петрухина, Массачусетс (2008). «Координация Buckybowls: первый вогнутый металлический комплекс». Angewandte Chemie International Edition на английском языке . 47 (9): 1550–1552. doi : 10.1002/anie.200704783 . PMID 18214869 .
- ^ Чжу, Б.; Эллерн, А.; Sygula, A.; Sygula, R.; Angelici, RJ (2007). «η6-координация изогнутой углеродной поверхности коранулена (C20H10) к (η6-арен) M2+(M = RU, OS)». Органометаллики . 26 (7): 1721–1728. doi : 10.1021/om0610795 .
- ^ Петрухина, Массачусетс; Sevryugina, Y.; Рогачев, да; Джексон, EA; Скотт, LT (2006). «Кораннулен: предпочтение для связывания экзо-метал. Органометаллики . 25 (22): 5492–5495. doi : 10.1021/om060350f .
- ^ Siegel, J.; Baldridge, K.; Линден, А.; Дорта Р. (2006). «D8 Rhodium и Iridium Complexes of Corannulene». Журнал Американского химического общества . 128 (33): 10644–10645. doi : 10.1021/ja062110x . PMID 16910635 .
- ^ Бандера, Д.; Baldridge, KK; Линден, А.; Дорта, Р.; Siegel, JS (2011). «Стереоселективная координация C5-симметричных производных коранулена с энантиометрически чистым комплексом [RHI (NBD*)] металла». Angewandte Chemie International Edition . 50 (4): 865–867. doi : 10.1002/anie.201006877 . PMID 21246679 .
- ^ Диана, Нурамалина; Ямада, Ясухиро; Года, Сюн; Оно, Хиронубу; Кубо, Шинго; Сато, Сатоши (2021-02-01). «Углеродные материалы с высокой плотностью Пентагона» . Журнал материаловедения . 56 (4): 2912–2943. Bibcode : 2021jmats..56.2912d . doi : 10.1007/s10853-020-05392-x . ISSN 1573-4803 . S2CID 224784081 .

![Циклопента [до н.э.] Коранулен](http://upload.wikimedia.org/wikipedia/commons/thumb/2/21/Cyclopenta-bc-corannulene.png/100px-Cyclopenta-bc-corannulene.png)