Ацетоацетатдекарбоксилаза
| Ацетоацетатдекарбоксилаза | |||
|---|---|---|---|
 ацетоацетатдекарбоксилазы додекамера Структура со связанным 2-пентаноном, связанным в его активных центрах. | |||
| Идентификаторы | |||
| Номер ЕС. | 4.1.1.4 | ||
| Номер CAS. | 9025-03-0 | ||
| Базы данных | |||
| ИнтЭнк | вид IntEnz | ||
| БРЕНДА | БРЕНДА запись | ||
| Экспаси | Просмотр NiceZyme | ||
| КЕГГ | КЕГГ запись | ||
| МетаЦик | метаболический путь | ||
| ПРЯМОЙ | профиль | ||
| PDB Структуры | RCSB PDB PDBe PDBsum | ||
| Генная онтология | АмиГО / QuickGO | ||
| |||
Ацетоацетатдекарбоксилаза ( AAD или ADC ) представляет собой фермент ( EC 4.1.1.4 ), участвующий как в пути производства кетоновых тел у людей и других млекопитающих, так и в сольвентогенезе у бактерий. Ацетоацетатдекарбоксилаза играет ключевую роль в производстве растворителей, катализируя декарбоксилирование ацетоацетата с образованием ацетона и диоксида углерода . [ 1 ]
Этот фермент представляет особый интерес, поскольку является классическим примером того, как значения pKa ионизируемых групп в активном центре фермента могут быть значительно нарушены. В частности, значение pKa лизина 115 в активном центре необычно низкое, что позволяет образовывать промежуточное соединение основания Шиффа и катализировать. [ 2 ]
| ацетоуксусная кислота | Ацетоацетатдекарбоксилаза | ацетон | |

|

| ||
| СО 2 | |||

| |||
История
[ редактировать ]Ацетоацетатдекарбоксилаза — это фермент, имеющий большое историческое значение, особенно в Первой мировой войне и в создании государства Израиль . [ 3 ] Во время войны союзникам требовался чистый ацетон в качестве растворителя нитроцеллюлозы — легковоспламеняющегося соединения, которое является основным компонентом пороха. [ 4 ] В 1916 году биохимик и будущий первый президент Израиля Хаим Вейцман первым выделил Clostridium acetobutylicum , грамположительные анаэробные бактерии, в которых обнаружена ацетоацетатдекарбоксилаза. Вейцману удалось использовать способность организма производить ацетон из крахмала для массового производства взрывчатых веществ во время войны. [ 3 ] Это побудило правительства США и Великобритании внедрить процесс, разработанный Хаимом Вейцманом, на нескольких крупных заводах в Англии, Франции, Канаде и США. Благодаря научному вкладу Вейцмана во время Первой мировой войны он сблизился с влиятельными британскими лидерами, рассказывая им о своих сионистских убеждениях. [ 5 ] Одним из них был Артур Бальфур, человек, в честь которого была названа Декларация Бальфура — первый документ, заявляющий о британской поддержке создания еврейской родины.
Производство ацетона ацетоацетатдекарбоксилазосодержащими или клостридиальными бактериями использовалось в крупномасштабных промышленных синтезах в первой половине двадцатого века. В 1960-х годах промышленность заменила этот процесс менее дорогим и более эффективным химическим синтезом ацетона из нефти и нефтепродуктов. [ 6 ] Однако растет интерес к производству ацетона, который является более экологически чистым, что приводит к возобновлению использования бактерий, содержащих ацетоацетатдекарбоксилазу. [ 7 ] Точно так же становится популярной ферментация изопропанола и бутанола с использованием клостридий.
Структура
[ редактировать ]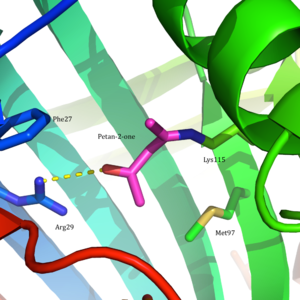
Ацетоацетатдекарбоксилаза представляет собой 365 кДа . комплекс гомододекамерной структуры массой [ 8 ] Общая структура состоит из антипараллельных β-листов и центрального семинитевого конусообразного β-цилиндра . Ядро этого β-цилиндра окружает активный центр каждого протомера фермента. Активный центр, состоящий из таких остатков, как Phe 27, Met97 и Tyr113 , в основном гидрофобен . Однако активный центр содержит два заряженных остатка: Arg29 и Glu76 .
Считается, что Arg29 играет роль в связывании субстрата, а Glu76, как полагают, играет роль в ориентации активного центра для катализа. Общая гидрофобная среда активного центра играет решающую роль в благоприятствовании нейтральной аминной формы Lys115, ключевого остатка, участвующего в образовании промежуточного соединения основания Шиффа . Считается, что другой важный остаток лизина, Lys116, играет важную роль в позиционировании Lys115 в активном сайте. Благодаря водородным связям с Ser16 и Met210 Lys116 позиционирует Lys115 в гидрофобном кармане активного центра, благоприятствуя нейтральной аминной форме.
Механизм реакции
[ редактировать ]
Ацетоацетатдекарбоксилаза Clostridium acetobutylicum катализирует декарбоксилирование ацетоацетата с образованием ацетона и диоксида углерода (рис. 1). Механизм реакции протекает через образование интермедиата основания Шиффа , ковалентно связанного с лизином 115 в активном центре. Первой линией поддержки этого механизма стал эксперимент по радиоактивному мечению , в котором исследователи пометили карбонильную группу ацетоацетата 18 О и заметил, что обмен кислорода на воду, используемую в качестве растворителя, является необходимой частью стадии декарбоксилирования. [ 9 ] Эти результаты подтвердили, что этот механизм реализуется через промежуточное соединение основания Шиффа между кетокислотой и аминокислотным остатком фермента.
Дальнейшие исследования привели к выделению пептидной последовательности активного центра и идентификации лизина активного центра, Lys115, который участвует в образовании промежуточного соединения основания Шиффа. [ 2 ] [ 10 ] Кроме того, более поздние эксперименты привели к открытию, что максимальная активность фермента наблюдается при pH 5,95, что позволяет предположить, что pK a ε-аммониевой группы Lys115 значительно нарушена в активном центре. [ 2 ] Если бы pK a не менялся в сторону понижения, остаток лизина оставался бы протонированным как катион аммония, что делало бы его нереактивным для нуклеофильного присоединения, необходимого для образования основания Шиффа.

Основываясь на этом открытии, Westheimer et al. непосредственно измерили pK a Lys115 в активном сайте, используя 5-нитросалициловый альдегид (5-NSA). Реакция 5-NSA с ацетоацетатдекарбоксилазой и последующее восстановление полученного основания Шиффа борогидридом натрия привела к включению репортерной молекулы 2-гидрокси-5-нитробензиламино в активный центр (рис. 2). Титрование фермента этой присоединенной репортерной группой показало, что pK a Lys115 снижается до 5,9 в активном сайте. [ 12 ] Эти результаты послужили основанием для предположения, что возмущение pK a Lys115 обусловлено его близостью к положительно заряженной ε-аммониевой группе Lys116 в активном центре. [ 2 ] Близлежащий положительный заряд может вызвать неблагоприятное электростатическое отталкивание, которое ослабляет связь NH Lys115. Предложение Вестхаймера и др. было дополнительно подтверждено исследованиями направленного мутагенеза . Когда Lys116 был мутирован на цистеин или аспарагин , было обнаружено, что pK a Lys115 значительно повышается до более чем 9,2, что указывает на то, что положительно заряженный Lys116 играет решающую роль в определении pK a Lys115. [ 2 ] Хотя кристаллическая структура еще не была решена, чтобы предоставить структурные доказательства, это предложение было широко принято и приведено в качестве хрестоматийного примера того, как можно точно организовать активный центр, чтобы нарушить pK a и повлиять на реакционную способность. [ 8 ]
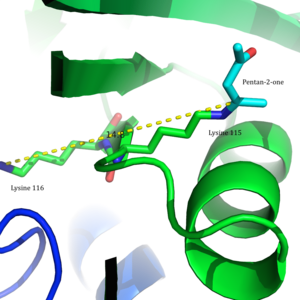
В 2009 году была расшифрована кристаллическая структура ацетоацетатдекарбоксилазы Clostridium acetobutylicum , что позволило оценить предложение Вестхаймера и др. с новой точки зрения. Из кристаллической структуры исследователи обнаружили, что Lys 115 и Lys 116 ориентированы в противоположных направлениях и разделены на 14,8 Å (рис. 3). [ 8 ] Такое расстояние делает маловероятным, что положительный заряд Lys116 способен влиять на pK a Lys115. Вместо этого Lys116 за счет водородных связей с Ser16 и Met210, вероятно, удерживает Lys115 в гидрофобном кармане активного сайта. Такое расположение нарушает стабильность протонированного катиона аммония Lys115, указывая тем самым, что возмущение pK a Lys115 происходит посредством « эффекта десольватации ».
Инактивация и ингибирование
[ редактировать ]Ацетоацетатдекарбоксилаза ингибируется рядом соединений. Уксусный ангидрид осуществляет электрофильную атаку на критический каталитический остаток Lys115 ацетоацетатдекарбоксилазы, инактивируя фермент. [ 13 ] Скорость инактивации оценивали по гидролизу синтетического субстрата 2,4-динитрофенилпропионата до динитрофенола ацетоацетатдекарбоксилазой. В присутствии уксусного ангидрида фермент инактивируется, не способный катализировать реакцию гидролиза 2,4-динитрофенилпропионата до динитрофенола. [ 14 ]
Ацетонилсульфонат действует как конкурентный ингибитор (K I =8,0 мМ), поскольку он имитирует характеристики природного субстрата, ацетоацетата (K M =8,0 мМ). [ 15 ] Моноанионная версия ацетонилфосфоната также является хорошим ингибитором (K I =0,8 мМ), более эффективным, чем моноэфир ацетонилфосфоната или дианион. [ 16 ] Эти данные указывают на то, что активный сайт очень дискриминационен и стерически ограничен.
Цианистый водород, по-видимому, является неконкурентным ингибитором , сочетаясь с основными соединениями Шиффа, образующимися в активном центре. [ 15 ] Добавление карбонильных соединений к ферменту в присутствии цианида водорода увеличивает способность цианида ингибировать ацетоацетатдекарбоксилазу, что позволяет предположить, что карбонильные соединения легко образуют основания Шиффа в активном центре. Цианистый водород наиболее эффективен в качестве ингибитора при pH 6, оптимальном pH для фермента, что позволяет предположить, что лимитирующей стадией катализа является образование промежуточного соединения основания Шиффа.
Бета-дикетоны , по-видимому, хорошо, но медленно ингибируют ацетоацетатдекарбоксилазу. Ацетоацетатдекарбоксилаза имеет K M для ацетоацетата 7×10. −3 M, тогда как фермент имеет K I для бензоилацетона 1,9×10. −6 М. [ 15 ] Енамин, скорее всего, образуется при взаимодействии бета-дикетонов со свободным ферментом.
Реакция ацетоацетатдекарбоксилазы с п- хлормеркурифенилсульфонатом (ЦМС) приводит к снижению каталитической активности при двух эквивалентах ЦМС на субъединицу фермента. [ 15 ] ЦМС взаимодействует с двумя сульфгидрильными группами, расположенными на каждой субъединице фермента. Дальнейшая инактивация происходит при добавлении третьего эквивалента CMS на субъединицу. Добавление свободного цистеина к ингибируемому ферменту способно обратить вспять ингибирование CMS ацетоацетатдекарбоксилазы.
Активность бактерий
[ редактировать ]Помимо Clostridium acetobutylicum, ацетоацетатдекарбоксилаза была обнаружена и изучена у следующих бактерий :
- Бацилла полимикса
- Хромобактерия фиолетовая
- Clostridium beijerinckii
- Клостридия целлюлолитическая
- Псевдомонас путида
Активность у человека и млекопитающих
[ редактировать ]Хотя этот фермент не был очищен из тканей человека, было показано, что его активность присутствует в сыворотке крови человека. [ 17 ] [ 18 ] Активность ацетоацетатдекарбоксилазы в основном приписывается сывороточному альбумину человека , однако активность составляет около раз больше, чем у реальной ацетоацетатдекарбоксилазы ( C. acetobutylicum ). [ 19 ]
У людей и других млекопитающих превращение ацетоацетата в ацетон и углекислый газ под действием ацетоацетатдекарбоксилазы является заключительным необратимым этапом пути кетоновые тела, который снабжает организм вторичным источником энергии. [ 20 ] В печени ацетил-ко-А, образующийся из жиров и липидов, трансформируется в три кетоновых тела: ацетоацетат , D-β-гидроксибутират и ацетон . Ацетоацетат и D-β-гидроксибутират экспортируются в непеченочные ткани, где они снова превращаются в ацетил-КоА и используются в качестве топлива. Ацетон и углекислый газ, с другой стороны, выдыхаются и не накапливаются в нормальных условиях.
Ацетоацетат и D-β-гидроксибутират свободно взаимопревращаются под действием D-β-гидроксибутиратдегидрогеназы. [ 20 ] Впоследствии одна функция ацетоацетатдекарбоксилазы может заключаться в регулировании концентрации других, двух 4-углеродных кетоновых тел.
Клиническое значение
[ редактировать ]Производство кетоновых тел значительно увеличивается, когда скорость метаболизма глюкозы недостаточна для удовлетворения энергетических потребностей организма. с высоким содержанием жиров К таким состояниям относятся кетогенные диеты , диабетический кетоацидоз или тяжелое голодание. [ 21 ]
При повышенных уровнях ацетоацетата и D-β-гидроксибутирата ацетоацетатдекарбоксилаза производит значительно больше ацетона. Ацетон токсичен и в таких условиях может накапливаться в организме. Повышенный уровень ацетона в дыхании человека можно использовать для диагностики диабета. [ 21 ]
Ссылки
[ редактировать ]- ^ Петерсон DJ, Беннетт Дж.Н. (1990). «Очистка ацетоацетатдекарбоксилазы из Clostridium acetobutylicum ATCC, клонирование ацетоацетатдекарбоксилазы в Escherichia coli» . Прикладная и экологическая микробиология . 56 (11): 3491–3498. дои : 10.1128/aem.56.11.3491-3498.1990 . ПМК 184997 . ПМИД 2268159 .
- ^ Перейти обратно: а б с д и ж Хайбаргер, Луизиана; Дж. А. Герлт; Г. Л. Кеньон (9 января 1996 г.). «Механизм реакции, катализируемой ацетоацетатдекарбоксилазой. Важность лизина 116 в определении pKa лизина 115 активного центра». Биохимия . 35 (1): 41–46. дои : 10.1021/bi9518306 . ПМИД 8555196 .
- ^ Перейти обратно: а б Бормон, С (2009). «Новая структура пересматривает историю». Структурная биология . 87 (21): 9.
- ^ «Британика Онлайн» .
- ^ «Еврейская виртуальная библиотека» .
- ^ «Моделирование ферментации ABE» (PDF) . Архивировано из оригинала (PDF) 8 августа 2014 г. Проверено 27 мая 2014 г.
- ^ Коллас, Флоран; Воутер Куит; Бенджамин Клемент; Реми Маршал; Ана М. Лопес-Контрерас; Фредерик Моно (21 августа 2012 г.). «Одновременное производство изопропонала, бутанола, этанола и 2,3-бутандиола с помощью сконструированных штаммов Clostridium acetobutylicum ATCC 824» . АМБ Экспресс . 2 (1): 45. дои : 10.1186/2191-0855-2-45 . ПМЦ 3583297 . ПМИД 22909015 .
- ^ Перейти обратно: а б с д и Хо MC, Менетрет Ж.Ф., Цурута Х., Аллен К.Н. (21 мая 2009 г.). «Происхождение электростатических возмущений в ацетоацетатдекарбоксилазе». Природа . 459 (7245): 393–397. Бибкод : 2009Natur.459..393H . дои : 10.1038/nature07938 . ПМИД 19458715 . S2CID 1651703 .
- ^ Гамильтон Джорджия, Вестхаймер ФХ (1959). «О механизме ферментативного декарбоксилирования ацетоацетата». Дж. Ам. хим. Соц . 81 (23): 6332–6333. дои : 10.1021/ja01532a058 .
- ^ Уоррен, Стюарт; Берт Цернер, Ф. Х. Вестхаймер (март 1966 г.). «Ацетоацетатдекарбоксилаза. Идентификация лизина в активном сайте». Биохимия . 5 (3): 817–823. дои : 10.1021/bi00867a002 . ПМИД 5911292 .
- ^ «История ацетоацетатдекарбоксилазы» . ДжинКай.орг. Архивировано из оригинала 3 марта 2016 года . Проверено 26 мая 2014 г.
- ^ Кокеш, Фриц К.; Ф. Х. Вестхаймер (29 декабря 1971 г.). «Репортерная группа в активном центре ацетоацетатдекарбоксилазы. Константа ионизации аминогруппы». Журнал Американского химического общества . 93 (26): 7270–7274. дои : 10.1021/ja00755a025 . ПМИД 5127416 .
- ^ О'Лири, Миннесота; Ф. Х. Вестхаймер (1968). «Ацетоацетатдекарбоксилаза. Селективное ацетилирование фермента». Биохимия . 7 (3): 913–919. дои : 10.1021/bi00843a005 . ПМИД 5657856 .
- ^ Шмидт, Дональд Э.; Ф. Х. Вестхаймер (1971). «pK аминогруппы лизина в активном сайте ацетоацетатдекарбоксилазы». Биохимия . 10 (7): 1249–1253. дои : 10.1021/bi00783a023 . ПМИД 4324206 .
- ^ Перейти обратно: а б с д Автор, Энн П.; И. Фридович (1970). «Взаимодействие ацетоацетатдекарбоксилазы с карбонильными соединениями, цианистым водородом и органическим ртутью» . Ж. Биол. Хим . 245 (20): 5214–5222. дои : 10.1016/S0021-9258(18)62743-7 . ПМИД 5469163 .
- ^ Клюгер, Рональд; Курт Накаока (1974). «Ингибирование ацетоацетатдекарбоксилазы кетофосфонатами. Структурные и динамические зонды активного центра». Биохимия . 13 (5): 910–914. дои : 10.1021/bi00702a013 . ПМИД 4360355 .
- ^ ван Стекеленбург Г.Дж., Куреваар Г. (июнь 1972 г.). «Доказательства существования ацетоацетатдекарбоксилазы млекопитающих: с особым упором на сыворотку крови человека». Клин. Хим. Акта . 39 (1): 191–9. дои : 10.1016/0009-8981(72)90316-6 . hdl : 1874/16479 . ПМИД 4624981 . S2CID 27339049 .
- ^ Куреваар Г., Ван Стекеленбург Г.Дж. (сентябрь 1976 г.). «Активность ацетоацетатдекарбоксилазы млекопитающих. Ее распределение в субфракциях человеческого альбумина и наличие в различных тканях крысы». Клин. Хим. Акта . 71 (2): 173–83. дои : 10.1016/0009-8981(76)90528-3 . ПМИД 963888 .
- ^ Кимура, Масако; Симосава, Мицуко; Кобаяши, Кунио; Сакогути, Такафуми; Игаки, Аюми; Хашимото, Марико; Мацуока, Акира; Кимура, Юкио (1986). «Ацетоацетатдекарбоксилазная активность компонентов плазмы». Японский журнал клинической химии . 15 (1): 37–43. дои : 10.14921/jscc1971b.15.1_37 .
- ^ Перейти обратно: а б «Метаболизм человека» (PDF) .
- ^ Перейти обратно: а б Галассетти П.Р., Новак Б., Немет Д., Роуз-Готтрон С., Купер Д.М., Мейнарди С., Ньюкомб Р., Залдивар Ф., Блейк Д.Р. (2005). «Энол и ацетон в выдыхаемом воздухе как индикаторы уровня глюкозы в сыворотке: первоначальный отчет» (PDF) . Диабетическая технология. Там . 7 (1): 115–23. дои : 10.1089/диа.2005.7.115 . ПМИД 15738709 . S2CID 8671477 .
Внешние ссылки
[ редактировать ]- ацетоацетат + декарбоксилаза Национальной медицинской библиотеки США по медицинским предметным рубрикам (MeSH)
- ЭК 4.1.1.4
- Бренда: Вступление ацетоацетатдекарбоксилазы.
- KEGG: проникновение ацетоацетатдекарбоксилазы
- InterPro: IPR010451 Ацетоацетатдекарбоксилаза
