ретозибан
 | |
| Клинические данные | |
|---|---|
| Другие имена | ГСК-221149-А |
| код АТС |
|
| Юридический статус | |
| Юридический статус |
|
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| Панель управления CompTox ( EPA ) | |
| Химические и физические данные | |
| Формула | С 27 Н 34 Н 4 О 5 |
| Молярная масса | 494.592 g·mol −1 |
| 3D model ( JSmol ) | |
Ретосибан, также известный как GSK-221,149-A. [ 1 ] [ 2 ] Это пероральный препарат , который действует как рецепторов окситоцина антагонист . разрабатывает его Компания GlaxoSmithKline для лечения преждевременных родов . [ 3 ] [ 4 ] Ретозибан обладает высоким сродством к рецептору окситоцина (K i = 0,65 нМ) и обладает более чем 1400-кратной селективностью. [ 5 ] над родственными вазопрессина рецепторами
Механизм действия
[ редактировать ]Ретосибан является конкурентным антагонистом рецепторов окситоцина, который блокирует опосредованное окситоцином сокращение гладких мышц матки в женской матке, которое происходит во время начала преждевременных родов. Это использовалось для предотвращения преждевременных родов и преждевременных родов .
Фармакология
[ редактировать ]Доказано, что ретосибан является эффективным токолитиком . При внутривенном и пероральном введении он вызывает дозозависимое снижение окситоцин-индуцированных сокращений матки у небеременных самок крыс. У крыс, беременных на поздних сроках, при внутривенном введении он значительно уменьшает спонтанные сокращения матки дозозависимым образом. [ 5 ] У людей ретозибан продлевает беременность и снижает риск преждевременных родов. Внутривенное введение ретозибана женщинам со спонтанными преждевременными родами было связано с увеличением времени до родов более чем на 1 неделю по сравнению с плацебо, значительным снижением частоты преждевременных родов, незначительным увеличением покоя матки и благоприятным профилем безопасности. Результаты демонстрируют эффективность концепции лечения угрозы самопроизвольных преждевременных родов. [ 6 ]
Фармакокинетика
[ редактировать ]Пероральная биодоступность ретозибана у крыс составляет порядка 100%, период полувыведения составляет 1,4 часа. Он имеет внутренний клиренс от низкого до умеренного в микросомах трех доклинических видов (крыса, собака, яванский макак) и низкий внутренний клиренс в микросомах человека. Он имеет хороший профиль цитохрома P450 (Cyp450) без значительного ингибирования, с IC50 > 100 мкм, низким связыванием с белками (<80%) и низким прогнозируемым проникновением в ЦНС. [ 4 ]
Физические и химические свойства
[ редактировать ]При физиологическом pH ретозибан существует в незаряженном состоянии. Он имеет хорошую растворимость (> 0,22 мг/мл) с logd 2,2. [ 4 ]

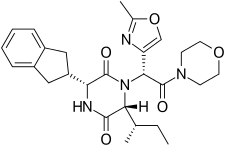
Ретозибан состоит из центрального 2,5-дикетопиперазинового кольца с R - инданильной группой в положении 3 и R ( S -втор-бутил) в положении 6, оба цис- по отношению друг к другу, а также с R -2- метилоксазола кольцом в положении 6. положение 7 в ациклическом амиде присоединено к N1-положению. Ретосибан представляет собой (3R , 6R , 7R ) -изомер и субнаномолярный (Ki = 0,65 нМ) рецептора окситоцина антагонист , тогда как (3R , 6R , 7S ) -изомер, в котором стереохимия в амидная боковая цепь в положении C-7 инвертирована и в 10 раз менее эффективна. Обычно в этой серии антагонистов 2,5-дикетопиперазина окситоцина (3S , 6S , 7S ) -изомер >500 менее активен, чем (3R , 6R , 7R ) -изомер. Помимо основного ядра 2,5-дикетопиперазина, ретозибан также содержит несколько структурных характеристик, которые повышают его эффективность и безопасность. Инданильная группа в положении 3 является лучшим выбором с точки зрения эффективности антагониста рецептора окситоцина, ее замена фенетильной и бензильной группами привела к прогрессивному ослаблению активности. Было показано, что при C-3 предпочтительным является разветвленный алкил с 4 атомами углерода. R ( S -втор-бутил) является лучшим; меньшие алкильные группы приводят к снижению антагонистической активности. [ 4 ] Кольцо 2-метилоксазола в положении 7 обеспечивает хорошую растворимость в воде, низкое связывание с белками и минимальное взаимодействие с Cyp450. Эта взаимосвязь структура-активность (SAR) поддерживается кристаллической структурой человеческого рецептора окситоцина в комплексе с ретозибаном. [ 7 ] где липофильный инданильный заместитель проникает в глубокую, преимущественно гидрофобную щель на дне связывающего кармана, тогда как оксазол-морфолинамидный фрагмент находится ближе всего к внеклеточной поверхности. Оксазольное кольцо является заместителем, наиболее подверженным воздействию растворителей, а морфолиновое кольцо не имеет прямого взаимодействия с рецептором. Ядро 2,5-дикетопиперазина специфически взаимодействует с рецептором через интерфейс полярного взаимодействия.
Синтез
[ редактировать ]Ретозибан представляет собой циклический дипептид или 2,5-дикетопиперазин , образующийся путем циклизации соответствующего линейного дипептида. В ходе короткого лабораторного и высокостереоселективного синтеза ретозибана 8 линейный пептид 5 образуется в результате четырехкомпонентной реакции Уги карбоксибензилового 1 (Cbz) защищенного R-инданилглицина , гидрохлорида метилового эфира D-аллоизолейцина 2 , 2-метилоксазол- 4-карбоксальдегид 3 и 2-бензилоксифенилизонитрил 4 . Гидрирование с целью удаления Cbz и бензильных защитных групп привело к циклизации линейного пептида 5 с образованием фенольного циклического дипептида 6 . Гидролиз фенольного амида по реакции с карбонилдиимидазолом (CDI) с последующим добавлением водного раствора соляной кислоты дает кислоту 7 , которую превращают в амид ретозибан 8 путем активации кислоты реагентом пептидного связывания PyBOP (бензотриазол-1-илокситрипирролидинофосфоний гексафторфосфат). ) с последующим добавлением морфолина . [ 4 ] Хотя линейный пептид 5 и циклический дипептид 6 представляют собой смесь диастереоизомеров (7 RS ) экзоциклического амида, солянокислотный гидролиз активированного фенольного амида вызвал эпимеризацию по экзоциклическому положению и привел к образованию кислоты 7 с необходимым (7 R )-стереохимия как основной продукт.
![Синтетическая схема производства ретозибана реакцией Уги.[4]](http://upload.wikimedia.org/wikipedia/commons/thumb/b/ba/Synthesis_of_Retosiban.svg/750px-Synthesis_of_Retosiban.svg.png)
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Лиддл Дж., Аллен М.Дж., Бортвик А.Д., Брукс Д.П., Дэвис Д.Э., Эдвардс Р.М. и др. (январь 2008 г.). «Открытие GSK221149A: мощного и селективного антагониста окситоцина». Письма по биоорганической и медицинской химии . 18 (1): 90–4. дои : 10.1016/j.bmcl.2007.11.008 . ПМИД 18032036 .
- ^ Бортвик А.Д., Лиддл Дж. (январь 2013 г.). «Ретосибан и Эпелсибан: мощные и селективные пероральные антагонисты окситоцина». В Домлинге А. (ред.). Методы и принципы медицинской химии: белок-белковые взаимодействия при открытии лекарств . Вайнхайм: Wiley-VCH. стр. 225–256. дои : 10.1002/9783527648207.ch10 . ISBN 978-3-527-33107-9 .
- ^ Совет USAN (2007). «Заявление о непатентованном названии, принятое Советом USAN» (PDF) .
- ^ Jump up to: а б с д и ж Бортвик А.Д., Лиддл Дж. (июль 2011 г.). «Разработка пероральных биодоступных антагонистов 2,5-дикетопиперазина окситоцина: от концепции к клиническому кандидату для преждевременных родов». Обзоры медицинских исследований . 31 (4): 576–604. дои : 10.1002/мед.20193 . ПМИД 20027670 . S2CID 22514154 .
- ^ Jump up to: а б Маккафферти ГП, Пуллен М.А., Ву С., Эдвардс Р.М., Аллен М.Дж., Вуллард П.М., Бортвик А.Д., Лиддл Дж., Хики Д.М., Брукс Д.П., Вестфолл Т.Д. (2007). «Использование нового и высокоселективного антагониста рецепторов окситоцина для характеристики сокращений матки у крыс». Американский журнал физиологии. Регуляторная, интегративная и сравнительная физиология . 293 (1): 299–305 рэндов. дои : 10.1152/ajpregu.00057.2007 . ПМИД 17395790 .
- ^ Торнтон С., Миллер Х., Валенсуэла Г., Снидоу Дж., Стир Б., Фосслер М.Дж., Монтегю Т.Х., Пауэлл М., Бич К.Дж. (октябрь 2015 г.). «Лечение спонтанных преждевременных родов ретозибаном: исследование фазы 2» . Британский журнал клинической фармакологии . 80 (4): 740–749. дои : 10.1111/bcp.12646 . ПМЦ 4594710 . ПМИД 25819462 .
- ^ Вальтеншпюль Й., Шёппе Й., Эренманн Й., Куммер Л., Плюктун А. (июль 2020 г.). «Кристаллическая структура рецептора окситоцина человека» . Достижения науки . 6 (29): eabb5419. Стартовый код : 2020SciA....6.5419W . дои : 10.1126/sciadv.abb5419 . ПМЦ 7439316 . ПМИД 32832646 .