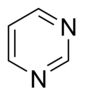
Аналог нуклеиновой кислоты
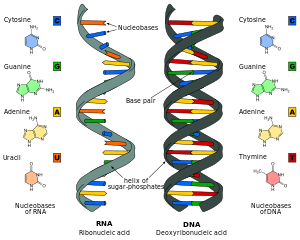
Аналоги нуклеиновой кислоты представляют собой соединения, которые являются аналогичными (структурно сходными) с естественным происходящим РНК и ДНК , используемыми в медицине и в исследованиях молекулярной биологии. Нуклеиновые кислоты представляют собой цепи нуклеотидов, которые состоит из трех частей: фосфатной охраны, пентозного сахара, рибозы или дезоксирибозы и одной из четырех нуклеобаз . Аналог может иметь что -либо из них изменено. [ 1 ] Как правило, аналоговые нуклеобазы придают, среди прочего, различные спаривания основания и свойства базового укладки. Примеры включают универсальные основания, которые могут сочетаться со всеми четырьмя каноническими основаниями, и аналоги фосфат-сахара, такие как PNA , которые влияют на свойства цепи (PNA может даже образовывать тройную спираль ). [ 2 ] Аналоги нуклеиновой кислоты также называются ксено-нуклеиновыми кислотами и представляют собой один из основных столбов ксенобиологии , дизайн форм жизни новых и народов, основанных на альтернативных биохимиях.
Искусственные нуклеиновые кислоты включают пептидные нуклеиновые кислоты (PNA), морфолино и заблокированные нуклеиновые кислоты (LNA), а также гликольные нуклеиновые кислоты (GNA), тросовые нуклеиновые кислоты (TNA) и гекситол нуклеиновые кислоты (HNA). Каждый из них отличается от естественной ДНК или РНК изменениями в основной цепи молекулы. Однако теория полиэлектролита гена предлагает, чтобы генетическая молекула требовала заряженной основы для функционирования.
В мае 2014 года исследователи объявили, что они успешно ввели два новых искусственных нуклеотида в бактериальную ДНК, и, включив отдельные искусственные нуклеотиды в культуральную среду, были способны проходить бактерии 24 раза; Они не создавали мРНК или белки, способные использовать искусственные нуклеотиды. Искусственные нуклеотиды имели 2 слитые ароматические кольца.
Лекарство
[ редактировать ]Несколько аналогов нуклеозидов используются в качестве противовирусных или противоопухолевых агентов. Вирусная . полимераза включает эти соединения с неканоническими основаниями Эти соединения активируются в клетках путем преобразования в нуклеотиды, они вводят в виде нуклеозидов, поскольку заряженные нуклеотиды не могут легко перекрестно клеточные мембраны. [ Цитация необходима ]
Молекулярная биология
[ редактировать ]
Аналоги нуклеиновой кислоты используются в молекулярной биологии для нескольких целей:
- Исследование возможных сценариев происхождения жизни: тестируя различные аналоги, исследователи пытаются ответить на вопрос о том, было ли выбран в жизнь использование ДНК и РНК в жизнь из -за его преимуществ или их выбрано произвольным шансом; [ 3 ]
- В качестве инструмента для обнаружения конкретных последовательностей: XNA может использоваться для помещения и идентификации широкого диапазона компонентов ДНК и РНК с высокой специфичностью и точностью; [ 4 ]
- В качестве фермента, действующего на ДНК, РНК и субстраты XNA - было показано, что XNA обладает способностью расщеплять и лигатировать ДНК, РНК и другие молекулы XNA, сходные с действиями РНК рибозимов ; [ 3 ]
- В качестве инструмента с устойчивостью к гидролизу РНК ;
- Исследование механизмов, используемых ферментом; и
- Исследование структурных особенностей нуклеиновых кислот.
Аналоги магистрали
[ редактировать ]Устойчивые к гидролизу РНК-аналоги
[ редактировать ]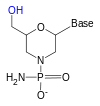
Группа гидрокси Ribose 'S 2' реагирует с связанной 3 'гидрокси -группой фосфата, что делает РНК слишком нестабильной для использования или надежно синтезированной. Чтобы преодолеть это, можно использовать аналог рибозы. Наиболее распространенными аналогами РНК являются 2'-O-метилзамещенная РНК, запертая нуклеиновая кислота (LNA) или мостовая нуклеиновая кислота (BNA), морфолино , [ 5 ] [ 6 ] и пептидная нуклеиновая кислота ( PNA ). Хотя эти олигонуклеотиды имеют другой сахар с основной, или, в случае PNA, аминокислотный остаток вместо рибозофосфата - они все еще связываются с РНК или ДНК в соответствии с парой Уотсона и Крика, будучи невосприимчивыми к активности нуклеазы. Они не могут быть синтезированы ферментативно и могут быть получены только синтетически с использованием стратегии фосфорамидита или, для PNA, другие методы синтеза пептидов . [ Цитация необходима ]
Другие известные аналоги, используемые в качестве инструментов
[ редактировать ]Дидеоксинуклеотиды используются в секвенировании . Эти нуклеозид-трифосфаты обладают неканоническим сахаром, дидеоксирибозой, в которой отсутствует 3 'гидроксильная группа, обычно присутствующая в ДНК и, следовательно, не может связываться со следующим основанием. Отсутствие 3 -х гидроксильной группы завершает цепную реакцию, поскольку ДНК -полимеразы принимают ее за регулярный дезоксирибонуклеотид. Еще один аналог, конечный, в котором отсутствует 3 'гидроксил и имитирует аденозин, называется Cordycepin . Cordycepin - это противоопухолевый препарат, который нацелен на репликацию РНК . Другим аналогом в секвенировании является аналог нуклеобазы, 7-деаза-GTP и используется для последовательности богатых CG областей, вместо этого 7-Deaza-ATP называется туберцидин , антибиотик. [ Цитация необходима ]
Предшественники мира РНК
[ редактировать ]Было высказано предположение, что миру РНК , возможно, предшествовал «РНК-подобный мир», в котором существовали другие нуклеиновые кислоты с другой основной цепью, такие как GNA , PNA и TNA , однако, доказательства этой гипотезы были названы «слабое» Полем [ 7 ]
Базовые аналоги
[ редактировать ]Структура нуклеобазы и номенклатура
[ редактировать ]Природные базы можно разделить на два класса в соответствии с их структурой:
- Пиримидины представляют собой шестибранные гетероциклические с атомами азота в положении 1 и 3.
- Пурины являются бициклическими, состоящим из пиримидина, слитого с кольцом имидазола.
Искусственные нуклеотиды ( неестественные пары оснований (UBP), названные D5SICS UBP и DNAM UBP ) были вставлены в бактериальную ДНК, но эти гены не имели матрицы мРНК или индуцировали синтез белка. Искусственные нуклеотиды имели два слитых ароматических кольца, которые образовали комплекс (D5SICS - DNAM), имитирующий натуральную (DG -DC) пару оснований. [ 8 ] [ 9 ] [ 10 ]
Мутагены
[ редактировать ]Одним из наиболее распространенных базовых аналогов является 5-бромурацил (5BU), аномальное основание, обнаруженное в аналоге мутагенного нуклеотида BRDU. Когда нуклеотид, содержащий 5-бромурацил, включен в ДНК, он, скорее всего, сочетается с аденином; Тем не менее, он может спонтанно перейти в другой изомер , который сочетается с другой нуклеобазой , гуанином . Если это произойдет во время репликации ДНК, в качестве аналога противоположного основания будет вставлен гуанин, а в следующей репликации ДНК гуанин будет сочетаться с цитозином. Это приводит к изменению одной пары основания ДНК, в частности, переходной мутации . [ Цитация необходима ]
Кроме того, азотисная кислота (HNO2) является мощным мутагеном, который действует на реплицирующую и не повторную ДНК. Это может вызвать дезаминирование аминогруппы аденина, гуанина и цитозина. Аденин деамизируется с гипоксантином , который основывает пары с цитозином вместо тимина. Цитозин деамизируется с урацилом, который пары оснований с аденином вместо гуанина. Деализация гуанина не является мутагенным. Мутации, индуцированные азотом, также индуцируются для мутата обратно в дикий тип. [ Цитация необходима ]
Флуорофоры
[ редактировать ]
Обычно флуорофоры (такие как родамин или флуоресцеин ) связаны с кольцом, связанным с сахаром (в пара -) через гибкую руку, предположительно, экстрагируя из основной канавки спирали. Из -за низкой обработки нуклеотидов, связанных с громоздкими аддуктами, такими как флофоры, с помощью [так -полимеразы] S, последовательность обычно копируется с использованием нуклеотида с рукой, а затем в сочетании с реактивным флуорофором (косвенная маркировка)::
- Аминовая реактивная: аминоально-нуклеотиды содержат первичную аминную группу на линкере, который реагирует с аминореактивным красителем, таким как цианиновые или флюорные красители, которые содержат реактивную группу, такую как сукцинимидиловый эфир (NHS). Аминогруппы базы не затронуты.
- Тиол реактивно: тиолисодержащие нуклеотиды реагируют с флуорофором, связанным с реактивной группой покинувшей, такой как Малеимид.
- Биотиновые нуклеотиды полагаются на тот же принцип косвенного маркировки (и флуоресцентного стрептавидина) и используются в Affymetrix Dnachips.
Флуорофоры находят различные применения в медицине и биохимии.
Флуоресцентные базовые аналоги
[ редактировать ]Наиболее часто используемый и коммерчески доступный флуоресцентный базовый аналог, 2-аминопурин (2-AP), имеет высокий флуоресцентный квантовый выход, свободный в растворе (0,68), который значительно снижен (APS 100 раз, но сильно зависит от базовой последовательности), когда), когда), когда), когда), когда), когда), когда он значительно снижен (APS 100 раз, но сильно зависит от базовой последовательности), когда включены в нуклеиновые кислоты. [ 11 ] Чувствительность излучения от 2-ap к непосредственному окружению разделяется другими многообещающими и полезными аналогами флуоресцентного основания, таких как 3-ми Mi, 6-Mi, 6-карма [ 12 ] Pyrrolo-DC (также коммерчески доступный), [ 13 ] модифицированные и улучшенные производные пирроло-DC, [ 14 ] Фуран-модифицированные основания [ 15 ] и многие другие (см. Недавние обзоры). [ 16 ] [ 17 ] [ 18 ] [ 19 ] [ 20 ] Эта чувствительность к микроокружении была использована в исследованиях EG-структуры и динамики в ДНК и РНК, динамике и кинетике взаимодействия ДНК-белок и переноса электронов в ДНК. [ Цитация необходима ]
Недавно разработанная и очень интересная группа аналогов флуоресцентного основания, которая имеет флуоресцентный квантовый выход, который почти нечувствителен к их непосредственному окружению, - это семейство трициклических цитозинов. 1,3-диаза-2-оксофенотиазин, TC, имеет флуоресцентный квантовый выход приблизительно 0,2 как в одно-, так и в двойных целях независимо от окружающих оснований. [ 21 ] [ 22 ] Также оксо-гомолог TC под названием TC А (Оба коммерчески доступны), 1,3-диаза-2-оксофеносазин, имеет квантовый выход 0,2 в двухцепочечных системах. [ 23 ] Однако он несколько чувствителен к окружающим основаниям в отдельных целях (квантовые выходы 0,14–0,41). Высокие и стабильные квантовые выходы этих базовых аналогов делают их очень яркими, и в сочетании с их хорошими базовыми аналоговыми свойствами (листья структура ДНК и стабильность рядом с невозмутимыми) они особенно полезны в анизотропии флуоресценции и измерения FRET, области, где другие Флуоресцентные базовые аналоги менее точны. Кроме того, был разработан в том же семействе аналогов цитозина, был разработан аналог основания-акцептора Fret-Acter, TC Nitro . [ 24 ] Вместе с TC А Как фрет-донор, это представляет собой первую аналоговую основу нуклеиновой кислоты, когда-либо развивавшуюся. Например, в исследованиях TC использовалась в исследованиях, связанных с ДНК-связывающими полимеразой ДНК-связывающими и ДНК-полимеризационными механизмами.
Природные неканонические основания
[ редактировать ]В клетке присутствует несколько неканонических оснований: острова CPG в ДНК (часто метилированные), вся эукариотическая мРНК (покрытая метил-7-гуанозином) и несколько оснований рРНК (метилированные). Часто тРНК сильно модифицированы попозиции, чтобы улучшить их конформацию или спаривание оснований, в частности, в или вблизи антикодона: Инозин может основывать пару с c, u и даже с A, тогда как тиоуридин (с а) более конкретный, чем урацил (с пурин). [ 25 ] Другими распространенными модификациями основания тРНК являются псевдоуридин (который дает свое название петле TψC ), дигидроридин (который не складывается, поскольку он не ароматный), кеуозин, вайозин и т. Д. Тем не менее, это все это модификации на нормальные основания и не помещаются полимеразой. [ 25 ]
Базовая партия
[ редактировать ]Канонические основания могут иметь либо карбонильную, либо аминную группу на углеродах, окружающих атом азота, далее от гликозидной связи, которая позволяет им основания пары (сопряжение основания Ватсон-Крика) через водородные связи (амин с кетоном, пурин с пиримидином) Полем Аденин и 2-аминоаденин имеют одну/две аминную группу (ы), тогда как тимин имеет две карбонильные группы, а цитозин и гуанин являются смешанными амином и карбонилом (перевернутыми друг с другом). [ Цитация необходима ]
| Натуральные басы | |
|---|---|

|

|
| GC Baseapair: пуриновый карбонил/амин образует три межмолекулярные водородные связи с пиримидиновым амином/карбонилом | AT BaseAir: пуриновый амин/- образует две межмолекулярные водородные связи с пиримидином карбонил/карбонил |
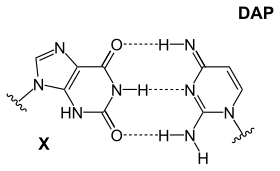
Точная причина, по которой обсуждается только четыре нуклеотида, но есть несколько неиспользованных возможностей. Кроме того, аденин не является наиболее стабильным выбором для спаривания оснований: в цианофаге S-2L диаминопурин (DAP). вместо аденина используется [ 26 ] Диаминопуриновые басы идеально отлично с тимином, так как он идентичен аденину, но имеет аминную группу в положении 2, образуя 3 внутримолекулярных водородных связей, что устраняет основное различие между двумя типами латей (слабые при сильном CG VS). Эта улучшенная стабильность влияет на белок-связывающие взаимодействия, которые полагаются на эти различия. Другая комбинация включает в себя:
- Изогуанин и изоцитозин, которые имеют инвертированный амин и кетон по сравнению со стандартным гуанином и цитозином. Они не используются, вероятно, так как таутомеры проблематичны для спаривания оснований, но ISOC и ISOG могут быть правильно усилены с помощью ПЦР даже в присутствии 4 канонических оснований. [ 27 ]
- Диаминопиримидин и ксантин, которые связываются как 2-аминоаденин и тимин, но с инвертированными структурами. Эта пара не используется, поскольку ксантин является продуктом дезаминирования.
| Неиспользованные базовые договоренности | ||
|---|---|---|

|
|

|
| Основание DAP-T: пуриновый амин/амин образует три межмолекулярные водородные связи с пиримидином кетоном/кетоном | Основание X-DAP: пуриновый кетон/кетон образует три межмолекулярные водородные связи с пиримидиновым амином/амином | Основание IG-IC: пуриновый амин/кетон образует три межмолекулярные водородные связи с пиримидином кетона/амина |
Тем не менее, правильная структура ДНК может образовываться, даже когда основания не соединены через водородную связь; То есть основы сочетаются благодаря гидрофобности, как показали исследования с изостерами ДНК (аналоги с тем же количеством атомов), такие как аналог тимина 2,4-дифторотолуена (F) или аналоговый 4-метилбензимидазол (z). [ 28 ] Альтернативной гидрофобной парой может быть изохинолин и пирроло [2,3-b] пиридин [ 29 ]
Другие примечательные басы:
- Также было сделано несколько флуоресцентных оснований, таких как 2-амино-6- (2-титил) пуриновый и пиррол-2-карбальдегид. [ 30 ]
- Координированные металлом основания, такие как спаривание между пиридин-2,6-дикарбоксилатом (тридентатный лиганд) и пиридин (монодентатный лиганд) посредством квадратной плоской координации с центральной медной ионом. [ 31 ]
- Универсальные основания могут без разбора сочетаться с любым другим основанием, но, в целом, значительно снизить температуру плавления последовательности; Примеры включают 2'-дезоксинозин (гипоксантиновые дезоксинуклеотидные) производные, аналоги нитроазолов и гидрофобные ароматические негидрогеновые основания (сильные эффекты штабелирования). Они используются в качестве доказательства концепции и, как правило, не используются в вырожденных праймерах (которые представляют собой смесь праймеров).
- Количество возможных пар оснований удваивается, когда XDNA рассматривается . XDNA содержит расширенные основания, в которых было добавлено бензольное кольцо, которое может сочетаться с каноническими основаниями, что приводит к четырем дополнительным возможным основным парам (XA-T, XT-A, XC-G, XG-C) с восемью основаниями ( или 16 оснований, если используются неиспользованные меры). Другая форма бензола, добавленных оснований, - идна, в которой основание расширяется бензолом. [ 32 ]
| Новые басы с особыми свойствами | ||
|---|---|---|

|

|

|
| Основание FZ: метилбензимидазол не образует межмолекулярные водородные связи с толуолом F/F | Основание S -PA: пуриновый тиенил/амин образует три межмолекулярные водородные связи с пирролом -/карбальдегидом | База XA-T: такая же связь, что и у |
Металлические базовые пары
[ редактировать ]В металлическом основании водородные связи Watson-Crick заменяются взаимодействием между ионом металла с нуклеозидами, действующими в качестве лигандов. Возможная геометрия металла, которая позволила бы создать дуплексное образование с двумя бидентатными нуклеозидами вокруг центрального атома металла, являются тетраэдрическими , додекаэдрическими и квадратными плоскими . Комплексование металла с ДНК может происходить путем образования неканонических пар оснований из натуральных нуклеобаз с участием ионами металлов, а также путем обмена атомами водорода, которые являются частью спаривания основания Ватсон-Крика ионами металлов. [ 33 ] Внедрение ионов металлов в дуплекс ДНК показал, что имеет потенциальные магнитные [ 34 ] или проводящие свойства, [ 35 ] а также повышенная стабильность. [ 36 ]
Было показано, что комплекс металла возникает между природными нуклеобазами . Хорошо документированный пример-образование T-HG-T, которое включает в себя две депротонированные тиминовые нуклеобазы, которые объединяются с HG 2+ и образует соединенную пару металлической базы. [ 37 ] Этот мотив не учитывает сложенную HG 2+ в дуплексе из -за процесса образования интратратрандной шпильки, который пользуется дуплексным образованием. [ 38 ] Два тимина напротив друг друга не образуют пару оснований Уотсон-Крика в дуплексе; Это пример, в котором несоответствие Watson-Crick Basepair стабилизируется образованием пары металлической базы. Другим примером металлического комплекса с природными нуклеобазами является образование A-ZN-T и G-ZN-C при высоком pH; Сопутствующий 2+ И ния ния Илипа 2+ также образуйте эти комплексы. Это пары оснований Уотсон-Крика, где дивалентный катион в координации с нуклеобазами. Точное обязательство обсуждается. [ 39 ]
Большое разнообразие искусственных нуклеобаз было разработано для использования в качестве пар металлических оснований. Эти модифицированные нуклеобазы имеют настраиваемые электронные свойства, размеры и сродство связывания, которые могут быть оптимизированы для определенного металла. Например, нуклеозид, модифицированный с помощью пиридина-2,6-дикарбоксилата, тесно связывается с CU 2+ , в то время как другие двухвалентные ионы только слабо связаны. Тридентатный символ способствует этой селективности. Четвертый координационный сайт на медь насыщается противоположно расположенной пиридиновой нуклеобазой. [ 40 ] Асимметричная система спаривания основания металла является ортогональной пары оснований Уотсон-Крика. Другим примером искусственной нуклеобазы является то, что с гидроксипиридонами нуклеобаз, которые способны связывать Cu 2+ Внутри дуплекса ДНК. Пять последовательных паров основания основания медного гидроксипиридона были включены в двойную цепь, которая была окружена только одной натуральной нуклеобазой на обоих концах. Данные EPR показали, что расстояние между медными центрами оценивалось как 3,7 ± 0,1 Å, в то время как натуральный дуплекс ДНК B-типа лишь немного больше (3,4 Å). [ 41 ] Привлечение на укладку ионов металлов внутри дуплекса ДНК-это надежда получить наноскопические металлические провода, хотя это еще не реализовано.
Неестественная пара оснований (UBP)
[ редактировать ]Неестественная пара оснований (UBP) представляет собой разработанную субъединицу (или нуклеобазу ) ДНК , которая создается в лаборатории и не встречается в природе. В 2012 году группа американских ученых во главе с Флойдом Ромесбергом, химическим биологом из Научно -исследовательского института Scripps в Сан -Диего, штат Калифорния, опубликовал, что его команда разработала две неестественные базы пары Назван D5SICS и DNAM . [ 42 ] Более технически, эти искусственные нуклеотиды , несущие гидрофобные нуклеобазы, оснащены двумя плавными ароматическими кольцами , которые образуют комплекс D5SICS -DNAM или пару оснований в ДНК. [ 10 ] [ 43 ] В 2014 году такая же команда сообщила, что они синтезировали плазмиду , содержащую естественные пары оснований TA и CG, а также наиболее эффективная лаборатория UBP Romesberg разработала и вставила ее в клетки общей бактерии E. coli , которая успешно повторила неестественное основание Пары через несколько поколений. [ 44 ] Это первый известный пример живого организма, передающего расширенный генетический код последующим поколениям. [ 10 ] [ 45 ] Частично это было достигнуто за счет добавления поддерживающего гена водорослей, который экспрессирует переносчика нуклеотида трифосфата , который эффективно импортирует трифосфаты как D5SICSTP, так и DNAMTP в E. coli . бактерии [ 10 ] Затем, натуральные пути репликации бактерий используют их для точной воспроизведения плазмиды, содержащей D5SICS -DNAM. [ Цитация необходима ]
Успешное включение третьей пары оснований является значительным прорывом для достижения цели значительного расширения количества аминокислот , которые могут быть закодированы ДНК, от существующих 20 аминокислот до теоретически возможных 172, тем самым расширяя потенциал для живых организмов, чтобы до производить новые белки . [ 44 ] Ранее искусственные строки ДНК не кодировали ни для чего, но ученые предположили, что они могут быть разработаны для производства новых белков, которые могли бы использовать промышленное или фармацевтическое использование. [ 46 ] Транскрипция ДНК, содержащей неестественные пары оснований и трансляция соответствующей мРНК, была фактически достигнута недавно. В ноябре 2017 года та же команда из исследовательского института Scripps , которая впервые ввела две дополнительные нуклеобазы в бактериальную ДНК, сообщила, что создала полусинтетические бактерии E. coli , способные создавать белки, используя такую ДНК. Его ДНК содержала шесть различных нуклеобаз : четыре канонических и двух искусственно добавленных, DNAM и DTPT3 (эти два образуют пару). Бактерии имели две соответствующие РНК -основания, включенные в два новых кодона: дополнительные тРНК распознавали эти новые кодоны (эти тРНК также содержали две новые основания РНК в их антикодонах) и дополнительные аминокислоты, что позволило бактериям синтезировать «неестественные» белки. [ 47 ] [ 48 ]
Другая демонстрация UBP была достигнута группой Ичиро Хирао в Институте Рикена в Японии. В 2002 году они разработали неестественную пару оснований между 2-амино-8- (2-титил) пуриновым (S) и пиридин-2-о-о-(Y), который функционирует in vitro в транскрипции и трансляции, для специфического для сайта включения Нестандартные аминокислоты в белки. [ 49 ] В 2006 году они создали 7- (2-ти-тихие) имидазо [4,5-B] пиридин (DS) и пиррол-2-карбальдегид (PA) в качестве третьей пары оснований для репликации и транскрипции. [ 50 ] После этого DS и 4- [3- (6-аминогексанамидо) -1-пропипин] -2-нитропиррол (PX) были обнаружены в виде пары с высокой точностью при амплификации ПЦР. [ 51 ] [ 52 ] В 2013 году они применили пару DS-PX к генерации аптамеров ДНК с помощью отбора in vitro (SELEX) и продемонстрировали генетическое расширение алфавита, значительно увеличивающее атамеры аптамеров ДНК к целевым белкам. [ 53 ]
Ортогональная система
[ редактировать ]Возможность была предложена и изучена как теоретически, так и экспериментально, для реализации ортогональной системы внутри клеток, независимо от клеточного генетического материала, чтобы создать совершенно безопасную систему, [ 54 ] с возможным увеличением потенциалов кодирования. [ 55 ] Несколько групп сосредоточились на разных аспектах:
- Новые основы и пары оснований, как обсуждалось выше;
- Искусственная репликация XNA и транскрипционные полимеразы, начинающиеся, обычно из РНК -полимеразы T7 ; [ 56 ]
- ( 16S рибосомные последовательности с измененными анти -сильных последовательностями, позволяющей трансляции только ортогональной мРНК с соответствующей измененной последовательности Shine-Dalgarno; [ 57 ] и
- Новая тРНК, кодирующая не натуральные аминокислоты для расширенного генетического кода .
Смотрите также
[ редактировать ]- Биотин
- Темный гаситель
- Дезоксирибозим
- Расширенный генетический код
- Флуорофор
- Генетика
- Молекулярная биология
- Нуклеиновая кислота
- Нуклеобаза
- Нуклеозид
- Нуклеотид
- Олигонуклеотидный синтез
- Рибозим
- Синтетическая биология
- Ксенобиология
- XDNA
- Хахимоджи ДНК
- Искусственно расширенная генетическая информационная система (Aegis)
- Ксено нуклеиновая кислота
Ссылки
[ редактировать ]- ^ Певица E (19 июля 2015 г.). «Химики изобретают новые буквы для генетического алфавита природы» . Проводной . Получено 20 июля 2015 года .
- ^ Петерссон Б., Нильсен Б.Б., Расмуссен Х., Ларсен Ик, Гаджед М., Нильсен П.Е., Кастрап Дж.С. (февраль 2005 г.). «Кристаллическая структура частично самообучения пептидной нуклеиновой кислоты (PNA) олигомер, показывающая сеть дуплекс-триплекс». Журнал Американского химического общества . 127 (5): 1424–30. doi : 10.1021/ja0458726 . PMID 15686374 .
- ^ Jump up to: а беременный Тейлор А.И., Пинхайро В.Б., Смола М.Дж., Моргунов А.С., Пик Чу С., Козенс С., Недели К.М., Хердевин П., Холлигер П (февраль 2015). «Катализаторы из синтетических генетических полимеров» . Природа . 518 (7539): 427–30. Bibcode : 2015natur.518..427t . doi : 10.1038/nature13982 . PMC 4336857 . PMID 25470036 .
- ^ Wang Q, Chen L, Long Y, Tian H, Wu J (2013). «Молекулярные маяки ксено-нуклеиновой кислоты для обнаружения нуклеиновой кислоты» . Тераностика . 3 (6): 395–408. doi : 10.7150/thno.5935 . PMC 3677410 . PMID 23781286 .
- ^ Summerton J, Weller D (июнь 1997 г.). «Морфолино антисмысловые олигомеры: дизайн, подготовка и свойства». Антисмысловая и нуклеиновая кислота. Разработка лекарственного средства . 7 (3): 187–95. doi : 10.1089/oli.1.1997.7.187 . PMID 9212909 . S2CID 19372403 .
- ^ Summerton J (декабрь 1999 г.). «Морфолино антисмысловые олигомеры: случай для RNase H-независимого структурного типа». Biochimica et Biophysica Acta (BBA) - структура и экспрессия гена . 1489 (1): 141–58. doi : 10.1016/s0167-4781 (99) 00150-5 . PMID 10807004 .
- ^ Робертсон, депутат; Джойс, Г.Ф. (2012-05-01). «Происхождение мира РНК» . Перспективы Cold Spring Harbor в биологии . 4 (5): A003608. doi : 10.1101/cshperspect.a003608 . ISSN 1943-0264 . PMC 3331698 . PMID 20739415 .
- ^ Поллак A (7 мая 2014 г.). «Исследователи сообщают о прорыве в создании искусственного генетического кода» . Нью -Йорк Таймс . Получено 7 мая 2014 года .
- ^ Callaway E (7 мая 2014 г.). «Первая жизнь с« инопланетной »ДНК». Природа . doi : 10.1038/nature.2014.15179 . S2CID 86967999 .
- ^ Jump up to: а беременный в дюймовый Малишев Д.А., Дэми К., Лавергне Т., Чен Т., Дай Н., Фостер Дж. М., Корэя Ир, Ромсберг Фе (май 2014). «Полусинтетический организм с расширенным генетическим алфавитом» . Природа . 509 (7500): 385–88. Bibcode : 2014natur.509..385m . doi : 10.1038/nature13314 . PMC 4058825 . PMID 24805238 .
- ^ Ward DC, Reich E, Stryer L (март 1969 г.). «Флуоресцентные исследования нуклеотидов и полинуклеотидов. I. Формицин, 2-аминопурин рибозид, 2,6-диаминопурин рибозид и их производные» . Журнал биологической химии . 244 (5): 1228–37. doi : 10.1016/s0021-9258 (18) 91833-8 . PMID 5767305 .
- ^ Хокинс я (2001). «Аналоги флуоресцентного птеридина нуклеозида: окно на взаимодействиях ДНК» . Клеточная биохимия и биофизика . 34 (2): 257–81. doi : 10.1385/cbb: 34: 2: 257 . PMID 11898867 . S2CID 12134698 .
- ^ Берри Д.А., Юнг К.Ю., Мудрый Д.С., Серсель А.Д., Пирсон В.Х., Маки Х., Рэндольф Дж.Б., Сомерс Р.Л. (2004). «Пирроло-DC и пирроло-C: флуоресцентные аналоги цитидина и 2 '-деоксицитидина для изучения олигонуклеотидов». Тетраэдр Летт . 45 (11): 2457–61. doi : 10.1016/j.tetlet.2004.01.108 .
- ^ Wojciechowski F, Hudson RH (сентябрь 2008 г.). «Флуоресцентные и гибридизационные свойства пептидной нуклеиновой кислоты, содержащей замещенного фенилпирролоцитозина, предназначенного для вовлечения гуанина с дополнительным H-связью». Журнал Американского химического общества . 130 (38): 12574–75. doi : 10.1021/ja804233g . PMID 18761442 .
- ^ Греко Нью -Джерси, Tor Y (август 2005 г.). «Простые флуоресцентные аналоги пиримидина обнаруживают присутствие абазических сайтов ДНК». Журнал Американского химического общества . 127 (31): 10784–85. doi : 10.1021/ja052000a . PMID 16076156 .
- ^ Rist MJ, Marino JP (2002). «Аналоги флуоресцентного нуклеотидного основания как зонды структуры нуклеиновой кислоты, динамики и взаимодействий». Карт Орг Химический 6 (9): 775–93. doi : 10.2174/1385272023373914 .
- ^ Wilson JN, Kool et (декабрь 2006 г.). «Флуоресцентные замены основания ДНК: репортеры и датчики для биологических систем». Органическая и биомолекулярная химия . 4 (23): 4265–74. doi : 10.1039/b612284c . PMID 17102869 .
- ^ Вильгельмссон и Тор (2016). Флуоресцентные аналоги биомолекулярных строительных блоков: проектирование и применение . Нью -Джерси: Уайли. ISBN 978-1-118-17586-6 .
- ^ Wilhelmsson LM (май 2010). «Аналоги флуоресцентной нуклеиновой кислоты» . Ежеквартальные обзоры биофизики . 43 (2): 159–83. doi : 10.1017/s0033583510000090 . PMID 20478079 . S2CID 10783202 .
- ^ Синдельдам Р.В., Греко Нью -Джерси, Тор Ю (май 2010 г.). «Флуоресцентные аналоги биомолекулярных строительных блоков: проектирование, свойства и применение» . Химические обзоры . 110 (5): 2579–619. doi : 10.1021/cr900301e . PMC 2868948 . PMID 20205430 .
- ^ Вильгельмссон Л.М., Холмен А., Линкольн П., Нильсен П.Е., Норз Б. (2001). «Высоко флуоресцентный аналог основания ДНК, который образует пары основания Уотсона-Крика с гуанином». J. Am. Химический Соц 123 (10): 2434–35. doi : 10.1021/ja0025797 . PMID 11456897 .
- ^ Сандин П., Вильгельмссон Л.М., Линкольн П., Пауэрс В.Е., Браун Т., Альбинссон Б. (2005). «Флуоресцентные свойства аналога основания ДНК при включении в ДНК - незначительное влияние соседних оснований на флуоресцентный квантовый выход» . Исследование нуклеиновых кислот . 33 (16): 5019–25. doi : 10.1093/nar/gki790 . PMC 1201328 . PMID 16147985 .
- ^ Sandin P, Börjesson K, Li H, Mårtensson J, Brown T, Wilhelmsson LM, Albinsson B (январь 2008 г.). «Характеристика и использование беспрецедентно яркого и структурно непротягивающего аналога флуоресцентного основания ДНК» . Исследование нуклеиновых кислот . 36 (1): 157–67. doi : 10.1093/nar/gkm1006 . PMC 2248743 . PMID 18003656 .
- ^ Börjesson K, Preus S, El-Sagheer AH, Brown T, Albinsson B, Wilhelmsson LM (апрель 2009 г.). «Аналоговая база нуклеиновой кислоты аналоговый фрет-пары, облегчающий подробные структурные измерения в системах, содержащей нуклеиновую кислоту» . Журнал Американского химического общества . 131 (12): 4288–93. doi : 10.1021/ja806944w . PMID 19317504 .
- ^ Jump up to: а беременный Родригес-Хернандес А., Спирс Дж.Л., Гастон К.В., Лимбах П.А., Гампер Х., Хоу Й.М., Кайзер Р., Агрис П.Ф., Перона Дж.Дж. (октябрь 2013). «Структурная и механистическая основа для повышенной трансляционной эффективности 2-тиоридина в положении антикодона тРНК» . Журнал молекулярной биологии . 425 (20): 3888–906. doi : 10.1016/j.jmb.2013.05.018 . PMC 4521407 . PMID 23727144 .
- ^ Kirnos MD, Khudyakov IY, Alexandrushkina Ni, Vanyushin BF (ноябрь 1977 г.). «2-аминоаденин является адениновым заменой основой в ДНК цианофага S-2L». Природа . 270 (5635): 369–70. Bibcode : 1977natur.270..369k . doi : 10.1038/270369a0 . PMID 413053 . S2CID 4177449 .
- ^ Johnson SC, Sherrill CB, Marshall DJ, Moser MJ, Prudent JR (2004). «Третья пара оснований для полимеразной цепной реакции: вставка ISOC и ISOG» . Исследование нуклеиновых кислот . 32 (6): 1937–41. doi : 10.1093/nar/gkh522 . PMC 390373 . PMID 15051811 .
- ^ Taniguchi Y, Kool et (июль 2007 г.). «Неполярные изостеры поврежденных оснований ДНК: эффективная мимикрия мутагенных свойств 8-оксопуринов». Журнал Американского химического общества . 129 (28): 8836–44. doi : 10.1021/ja071970q . PMID 17592846 .
- ^ Hwang GT, Romesberg FE (ноябрь 2008 г.). «Неестественный субстратный репертуар A, B и X -полимеразы семейства» . Журнал Американского химического общества . 130 (44): 14872–82. doi : 10.1021/ja803833h . PMC 2675700 . PMID 18847263 .
- ^ Кимото М., Мицуи Т., Харада Ю., Сато А., Йокояма С., Хирао I (2007). «Флуоресцентное исследование для молекул РНК неестественной системой базовой пары» . Исследование нуклеиновых кислот . 35 (16): 5360–69. doi : 10.1093/nar/gkm508 . PMC 2018647 . PMID 17693436 .
- ^ Этвелл, Шейн; Меггерс, Эрик; Spraggon, Glen; Шульц, Питер Г. (декабрь 2001 г.). «Структура меди-опосредованной пары оснований в ДНК» . Журнал Американского химического общества . 123 (49): 12364–12367. doi : 10.1021/ja011822e . ISSN 0002-7863 . PMID 11734038 .
- ^ Liu H, Gao J, Lynch SR, Saito YD, Maynard L, Kool et (октябрь 2003 г.). «Парная генетическая спираль с четырьмя базой с расширенным размером». Наука . 302 (5646): 868–71. Bibcode : 2003sci ... 302..868L . doi : 10.1126/science.1088334 . PMID 14593180 . S2CID 37244007 .
- ^ Wettig SD, Lee JS (2003). «Термодинамическое исследование М-ДНК: новый комплекс ион-ДНК металла». Журнал неорганической биохимии . 94 (1–2): 94–99. doi : 10.1016/s0162-0134 (02) 00624-4 . PMID 12620678 .
- ^ Zhang HY, Calzolari A, Di Felice R (август 2005 г.). «О магнитном выравнивании ионов металлов в двойной спиралью ДНК-мимической спирали». Журнал физической химии б . 109 (32): 15345–48. doi : 10.1021/jp052202t . PMID 16852946 .
- ^ AICH P, Skinner RJ, Wettig SD, Steer RP, Lee JS (август 2002 г.). «Поведение молекулярной проволоки длинного расстояния в металлическом комплексе ДНК». Журнал биомолекулярной структуры и динамики . 20 (1): 93–98. doi : 10.1080/07391102.2002.10506826 . PMID 12144356 . S2CID 41568646 .
- ^ Clever GH, Polborn K, Carell T (2005). «Стабилизирующая пары оснований металлуплеров с ДНК-дуплексом». Применяемый Хим. Редакция 117 (44): 7370–74. Bibcode : 2005angch.117.7370c . Doi : 10.1002/Прилагается 200501589 .
- ^ Бункел Э., Бун С., Джоли Х, Кумар Р., Норрис А.Р. (1985). «Металлические ионно-биомолекулярные взаимодействия. XII. 1H и 13C ЯМР Данные о предпочтительной реакции тимидина на гуанозин в реакциях обмена и конкуренции с ртутью (II) и метилртути (II)». Inorg. Биохимия . 25 : 61–73. doi : 10.1016/0162-0134 (85) 83009-9 .
- ^ Ono A, Togashi H (август 2004 г.). «Высокоселективный датчик на основе олигонуклеотидов для ртути (II) в водных растворах». Angewandte Chemie . 43 (33): 4300–02. doi : 10.1002/anie.200454172 . PMID 15368377 .
- ^ Meggers E, Holland PL, Tolman WB, Romesberg FE, Schultz PG (2000). «Новая медная опосредованная пара оснований ДНК». J. Am. Химический Соц 122 (43): 10714–15. doi : 10.1021/ja0025806 .
- ^ Lee JS, Latimer LJ, Reid RS (1993). «Кооперативное конформационное изменение в дуплексной ДНК, индуцированное Zn2+ и другими ионами двухвалентных металлов». Биохимия и клеточная биология . 71 (3–4): 162–68. doi : 10.1139/O93-026 . PMID 8398074 .
- ^ Танака К., Тенгиджи А., Като Т., Тояма Н., Шионья М (февраль 2003 г.). «Дискретный самосборный металлический массив в искусственной ДНК». Наука . 299 (5610): 1212–13. Bibcode : 2003sci ... 299.1212T . doi : 10.1126/science.1080587 . PMID 12595687 . S2CID 22413126 .
- ^ Малишев Д.А., Дэми К., Квач Х.Т., Лавергне Т., Оркукханян П., Торкамани А., Ромсберг Фе (июль 2012 г.). «Эффективная и независимая от последовательности репликация ДНК, содержащей третью пару оснований, устанавливает функциональный генетический алфавит с шестью буквами» . Труды Национальной академии наук Соединенных Штатов Америки . 109 (30): 12005–10. Bibcode : 2012pnas..10912005M . doi : 10.1073/pnas.1205176109 . PMC 3409741 . PMID 22773812 .
- ^ Callaway E (7 мая 2014 г.). «Ученые создают первый живой организм с« искусственной »ДНК» . Nature News . Huffington Post . Получено 8 мая 2014 года .
- ^ Jump up to: а беременный Fikes BJ (8 мая 2014 г.). «Жизнь спроектирована с расширенным генетическим кодом» . Сан -Диего Юнион Трибьюн . Получено 8 мая 2014 года .
- ^ Образец I (7 мая 2014 г.). «Первая жизнь формирует искусственную ДНК, спроектированную американскими учеными» . Хранитель . Получено 8 мая 2014 года .
- ^ Поллак A (7 мая 2014 г.). «Ученые добавляют буквы в алфавит ДНК, поднимая надежду и страх» . Нью -Йорк Таймс . Получено 8 мая 2014 года .
- ^ Zhang Y, Ptacin JL, Fischer EC, Aerni HR, Caffaro CE, San Hose K, Feldman AW, Turner CR, Romesberg FE (2017). «Полусинтетический организм, который хранит и извлекает повышенную генетическую информацию» . Природа . 551 (7682): 644–47. Bibcode : 2017natur.551..644Z . doi : 10.1038/nature24659 . PMC 5796663 . PMID 29189780 .
- ^ «Неестественный» микроб может делать белки . BBC News . 29 ноября 2017 года.
- ^ Hirao I, Ohtsuki T, Fujiwara T, Mitsui T, Yokogawa T, Okuni T, Nakayama H, Takio K, Yabuki T, Kigawa T, Kodama K, Yokogawa T, Nishikawa K, Yo Koyama S (февраль 2002 года) Пара оснований для включения аналогов аминокислот в белки ». Nature Biotechnology . 20 (2): 177–82. : 10.1038 /nbt0202-177 . PMID 11821864. . S2CID 220 55476 DOI
- ^ Хирао I, Кимото М., Мицуи Т., Фудзивара Т., Кавай Р., Сато А., Харада Ю., Йокояма С. (сентябрь 2006 г.). «Неестественная гидрофобная система пары оснований: сайт-специфическое включение нуклеотидных аналогов в ДНК и РНК». Природные методы . 3 (9): 729–35. doi : 10.1038/nmeth915 . PMID 16929319 . S2CID 6494156 .
- ^ Кимото М., Каваи Р., Мицуи Т., Йокояма С., Хирао I (февраль 2009 г.). «Неестественная система пары оснований для эффективной амплификации ПЦР и функционализации молекул ДНК» . Исследование нуклеиновых кислот . 37 (2): E14. doi : 10.1093/nar/gkn956 . PMC 2632903 . PMID 19073696 .
- ^ Yamashige R, Kimoto M, Takzawa Y, Sato A, Mitsui T, Yokoyama S, Hirao I (март 2012 г.). «Очень специфические неестественные системы пары оснований в качестве третьей пары оснований для амплификации ПЦР» . Исследование нуклеиновых кислот . 40 (6): 2793–806. doi : 10.1093/nar/gkr1068 . PMC 3315302 . PMID 22121213 .
- ^ Кимото М., Ямашиге Р., Мацунага К., Йокояма С., Хирао I (май 2013). «Генерация высокоаффинных аптамеров ДНК с использованием расширенного генетического алфавита». Nature Biotechnology . 31 (5): 453–57. doi : 10.1038/nbt.2556 . PMID 23563318 . S2CID 23329867 .
- ^ Шмидт М. "Ксенобиология: новая форма жизни как Ultimate Biosafety Tool" Bioessays Vol 32 (4): 322–31
- ^ Herdewijn P, Marlière P (июнь 2009 г.). «В направлении безопасных генетически модифицированных организмов посредством химической диверсификации нуклеиновых кислот». Химия и биоразнообразие . 6 (6): 791–808. doi : 10.1002/cbdv.200900083 . PMID 19554563 . S2CID 8572188 .
- ^ Shinkai A, Patel PH, Loeb LA (июнь 2001 г.). «Консервативный мотив активного сайта Escherichia coli ДНК -полимераза I очень изменен» . Журнал биологической химии . 276 (22): 18836–42. doi : 10.1074/jbc.m011472200 . PMID 11278911 .
- ^ Rackham O, Chin JW (август 2005 г.). «Сеть ортогональной пары мРНК рибосомы x». Природная химическая биология . 1 (3): 159–66. doi : 10.1038/nchembio719 . PMID 16408021 . S2CID 37181098 .