Бергаптен
| |

| |

| |
| Имена | |
|---|---|
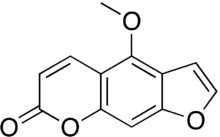
| Предпочтительное название ИЮПАК
4-Метокси- 7H -фуро[3,2- g ][1]бензопиран-7-он | |
Другие имена
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| КЭБ | |
| ХЭМБЛ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.006.913 |
| Номер ЕС |
|
| КЕГГ | |
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
| Число | 1759 |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 12 Н 8 О 4 | |
| Молярная масса | 216.192 g/mol |
| Фармакология | |
| D05BA03 ( ВОЗ ) | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Бергаптен ( 5-метоксипсорален ) представляет собой встречающееся в природе органическое химическое соединение, вырабатываемое многочисленными видами растений, особенно из семейства моркови Apiaceae и семейства цитрусовых Rutaceae . Например, бергаптен был извлечен из 24 видов рода Heracleum семейства Apiaceae. [ 1 ] [ 2 ] семейства Рутовые Различные виды цитрусовых содержат значительное количество бергаптена. [ 3 ] особенно бергамот , микранта и некоторые сорта лайма и горького апельсина .
Бергаптен принадлежит к классу химических соединений, известных как фуранокумарины . В 1834 году Кальбруннер выделил из эфирного масла бергамота 5-метоксипсорален . [ 4 ] отсюда и общее название «бергаптен». Это был первый фуранокумарин, который был выделен и идентифицирован.
Токсичность
[ редактировать ]Бергаптен является производным псоралена , исходного соединения семейства встречающихся в природе органических соединений, известных как линейные фуранокумарины (названные так, поскольку они обладают линейной химической структурой). Некоторые из линейных фуранокумаринов, в том числе бергаптен, действуют как сильные фотосенсибилизаторы при местном нанесении на кожу .
Бергаптен часто встречается в растениях, вызывающих фитофотодерматит . [ 5 ] потенциально серьезное воспаление кожи. Контакт с частями растений, содержащими бергаптен (и другие линейные фуранокумарины), с последующим воздействием ультрафиолета может привести к фитофотодерматиту. В частности, бергаптен, по-видимому, является основным фототоксичным соединением, ответственным за фитофотодерматит, вызванный цитрусовыми . [ 3 ]
Бергаптен и другие линейные фуранокумарины вызывают потерю активности матрицы для синтеза РНК. 5-метоксипсорален также известен своими мутагенными эффектами, а также способностью быть очень мощным агентом, вызывающим хромосомные аберрации. При достаточно высокой концентрации наблюдалось полное митотическое ингибирование. [ 4 ]
Существует достаточно доказательств того, что бергаптен способствует развитию рака у животных, но такие доказательства канцерогенности у людей отсутствуют. По данным Международного агентства по изучению рака , бергаптен, вероятно, канцерогенен для человека. [ 6 ]
Медицинское использование
[ редактировать ]Бергаптен помогает коже поглощать больше света, а пигментные заболевания, такие как витилиго (лейкодермия) и псориаз, требуют лечения фуранокумаринами, часто в сочетании с воздействием солнца или солнечной радиацией. У людей, которые легко обгорают, фуранокумарины также могут повысить толерантность кожи к солнечному излучению. [ 4 ] Было показано, что бергаптен вызывает определенные кожные реакции, чтобы выровнять осветление пигментации у пациентов с витилиго, в зависимости от различных факторов, таких как восприимчивость субъекта, дозировка и влажность, но эффекты могут быть непостоянными. [ 7 ]
При псориазе бергаптен ценится в качестве перорального средства фотохимиотерапии из-за его эффективности и отсутствия фототоксических и нечувствительных к лекарствам реакций. Он действует как фотосенсибилизирующий препарат, который столь же эффективен или, при достаточно высоких дозировках, более эффективен, чем 8-метоксипсорален, при лечении псориатических поражений. [ 8 ] Было показано, что он является ценной альтернативой 8-метоксипсоралену из-за относительного отсутствия побочных эффектов во время лечения, таких как эритма, зуд и тошнота. [ 9 ]
Бергаптен также считается потенциальным методом профилактики рака кожи, вызванного солнечным светом. Одно исследование показало, что загар, полученный с помощью бергаптена, вызывает меньше повреждений ДНК у людей. [ 10 ] Было показано, что бергаптен обладает противоопухолевым действием, например, его способностью индуцировать аутофагический процесс в клетках рака молочной железы. Одно исследование показало, что это возможно благодаря усилению экспрессии гена PTEN в клетках рака молочной железы. [ 11 ]
Бергаптен, наряду с другими фуранокумаринами, также участвует в ингибировании цитохрома P450 . [ 12 ]
Синтез
[ редактировать ]
Бергаптен — это природное соединение, получаемое из растений, таких как инжир обыкновенный, но его также можно синтезировать. Большинство синтезов линейных фуранокумаринов включают начало с центральной ароматической единицы и добавление двух гетероциклических колец. Альтернативные пути синтеза желательны, чтобы избежать региохимических проблем и умеренных выходов. В описанном здесь синтезе йод используется в качестве удаляемой группы для обеспечения региохимической целостности и конвергенции. [ 13 ] Как показано на схеме, исходным материалом был флороглюцин (соединение 1). Проводили монометилирование с последующей реакцией с этилпропиолатом в присутствии ZnCl 2 с получением 7-гидрокси-5-метоксикумарина (продукт 3, не показан) с выходом 68%. Затем 8-положение 7-гидрокси-5-метоксикумарина защищали йодом, чтобы избежать образования углового фуранокумарина. Продукт 4 на схеме – результат йодной защиты. Продукт 5 был результатом аллилирования продукта 4. Тетраоксид осмия и метапериодат натрия использовались для окислительного расщепления O-аллильного производного на альдегидный продукт 7 через промежуточный диол (продукт 6, не показан). Затем была проведена циклизация альдегидного продукта 7 с использованием BF 3 -Et 2 O в бромиде тетра -н- бутиламмония для построения фуранового кольца. Последним шагом было удаление йодзащитной группы с помощью Pd(OAc) 2 с получением бергаптена (продукт 9) с выходом 90%. Синтетический бергаптен выделен в виде бесцветного соединения, спектроскопически идентичного природному продукту.
Известное применение бергаптена находится в синтезе фраксинола . [ 14 ] Ключевой реакцией в этом синтезе является окисление фуранового кольца виснагина и бергаптена хромовой кислотой. [ 14 ]
Ссылки
[ редактировать ]- ^ Нильсен, Б.Е. (1970). Кумарины зонтичных растений . Копенгаген: Датская королевская фармацевтическая школа. Цитируется Митчеллом и Руком (1979).
- ^ Митчелл, Джон; Рук, Артур (1979). Ботаническая дерматология: растения и растительные продукты, вредные для кожи . Ванкувер: Гринграсс. стр. 692–699.
- ^ Перейти обратно: а б Дюгран-Жудек, Одрэ; Олри, Александр; Хен, Ален; Константино, Жиль; Оллитро, Патрик; Фрёлихер, Янн; Бурго, Фредерик (ноябрь 2015 г.). «Распределение кумаринов и фуранокумаринов у видов цитрусовых точно соответствует филогении цитрусовых и отражает организацию биосинтетических путей» . ПЛОС ОДИН . 10 (11): e0142757. Бибкод : 2015PLoSO..1042757D . дои : 10.1371/journal.pone.0142757 . ПМЦ 4641707 . ПМИД 26558757 .
- ^ Перейти обратно: а б с Скотт, БР; Патхак, Массачусетс; Мон, GR (1976). «Молекулярно-генетические основы реакций фурокумарина» . Мутат Рес . 39 (1): 29–74. дои : 10.1016/0165-1110(76)90012-9 . ПМИД 13299 .
- ^ Макговерн, Томас В.; Баркли, Теодор М. (2000). «Ботаническая дерматология» . Электронный учебник дерматологии . Общество интернет-дерматологов. Раздел Фитофотодерматит . Проверено 29 ноября 2018 г.
- ^ «Монографии по оценке канцерогенного риска химических веществ для человека» . Женева: Всемирная организация здравоохранения, Международное агентство по исследованию рака, 1972 г. – настоящее время. 1987. с. С7 66 . Проверено 4 января 2019 г.
- ^ «Побочные эффекты чая Эрл Грей» .
- ^ Хонигсманн (октябрь 1979 г.). «5-Метоксипсорален (Бергаптен) в фотохимиотерапии псориаза». Британский журнал дерматологии . 101 (4): 369–378. дои : 10.1111/j.1365-2133.1979.tb00014.x . ПМИД 508604 . S2CID 46371217 .
- ^ Танью, Адриан (февраль 1988 г.). «5-Метоксипсорален (бергаптен) для фотохимиотерапии: биодоступность, фототоксичность и клиническая эффективность при псориазе нового лекарственного препарата». Журнал Американской академии дерматологии . 18 (2 ч. 1): 333–338. дои : 10.1016/S0190-9622(88)70048-1 . ПМИД 3279089 .
- ^ Тиссеран, Роберт (2014). Безопасность эфирных масел . Черчилль Ливингстон.
- ^ Де Амицис, Франческа (2015). «Бергаптен стимулирует аутофагию посредством усиления экспрессии PTEN в клетках рака молочной железы» . Молекулярный рак . 14 : 130. дои : 10.1186/s12943-015-0403-4 . ПМЦ 4498523 . ПМИД 26148846 .
- ^ Олдред, Элейн (2009). Справочник Гашека и Руссо по токсикологической патологии (Третье изд.). Черчилль Ливингстон.
- ^ Ода, Кадзуаки (июнь 2005 г.). «Эффективный синтез бергаптена». Гетероциклы . 65 (8): 1985–1988. doi : 10.3987/com-05-10451 (неактивен 17 февраля 2024 г.) – через ResearchGate.
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на февраль 2024 г. ( ссылка ) - ^ Перейти обратно: а б Шенберг, Александр; Бадран, Насри; Старковский, Николай А. (1955). «Фурохромоны и -кумарины. XII. Синтез фраксинола из бергаптена и байкалеина из виснагина». Журнал Американского химического общества . 77 (20): 5390–5392. дои : 10.1021/ja01625a055 . ISSN 0002-7863 .