Развитие нервной системы у человека
| Эта статья является частью серии статей о |
| Развитие систем органов |
|---|
Эта статья нуждается в дополнительных цитатах для проверки . ( декабрь 2023 г. ) |
Развитие нервной системы у человека, или нервное развитие, или нейроразвитие, включает в себя исследования эмбриологии , биологии развития и нейробиологии . Они описывают клеточные и молекулярные механизмы, с помощью которых сложная нервная система формируется у человека, развивается во время внутриутробного развития и продолжает развиваться постнатально.
Некоторые ориентиры развития нейронов у эмбриона включают:
- Образование и нейронов из ) предшественников стволовых клеток ( нейрогенез дифференцировка
- Миграция незрелых нейронов из мест их рождения в эмбрионе в конечные позиции.
- Отрастание аксонов от нейронов и направление подвижного конуса роста через эмбрион к постсинаптическим партнерам.
- Образование синапсов между аксонами и их постсинаптическими партнерами.
- Синаптическая обрезка , которая происходит в подростковом возрасте .
- Пожизненные изменения в синапсах, которые, как считается, лежат в основе обучения и памяти.
Обычно эти процессы нервного развития можно разделить на два класса:
- Активно-независимые механизмы. Обычно считается, что независимые от активности механизмы происходят как запрограммированные процессы, определяемые генетическими программами, которые реализуются внутри отдельных нейронов. К ним относятся дифференциация , миграция и направление аксонов к их первоначальным целевым областям. Считается, что эти процессы не зависят от нервной активности и сенсорного опыта.
- Активно-зависимые механизмы. Как только аксоны достигают своих целевых областей, в игру вступают механизмы, зависящие от активности. Нейронная активность и сенсорный опыт будут способствовать образованию новых синапсов , а также синаптической пластичности , которая будет отвечать за совершенствование зарождающихся нейронных цепей. [ нужна ссылка ]
Развитие человеческого мозга
[ редактировать ]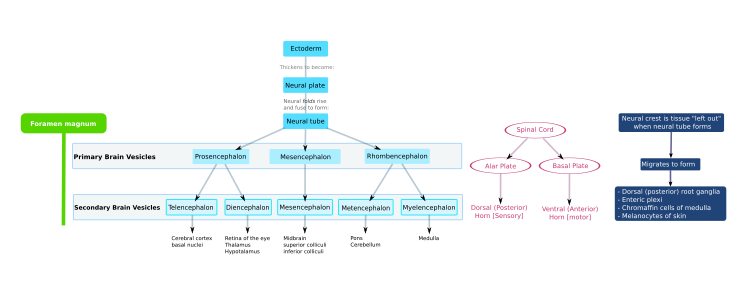
Обзор
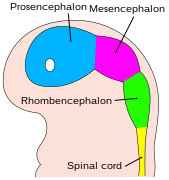
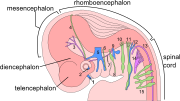
[ редактировать ]Центральная нервная система (ЦНС) происходит из эктодермы — самого внешнего слоя ткани эмбриона. На третьей неделе эмбрионального развития человека появляется нейроэктодерма нервную , образующая пластинку вдоль дорсальной стороны эмбриона. Нервная пластинка является источником большинства нейронов и глиальных клеток ЦНС. Вдоль длинной оси нервной пластинки формируется бороздка, и к четвертой неделе развития нервная пластинка сворачивается сама в себя, образуя нервную трубку , наполненную спинномозговой жидкостью (СМЖ). [1] По мере развития эмбриона передняя часть нервной трубки образует три первичных мозговых пузырька , которые становятся первичными анатомическими областями головного мозга: передний мозг ( прозэнцефалон ), средний мозг ( мезенцефалон ) и задний мозг ( ромбэнцефалон ). [2] Эти простые ранние пузырьки увеличиваются и далее делятся на пять вторичных пузырьков головного мозга – телэнцефалон (будущие кора головного мозга и базальные ганглии ), промежуточный мозг (будущие таламус и гипоталамус ), средний мозг (будущие холмики ), метэнцефалон (будущие мост и мозжечок ) и продолговатый мозг (будущий мозговой мозг ). [3] Заполненная спинномозговой жидкостью центральная камера непрерывна от конечного мозга до спинного мозга и представляет собой развивающуюся желудочковую систему ЦНС. Поскольку нервная трубка дает начало головному и спинному мозгу, любые мутации на этой стадии развития могут привести к фатальным уродствам, таким как анэнцефалия , или пожизненным инвалидностям, таким как расщелина позвоночника . В это время стенки нервной трубки содержат нервные стволовые клетки , которые способствуют росту мозга, поскольку они многократно делятся. Постепенно некоторые клетки перестают делиться и дифференцируются в нейроны и глиальные клетки , которые являются основными клеточными компонентами ЦНС. [2] Вновь созданные нейроны мигрируют в разные части развивающегося мозга, чтобы самоорганизоваться в разные структуры мозга. Как только нейроны достигают своих региональных позиций, они расширяют аксоны и дендриты , что позволяет им взаимодействовать с другими нейронами через синапсы . Синаптическая связь между нейронами приводит к созданию функциональных нейронных цепей , которые опосредуют сенсорную и моторную обработку и лежат в основе поведения. [4]
Нейронная индукция
[ редактировать ]На ранних стадиях эмбрионального развития эктодерма становится специфической, дающей начало эпидермису (коже) и нервной пластинке. Преобразование недифференцированной эктодермы в нейроэктодерму требует сигналов от мезодермы . В начале гаструляции презумптивные мезодермальные клетки перемещаются через дорсальную губу бластопора и образуют слой между энтодермой и эктодермой. Эти мезодермальные клетки, мигрирующие вдоль дорсальной срединной линии, образуют структуру, называемую хордой . Эктодермальные клетки, покрывающие хорду, развиваются в нервную пластинку в ответ на диффузный сигнал, вырабатываемый хордой. Остальная часть эктодермы дает начало эпидермису (коже). Способность мезодермы превращать вышележащую эктодерму в нервную ткань называется нейронной индукцией.
Нервная пластинка складывается наружу на третьей неделе беременности, образуя нервную борозду . Начиная с области будущей шеи, нервные складки этой борозды смыкаются, образуя нервную трубку . Образование нервной трубки из эктодермы называется нейруляцией . Вентральная часть нервной трубки называется базальной пластинкой ; спинная часть называется крыловой пластинкой . Полая внутренняя часть называется нервным каналом . К концу четвертой недели беременности открытые концы нервной трубки, называемые нейропорами, закрываются. [5]
Пересаженная губа бластопора может превращать эктодерму в нервную ткань и, как говорят, оказывает индуктивный эффект. Нейронные индукторы представляют собой молекулы, которые могут индуцировать экспрессию нервных генов в эксплантатах эктодермы, не индуцируя также мезодермальные гены. Нейральную индукцию часто изучают на эмбрионах xenopus, поскольку они имеют простое строение тела и имеются хорошие маркеры, позволяющие различать нервную и ненервную ткани. Примерами нейронных индукторов являются молекулы noggin и chordin .
Когда эмбриональные эктодермальные клетки культивируются при низкой плотности в отсутствие мезодермальных клеток, они подвергаются нейральной дифференцировке (экспрессируют нервные гены), указывая тем самым, что нервная дифференцировка является судьбой эктодермальных клеток по умолчанию. В культурах эксплантатов (которые допускают прямое межклеточное взаимодействие) одни и те же клетки дифференцируются в эпидермис. Это связано с действием BMP4 ( белок семейства TGF-β ), который индуцирует дифференцировку эктодермальных культур в эпидермис. Во время нейронной индукции noggin и chordin продуцируются дорсальной мезодермой (нотохордой) и диффундируют в вышележащую эктодерму, ингибируя активность BMP4. Это ингибирование BMP4 заставляет клетки дифференцироваться в нервные клетки. Ингибирование передачи сигналов TGF-β и BMP (костного морфогенетического белка) может эффективно индуцировать нервную ткань из плюрипотентных стволовых клеток человека . [6] Модель раннего развития человека.
Ранний мозг
[ редактировать ]В конце четвертой недели верхняя часть нервной трубки сгибается на уровне будущего среднего мозга — среднего мозга . Над средним мозгом находится прозэнцефалон (будущий передний мозг), а под ним — ромбэнцефалон (будущий задний мозг). Оптический пузырек (который в конечном итоге станет зрительным нервом, сетчаткой и радужной оболочкой) формируется в базальной пластинке переднего мозга.
Спинной мозг формируется из нижней части нервной трубки. Стенка нервной трубки состоит из нейроэпителиальных клеток, которые дифференцируются в нейробласты, образуя мантийный слой (серое вещество). Нервные волокна выходят из этих нейробластов и образуют маргинальный слой (белое вещество). Вентральная часть мантийного слоя (базальные пластинки) образует двигательные области спинного мозга, а дорсальная часть (крыльные пластинки) — сенсорные области. Между базальной и крыловой пластинками находится промежуточный слой, содержащий нейроны вегетативной нервной системы. [7]
На пятой неделе крыловидная пластинка переднего мозга расширяется и образует полушария головного мозга ( конечный мозг ). Базальная пластинка становится промежуточным мозгом .
Промежуточный мозг, средний мозг и ромбенцефалон составляют ствол мозга эмбриона. Он продолжает сгибаться в среднем мозге. Ромбэнцефалон складывается назад, в результате чего его крыльная пластинка расширяется и образует четвертый желудочек мозга. Мост формируются в верхней части ромбовидного мозга, а и мозжечок продолговатый мозг - в нижней части.
Нейровизуализация
[ редактировать ]Нейровизуализация позволила добиться больших успехов в понимании того, как развивается мозг. ЭЭГ и ERP — эффективные методы визуализации, используемые в основном у младенцев и детей раннего возраста, поскольку они более щадящие. Младенцев обычно проверяют с помощью fNIRS . МРТ фМРТ и широко используются для исследования мозга благодаря качеству изображений и возможному их анализу.
Магнитно-резонансная томография
[ редактировать ]МРТ помогает проанализировать многие аспекты работы мозга. Коэффициент намагничивания-передачи (MTR) измеряет целостность с помощью намагничивания. Фракционная анизотропия (ФА) измеряет организацию с помощью диффузии молекул воды. Кроме того, средняя диффузия (MD) измеряет прочность участков белого вещества . [8]
Структурная магнитно-резонансная томография
[ редактировать ]С помощью структурной МРТ можно провести количественную оценку ряда процессов развития, включая определение моделей роста, [9] и характеризующие последовательность миелинизации. [10] Эти данные дополняют данные исследований диффузионно-тензорной визуализации (DTI), которые широко использовались для изучения развития белого вещества.
Функциональная магнитно-резонансная томография
[ редактировать ]Тест ментализации с помощью фМРТ, который представляет собой теорию разума путем активации сети. Задне-верхняя височная борозда (pSTS) и височно-теменной переход (TPJ) помогают прогнозировать движение. У взрослых правый pSTS показал больший ответ, чем тот же регион у подростков, при тестировании на намеренную причинно-следственную связь. Эти области также были активированы во время упражнения «разум в глазах», где эмоции необходимо оценивать на основе различных изображений глаз. Другой ключевой областью является передняя височная кора (АТК) в задней области. У взрослых левый АТС показал больший ответ, чем тот же регион у подростков, при тестировании на эмоциональные тесты на ментализацию. Наконец, медиальная префронтальная кора (MPFC) и передняя дорсальная MPFC (dMPFC) активируются, когда разум стимулируется психологией. [8]
Трехмерная сонография
[ редактировать ]Визуализация с более высоким разрешением позволила трехмерному ультразвуку помочь определить развитие мозга человека на эмбриональных стадиях. формируются три первичные структуры Исследования сообщают, что на шестой неделе беременности . Это передний мозг , средний мозг и задний мозг , также известные как передний мозг, средний мозг и ромбовидный мозг соответственно. Пять вторичных структур из них на седьмой неделе беременности. Это телэнцефалон, промежуточный мозг, средний мозг, метэнцефалон и продолговатый мозг, которые позже во взрослом возрасте становятся боковыми желудочками, третьими желудочками, водопроводом, а также верхней и нижней частями четвертого желудочка от конечного мозга до продолговатого мозга. 3D-ультразвуковая визуализация позволяет in vivo визуализировать идеальное развитие мозга, что может помочь распознать нарушения во время беременности. [11]
Развитие белого вещества
[ редактировать ]Исследования с помощью МРТ показали, что в то время как белое вещество увеличивается с детства (~ 9 лет) до подросткового возраста (~ 14 лет), серое вещество уменьшается. Это наблюдалось преимущественно в лобной и теменной коре. Теории относительно того, почему это происходит, различаются. Одна из предположений состоит в том, что внутрикорковая миелинизация в сочетании с увеличением калибра аксонов увеличивает объем ткани белого вещества. Другая причина состоит в том, что синаптическая реорганизация происходит в результате пролиферации и последующего сокращения. [8]
Развитие серого вещества
[ редактировать ]Подъем и падение объема серого вещества в лобных и теменных долях достигали максимума примерно в 12-летнем возрасте. Пик развития височных долей составил ~17 лет, при этом верхняя височная кора созревала последней. Сначала созревают сенсорная и моторная области, а затем развивается остальная часть коры. Это характеризовалось потерей серого вещества и происходило от задней части к передней. Эта потеря серого вещества и увеличение количества белого вещества могут происходить на протяжении всей жизни, хотя более сильные изменения происходят с детства до подросткового возраста. [8]
Нейрональная миграция
[ редактировать ]Миграция нейронов — это метод, с помощью которого нейроны перемещаются от места своего происхождения или места рождения до конечного положения в мозге. Наиболее распространенными способами миграции являются радиальная и тангенциальная миграция.
Радиальная миграция
[ редактировать ]Нейральные стволовые клетки пролиферируют в желудочковой зоне развивающегося неокортекса . Первые постмитотические клетки, мигрирующие из препластинки, которым суждено стать клетками Кахаля-Ретциуса и нейронами субпластинки . Эти клетки делают это путем сомальной транслокации. Нейроны, мигрирующие при таком способе передвижения, являются биполярными и прикрепляют передний край отростка к мягкой мозговой оболочке . Затем сома « транспортируется на поверхность пиальной оболочки посредством нуклеокениса, процесса, при котором клетка» микротрубочек вокруг ядра удлиняется и сжимается вместе с центросомой , направляя ядро к конечному пункту назначения. [12] Радиальные волокна (также известные как радиальная глия) могут перемещаться в кортикальную пластинку и дифференцироваться либо в астроциты , либо в нейроны . [13] Сомальная транслокация может произойти в любой момент развития. [14]
Последующие волны нейронов расщепляют препластинку, мигрируя по радиальным глиальным волокнам, образуя кортикальную пластинку. Каждая волна мигрирующих клеток проходит мимо своих предшественников, образуя слои изнутри наружу, а это означает, что самые молодые нейроны находятся ближе всего к поверхности. [15] [16] Подсчитано, что миграция, управляемая глией, представляет собой 80-90% мигрирующих нейронов. [17]
Аксофильная миграция
[ редактировать ]Многие нейроны, мигрирующие вдоль передне-задней оси тела, используют существующие аксонные пути для миграции в процессе, называемом аксофильной миграцией. [18] Примером такого способа миграции являются нейроны, экспрессирующие ГнРГ , которые совершают долгий путь от места своего рождения в носу через передний мозг в гипоталамус. [19] Многие механизмы этой миграции были разработаны, начиная с внеклеточных сигналов. [20] которые запускают внутриклеточную передачу сигналов. Эти внутриклеточные сигналы, такие как передача сигналов кальция , приводят к образованию актина. [21] и микротрубочки [22] цитоскелетная динамика, которая создает клеточные силы, которые взаимодействуют с внеклеточной средой через белки клеточной адгезии. [23] вызвать движение этих клеток. Нейрофильная миграция означает миграцию нейронов по аксону, принадлежащему другому нерву. Глиофильная миграция — это миграция глии по глиальным волокнам. [24]
Тангенциальная миграция
[ редактировать ]Большинство интернейронов мигрируют по касательной, используя несколько способов миграции, чтобы достичь подходящего места в коре. Примером тангенциальной миграции является перемещение клеток Кахаля-Ретциуса внутри маргинальной зоны кортикального нейроэпителия. [25]
Другие
[ редактировать ]Существует также метод миграции нейронов, называемый мультиполярной миграцией . [26] [27] Это наблюдается в мультиполярных клетках, которые в изобилии присутствуют в промежуточной зоне коры . Они не похожи на клетки, мигрирующие посредством локомоции или сомальной транслокации. Вместо этого эти мультиполярные клетки экспрессируют нейрональные маркеры и расширяют множество тонких отростков в различных направлениях независимо от радиальных глиальных волокон. [26]
Нейротрофические факторы
[ редактировать ]Нейротрофические факторы — это молекулы, которые способствуют и регулируют выживаемость нейронов в развивающейся нервной системе. Они отличаются от вездесущих метаболитов, необходимых для поддержания и роста клеток, своей специфичностью; каждый нейротрофический фактор способствует выживанию только определенных видов нейронов на определенном этапе их развития. Кроме того, утверждалось, что нейротрофические факторы участвуют во многих других аспектах развития нейронов, начиная от направления аксонов и заканчивая регуляцией синтеза нейромедиаторов. [28]
Нервное развитие взрослых
[ редактировать ]Нейроразвитие во взрослой нервной системе включает такие механизмы, как ремиелинизация , образование новых нейронов , глии , аксонов , миелина или синапсов . Нейрорегенерация различается в периферической нервной системе (ПНС) и центральной нервной системе (ЦНС) по функциональным механизмам и особенно по объему и скорости.
Нервная система продолжает развиваться в зрелом возрасте вплоть до смерти мозга . [ необходимы дополнительные ссылки ] Например:
- физические упражнения имеют нейробиологический эффект
- потребление продуктов питания (или питательных веществ ), ожирение, [29] изменения микробиома , напитки, пищевые добавки , легкие наркотики и лекарства [30] [31] возможно, также оказывает влияние на развитие нервной системы
- различные заболевания, такие как COVID-19 , влияют на развитие нервной системы.
- Например, было идентифицировано несколько генов, которые связаны с изменениями в структуре мозга в течение жизни и являются потенциальными болезни Альцгеймера . мишенями для терапии [32] [33]
- психологические события, такие как психическая травма и повышение устойчивости
- воздействие загрязнения окружающей среды и токсинов, таких как загрязнение воздуха, может повлиять на дальнейшее развитие нервной системы.
- другие виды деятельности также могут оказывать влияние на развитие нервной системы, например, непрерывное обучение , переподготовка , а также виды медиа- и экономической деятельности.
- в общем, старение мозга
Исследования, методы лечения и политика часто различают «зрелый» мозг и «развивающийся» мозг, в то время как ученые отмечают, что «сложная природа нейроразвития сама по себе создает проблемы для установления точки отсчета, которая будет указывать на то, когда мозг созревает» и что различные структурные показатели мозга постоянно меняются на протяжении взрослой фазы жизни, [34] хотя детский уровень нейропластичности , возможно, не будет снова достигнут [ нужна ссылка ] и считается, что существуют различные критические и чувствительные периоды развития мозга. [35]
Различия в обучении детей
[ редактировать ]Обучение часто более эффективно у детей занимает больше времени или становится более трудным и с возрастом . Исследование с использованием нейровизуализации выявило быстрое усиление нейромедиатора ГАМК в качестве основного потенциального компонента объяснения того, почему это происходит. [36] [37]
Детский мозг содержит больше « тихих синапсов », которые неактивны до тех пор, пока не задействованы в рамках нейропластичности и гибкого обучения или памяти . [38] [39] Нейропластичность повышается в критические или чувствительные периоды развития мозга, что в основном относится к развитию мозга во время развития ребенка . [40]
То, чему люди учатся на ранних стадиях, и то, что они учатся применять, направляет людей на жизненный путь или оказывает непропорциональное влияние. [41] Взрослые обычно имеют более высокую способность выбирать, что они изучают, в какой степени и как. Например, дети могут изучать определенные предметы и темы школьной программы, используя почерк на классной доске , вместо того, чтобы иметь возможность выбирать конкретные темы/навыки или профессии для изучения и стили обучения. Например, у детей могут не развиться консолидированные интересы, этика, интерес к цели и значимой деятельности, знания о требованиях и требованиях реального мира, а также приоритетах.Исследовать
[ редактировать ]Пространственно-временное моделирование развития мозга
[ редактировать ]На раннем этапе развития (до рождения и в течение первых нескольких месяцев) мозг претерпевает больше изменений в размере, форме и структуре, чем в любой другой период жизни. Лучшее понимание развития головного мозга в этот критический период важно для картирования нормального роста и для исследования механизмов травм, связанных с факторами риска пороков развития, такими как преждевременные роды. Следовательно, существует необходимость в плотном охвате этого возрастного диапазона с помощью изменяющегося во времени и зависящего от возраста атласа. Такие пространственно-временные атласы могут точно отражать динамические изменения, происходящие на ранних стадиях развития мозга. [9] и может использоваться в качестве нормативного справочного пространства.
Кроме того, были проведены крупномасштабные исследования экспрессии генов в различных областях мозга от раннего периода беременности до старения. Данные такого рода дают уникальное представление об изменениях, происходящих в мозге в течение этого длительного периода. Этот подход показал, что 86 процентов генов были экспрессированы и что 90 процентов из них дифференцированно регулировались на уровне всего транскрипта или экзона в разных областях мозга и/или во времени. Большинство этих пространственно-временных различий было обнаружено до рождения с последующим увеличением сходства между региональными транскриптомами. Более того, межрегиональные различия демонстрируют временной паттерн «песочные часы», разделяя развитие неокортекса человека на три основные фазы. На первом этапе, в первые шесть месяцев после зачатия, общая архитектура областей мозга во многом формируется за счет всплеска генетической активности, характерного для конкретных участков неокортекса. За этим приливом следует своего рода перерыв, начинающийся в третьем триместре беременности. В этот период подавляется большинство генов, которые активны в определенных областях мозга, за исключением генов, которые стимулируют связи между всеми областями неокортекса. Затем, в позднем детстве и раннем подростковом возрасте, генетический оркестр возобновляет работу и помогает тонко формировать области неокортекса, которые постепенно выполняют более специализированные задачи, и этот процесс продолжается и во взрослом возрасте. [42] [43] [44]
Исследования развития эмбрионального мозга
[ редактировать ]Этот раздел нуждается в расширении . Вы можете помочь, добавив к нему . ( ноябрь 2022 г. ) |
Подходы к исследованию органогенеза и раннего развития человеческого мозга или нервной системы включают:
- Мозговые органоиды и « ассамблоиды ». [45] [46] (см. также: Генетические факторы недавней эволюции мозга )
- Синтетические эмбрионы/модели эмбрионов [47] [48] [49] [50] [51] [52]
- Модели животных
- Посмертные исследования [53]
- Неинвазивная визуализация in vivo [53] По состоянию на 2014 год визуализация внутриутробного развития обычно не проводится без веских медицинских аргументов; [53] В 2019 году исследование показало, что « подходы нейровизуализации внесли значительный вклад в наше понимание раннего развития мозга». [54]
Недоступность человеческих тканей препятствовала молекулярному пониманию формирования когнитивных способностей. [45] Плацента . также исследуется [55] [56] [54]
Лучшее понимание развития потенциально может позволить глубже понять заболевания нервной системы, улучшить интеллект и улучшить защиту от вредного воздействия выявленных факторов развития плода (потенциально в том числе от болезней матери, различных событий и ксенобиотиков ). [53] [54] [ необходимы дополнительные ссылки ]
Конкретные регионы
[ редактировать ]Исследования смогли сделать новые открытия в различных частях мозга благодаря доступным неинвазивным методам визуализации.
- Медиальная префронтальная кора (MPFC)
В этом регионе у подростков отмечается большая активность, чем у взрослых, при выполнении тестов на ментализирующие задачи, а также коммуникативную и личностную интенцию. Снижение активности от подросткового возраста до взрослой жизни. В задаче по ментализации с использованием анимации dMPFC больше стимулировалась у взрослых, тогда как вентральная MPFC больше стимулировалась у детей. Их можно отнести к использованию объективной стратегии, связанной с dMPFC. Теории снижения активности от подросткового возраста до взрослой жизни различаются. Одна теория состоит в том, что когнитивная стратегия становится более автоматической с возрастом, а другая заключается в том, что функциональные изменения происходят параллельно с нейроанатомическими изменениями, которые характеризуются синаптогенезом и обрезкой. [8]
MPFC является примером одного конкретного региона, который стал лучше изучен с помощью современных методов визуализации. Текущие исследования дают еще много подобных результатов.
Стресс в раннем возрасте
[ редактировать ]Стресс в раннем возрасте определяется как воздействие обстоятельств в детстве, которые подавляют ресурсы ребенка и приводят к длительным периодам стресса. [57] Результаты многочисленных исследований показывают, что влияние стресса в раннем возрасте на развивающийся мозг является значительным и включает, помимо прочего, следующее: увеличение объема миндалевидного тела, [58] [59] снижение активности лобных корковых и лимбических структур мозга, [60] и измененные структуры белого вещества. [61]
Считается, что стресс в раннем возрасте вызывает изменения в развитии мозга, вмешиваясь в нейрогенез, производство синапсов и сокращение синапсов и рецепторов. [57] Вмешательство в эти процессы может привести к увеличению или уменьшению объемов областей мозга, что потенциально объясняет результаты о том, что стресс в раннем возрасте связан с увеличением объема миндалины и уменьшением объема передней поясной извилины. [58] [62]
Из литературы было сделано несколько важных выводов. Области мозга, которые претерпевают значительное постнатальное развитие, например те, которые отвечают за память и эмоции, более уязвимы к последствиям стресса в раннем возрасте. [57] [63] Например, гиппокамп продолжает развиваться после рождения и представляет собой структуру, на которую влияет жестокое обращение в детстве. [63] Стресс в раннем возрасте, по-видимому, препятствует перепроизводству синапсов, типичному для детства, но не препятствует сокращению синапсов в подростковом возрасте. Это приводит к меньшим объемам гиппокампа, что потенциально объясняет связь между стрессом в раннем возрасте и уменьшением объема гиппокампа. [62] Это уменьшение объема может быть связано с дефицитом регуляции эмоций, наблюдаемым у тех, кто подвергался стрессу в раннем возрасте.
Миндалевидное тело особенно уязвимо к стрессу в раннем возрасте. [57] Миндалевидное тело также претерпевает значительное развитие в детстве, структурно и функционально изменяется у людей, переживших стресс в раннем возрасте, и связано с социально-эмоциональными трудностями, связанными со стрессом в раннем возрасте.
Тип рецептора является еще одним фактором, который следует учитывать при определении того, чувствительна ли область мозга к воздействию стресса в раннем возрасте. Области мозга с высокой плотностью глюкокортикоидных рецепторов особенно уязвимы к воздействию стресса в раннем возрасте, вероятно, потому, что глюкокортикоиды связываются с этими рецепторами во время воздействия стресса, способствуя развитию реакций выживания за счет других важных нервных путей. [63] Некоторыми примерами областей мозга с высокой плотностью глюкокортикоидных рецепторов являются гиппокамп и червь мозжечка. Стресс активирует ось HPA и приводит к выработке глюкокортикоидов. Увеличение производства глюкокортикоидов приводит к усилению активации этих областей мозга, способствуя развитию одних нервных путей за счет других.
Нарушения в структуре и функциях мозга часто связаны с нарушениями, которые могут сохраняться в течение многих лет после снятия стресса и могут быть фактором риска будущих психопатологий. [57] Области мозга, наиболее чувствительные к стрессу в раннем возрасте, — это те, которые претерпевают изменения в развитии во время воздействия стресса. В результате стресс меняет траекторию развития этой области мозга, вызывая долговременные изменения в структуре и функциях.
Задокументированные распространенные типы стресса в раннем возрасте включают жестокое обращение, пренебрежение и предыдущую институционализацию. Было также доказано, что жизнь в бедности аналогичным образом влияет на функцию мозга. [64]
См. также
[ редактировать ]- Хронология развития человеческого мозга
- КСС2
- Нарушения нервно-психического развития
- Нейронный дарвинизм
- Пре- и перинатальная психология
Внешние ссылки
[ редактировать ]- Промежуточные последовательности радиальной миграции (также известной как глиальное наведение) и сомальной транслокации. [14]
Ссылки
[ редактировать ]- ^ Саладин, К. (2011). Анатомия и физиология: единство формы и функции (6-е изд.). МакГроу-Хилл. п. 541. ИСБН 9780073378251 .
- ^ Перейти обратно: а б Чжоу, И; Сон, Хунцзюнь; Мин, Го-Ли (28 июля 2023 г.). «Генетика развития мозга человека» . Обзоры природы. Генетика . 25 (1): 26–45. дои : 10.1038/s41576-023-00626-5 . ISSN 1471-0064 . ПМЦ 10926850 . ПМИД 37507490 .
- ^ Гилберт, Скотт (2013). Биология развития (Десятое изд.). Sinauer Associates Inc. ISBN 978-1605351926 .
- ^ Кандел, Эрик Р. (2006). Принципы нейронауки (5-е изд.). Эпплтон и Ланге: МакГроу Хилл. ISBN 978-0071390118 .
- ^ Эстомих Мтуи; Грегори Грюнер (2006). Клиническая нейроанатомия и неврология . Филадельфия: Сондерс. п. 1. ISBN 978-1-4160-3445-2 .
- ^ Чемберс, С.М.; и др. (2009). «Высокоэффективное нейронное преобразование ES и iPS клеток человека путем двойного ингибирования передачи сигналов SMAD» . Природная биотехнология . 27 (3): 275–280. дои : 10.1038/nbt.1529 . ПМЦ 2756723 . ПМИД 19252484 .
- ^ Атлас эмбриологии человека, Chronolab. Архивировано 27 декабря 2007 г. в Wayback Machine . Последний доступ: 30 октября 2007 г.
- ^ Перейти обратно: а б с д и Блейкмор, SJ (июнь 2012 г.). «Визуализация развития мозга: мозг подростка». НейроИмидж . 61 (2): 397–406. doi : 10.1016/j.neuroimage.2011.11.080 . ПМИД 22178817 . S2CID 207182527 .
- ^ Перейти обратно: а б Сераг, А.; и др. (2012). «Построение последовательного пространственно-временного атласа развивающегося мозга высокой четкости с использованием адаптивной регрессии ядра». НейроИмидж . 59 (3): 2255–2265. doi : 10.1016/j.neuroimage.2011.09.062 . ПМИД 21985910 . S2CID 9747334 .
- ^ Сераг, Ахмед; и др. (2011). «Отслеживание изменений в развитии подкорковых структур мозга недоношенных с помощью мультимодальной МРТ». Международный симпозиум IEEE 2011 по биомедицинской визуализации: от нано к макро . стр. 349–352. дои : 10.1109/ISBI.2011.5872421 . ISBN 978-1-4244-4127-3 . S2CID 5785586 .
- ^ Ким, MS; и др. (январь 2008 г.). «Трехмерная сонографическая оценка развития эмбрионального мозга» . Журнал ультразвука в медицине . 27 (1): 119–124. дои : 10.7863/jum.2008.27.1.119 . ПМИД 18096737 .
- ^ Сэмюэлс Б.А., Цай Л.Х. (ноябрь 2004 г.). «Нуклеокинез освещен». Природа Нейронауки . 7 (11): 1169–70. дои : 10.1038/nn1104-1169 . ПМИД 15508010 . S2CID 11704754 .
- ^ Кэмпбелл К., Гетц М. (май 2002 г.). «Радиальная глия: многоцелевые клетки для развития мозга позвоночных». Тенденции в нейронауках . 25 (5): 235–8. дои : 10.1016/S0166-2236(02)02156-2 . ПМИД 11972958 . S2CID 41880731 .
- ^ Перейти обратно: а б Надараджа Б., Брунстрем Дж. Э., Грутцендлер Дж., Вонг Р.О., Перлман А.Л. (февраль 2001 г.). «Два режима радиальной миграции в раннем развитии коры головного мозга». Природа Нейронауки . 4 (2): 143–50. дои : 10.1038/83967 . ПМИД 11175874 . S2CID 6208462 .
- ^ Надараджа Б., Парнавелас Дж.Г. (июнь 2002 г.). «Режимы миграции нейронов в развивающейся коре головного мозга». Обзоры природы. Нейронаука . 3 (6): 423–32. дои : 10.1038/nrn845 . ПМИД 12042877 . S2CID 38910547 .
- ^ Ракич П. (май 1972 г.). «Режим миграции клеток в поверхностные слои неокортекса плода обезьяны». Журнал сравнительной неврологии . 145 (1): 61–83. дои : 10.1002/cne.901450105 . ПМИД 4624784 . S2CID 41001390 .
- ^ Хаттен, Мэри (1999). «Миграция нейронов центральной нервной системы» (PDF) . Ежегодный обзор неврологии . 22 . Ежегодные обзоры по неврологии: 511–539. дои : 10.1146/annurev.neuro.22.1.511 . ПМИД 10202547 .
- ^ Казони, Ф; Хатчинс, Б.И.; Донохью, Д; Форнаро, М; Конди, Б.Г.; Рэй, С. (1 ноября 2012 г.). «SDF и ГАМК взаимодействуют, регулируя аксофильную миграцию нейронов GnRH» . Журнал клеточной науки . 125 (Часть 21): 5015–25. дои : 10.1242/jcs.101675 . ПМЦ 3533389 . ПМИД 22976302 .
- ^ Рэй С. (июль 2010 г.). «От носа к мозгу: развитие нейронов гонадотропин-рилизинг-гормона-1» . Журнал нейроэндокринологии . 22 (7): 743–53. дои : 10.1111/j.1365-2826.2010.02034.x . ПМЦ 2919238 . ПМИД 20646175 .
- ^ Джакобини П., Мессина А., Рэй С., Джампьетро С., Крепальди Т., Кармелиет П., Фасоло А. (январь 2007 г.). «Фактор роста гепатоцитов действует как мотоген и направляющий сигнал для миграции нейронов, высвобождающих гонадотропин-рилизинг-гормон-1» . Журнал неврологии . 27 (2): 431–45. doi : 10.1523/JNEUROSCI.4979-06.2007 . ПМК 6672060 . ПМИД 17215404 .
- ^ Хатчинс Б.И., Кленке У., Рэй С. (июль 2013 г.). «Зависимый от высвобождения кальция поток актина в ведущем процессе опосредует аксофильную миграцию» . Журнал неврологии . 33 (28): 11361–71. doi : 10.1523/JNEUROSCI.3758-12.2013 . ПМЦ 3724331 . ПМИД 23843509 .
- ^ Хатчинс Б.И., Рэй С. (2014). «Захват плюс-концов микротрубочек в актиновой коре способствует аксофильной миграции нейронов за счет усиления натяжения микротрубочек в ведущем отростке» . Границы клеточной нейронауки . 8 : 400. дои : 10.3389/fncel.2014.00400 . ПМК 4245908 . ПМИД 25505874 .
- ^ Паркаш Дж., Чимино И., Феррарис Н., Касони Ф., Рэй С., Кэппи Х., Прево В., Джакобини П. (ноябрь 2012 г.). «Подавление β1-интегрина в клетках, высвобождающих гонадотропин, нарушает миграцию и расширение аксонов, что приводит к серьезным репродуктивным изменениям» . Журнал неврологии . 32 (47): 16992–7002. doi : 10.1523/JNEUROSCI.3057-12.2012 . ПМК 5238668 . ПМИД 23175850 .
- ^ Купер, Джонатан А. (2 сентября 2013 г.). «Механизмы миграции клеток в нервной системеМеханизмы миграции клеток в нервной системе» . Журнал клеточной биологии . 202 (5): 725–734. дои : 10.1083/jcb.201305021 . ПМК 3760606 . ПМИД 23999166 .
- ^ Чен Дж.П., Чжан Д.В., Лю Дж.М. (июль 2016 г.). «Экзотические кристаллы скирмиона в хиральных магнитах с компасной анизотропией» . Научные отчеты . 6 : 29126. Бибкод : 2016NatSR...629126C . дои : 10.1038/srep29126 . ПМЦ 4932608 . ПМИД 27377149 .
- ^ Перейти обратно: а б Табата Х., Накадзима К. (ноябрь 2003 г.). «Мультиполярная миграция: третий способ радиальной миграции нейронов в развивающейся коре головного мозга» . Журнал неврологии . 23 (31): 9996–10001. doi : 10.1523/JNEUROSCI.23-31-09996.2003 . ПМК 6740853 . ПМИД 14602813 .
- ^ Надараджа Б., Алифрагис П., Вонг Р.О., Парнавелас Дж.Г. (июнь 2003 г.). «Миграция нейронов в развивающейся коре головного мозга: наблюдения, основанные на визуализации в реальном времени» . Кора головного мозга . 13 (6): 607–11. дои : 10.1093/cercor/13.6.607 . ПМИД 12764035 .
- ^ Алан М. Дэвис (1 мая 1988 г.) «Тенденции в генетике», том 4-выпуск 5; Кафедра анатомии, Медицинская школа больницы Святого Георгия, Кранмер-Террас, Тутинг, Лондон SW17 0RE, Великобритания
- ^ Дай, Луиза; Бойл, Нил Бернард; Чемп, Клэр; Лоутон, Клэр (ноябрь 2017 г.). «Взаимосвязь между ожирением и когнитивным здоровьем и упадком» . Труды Общества питания . 76 (4): 443–454. дои : 10.1017/S0029665117002014 . ISSN 1475-2719 . ПМИД 28889822 . S2CID 34630498 .
- ^ Шпиндлер, Кэролин; Маллиен, Луиза; Траутманн, Себастьян; Александр, Нина; Мюльхан, Маркус (27 января 2022 г.). «Координатный метаанализ изменений белого вещества у пациентов с расстройством, связанным с употреблением алкоголя» . Трансляционная психиатрия . 12 (1): 40. дои : 10.1038/s41398-022-01809-0 . ISSN 2158-3188 . ПМЦ 8795454 . ПМИД 35087021 . S2CID 246292525 .
- ^ Уоллман, Скотт С.; Альхассун, Омар М.; Холл, Мэтью Г.; Стерн, Марк Дж.; Коннорс, Эрик Дж.; Киммел, Кристин Л.; Аллен, Кеннет Э.; Стефан, Рик А.; Радуа, Хоаким (сентябрь 2017 г.). «Нарушения серого вещества у пациентов с опиоидной зависимостью: метаанализ нейровизуализации». Американский журнал о злоупотреблении наркотиками и алкоголем . 43 (5): 505–517. дои : 10.1080/00952990.2016.1245312 . ISSN 1097-9891 . ПМИД 27808568 . S2CID 4775912 .
- ^ «Генетические «горячие точки», которые ускоряют и замедляют старение мозга, могут стать новыми мишенями для лекарств от болезни Альцгеймера» . Университет Южной Калифорнии . Проверено 15 мая 2022 г.
- ^ Брауэр, Рэйчел М.; Кляйн, Марике; Грасби, Катрина Л.; Шнак, Хьюго Г.; и др. (апрель 2022 г.). «Генетические варианты, связанные с продольными изменениями структуры мозга на протяжении всей жизни» . Природа Нейронауки . 25 (4): 421–432. дои : 10.1038/s41593-022-01042-4 . ISSN 1546-1726 . ПМК 10040206 . ПМИД 35383335 . S2CID 247977288 .
- ^ Сомервилл, Лия Х. (21 декабря 2016 г.). «В поисках признаков зрелости мозга: что мы ищем?» . Нейрон . 92 (6): 1164–1167. дои : 10.1016/j.neuron.2016.10.059 . ISSN 0896-6273 . ПМИД 28009272 . S2CID 207217254 .
- ^ Исмаил, Фатима Юсиф; Фатеми, Али; Джонстон, Майкл В. (январь 2017 г.). «Церебральная пластичность: окна возможностей в развивающемся мозге». Европейский журнал детской неврологии . 21 (1): 23–48. дои : 10.1016/j.ejpn.2016.07.007 . ISSN 1532-2130 . ПМИД 27567276 .
- ^ «Сканирование мозга проливает свет на то, почему дети учатся быстрее, чем взрослые» . УПИ . Проверено 17 декабря 2022 г.
- ^ Франк, Себастьян М.; Беккер, Маркус; Ци, Андреа; Гейгер, Патрисия; Франк, Ульрика И.; Роуздал, Люк А.; Маллони, Вильгельм М.; Сасаки, Юка; Гринли, Марк В.; Ватанабэ, Такео (5 декабря 2022 г.). «Эффективное обучение детей с быстрым повышением ГАМК во время и после тренировки» . Современная биология . 32 (23): 5022–5030.e7. bioRxiv 10.1101/2022.01.02.474022 . дои : 10.1016/j.cub.2022.10.021 . ISSN 0960-9822 . ПМИД 36384138 . S2CID 253571891 .
- ^ Льореда, Клаудия Лопес (16 декабря 2022 г.). «Мозг взрослой мыши изобилует «тихими синапсами» » . Новости науки . Проверено 18 декабря 2022 г.
- ^ Вардалаки, Димитра; Чунг, Кванхун; Харнетт, Марк Т. (декабрь 2022 г.). «Филоподии являются структурным субстратом для молчащих синапсов в неокортексе взрослых» . Природа . 612 (7939): 323–327. Бибкод : 2022Natur.612..323V . дои : 10.1038/s41586-022-05483-6 . ISSN 1476-4687 . ПМИД 36450984 . S2CID 254122483 .
- Пресс-релиз университета: Трафтон, Энн. «Во взрослом мозге много тихих синапсов» . Массачусетский технологический институт (medicalxpress.com) . Проверено 18 декабря 2022 г.
- ^ Исмаил, Фатима Юсиф; Фатеми, Али; Джонстон, Майкл В. (1 января 2017 г.). «Церебральная пластичность: окна возможностей в развивающемся мозге». Европейский журнал детской неврологии . 21 (1): 23–48. дои : 10.1016/j.ejpn.2016.07.007 . ISSN 1090-3798 . ПМИД 27567276 .
- ^ Бакстон, Алекс (10 февраля 2016 г.). «Что происходит в мозгу, когда дети учатся?» . Новости неврологии . Проверено 11 января 2023 г.
- ^ Плетикос, М; и др. (22 января 2014 г.). «Временная спецификация и двусторонность экспрессии топографических генов неокортекса человека» . Нейрон . 81 (2): 321–32. дои : 10.1016/j.neuron.2013.11.018 . ПМК 3931000 . ПМИД 24373884 .
- ^ Кан, Хё Чон; и др. (27 октября 2011 г.). «Пространственно-временной транскриптом человеческого мозга» . Природа . 478 (7370): 483–489. Бибкод : 2011Natur.478..483K . дои : 10.1038/nature10523 . ПМЦ 3566780 . ПМИД 22031440 .
- ^ «Развитие человеческого мозга – это симфония в трех частях» . Йельские новости . 26 декабря 2013 г. Проверено 26 декабря 2013 г.
- ^ Перейти обратно: а б Келли, Кевин В.; Пашка, Сергей П. (6 января 2022 г.). «Органогенез человеческого мозга: на пути к клеточному пониманию развития и болезней» . Клетка . 185 (1): 42–61. дои : 10.1016/j.cell.2021.10.003 . ISSN 0092-8674 . ПМИД 34774127 . S2CID 244038503 .
- ^ Кьярадиа, Илария; Ланкастер, Мэдлин А. (декабрь 2020 г.). «Мозговые органоиды для изучения нейробиологии человека на стыке in vitro и in vivo». Природа Нейронауки . 23 (12): 1496–1508. дои : 10.1038/s41593-020-00730-3 . ПМИД 33139941 . S2CID 226242709 .
- ^ Уилльярд, Кассандра (25 августа 2022 г.). «Мышиные эмбрионы, выращенные без яйцеклеток и сперматозоидов: почему и что дальше?» . Природа . 609 (7926): 230–231. Бибкод : 2022Natur.609..230W . дои : 10.1038/d41586-022-02334-2 . ПМИД 36008716 . S2CID 251843735 .
- ^ «Синтетический эмбрион развивает органы» . www.sciencemediacenter.de . Проверено 16 сентября 2022 г.
- ^ Холкомб, Мэдлин. «Синтетический эмбрион, созданный без сперматозоидов и яйцеклеток, может привести к лечению бесплодия» . CNN . Проверено 16 сентября 2022 г.
- ^ Амадей, Джанлука; Хэндфорд, Шарлотта Э.; Цю, Чэнсян; Де Йонге, Иоахим; Гринфельд, Ханна; Тран, Мартин; Мартин, Бет К.; Чен, Дун-Юань; Агилера-Кастрехон, Алехандро; Ханна, Джейкоб Х.; Еловиц, Майкл; Холлфельдер, Флориан; Шендюр, Джей; Гловер, Дэвид М.; Зерницка-Гетц, Магдалена (25 августа 2022 г.). «Синтетические эмбрионы завершают гаструляцию, нейруляцию и органогенез» . Природа . 610 (7930): 143–153. дои : 10.1038/s41586-022-05246-3 . ISSN 1476-4687 . ПМЦ 9534772 . ПМИД 36007540 . S2CID 251843659 .
- ^ «Ученые создали первые в мире «синтетические эмбрионы» » . Хранитель . 3 августа 2022 г. Проверено 16 сентября 2022 г.
- ^ Тарази, Шейди; Агилера-Кастрехон, Алехандро; Жубран, Карин; Ганем, Надир; Ашуохи, Шахд; Ронкато, Франческо; Вильдшуц, Эмили; Хаддад, Монтасер; Олдак, Бернардо; Гомес-Сезар, Элидет; Ливнат, Нир; Вьюков, Сергей; Локштанов Дмитрий; Наве-Тасса, Сегев; Роуз, Макс; Ханна, Сухейр; Раанан, Каланит; Бреннер, Ори; Кедми, Мерав; Керен-Шауль, Хадас; Лапидот, Цвее; Маза, Италия; Новерстерн, Ноа; Ханна, Джейкоб Х. (1 сентября 2022 г.). «Синтетические эмбрионы после гаструляции, полученные ex utero из наивных ЭСК мыши» . Клетка . 185 (18): 3290–3306.e25. дои : 10.1016/j.cell.2022.07.028 . ISSN 0092-8674 . ПМЦ 9439721 . ПМИД 35988542 .
- ^ Перейти обратно: а б с д Дюбуа, Ж.; Деэн-Ламбертц, Г .; Куликова С.; Пупон, К.; Хуппи, PS; Герц-Паннье, Л. (сентябрь 2014 г.). «Раннее развитие белого вещества головного мозга: обзор исследований визуализации у плодов, новорожденных и младенцев» (PDF) . Нейронаука . 276 : 48–71. doi : 10.1016/j.neuroscience.2013.12.044 . ПМИД 24378955 . S2CID 8593971 .
- ^ Перейти обратно: а б с Васунг, Лана; Абаки Тюрк, Эсра; Феррадаль, Сильвина Л.; Сутин, Джейсон; Стаут, Джеффри Н.; Ахтам, Бану; Линь, Пей-И; Грант, П. Эллен (15 февраля 2019 г.). «Изучение раннего развития мозга человека с помощью структурной и физиологической нейровизуализации» . НейроИмидж . 187 : 226–254. doi : 10.1016/j.neuroimage.2018.07.041 . ISSN 1053-8119 . ПМК 6537870 . ПМИД 30041061 .
- ^ «Микропластик обнаружен в плацентах неродившихся детей» . Хранитель . 22 декабря 2020 г. Проверено 16 января 2021 г.
- ^ Рагуза, Антонио; Раскрыто, Александр; Сантакроче, Крисельда; Каталано, Пьера; Нотарстефано, Валентина; Карнавалы, Олиана; Папа, Фабрицио; Ронджолетти, Мауро Чиро Антонио; Байокко, Федерико; Драги, Симонетта; д'Амор, Элизабетта; Ринальдо, Дениз; Матта, Мария; Джорджини, Элизабетта (1 января 2021 г.). «Пластицента: первые доказательства наличия микропластика в плаценте человека» . Интернационал окружающей среды . 146 : 106274. Бибкод : 2021EnInt.14606274R . дои : 10.1016/j.envint.2020.106274 . hdl : 11566/286406 . ISSN 0160-4120 . ПМИД 33395930 . S2CID 229444649 .
- ^ Перейти обратно: а б с д и Печтель, Пиа; Пиццагалли, Диего А. (2010). «Влияние стресса в раннем возрасте на когнитивные и аффективные функции: комплексный обзор человеческой литературы» . Психофармакология . 214 (1): 55–70. дои : 10.1007/s00213-010-2009-2 . ПМК 3050094 . ПМИД 20865251 .
- ^ Перейти обратно: а б Мехта, Митул А.; Голембо, Николь И.; Носарти, Кьяра; Колверт, Эмма; Мота, Эшли; Уильямс, Стивен CR; Раттер, Майкл; Сонуга-Барк, Эдмунд Дж.С. (2009). «Размер миндалины, гиппокампа и мозолистого тела после тяжелой ранней институциональной депривации: пилотное исследование английских и румынских усыновленных». Журнал детской психологии и психиатрии . 50 (8): 943–51. дои : 10.1111/j.1469-7610.2009.02084.x . ПМИД 19457047 .
- ^ Тоттенхэм, Ним; Заяц, Тодд А.; Куинн, Брайан Т.; Маккерри, Томас В.; Медсестра Марселла; Гилхули, Тара; Миллнер, Александр; Гальван, Адриана; Дэвидсон, Мэтью С.; Эйгсти, Инге-Мари; Томас, Кэтлин М.; Фрид, Питер Дж.; Бума, Элизабет С.; Гуннар, Меган Р.; Альтемус, Маргарет; Аронсон, Джейн; Кейси, Би Джей (2010). «Длительное воспитание в специальных учреждениях связано с атипично большим объемом миндалевидного тела и трудностями в регуляции эмоций» . Наука развития . 13 (1): 46–61. дои : 10.1111/j.1467-7687.2009.00852.x . ПМК 2817950 . ПМИД 20121862 .
- ^ Чугани, Гарри Т.; Бехен, Майкл Э.; Музик, Отто; Юхас, Чаба; Надь, Ференц; Чугани, Дайан К. (2001). «Локальная функциональная активность мозга после ранней депривации: исследование постинституционализированных румынских сирот». НейроИмидж . 14 (6): 1290–301. дои : 10.1006/нимг.2001.0917 . ПМИД 11707085 . S2CID 30892 .
- ^ Элуватингал, Ти Джей; Чугани, ХТ; Бехен, МЭ; Юхас, К; Музик, О; Макбул, М; Чугани, округ Колумбия; Макки, М (2006). «Аномальная связь мозга у детей после ранней тяжелой социально-эмоциональной депривации: исследование диффузионной тензорной визуализации». Педиатрия . 117 (6): 2093–100. дои : 10.1542/пед.2005-1727 . ПМИД 16740852 . S2CID 30359252 .
- ^ Перейти обратно: а б Бейкер, Лори М.; Уильямс, Линн М.; Коргаонкар, Маюреш С.; Коэн, Рональд А.; Хипс, Джоди М.; Пол, Роберт Х. (2012). «Влияние стресса в раннем и позднем детстве на морфометрию мозга» . Мозговые изображения и поведение . 7 (2): 196–203. дои : 10.1007/s11682-012-9215-y . ПМЦ 8754232 . ПМИД 23247614 . S2CID 90644 .
- ^ Перейти обратно: а б с Тейчер, Мартин Х.; Андерсен, Сьюзен Л.; Полкари, Энн; Андерсон, Карл М.; Навальта, Кэррил П.; Ким, Деннис М. (2003). «Нейробиологические последствия раннего стресса и жестокого обращения в детстве». Неврологические и биоповеденческие обзоры . 27 (1–2): 33–44. дои : 10.1016/S0149-7634(03)00007-1 . ПМИД 12732221 . S2CID 15557040 .
- ^ Ким, П.; Эванс, GW; Ангштадт, М.; Хо, СС; Шрипада, Ч.С.; Суэйн, Дж. Э.; Либерзон, И.; Фан, КЛ (2013). «Влияние детской бедности и хронического стресса на функцию мозга, регулирующую эмоции, во взрослом возрасте» . Труды Национальной академии наук . 110 (46): 18442–7. Бибкод : 2013PNAS..11018442K . дои : 10.1073/pnas.1308240110 . ПМК 3831978 . ПМИД 24145409 .