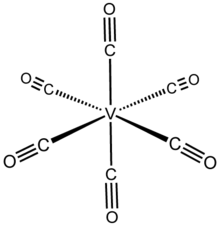
Гексакарбонил ванадия
 | |
| Имена | |
|---|---|
| Название ИЮПАК гексакарбонилванадий(0) | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ЧЭБИ | |
| Информационная карта ECHA | 100.039.928 |
ПабХим CID | |
| НЕКОТОРЫЙ | |
| Характеристики | |
| С 6 О 6 В | |
| Молярная масса | 219.00 g/mol |
| Появление | сине-зеленые кристаллы желтые растворы |
| Плотность | 1,7 г/см 3 |
| Температура плавления | разлагается |
| Точка кипения | сублимируется при 50 ° C (122 ° F; 323 К) (15 мм рт. ст.) |
| нерастворимый | |
| Растворимость в других растворителях | 5 г/л гексана ; более растворим в дихлорметане |
| Структура | |
| орторомбический | |
| октаэдрический | |
| 0 Д | |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности | источник CO |
| Родственные соединения | |
Родственные соединения |
|
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Гексакарбонил ванадия – неорганическое соединение формулы V (CO) 6 . Это летучее твердое вещество сине-черного цвета. Этот высокореактивный вид примечателен с теоретической точки зрения как редкий изолируемый гомолептический карбонил металла , который является парамагнитным. Большинство видов с формулой M x (CO) y следуют правилу 18 электронов , тогда как V (CO) 6 имеет 17 валентных электронов. [1]
Синтез
[ редактировать ]Согласно оригинальному синтезу Кальдераццо , V(CO) 6 получается в две стадии при посредничестве V(CO) −
6 . На первом этапе VCl 3 восстанавливают металлическим натрием при давлении CO 200 атм и температуре 160 °C. Растворителем для этого восстановления обычно является диглим CH 3 OCH 2 CH 2 OCH 2 CH 2 OCH 3 . Этот триэфир растворяет соли натрия, аналогично поведению краун-эфира :
- 4 Na + VCl 3 + 6 CO + 2 diglyme → [Na(diglyme) 2 ][V(CO) 6 ] + 3 NaCl
Образовавшийся анион окисляется кислотой: [2]
- 2 В (СО) −
6 + 2 H 3 PO 4 → 2 В(CO) 6 + H 2 + 2 H
2 ПО −
4
Реакции
[ редактировать ]Гексакарбонил ванадия термически нестабилен. Его основная реакция - восстановление до моноаниона V (CO). −
6 , соли которого хорошо изучены. Он также подвержен замещению третичными фосфиновыми лигандами , что часто приводит к диспропорционированию .
V(CO) 6 реагирует с источниками циклопентадиенильного аниона с образованием оранжевого комплекса четвероногого рояльного стула (C 5 H 5 )V(CO) 4 (т. пл. 136 °C). Как и многие металлоорганические соединения с нейтральным зарядом, этот полусэндвич-образец летуч. В оригинальном препарате этого вида использовался C 5 H 5 HgCl. в качестве источника C
55Ч −
5 .
Структура
[ редактировать ]V(CO) 6 имеет октаэдрическую координационную геометрию и изоструктурен гексакарбонилу хрома , хотя у них разное количество валентных электронов. Рентгеновская кристаллография высокого разрешения показывает, что молекула слегка искажена с двумя ( аксиальными ) более короткими расстояниями V–C, равными 1,993 (2) Å, по сравнению с четырьмя (экваториальными) 2,005 (2) Å. Несмотря на то, что V (-I) является ионом большего размера, чем V (0), расстояния V – C в V (CO) −
6 на 0,07 Å короче, чем у нейтрального предшественника. [3]
Ссылки
[ редактировать ]- ^ Эльшенбройх, К.; Зальцер, А. (1992). Металлоорганические соединения: краткое введение (2-е изд.). Вайнхайм: Wiley-VCH. ISBN 3-527-28165-7 .
- ^ Лю, X.; Эллис, Дж. Э. (2004). «Гексакарбонилванадат (1-) и гексакарбонилванадий (0)». Неорг. Синтез . 34 : 96–103. дои : 10.1002/0471653683.ch3 . ISBN 0-471-64750-0 .
- ^ Беллард, С.; Рубинсон, Калифорния; Шелдрик, генеральный директор (1979). «Кристаллическая и молекулярная структура гексакарбонила ванадия». Акта Кристаллографика . Б35 (2): 271–274. Бибкод : 1979AcCrB..35..271B . дои : 10.1107/S0567740879003332 .
Дальнейшее чтение
[ редактировать ]- Оригинальный синтез: Эрколи, Р.; Кальдераццо, Ф.; Альберола, А. (1960). «Синтез гексакарбонила ванадия». Дж. Ам. хим. Соц . 81 (11): 2966–2967. дои : 10.1021/ja01496a073 .