Никель (ii) бис (ацетилацетонат)
| |

| |
| Имена | |
|---|---|
| Другие имена
Ni (ACAC) 2 , никель ACAC
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| Chemspider | |
| Echa Infocard | 100.019.887 |
| ЕС номер |
|
PubChem CID
|
|
| НЕКОТОРЫЙ | |
Comptox Dashboard ( EPA )
|
|
| Характеристики | |
| C 30 H 42 Ni 3 O 12 | |
| Молярная масса | 770.734 g·mol −1 |
| Появление | темно -зеленый |
| Плотность | 1,455 г/см 3 |
| Точка плавления | 229,5 ° C (445,1 ° F; 502,6 К) (разлагаются) |
| H 2 o | |
| Опасности | |
| GHS Маркировка : | |
 
| |
| Опасность | |
| H302 , H317 , H334 , H350 | |
| P201 , P202 , P261 , P264 , P270 , P272 , P280 , P285 , P281 , P301+P312 , P302+P352 P308 +P313 , P304+P341, , P321 , P330 P36, P336, P365 , , P333+P313 , P342+P311 , P36, P336, P336, P336, P336 , P336 , стр. P501 | |
За исключением случаев, когда отмечены, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа).
| |
Никель (II) BIS (ацетилацетонат) является координационным комплексом с формулой [Ni (ACAC) 2 ] 3 , где ACAC - это анион C 5 H 7 O 2 − из депротонирования ацетилацетона получен . Это темно -зеленое парамагнитное твердое вещество, которое растворится в органических растворителях, таких как толуол . Он реагирует с водой с получением сине-зеленого комплекса Diaquo Ni (ACAC) 2 (H 2 O) 2 . [ 1 ]
Структура и свойства
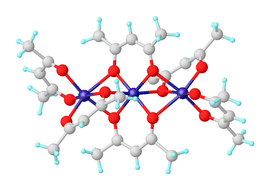
[ редактировать ]Безводная никель (II) ацетилацетонат существует в виде молекул Ni 3 (ACAC) 6 . Три атома никеля приблизительно коллинеарны, и каждая из них соединяется двумя μ 2 атомами кислорода. Каждый атом никеля имеет тетрагонально искаженную октаэдрическую геометрию , вызванную разницей в длине связей Ni-O между мостовыми и не мостиковыми оксигенами. [ 2 ] Ni 3 (ACAC) 6 молекулы практически центрозимметричные , несмотря на нецентрозимметричную точечную группу мономеров цис -Ni (ACAC) 2 , что является редко. [ 3 ] Тримерная структура позволяет всем никелевым центрам достичь октаэдрической координации. Тример образуется только в случае внутримолекулярного распределения кислородных центров между парами никелевых центров. Безводный комплекс обладает интересными магнитными свойствами . До примерно 80 К, он демонстрирует нормальный парамагнетизм с эффективным магнитным моментом 3,2 мкл , близко к моменту только с спинкой, ожидаемым от AD 8 Ион с двумя непарными электронами. Эффективный момент возрастает до 4,1 мкБ при 4,3 К из -за ферромагнитных обмена взаимодействий с участием всех трех ионов никеля. [ 4 ]
Когда он связан с более крупными аналогами ацетилацетонатного лиганда, стерические препятствия способствуют образованию производных мононикель. Это поведение наблюдается для производной 3-метилацетилацетоната. [ 5 ]
Дигидрат
[ редактировать ]
Как и в безводной форме, центры Ni (II) занимают октаэдрические координационные места. Координационная сфера обеспечивается двумя бидентатными ацетилацетонатными (ACAC) лигандами и двумя лигандами Aquo . Ni (ACAC) 2 (H 2 O) 2 существует в виде цис и транс -изомеров . [ 6 ] Транс-изомеры также наблюдаются для Ni (ACAC) 2 ( пиридин-N-оксид ) 2 . [ 7 ] У транс-изомеров осевые связи Ni-O имеют большую длину (2,1000 Å), чем экваториальные связи Ni-O (2,0085 Å и 1,9961 Å). [ 8 ]

Синтез
[ редактировать ]Бис (2,4-пентанедионато) никель (II) готовит путем обработки нитрата никеля ацетилацетоном в присутствии основания . Продукт представляет собой сине-зеленый комплекс Diaquo Ni (Ch 3 Cochcoch 3 ) 2 (H 2 O) 2 . [ 9 ]
- Ni (no 3 ) 2 + 2 ch 3 coch 2 coch 3 + 2 h 2 o + 2 naOH → ni (ch 3 cochcoch 3 ) 2 (h 2 o) 2 + 2 nano 3
Этот комплекс может быть обезвожен с использованием ловушки для декана -старь с помощью азеотропной дистилляции : [ 9 ]
- 3 Ni (Ch 3 Cochcoch 3 ) 2 (H 2 O) 2 → [Ni (Ch 3 Cochcoch 3 ) 2 ] 3 + 6 H 2 O
После нагрева Ni (ACAC) 2 H 2 O) При 170–210 ° C при пониженном давлении (0,2–0,4 мм рт. ( 2 [ 3 ]
Реакция
[ редактировать ]Безводный комплекс реагирует с различными базами Льюиса, чтобы дать мономерные аддукты . [ 10 ] Иллюстрирующим является реакция с тетраметилентилендиамином (TMEDA): [ 11 ]
- [Ni (ch Cochcoch cochcoch 3 ) 2 ] 3 + 3 tmeda → 3 ni (Ch 3 3 3 ) 2 (tmeda)
Ni (ACAC) 2 (H 2 O) 2 быстро реагирует с высоким выходом в метиновых положениях, производя диамиды из изоцианатов. Связанные реакции встречаются с диэтилаазодикарбоксилатом и диметилосетилендикарбоксилатом :
- Ni (acac) 2 (h 2 o) 2 + 2 phnco → ni (o 2 c 5 me 2 c (o) nhph) 2 + 2 h 2 o
Приложения
[ редактировать ]Безводный комплекс является предшественником катализаторов на основе никеля, таких как никель бис (циклооктадиен) и тетраметилентилендиалиамин (диметил) никель (II) . [ 12 ] [ 11 ]
[Ni (ACAC) 2 ] 3 является предшественником для осаждения тонкой пленки NIO GEL на проводящих стеклянных субстратах с использованием методов Sol- . [ 10 ]

Смотрите также
[ редактировать ]Ссылки
[ редактировать ]- ^ RC Mehrotra; Р. Бора; DP Gaur (1978). Металл β -ндитоны и союзные дерил . Академическая пресса. ISBN 0124881505 .
- ^ GJ Bullen, R. Mason & P. Pauling (1961). «Октаэдрическая координация никеля в никеле (II) бисацетилацетон». Природа . 189 (4761): 291–292. doi : 10.1038/189291a0 . S2CID 37394858 .
- ^ Jump up to: а беременный GJ Bullen, R. Mason & P. Pauling. (1965). «Кристаллическая и молекулярная структура бис (ацетилацетонато) никеля (II)». Неорганическая химия . 4 (4): 456–462. doi : 10.1021/ic50026a005 .
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2 -е изд.). Баттерворт-Хейнеманн . п. 1157. ISBN 978-0-08-037941-8 .
- ^ 1. A. Döhring, R. Goddard, PW Jolly, C. Krüger, VR Polyakov, «Мономер-тример изомеризм в трехзамещенных пентане-2,4-дионевых производных никеля (II)», Inorg. Химия 1997, 36, 177–183. два : 10.1021/ic960441c
- ^ М. Овощи-Э-Захан, y. «Идентификация цис/транспортеров бис (ацетилацетононато) комплексов (II) в растворе на основе электронных спектров» Inorica Chimica Acta 363 : 168–1 Doi : 10.1016/ j.ica.2009.09.0
- ^ BN Figgis; Ма Хичман (2000). «Теория поля лиганда и ее применение».
{{cite journal}}: CITE Journal требует|journal=( помощь ) - ^ O. Metin, Lt Yildirim & S. Ozkar (2007). «Синтез, характеристика и кристаллическая структура бис (ацетилацетонато) dimethanolnickel (II)». Неорганическая химия . 10 (9): 1121–1123. doi : 10.1016/j.inoche.2007.06.011 .
- ^ Jump up to: а беременный Wielandt, JW; Ruckerbauer, D. (2010). Бис (1,5-циклоктадиен) никель (0) . Неорганические синтезы. Тол. 35. с. 120. DOI : 10.1002/9780470651568.CH6 .
- ^ Jump up to: а беременный Пол А. Уильямс; Энтони С. Джонс; Джейми Ф. Бикли; Александр Штайнер; Хайвел О. Дэвис; Тимоти Дж. Лидхэм; Сьюзен А. Импи; Джоан Гарсия; Стивен Аллен; Алин Ружье ; Александра Блайр (2001). «Синтез и кристаллические структуры диметиламиноэтанол аддуктов ацетата ацетата Ni (II) ацетилацетоната Ni (II (II) Ni (II (II). Предшественники для осаждения золь -геля тонких пленок из оксида никеля». Журнал материалов Химия . 11 (9): 2329–2334. doi : 10.1039/b103288g .
- ^ Jump up to: а беременный Касчуб, Уилфрид; Пёршке, Клаус Р.; Уилке, Гюнтер (1988). "Tmeda-Nickel-Komplexe". Журнал органометаллической химии . 355 (1–3): 525–532. doi : 10.1016/0022-328x (88) 89050-8 .
- ^ Göttker-Schnemann, Inigo; Мик, Стефа (2020). синтез (tmeda) ni (ch 3 ) " Практический , iStopyly Labeed (tmeda) Ni 13 Ch 3 ) 2 , и нейтральные хелат-никелевые метильные комплексы ». Органометаллические . 39 (18): 3433–3440. DOI : 10.1021/acs.organomet.0C00500 . S2CID 224930545 .
- ^ Shresta, Ruja; Дорн, Стефани С.М.; Вейкс, Даниэль Дж. (2013-01-16). «Катализируемое никель-восстановительное сопряжение в энонах через промежуточные продукты Allylnickel» . Журнал Американского химического общества . 135 (2): 751–762. doi : 10.1021/ja309176h . PMC 3547151 . PMID 23270480 .