Йодат кальция
Эта статья в значительной степени или полностью опирается на один источник . ( ноябрь 2023 г. ) |
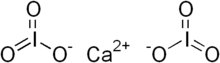 | |
| Имена | |
|---|---|
| Название ИЮПАК Дииодат кальция | |
| Другие имена Лаутарит | |
| Идентификаторы | |
| |
3D model ( JSmol ) | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.029.265 |
| Номер ЕС |
|
| номер Е | E916 (глянцеватели, ...) |
ПабХим CID | |
| НЕКОТОРЫЙ |
|
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| Са(IO 3 ) 2 | |
| Молярная масса | 389,88 г/моль (безводный) 407,90 г/моль (моногидрат) |
| Появление | белое твердое вещество |
| Плотность | 4,519 г/см 3 (моногидрат) |
| Температура плавления | 540 ° C (1004 ° F, 813 К) (моногидрат) |
| Точка кипения | разлагается |
| 0,09 г/100 мл (0 °С) 0,24 г/100 мл (20 °С) 0,67 г/100 мл (90 °С) | |
Произведение растворимости ( K sp ) | 6.47 × 10 −6 |
| Растворимость | растворим в азотной кислоте нерастворим в спирте |
| -101.4·10 −6 см 3 /моль | |
| Структура | |
| моноклинный (безводный) кубический (моногидрат) орторомбический (гексагидрат) | |
| Опасности | |
| точка возгорания | негорючий |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Йодат кальция представляет собой любое из двух неорганических соединений с формулой Ca(IO 3 ) 2 (H 2 O) x , где x = 0 или 1. Оба представляют собой бесцветные соли, которые встречаются в виде минералов лаутарита и бруггенита соответственно. Третья минеральная форма йодата кальция — дицеит , соль, содержащая хромат формулы Ca 2 (IO 3 ) 2 CrO 4 . [1] Эти минералы являются наиболее распространенными соединениями, содержащими йодат .
Производство и использование
[ редактировать ]Лаутарит, называемый наиболее важным минеральным источником йода, добывается в пустыне Атакама . [1] Переработка руды включает восстановление ее водных вытяжек бисульфитом натрия с получением йодида натрия . Эта реакция сопропорционирования является основным источником йодида натрия. [1]
Йодат кальция можно получить анодным окислением йодида кальция или пропусканием хлора в горячий раствор извести, в котором йод растворен .
Йодат кальция используется в качестве йодной добавки в корм для кур . [1] Дигидройодид этилендиамина (EDDI) является более типичным источником пищевого йода .
Ссылки
[ редактировать ]- ^ Jump up to: а б с д Лидей, Филлис А.; Кайхо, Тацуо (2015). «Йод и соединения йода». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. стр. 1–13. дои : 10.1002/14356007.a14_381.pub2 . ISBN 978-3527306732 .