Трикальцийфосфат
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Фосфат кальция | |
| Другие имена трехосновный фосфат кальция, трикальций бис(фосфат) | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ЧЭБИ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.028.946 |
| Номер ЕС |
|
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| Са 3 (РО 4 ) 2 | |
| Молярная масса | 310.18 g/mol |
| Появление | Белый аморфный порошок |
| Плотность | 3,14 г/см 3 [1] |
| Температура плавления | 1670 ° C (3040 ° F; 1940 К) [1] |
| 1,2 мг/кг [1] | |
Произведение растворимости ( K sp ) | 2.07 × 10 −33 [2] |
| Термохимия | |
Стандартная энтальпия образование (Δ f H ⦵ 298 ) | −4126 кДж/моль (α-форма) [3] |
| Фармакология | |
| A12AA01 ( ВОЗ ) | |
| Опасности | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | Невоспламеняющийся |
| Родственные соединения | |
Другие анионы | Пирофосфат кальция |
Другие катионы | Тримагнийфосфат Тринатрийфосфат Трикалийфосфат |
Родственные соединения | Монокальцийфосфат Дикальцийфосфат |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
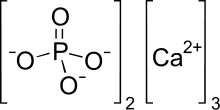
Трикальцийфосфат (иногда сокращенно TCP ), более известный как фосфат кальция , представляет собой кальциевую соль фосфорной кислоты с химической формулой Ca 3 (PO 4 ) 2 . Он также известен как трехосновный фосфат кальция и костный фосфат извести ( BPL ). Это белое твердое вещество с низкой растворимостью. Большинство коммерческих образцов «трикальцийфосфата» на самом деле представляют собой гидроксиапатит . [4] [5]
Он существует в виде трех кристаллических полиморфов α, α’ и β. Состояния α и α’ стабильны при высоких температурах.
Номенклатура
[ редактировать ]Фосфат кальция относится к многочисленным материалам, состоящим из ионов кальция (Ca 2+ ) вместе с ортофосфатами ( PO 3−
4 ), метафосфаты или пирофосфаты ( P
22О 4−
7 ) и иногда оксидные и гидроксид- ионы. В частности, обычный минерал апатит имеет формулу Ca 5 (PO 4 ) 3 X , где X представляет собой F , Cl , OH или смесь; это гидроксиапатит , если дополнительный ион представляет собой главным образом гидроксид. Большая часть «трикальцийфосфата», представленного на рынке, на самом деле представляет собой порошкообразный гидроксиапатит . [5]
Подготовка
[ редактировать ]Трикальцийфосфат получают в промышленных масштабах путем обработки гидроксиапатита фосфорной кислотой и гашеной известью . [4]
Его нельзя осаждать непосредственно из водного раствора. Обычно используются реакции двойного разложения с участием растворимого фосфата и солей кальция, например (NH 4 ) 2 HPO 4 + Ca(NO 3 ) 2 . [6] проводится в тщательно контролируемых условиях pH. Осадок будет представлять собой либо «аморфный трикальцийфосфат», ATCP, либо гидроксиапатит с дефицитом кальция, CDHA, Ca 9 (HPO 4 )(PO 4 ) 5 (OH) (обратите внимание, что CDHA иногда называют апатитовым трифосфатом кальция). [6] [7] [8] Кристаллический трикальцийфосфат можно получить прокаливанием осадка. Обычно образуется β-Ca 3 (PO 4 ) 2 требуются более высокие температуры , для образования α-Ca 3 (PO 4 ) 2 .
Альтернативой влажной процедуре является нагревание смеси пирофосфата кальция и карбоната кальция: [7]
- CaCO 3 + Ca 2 P 2 O 7 → Ca 3 (PO 4 ) 2 + CO 2
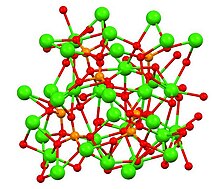
Структура β-, α- и α'-Ca 3 (PO 4 ) 2 полиморфов
[ редактировать ]Трикальцийфосфат имеет три признанных полиморфа: ромбоэдрическую β-форму (показана выше) и две высокотемпературные формы: моноклинную α и гексагональную α'. β-трикальцийфосфат имеет кристаллографическую плотность 3,066 г/см. −3 в то время как высокотемпературные формы менее плотны, α-трикальцийфосфат имеет плотность 2,866 г · см. −3 а α'-трикальцийфосфат имеет плотность 2,702 г/см. −3 Все формы имеют сложную структуру, состоящую из тетраэдрических фосфатных центров, связанных через кислород с ионами кальция. [9] Каждая из высокотемпературных форм имеет два типа колонок: одна содержит только ионы кальция, а другая - и кальций, и фосфат. [10]
Между β- и α-формами существуют различия в химических и биологических свойствах, α-форма более растворима и биоразлагаема. Обе формы коммерчески доступны и присутствуют в составах, используемых в медицине и стоматологии. [10]
возникновение
[ редактировать ]Фосфат кальция — один из основных сгорания продуктов костей (см. Костная зола ). Фосфат кальция также обычно получают из неорганических источников, таких как минеральная порода. [11] Трикальцийфосфат встречается в природе в нескольких формах, в том числе:
- в виде камня в Марокко , Израиле , Филиппинах , Египте и Кольском полуострове ( Россия ) и в меньших количествах в некоторых других странах. Природная форма не является полностью чистой, и есть некоторые другие компоненты, такие как песок и известь, которые могут изменить состав. Содержание P 2 O 5 в большинстве кальциево-фосфатных пород составляет от 30 до 40% P 2 O 5 по массе.
- в скелетах и зубах позвоночных животных
- в молоке .
Двухфазный фосфат кальция, BCP
[ редактировать ]Двухфазный фосфат кальция, BCP, первоначально сообщалось как трикальцийфосфат, но методы рентгеновской дифракции показали, что материал представляет собой смесь двух фаз: гидроксиапатита (НА) и β-трикальцийфосфата. [12] Это керамика. [13] Приготовление включает спекание , вызывающее необратимое разложение апатитов с дефицитом кальция. [7] альтернативно называемые нестехиометрическими апатитами или основным фосфатом кальция. [14] Пример: [15]
- Ca 10− δ (PO 4 ) 6− δ (HPO 4 ) δ (OH) 2− δ → (1− δ ) Ca 10 (PO 4 ) 6 (OH) 2 + 3 δ Ca 3 (PO 4 ) 2
β-ТКФ может содержать примеси, например пирофосфат кальция, Ca 2 P 2 O 7 и апатит. β-TCP биорезорбируем. Биодеградация BCP включает более быстрое растворение фазы β-TCP с последующим удалением кристаллов HA. β-TCP не растворяется в жидкостях организма при физиологическом уровне pH, для растворения необходима активность клеток, обеспечивающая кислый pH. [7]
Использование
[ редактировать ]Пищевая добавка
[ редактировать ]Трикальцийфосфат используется в порошкообразных специях в качестве средства, препятствующего слеживанию , например, для предотвращения слеживания поваренной соли. Фосфатам кальция присвоен европейский пищевой добавки номер E341 .
Товары для здоровья и красоты
[ редактировать ]Он также содержится в детской присыпке , антацидах и зубной пасте . [4] Зубные пасты с функционализированным β-трикальцийфосфатом (fTCP) могут помочь реминерализовать зубную эмаль . [16] [17] [18]
Биомедицинский
[ редактировать ]Он также используется в качестве пищевой добавки. [19] и встречается в природе в коровьем молоке , [ нужна ссылка ] хотя наиболее распространенными и экономичными формами добавок являются карбонат кальция (который следует принимать во время еды) и цитрат кальция (который можно принимать без еды). [20] Ведутся споры о разной биодоступности разных солей кальция.
Его можно использовать в качестве заменителя ткани для устранения костных дефектов, когда аутогенный костный трансплантат невозможен или невозможен. [21] [22] [23] Его можно использовать отдельно или в сочетании с биоразлагаемым , рассасывающимся полимером , таким как полигликолевая кислота . [24] Его также можно комбинировать с аутологичными материалами для костного трансплантата. [25] [26]
Пористые каркасы из β-трикальцийфосфата используются в качестве систем-носителей лекарств для местной доставки лекарств в кости. [27]
Естественное явление
[ редактировать ]Туит , природный аналог трикальцийортофосфата(V), является редким компонентом некоторых метеоритов. Его образование связано с ударным метаморфизмом. [28]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с Хейнс, Уильям М., изд. (2016). Справочник CRC по химии и физике (97-е изд.). Бока-Ратон, Флорида: CRC Press . п. 4.54. ISBN 9781498754293 .
- ^ Джон Рамбл (18 июня 2018 г.). Справочник CRC по химии и физике (99 изд.). ЦРК Пресс. стр. 5–188. ISBN 978-1-138-56163-2 .
- ^ Зумдал, Стивен С. (2009). Химические принципы 6-е изд . Компания Хоутон Миффлин. п. А21. ISBN 978-0-618-94690-7 .
- ^ Перейти обратно: а б с Клаус Шредер; Герхард Беттерманн; Томас Стаффель; Фридрих Валь; Томас Кляйн; Томас Хофманн (2012). «Фосфорная кислота и фосфаты». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a19_465.pub3 . ISBN 978-3527306732 .
- ^ Перейти обратно: а б Эль Муссауи, Юсеф; Террисс, Элен; Квиллард, Софи; Роперс, Мари-Элен; Гумберт, Бернар (январь 2023 г.). «Истинная природа трикальцийфосфата, используемого в качестве пищевой добавки (E341(iii))» . Наноматериалы . 13 (12): 1823. дои : 10.3390/nano13121823 . ISSN 2079-4991 . ПМЦ 10303396 . ПМИД 37368253 .
- ^ Перейти обратно: а б Дестейнвилл, А.; Чемпион, Э.; Бернаш-Ассоллан, Д.; Лаборд, Э. (2003). «Синтез, характеристика и термическое поведение апатитового трикальцийфосфата». Химия и физика материалов . 80 (1): 269–277. дои : 10.1016/S0254-0584(02)00466-2 .
- ^ Перейти обратно: а б с д Рей, К.; Комбс, К.; Друэ, К.; Гроссин, Д. (2011). «1.111 – Биоактивная керамика: физическая химия». В Дюшейне, Пол (ред.). Комплексные биоматериалы . Том. 1. Эльзевир. стр. 187–281. дои : 10.1016/B978-0-08-055294-1.00178-1 . ISBN 978-0-08-055294-1 .
- ^ Дорожкин, Сергей В. (декабрь 2012 г.). «Аморфные (орто)фосфаты кальция». Акта Биоматериалы . 6 (12): 4457–4475. doi : 10.1016/j.actbio.2010.06.031 . ПМИД 20609395 .
- ^ Яшима, М.; Сакаи, А.; Камияма, Т.; Хошикава, А. (2003). «Анализ кристаллической структуры β-трикальцийфосфата Ca 3 (PO 4 ) 2 методом нейтронной порошковой дифракции». РНКл химии твердого тела . 175 (2): 272–277. Бибкод : 2003JSSCh.175..272Y . дои : 10.1016/S0022-4596(03)00279-2 .
- ^ Перейти обратно: а б Карродегуас, Р.Г.; Де Аза, С. (2011). «А-трикальцийфосфат: синтез, свойства и биомедицинское применение». Акта Биоматериалы . 7 (10): 3536–3546. doi : 10.1016/j.actbio.2011.06.019 . ПМИД 21712105 .
- ^ Якубу, Жанна, MS. Путеводитель по пищевым ингредиентам журнала Vegetarian Journal «Путеводитель по пищевым ингредиентам». Вегетарианская ресурсная группа и Интернет. 14 сентября 2012 г.
- ^ Дакулси, Г.; Легерос, Р. (2008). «17 – Двухфазная керамика трикальцийфосфат/гидроксиапатит». В Кокубо, Тадаши (ред.). Биокерамика и ее клиническое применение . Издательство Вудхед. стр. 395–423. дои : 10.1533/9781845694227.2.395 . ISBN 978-1-84569-204-9 .
- ^ Салинас, Антонио Дж.; Валлет-Реги, Мария (2013). «Биоактивная керамика: от костных трансплантатов до тканевой инженерии». РСК Прогресс . 3 (28): 11116–11131. Бибкод : 2013RSCAd...311116S . дои : 10.1039/C3RA00166K .
- ^ Эллиотт, Дж. К. (1994). «3 – Гидроксиапатит и нестехиометрические апатиты». Исследования по неорганической химии . Том. 18. Эльзевир. стр. 111–189. дои : 10.1016/B978-0-444-81582-8.50008-0 . ISBN 978-0-444-81582-8 .
- ^ Валлет-Реги, М.; Родригес-Лоренцо, LM (ноябрь 1997 г.). «Синтез и характеристика апатита с дефицитом кальция». Ионика твердого тела . 101–103, Часть 2: 1279–1285. дои : 10.1016/S0167-2738(97)00213-0 .
- ^ Хамба Х., Накамура К., Никайдо Т., Тагами Дж., Мурамацу Т. (октябрь 2020 г.). «Реминерализация подповерхностных поражений эмали с использованием зубной пасты, содержащей трикальцийфосфат и фторид: микроКТ-анализ in vitro» . BMC Здоровье полости рта . 20 (1): 292. дои : 10.1186/s12903-020-01286-1 . ПМК 7590595 . ПМИД 33109184 .
- ^ Мейер Ф., Амаечи Б.Т., Фабрициус Х.О., Энакс Дж. (2018). «Обзор фосфатов кальция, используемых в биомиметическом уходе за полостью рта» . Открытый стоматологический журнал . 12 : 406–423. дои : 10.2174/1874210601812010406 . ПМЦ 5997847 . ПМИД 29988215 .
- ^ Лаймбэк Х., Энакс Дж., Мейер Ф. (июль 2023 г.). «Улучшение здоровья полости рта с помощью биомиметических зубных паст на основе фосфата кальция, не содержащих фтор: обновленные клинические данные» . Биомиметика . 8 (4): 331. doi : 10.3390/biomimetics8040331 . ПМЦ 10452078 . ПМИД 37622936 .
- ^ Бонжур Дж.П., Кэрри А.Л., Феррари С., Клавиен Х., Слосман Д., Тейнц Дж., Риццоли Р. (март 1997 г.). «Продукты, обогащенные кальцием, и рост костной массы у девочек препубертатного возраста: рандомизированное двойное слепое плацебо-контролируемое исследование» . Дж. Клин. Инвестируйте. 99 (6): 1287–1294. дои : 10.1172/JCI119287 . ПМК 507944 . ПМИД 9077538 .
- ^ Штрауб Д.А. (июнь 2007 г.). «Добавки кальция в клинической практике: обзор форм, доз и показаний». Нутр Клин Практика . 22 (3): 286–296. дои : 10.1177/0115426507022003286 . ПМИД 17507729 .
- ^ Падерни С., Терзи С., Амендола Л. (сентябрь 2009 г.). «Лечение крупных костных дефектов остеокондуктивным костным заменителем». Скелетно-мышечная хирургия . 93 (2): 89–96. дои : 10.1007/s12306-009-0028-0 . ПМИД 19711008 . S2CID 33413039 .
- ^ Мур, округ Колумбия, Чепмен М.В., Манске Д. (1987). «Оценка двухфазной керамики на основе фосфата кальция для использования при пластике диафизарных дефектов длинных костей». Журнал ортопедических исследований . 5 (3): 356–365. дои : 10.1002/jor.1100050307 . ПМИД 3040949 . S2CID 41579389 .
- ^ Ланге Т.А., Зервех Дж.Э., Пик Р.Д., Муни В., Харрисон Б.Х. (1986). «Гранулированный трикальцийфосфат при крупных губчатых дефектах». Анналы клинической и лабораторной науки . 16 (6): 467–472. ПМИД 3541772 .
- ^ Цао Х, Кубояма Н (сентябрь 2009 г.). «Биоразлагаемый пористый композитный каркас из PGA/β-TCP для инженерии костной ткани». Кость . 46 (2): 386–395. дои : 10.1016/j.bone.2009.09.031 . ПМИД 19800045 .
- ^ Эрбе Э.М., Маркс Дж.Г., Клинефф Т.Д., Беллинкампи Л.Д. (октябрь 2001 г.). «Потенциал ультрапористого синтетического губчатого заполнителя костных пустот β-трикальцийфосфата и композитного трансплантата из аспирата костного мозга» . Европейский журнал позвоночника . 10 (Приложение 2): S141–S146. дои : 10.1007/s005860100287 . ПМЦ 3611552 . ПМИД 11716011 .
- ^ Бансал С., Чаухан В., Шарма С., Махешвари Р., Джуял А., Рагуванши С. (июль 2009 г.). «Оценка гидроксиапатита и бета-трикальцийфосфата, смешанного с аспиратом костного мозга, в качестве заменителя костного трансплантата при заднелатеральном спондилодезе» . Индийский журнал ортопедии . 43 (3): 234–239. doi : 10.4103/0019-5413.49387 (неактивен 24 апреля 2024 г.). ПМЦ 2762171 . ПМИД 19838344 .
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на апрель 2024 г. ( ссылка ) - ^ Кунду, Б; Лемос А; Саундрапандиан C; Сен PS; Датта С; Феррейра JMF; Басу Д (2010). «Разработка пористых каркасов HAp и β-TCP путем консолидации крахмала методом вспенивания и системы доставки лекарств на основе двухслойного каркаса из лекарственного средства и хитозана». Дж. Матер. наук. Матер. Мед . 21 (11): 2955–2969. дои : 10.1007/s10856-010-4127-0 . ПМИД 20644982 . S2CID 6483779 .
- ^ Твит Mindat.org
