Хромат кальция
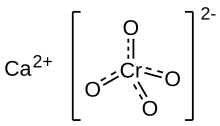 Безводный хромат кальция | |
 Пигмент хромат кальция | |
| Имена | |
|---|---|
| Название ИЮПАК Хромат кальция | |
| Другие имена Хромат кальция (VI) Монохромат кальция Кальций Хром Желтый CI Пигмент Желтый 33 Ну давай же Желтый Ультрамарин | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.033.955 |
| Номер ЕС |
|
ПабХим CID | |
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| КаКрО 4 | |
| Молярная масса | 156.072 g/mol |
| Появление | ярко-желтый порошок |
| Плотность | 3,12 г/см 3 |
| Температура плавления | 2710 ° C (4910 ° F; 2980 К) |
| безводный 4,5 г/100 мл (0 °С) 2,25 г/100 мл (20 °С) дигидрат 16,3 г/100 мл (20 °С) 18,2 г/100 мл (40 °С) | |
| Растворимость | растворим в кислоте практически нерастворим в спирте |
| Структура | |
| моноклинический | |
| Родственные соединения | |
Другие анионы | Дихромат кальция |
Другие катионы | Хромат бериллия Хромат магния Хромат стронция Хромат бария Хромат радия |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности | высокотоксичный, канцероген, мутаген |
| NFPA 704 (огненный алмаз) | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Хромат кальция неорганическое соединение с формулой CaCrO 4 , т.е. хроматная – соль кальция . Это ярко-желтое твердое вещество, которое обычно встречается в виде дигидрата CaCrO 4 ·2H 2 O. В природе существует очень редкая безводная минеральная форма, известная как хроматит . [1]
Это соединение иногда используется в качестве пигмента, но это использование ограничено из-за очень токсичной и канцерогенной природы соединений шестивалентного хрома, таких как соли хромата.
Синтез и реакции
[ редактировать ]Хромат кальция образуется в результате реакции солевого обмена и хромата натрия хлорида кальция :
- Na 2 CrO 4 + CaCl 2 → CaCrO 4 + 2 NaCl
В водном растворе получается дигидрат, который теряет воду с образованием ангидрата при 200 °C. [ нужна ссылка ]
Это окислитель , окисляющий органические соединения ( например, спирты) или восстановители ( например, металлы) до соответствующих карбонильных соединений или оксидов металлов , в то время как центр хрома (VI) в CaCrO 4 восстанавливается до хрома (III) .
Твердый хромат кальция вступает в реакцию с гидразином взрывоопасно . Он также будет сильно гореть, если его смешать с бором и воспламенить, создавая тем самым опасность пожара. [2]
Использование
[ редактировать ]Соединение иногда используется в качестве желтого неорганического пигмента или ингибитора коррозии в рамках процедуры нанесения хроматного конверсионного покрытия . [ нужна ссылка ]
Он также использовался при гальванике хрома , в фотохимической обработке и при переработке промышленных отходов . [ нужна ссылка ]
Все виды применения страдают от высокой токсичности видов хрома (VI) для человека: хроматы внесены в список IARC группы 1, канцерогенов а также очень агрессивны ( например, способны вызвать необратимое повреждение глаз) и генотоксичны . [3] [4]
Ссылки
[ редактировать ]- ^ "Дом" . Mindat.org .
- ^ Руководство по безопасности и гигиене труда для хромата кальция. Архивировано 8 августа 2007 г., в Wayback Machine.
- ^ МАИР (2012) [17-24 марта 2009 г.]. Том 100C: Мышьяк, металлы, волокна и пыль (PDF) . Лион: Международное агентство по исследованию рака. ISBN 978-92-832-0135-9 . Архивировано из оригинала (PDF) 17 марта 2020 г. Проверено 5 января 2020 г.
Имеется достаточно доказательств канцерогенности соединений хрома (VI) для человека. Соединения хрома (VI) вызывают рак легких. Также наблюдалась положительная связь между воздействием соединений хрома (VI) и раком носа и носовых пазух. Имеются достаточные доказательства канцерогенности соединений хрома (VI) на экспериментальных животных. Соединения хрома (VI) канцерогенны для человека (группа 1) .
- ^ «Хромат кальция 10827-В» . ntp.niehs.nih.gov . Национальная программа токсикологии (Министерство здравоохранения и социальных служб США) . Проверено 30 марта 2021 г.
