Бабезия
В этой статье есть несколько проблем. Пожалуйста, помогите улучшить его или обсудите эти проблемы на странице обсуждения . ( Узнайте, как и когда удалять эти шаблонные сообщения )
|
| Бабезия | |
|---|---|
 | |
| Мазок крови Babesia microti | |
| Научная классификация | |
| Домен: | Эукариоты |
| Клэйд : | потогонные средства |
| Клэйд : | САР |
| Клэйд : | Альвеолата |
| Тип: | Апикомплекса |
| Сорт: | Аконоидасида |
| Заказ: | Пироплазмида |
| Семья: | Бабезииды |
| Род: | Бабезия Старковичи, 1893 г. |
| Разновидность | |
Группа B. microti («Археопироплазмиды»): [1] [2] Группа западных США («Прототейлериды»): | |
Бабезия , [3] [4] также называется Нутталия , [5] Апикомплексный паразит , поражающий эритроциты и передающийся клещами . Первоначально обнаруженный румынским бактериологом Виктором Бабешем более 100 видов бабезий . в 1888 году, с тех пор было идентифицировано [6] [7]
Бабезии включают более 100 видов клещевых паразитов, которые поражают эритроциты (эритроциты) у многих позвоночных-хозяев. [8]
Виды Babesia поражают домашний скот во всем мире, диких и домашних позвоночных животных, а иногда и человека, вызывая заболевание бабезиоз . [9] [7] В Соединенных Штатах B. microti является наиболее распространенным штаммом из немногих, которые, как документально подтверждено, вызывают заболевания у людей.
Классификация
[ редактировать ]| Филогения пироплазмид (мтДНК) [2] |

Бабезия — простейший паразит, поражающий позвоночных животных, в основном сельскохозяйственных млекопитающих и птиц, но иногда и людей. Распространенными названиями болезней, вызываемых Babesia microti, являются техасская лихорадка крупного рогатого скота, красноводная лихорадка, клещевая лихорадка и лихорадка Нантакета. [7] Заболевание, которое он вызывает у человека, бабезиоз, также называют пироплазмозом. [9]
Однако Babesia microti не относится к роду Babesia . Из-за исторических ошибочных классификаций простейшим дали множество названий, в том числе Нутталлия, [5] и был переименован из Babesia microti в Theileria microti на основании данных 2006 года. Его генетическая последовательность , опубликованная в 2012 году, показывает, что этот вид не принадлежит ни к Babesia , ни к Theileria, а к отдельному роду. [10] Другая «западная» группа также отделена от ядра Babesia . [2]
Для птичьих видов Babesia характерны кольцевидная и амебоидная формы, а также веерообразные или крестообразные (крестообразные) тетрадные шизонты . Сообщалось о развитии паразитов только в эритроцитах. [11]
История
[ редактировать ]На протяжении веков было известно, что эта болезнь животных является серьезной болезнью диких и домашних животных, особенно крупного рогатого скота. В 1888 году Виктор Бабеш впервые идентифицировал возбудителя в Румынии и предположил, что он вызван бактерией, которую он назвал Haematococcus bovis . Он задокументировал болезнь, описав признаки тяжелой гемолитической болезни, наблюдаемой исключительно у крупного рогатого скота и овец. [7] [12]
В 1893 году американцы Теобальд Смит и Фред Килборн определили, что паразит является причиной техасской лихорадки крупного рогатого скота, той же болезни, которую описал Бабеш. Они также идентифицировали клеща как агента-переносчика, и это открытие впервые представило концепцию членистоногих, функционирующих как переносчики болезней . [13]
Считалось, что это заболевание поражает только млекопитающих, но в 1957 году первый случай бабезиоза был обнаружен у человека. [9] Человеку была сделана спленэктомия , как и всем людям с диагнозом бабезиоз до 1969 года, когда первый случай бабезиоза был диагностирован у человека, у которого еще была селезенка . Это доказало, что паразит является потенциальным патогеном для любого человека. [14]
Генетика
[ редактировать ]Бабезии демонстрируют специфичность хозяина , что позволяет появиться множеству различных подвидов бабезий , каждый из которых заражает разные виды позвоночных организмов. [15] Хотя B. bovis и Babesia bigemina предпочитают заражать крупный рогатый скот в тропических условиях, они могут заразить и других животных, таких как белохвостый олень . [15] Таким образом, хотя организм обладает способностью проявлять специфичность хозяина и, таким образом, повышать эффективность передачи, он все же может заражать различных хозяев. [15] Это достигается за счет мутаций и естественного отбора. В разных средах у отдельных простейших могут возникать мутации, которые, повышая приспособленность простейших , позволяют популяции увеличивать их численность. Эта особенность объясняет, почему у бабезий такое большое генетическое разнообразие. [15]
Бабезия эгоистично долгосрочно сохраняется в организме хозяина: хозяин не получает никакой выгоды от вторжения паразита и только страдает. Это позволяет паразиту использовать все ресурсы, предлагаемые хостом, увеличивать их количество и скорость передачи. [15] Слишком смертельная инфекция приводит к гибели хозяина, и паразит не может распространяться, что является потерей с эволюционной точки зрения. [15] Различные виды бабезий способны противостоять стрессу иммунной системы хозяина. Инфекция обычно стимулирует врожденную иммунную систему , а не гуморальную иммунную систему . [15] Это приводит к контролю над инфекцией, но также к сохранению, а не к уничтожению паразита. [15]
Геномика
[ редактировать ]Геном B. microti был секвенирован и показывает, что этот вид принадлежит не к Babesia или Theileria, а к отдельному роду. [10] По состоянию на 2013 год [update], известно, что митохондриальный геном является линейным, как и другие секвенированные митохондриальные геномы Apicomplexa , хотя первоначально сообщалось, что он имеет кольцевую форму. [16]
Частичное секвенирование РНК собак пироплазм выявило ряд дополнительных видов. [ нужна ссылка ]
Жизненный цикл
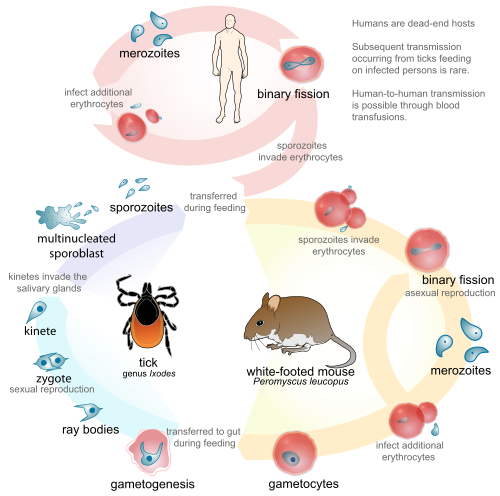
[ редактировать ]Жизненный цикл B. microti , типичный для паразитов этого рода, требует биологической стадии у хозяина -грызуна или оленя . Между этими хозяевами он передается клещами семейства Ixodidae . Начнем с того, что клещ как окончательный хозяин заражается сам, поскольку он поглощает гаметоциты , прикрепляясь к ним для питания кровью. Он также заносит бабезий промежуточному хозяину (например, крупному рогатому скоту) при приеме пищи с кровью. Когда бабезии (эритроциты) животных проникают в красные кровяные тельца , их называют спорозоитами . Внутри эритроцитов простейшие становятся циклическими и развиваются в трофозоитное кольцо. Трофозоиты линяют в мерозоиты , которые имеют тетрадную структуру, называемую формой мальтийского креста . [17] Рост трофозоитов и мерозоитов приводит к разрыву эритроцита хозяина, что приводит к высвобождению вермикул — инфекционных паразитических тел, которые быстро распространяют простейших по крови. [9] Вместо того, чтобы производить все больше и больше трофозоитов, некоторые мерозоиты производят гаметоциты . Гаметы в оплодотворяются спорозоиты в кишечнике клеща и развиваются в . слюнных железах Это спорозоиты, которые инфицированный клещ заносит при укусе промежуточного хозяина. Даже в качестве случайного хозяина фазовые изменения, происходящие у паразита, у человека такие же, как и у биологических хозяев. Бабезия может быть диагностирована на стадии трофозоита, а также может передаваться от человека к человеку через клещевого переносчика, при переливании крови или врожденным путем (инфицированная мать своему ребенку). [18] [6]
Сезонность
[ редактировать ]Температура
[ редактировать ]Холодная погода полностью прерывает передачу. [19] Было обнаружено, что появление клещевых заболеваний совпало с изменением климата. [20] Корреляция между изменением климата и заболеваемостью клещевыми заболеваниями не является достаточно сильной, чтобы считаться основным фактором. [20]
Влажность
[ редактировать ]Высокая влажность и осадки способствуют распространению клещей-переносчиков бабезий . [21] Это может объяснить заражения крупного рогатого скота B. bigemina в холмистом районе Мегхалая . рост [21] Продолжительность жизни и количество поколений Babesia microplus коррелируют с увеличением продолжительности жизни личинок и числа годовых поколений. [21] Теплая и сухая погода препятствует жизненному циклу бабезий внутри клеща. [19] Теплая и влажная погода увеличивает интенсивность заражения — популяция может процветать благодаря относительно жидкой среде, делающей воду и питательные вещества более доступными. [19]
Передача инфекции
[ редактировать ]Виды Babesia передаются через слюну клеща при его укусе. Уже на стадии нимфы клещ вгрызается в кожу для питания кровью. Клещ, если его не удалить, остается прикрепленным в течение трех-четырех дней, причем более длительные периоды кормления связаны с более высокой вероятностью заражения паразитом. Паразит может выжить в клеще, пока он линяет на различных стадиях развития, в результате чего все стадии клеща становятся потенциально заразными. Некоторые виды бабезий могут передаваться от самки клеща своему потомству перед миграцией в слюнные железы для питания. [9] B. microti , наиболее распространенный вид у людей, не имеет трансовариальной передачи . [6]
К клещам домашних животных , которые переносят бабезий и вызывают множество заболеваний, относятся очень широко распространенные клещи крупного рогатого скота Rhipicephalus (Boophilus) microplus и R.(B.) decoloratus . Эти клещи имеют строгий цикл кормления крупного рогатого скота одним хозяином, поэтому бабезии могут передаваться только трансовариальным путем.
В Америке Ixodes scapularis является наиболее распространенным переносчиком. Этот твердый клещ, широко известный как оленьий клещ, также является переносчиком других заболеваний, связанных с клещами, таких как болезнь Лайма . Многие виды бабезий заражают только хозяев-млекопитающих, кроме человека, чаще всего крупный рогатый скот, лошадей и овец. B. microti и B. divergens являются двумя основными патогенными видами для человека. Их резервуарами предположительно являются белоногая мышь ( Peromyscus leucopus ), полевки из Microtus рода и белохвостый олень ( Odocoileus Virginianus ). [22] Эти лесные виды являются предполагаемыми резервуарами, поскольку, хотя известно, что они являются переносчиками болезни, полная компетентность резервуаров еще не доказана. [23]
Большинство случаев передачи инфекции между людьми связано с клещевым переносчиком. По состоянию на 2003 год Центры по контролю и профилактике заболеваний (CDC) признали более 40 случаев бабезиоза, заразившихся в результате переливания эритроцитов (PRBC), а также две инфекции, зарегистрированные при трансплантации органов. Переливания PRBC, вызывающие инфекции, были выявлены путем тестирования донорской крови на антитела B. microti . [24] Случаи передачи бабезий при переливании крови PRBC оказывают давление на правительственные организации (такие как CDC) с необходимостью ужесточить стандартные меры по проверке донорской крови . [ нужна ссылка ]
Передача возможна и врожденным путем (от инфицированной матери к ребенку). Поскольку симптомы могут не проявляться, многие женщины могут не знать, что они инфицированы во время беременности, и поэтому в настоящее время данные о скорости врожденной передачи инфекции неизвестны. [18]
В настоящее время переносчики птичьего бабезия не выявлены, но предполагается, что ими являются клещи. [11] Виды Babesia требуют компетентных хозяев-позвоночных и беспозвоночных для поддержания циклов передачи. [25]
Эпидемиология
[ редактировать ]Из видов, заражающих человека, B. microti наиболее распространен в Америке, тогда как B. divergens является преобладающим штаммом, обнаруженным в Европе. Эндемичными территориями являются регионы обитания клещей, включая лесные районы северо-востока США и регионы Европы с умеренным климатом. [26] Ixodidae, клещи-переносчики B. microti , также передают более известную Borrelia burgdorferi , возбудителя болезни Лайма. По причинам, которые остаются неясными, в районах, эндемичных как по болезни Лайма, так и по бабезиозу, передача болезни Лайма преобладает и является более преобладающей в регионе. [9] Распространенность бабезиоза в эндемичных по малярии регионах остается неизвестной из-за вероятности ошибочного диагноза малярии. [27] Поскольку заболевание приводит к большому числу бессимптомных людей, многие группы населения могут иметь высокую серологическую распространенность без особого документирования заболевания. Например, в Род-Айленде и Нантакете серологическая распространенность составила 20–25%. [9] Распространенность бабезиоза чаще всего регистрируется в период с мая по сентябрь, когда активность клещей в эндемичных регионах высока. [26]
Существует 15 видов бабезий, четыре из которых зарегистрированы у морских хозяев. Babesia poelea была описана у коричневых олушей ( Sula leucogaster ) на острове Сэнд, атолл Джонстон, центральная часть Тихого океана. [28] B. poelea была зарегистрирована от олуши в маске ( Sula dactylatra melanops ) с острова Десноефс , Амирантес , Сейшельские острова . [29] Babesia peircei наблюдалась у двух видов пингвинов: пингвина-ослика ( Sphenicus demersus ) из Южной Африки и малого пингвина ( Eduyptula major ) из южной Австралии. [30] [31] Babesia bennetti произошла от желтоногой чайки ( Larus cachinnans ) с острова Бенидорм у побережья Испании. [31] Babesia uriae была обнаружена у обыкновенных кайр в Калифорнии.
около 40 случаев бабезиоза человека, вызванного внутриэритроцитарными простейшими (простейшими внутри эритроцитов) рода Babesia . В Европе зарегистрировано [32]
Болезнь
[ редактировать ]Бабезиоз крупного рогатого скота, вызываемый B. bovis, является важным препятствием для животноводства во всем мире. [ нужна ссылка ]
У людей
[ редактировать ]Признаки заражения B. microti обычно возникают через одну-восемь недель после укуса инфекционного клеща. [26] Инфекции, вызванные B. divergens , имеют более короткий латентный период, обычно составляющий от одной до трех недель. [27] Тяжесть инфекции B. microti варьируется. В 25% случаев у взрослых и в 50% случаев у детей заболевание протекает бессимптомно или в легкой форме с гриппоподобными симптомами. В других случаях симптомы характеризуются нерегулярной лихорадкой, ознобом, головными болями, общей вялостью, болью и недомоганием . [9] эффекты размножения паразитов, такие симптомы, как гемолитическая анемия , желтуха , одышка и гемоглобинурия . В тяжелых случаях были зарегистрированы [7] [27] Люди с нормальной иммунной функцией и здоровой селезенкой часто выздоравливают без лечения. [9]
Пациенты, подвергшиеся спленэктомии, более восприимчивы к заражению этой болезнью и могут умереть в течение пяти-восьми дней после появления симптомов. [26] У них тяжелая гемолитическая анемия, и иногда гепатомегалия регистрируется . Уровни паразитемии могут достигать 85% у пациентов без селезенки по сравнению с 1–10% у людей с селезенкой и эффективной иммунной системой. [27]
Осложнения включают острую дыхательную недостаточность , застойную сердечную недостаточность и почечную недостаточность . Инфекции могут привести к летальному исходу у 5–10% госпитализированных пациентов, с повышенным риском смерти у людей с ослабленным иммунитетом , пожилых людей, а также у людей, инфицированных болезнью Лайма . [27] Инфекции B. divergens имеют гораздо более высокий уровень смертности (42%) и проявляются более тяжелыми симптомами. У инфицированных людей наблюдается гемоглобинурия, за которой следует желтуха, постоянно высокая температура, озноб и потливость. Если не лечить, инфекция B. divergens может перерасти в шокоподобные симптомы с отеком легких и почечной недостаточностью. [27]
У птиц
Патогенность в B. uriae для кайр настоящее время неизвестна. Птицы были обнаружены с поражениями , анемией и затрудненным дыханием, а также были поражены ткани птиц-хозяев. [11] Инфекции Babesia peircei могут вызывать легкую анемию, лейкоцитоз и нарушение функции печени у африканских пингвинов . [33]
Диагностические тесты
[ редактировать ]являются простейшими паразитами, наиболее эффективным способом выявления Поскольку бабезии инфекции является анализ образцов крови .
Морфология
[ редактировать ]Babesia Виды проникают в эритроциты (эритроциты) на стадии спорозоитов. Внутри эритроцитов простейшие становятся циклическими и развиваются в трофозоитное кольцо. Трофозоиты линяют в мерозоиты, которые имеют тетрадную структуру, называемую формой мальтийского креста . [17] Эта тетрадная морфология, наблюдаемая при окрашивании по Гимзе тонкого мазка крови , уникальна для бабезий и отличает ее от Plasmodium falciparum , простейшего сходной морфологии, вызывающего малярию. Рост трофозоитов и мерозоитов приводит к разрыву эритроцита хозяина, что приводит к высвобождению вермикул — инфекционных паразитических тел, которые быстро распространяют простейших по крови. [9] Важно обратить внимание на особенности морфологии бабезий в мазках крови из-за их большого сходства с малярийным паразитом Plasmodium falciparum . Это привело к тому, что многим пациентам с бабезиозом был поставлен неверный диагноз. К немногим отличительным факторам бабезий относятся простейшие различной формы и размера, способность содержать вакуоли и отсутствие выработки пигментов. Трофозоиты, появляющиеся в форме тетрады внутри эритроцита, также указывают на бабезий . [ нужна ссылка ]
Несмотря на многочисленные исследования бабезиоза и малярии, ошибочный диагноз на основании мазка крови может быть частым и проблематичным. В дополнение к мазку крови диагноз следует ставить с помощью непрямого флуоресцентного теста на антитела (НФА). ИФА-тест имеет гораздо более высокую специфичность , чем окрашенные мазки крови: антитела обнаруживаются у 88-96% инфицированных пациентов. [6] Диагностические меры посредством тестирования на антитела также особенно полезны для выявления распространенности в сыворотке крови у бессимптомных лиц. Из-за передачи бабезий при переливании крови тестирование IFA может стать эффективным средством скрининга заболевания при донорстве крови.
Исторически диагностику бабезиоза осуществляли с помощью ксенодиагностики у хомяков на B. microti и у песчанок на B. divergens . [9] От этого диагностического метода отказались в пользу более быстрых диагностических мер.
Уход
[ редактировать ]Существует несколько методов лечения бабезиоза у животных. [ нужна ссылка ]
У людей многие из них выздоравливают спонтанно, испытывая лишь легкие симптомы, не диагностированные как болезнь. Это почти всегда наблюдается при инфекциях B. microti , которые обычно более распространены в Соединенных Штатах. Исторически сложилось так B. divergens , и более тяжелых инфекций, вызванных B. microti , что стандартным лечением лиц с симптомами заболевания, вызванных , было пероральное или внутривенное введение клиндамицина с пероральным хинином . [6] Однако по результатам исследований, завершенных в 2000 году, схемы лечения все больше склоняются к пероральному приему атоваквона с пероральным азитромицином . Последние предпочтительнее, поскольку они одинаково эффективны во всех случаях, кроме самых тяжелых, и вызывают меньше побочных реакций . [34] В тяжелых случаях обменные переливания крови . для снижения паразитарной нагрузки у человека проводятся [9] Другие меры включают устранение и коррекцию аномальных клинических признаков. [7]
В исследовании морских птиц примахин использовался для демонстрации эффективности лечения инфицированных хозяев. [35] Лечение бабезиоза включало примахин (1 мг/кг перорально каждые 24 часа в течение 10 дней; фосфат примахина 1,76% масс./об. в стабилизированном растворе, Primaquin Solution, MedPet Ltd, Бенроуз , Южная Африка). После лечения следовали добавки с фосфолипидами (1 капсула на птицу перорально каждые 24 часа в течение 12 дней; обезжиренные, обогащенные фосфолипидами из соевых бобов, 300 мг/капсула, Essentiale Extreme, Sanofi Aventis Ltd, Мидранд , Южная Африка); как попытка смягчить потенциальные гепатотоксические эффекты примахина. Для предотвращения передачи бабезий и других клещевых возбудителей всех птиц с видимыми эктопаразитами при поступлении обрабатывают пестицидным порошком ( карбарил 50 г/кг), ежедневно проводят тщательную уборку помещений. [35]
Профилактика у животных
[ редактировать ]В 1906 году были предприняты усилия по искоренению клещевого переносчика бабезиоза крупного рогатого скота в Соединенных Штатах. Было зарегистрировано, что это искоренение было успешно завершено четыре десятилетия спустя. [7]
Эффективного контроля можно достичь путем вакцинации живыми аттенуированными фенотипами паразита. Вакцины имеют ряд недостатков, поэтому исследования по созданию более эффективных и безопасных вакцин все еще ведутся. [ нужна ссылка ] В последнее время [ когда? ] ряд белков паразитов, обладающих иммуногенным лет был открыт потенциалом. С помощью полимеразной цепной реакции , генетического секвенирования и биоинформатического анализа генов была обнаружена высокая степень консервативности (98–100%) среди бразильских изолятов B. bovis и изолята T2Bo . Таким образом, эти гены рассматриваются для включения в рекомбинантную коктейльную вакцину против бабезиоза крупного рогатого скота, вызываемого B. bovis . [ нужна ссылка ]
Профилактика у человека
[ редактировать ]Наиболее эффективной мерой общественного здравоохранения в отношении бабезий является предотвращение заражения клещами. Это можно сделать с помощью личной профилактики, например, избегать мест, зараженных клещами (особенно в период высокого уровня клещей с мая по сентябрь), оставаться прикрытым легкой одеждой, искать клещей после пребывания на открытом воздухе и удалять обнаруженных клещей с кожи. [27] Другие меры включают применение ДЭТА , обычного репеллента, эффективного против клещей и насекомых. (Для людей, которые отрицательно реагируют на ДЭТА, следует использовать альтернативные репелленты от насекомых.) На уровне штата, если департаменты здравоохранения особенно мотивированы, уничтожение клещей возможно. В 1906 году были предприняты усилия по искоренению клещевого переносчика бабезиоза крупного рогатого скота в Соединенных Штатах. Было зарегистрировано, что это искоренение было успешно завершено четыре десятилетия спустя. [7]
Полное искоренение посредством борьбы с переносчиками будет долгосрочным проектом, который значительно снизит распространенность как бабезиоза, так и болезни Лайма, но, поскольку департаментам общественного здравоохранения часто не хватает финансирования, более рекомендуются профилактические меры. [ нужна ссылка ]
Из-за относительно низкой распространенности заболевания у людей и наличия нескольких резервуаров бабезиоз не является кандидатом на вакцинацию. В регионах, где клещи домашних животных регулярно контролируются химическими акарицидами для снижения заболеваемости B. bovis и B. bigemina , риск заражения этими паразитами для человека будет снижен.
Ссылки
[ редактировать ]- ^ Лак Дж.Б., Райхард М.В., Ван Ден Буше Р.А. (2012). «Филогения и эволюция пироплазмид, выведенная из последовательностей 18S рРНК». Международный журнал паразитологии . 42 (4): 353–363. дои : 10.1016/j.ijpara.2012.02.005 . ПМИД 22429769 .
- ^ Перейти обратно: а б с Шрег М.Э., Марр Х.С., Тариго Дж.Л., Кон Л.А., Берд Д.М., Шолль Э.Х., Леви М.Г., Вигманн Б.М., Биркенхойер А.Дж. (2016). «Последовательности и структуры митохондриального генома помогают в разрешении филогении пироплазмид» . ПЛОС ОДИН . 11 (11): e0165702. Бибкод : 2016PLoSO..1165702S . дои : 10.1371/journal.pone.0165702 . ПМК 5104439 . ПМИД 27832128 .
- ^ Хаят А, Ратор М (2008). «Гл. 36: бабезий Виды » . В Бартон Л.Л., Вольпе Дж.Дж., Фридман Н.Р. (ред.). Неврологические проявления детских инфекционных заболеваний и синдромов иммунодефицита . Хумана Пресс. стр. 343–6. ISBN 978-1-59745-391-2 .
- ^ « Бабезия » . Браузер таксономии NCBI . 5864.
- ^ Перейти обратно: а б Ноуэлл Ф. (ноябрь 1969 г.). «Картина крови в результате инфекций Nuttallia (= Babesia) Rodhaini и Nuttallia (= Babesia) microti у крыс и мышей». Паразитология . 59 (4): 991–1004. дои : 10.1017/S0031182000070475 . ПМИД 4982449 . S2CID 43157316 .
- ^ Перейти обратно: а б с д и «DPDx: Лабораторная идентификация паразитов, вызывающих обеспокоенность общественного здравоохранения. Бабезиоз» . CDC. 05.03.2009. Архивировано из оригинала 7 марта 2013 г.
- ^ Перейти обратно: а б с д и ж г час Ристич М., Амбруаз-Томас П., Крейер Дж. П. (1984). Малярия и бабезиоз: результаты исследований и меры борьбы . Новые перспективы в клинической микробиологии. Том. 7. М. Найхофф. стр. 100–170. ISBN 978-0-89838-675-2 . OCLC 709342375 .
- ^ Спилман А., Уилсон М.Л., Левин Дж.Ф., Писман Дж. (январь 1985 г.). «Экология бабезиоза человека, передающегося иксодами даммини, и болезни Лайма». Ежегодный обзор энтомологии . 30 (1): 439–460. doi : 10.1146/annurev.en.30.010185.002255 . ISSN 0066-4170 . ПМИД 3882050 .
- ^ Перейти обратно: а б с д и ж г час я дж к л Деспомье Д.Д. (1995). Паразитарные болезни (3-е изд.). Спрингер-Верлаг. стр. 224–6. ISBN 978-0-387-94223-0 .
- ^ Перейти обратно: а б Корнильо Э., Хадж-Каддур К., Дассули А. и др. (октябрь 2012 г.). «Секвенирование наименьшего генома апикомплекса человеческого патогена Babesia microti » . Нуклеиновые кислоты Рез . 40 (18): 9102–14. дои : 10.1093/nar/gks700 . ПМК 3467087 . ПМИД 22833609 .
- ^ Перейти обратно: а б с Ябсли М., Грейнер Э., Ценг Ф., Гарнер М., Нордхаузен Р., Зиккарди М., Боржессон Д., Заболоцкий С. (01.05.2009). «Описание новых видов бабезий и связанных с ними поражений обыкновенных кайр (Uria aalge) из Калифорнии» . Журнал паразитологии . 95 (5): 1183–8. дои : 10.1645/GE-1955.1 . ПМИД 19348514 . S2CID 6677489 .
- ^ Ваннье Э., Краузе П.Дж. (июнь 2012 г.). «Бабезиоз человека». Н. англ. Дж. Мед . 366 (25): 2397–407. дои : 10.1056/NEJMra1202018 . ПМИД 22716978 . S2CID 205116383 .
- ^ Шульц М. (декабрь 2008 г.). «Фотовикторина: Теобальд Смит» . Экстренное заражение Dis . 14 (12): 1940–1942. дои : 10.3201/eid1412.081188 . ISSN 1080-6059 . ПМК 2634653 .
- ^ Бивер ПК, Юнг Р.К., Капп Э.В., Крейг К.Ф. (1984). Клиническая паразитология (9-е изд.). Леа и Фебигер. стр. 205–8. ISBN 978-0-8121-0876-7 .
- ^ Перейти обратно: а б с д и ж г час Шовен А., Моро Э., Бонне С., Плантар О., Маландрин Л. (21 апреля 2009 г.). «Бабезия и ее хозяева: адаптация к длительным взаимодействиям как способ достижения эффективной передачи» . Ветеринарное исследование . 40 (2): 37. doi : 10.1051/vetres/2009020 . ПМК 2695028 . ПМИД 19379662 .
- ^ Корнильо Э., Дассули А., Гарг А. и др. (2013). «Полное картирование генома и реорганизация ядерного и митохондриального генома изолятов Babesia microti » . ПЛОС ОДИН . 8 (9): е72657. Бибкод : 2013PLoSO...872657C . дои : 10.1371/journal.pone.0072657 . ПМЦ 3762879 . ПМИД 24023759 .
- ^ Перейти обратно: а б Хервальдт Б.Л., Каччио С., Герлинцони Ф. и др. (август 2003 г.). «Молекулярная характеристика организма, не относящегося к Babesia divergens, вызывающего зоонозный бабезиоз в Европе» . Возникающая инфекция. Дис . 9 (8): 942–8. дои : 10.3201/eid0908.020748 . ПМК 3020600 . ПМИД 12967491 .
Рисунок 2. Панель компьютерных электронных изображений микрофотографий эритроцитов, инфицированных бабезией, в мазке периферической крови, окрашенном по Гимзе...
- ^ Перейти обратно: а б «CDC2 - Бабезиоз» (PDF) . www.cdc.gov . Центры по контролю и профилактике заболеваний . Проверено 20 сентября 2018 г.
- ^ Перейти обратно: а б с Кинтао-Сильва М.Г. (декабрь 2003 г.). «Уровень заражения спорокинетами Babesia spp. у набухшего Boophilus microplus из зоны энзоотической стабильности в штате Минас-Жерайс, Бразилия» . Память Инст. Освальдо Круз . 98 (8): 999–1002. дои : 10.1590/S0074-02762003000800003 . HDL : 1807/1717 . ПМИД 15049079 .
- ^ Перейти обратно: а б Рэндольф, SE (2004). «Доказательства того, что изменение климата вызвало «появление» клещевых заболеваний в Европе?». Международный журнал медицинской микробиологии . 293 : 5–15. дои : 10.1016/s1433-1128(04)80004-4 . ПМИД 15146980 .
- ^ Перейти обратно: а б с Лаха, Рамгопал, М. Дас, А. Сен (2015). «Морфология, эпидемиология и филогения бабезий: обзор» . Тропическая паразитология . 5 (2): 94–100. дои : 10.4103/2229-5070.162490 . ПМЦ 4557164 . ПМИД 26629451 .
- ^ Карбовяк Г. (2004). «Зоонозный резервуар Babesia microti в Польше». Пол. Дж. Микробиол . 53 Приложение: 61–65. ПМИД 15787199 .
- ^ Телфорд С.Р., Спилман А. (январь 1993 г.). «Резервуарная компетентность белоногих мышей к Babesia microti ». Дж. Мед. Энтомол . 30 (1): 223–227. дои : 10.1093/jmedent/30.1.223 . ПМИД 8433329 .
- ^ Люкс Дж.З., Вайс Д., Линден Дж.В. и др. (январь 2003 г.). «Трансфузионно-ассоциированный бабезиоз после трансплантации сердца» . Возникающая инфекция. Дис . 9 (1): 116–119. дои : 10.3201/eid0901.020149 . ПМЦ 2873739 . ПМИД 12533293 .
- ^ Гомер М.Дж., Агилар-Дельфин I, Телфорд С.Р., Краузе П.Дж., Персинг Д.Х. (01 июля 2000 г.). «Бабезиоз» . Обзоры клинической микробиологии . 13 (3): 451–469. дои : 10.1128/cmr.13.3.451 . ISSN 0893-8512 . ПМЦ 88943 . ПМИД 10885987 .
- ^ Перейти обратно: а б с д «Бабезиоз» . Национальный институт аллергии и инфекционных заболеваний, Национальные институты здравоохранения. 19 февраля 2009 г. Архивировано из оригинала 5 марта 2009 г.
- ^ Перейти обратно: а б с д и ж г Гельфанд Дж. А., Ваннье Э. (6 марта 2008 г.). «Гл. 204: Бабезиоз» . Принципы внутренней медицины Харрисона, 17e . Доступная медицина МакГроу-Хилла. ISBN 978-0071466332 .
- ^ Work TM, Rameyer RA (август 1997 г.). «Описание и эпизоотология Babesia poelea n. sp. у бурых олушей (Sula leucogaster (Boddaert)) на Песчаном острове, атолл Джонстон, центральная часть Тихого океана». Журнал паразитологии . 83 (4): 734–738. дои : 10.2307/3284253 . ISSN 0022-3395 . JSTOR 3284253 . ПМИД 9267418 . S2CID 17889397 .
- ^ Пирс М. (июнь 1975 г.). «Nuttallia França, 1909 (babesiidae), озабоченная Nuttallia Dall, 1898 (psammobiidae): переоценка таксономического положения птичьих пироплазм». Международный журнал паразитологии . 5 (3): 285–287. дои : 10.1016/0020-7519(75)90075-2 . ISSN 0020-7519 . ПМИД 1126783 .
- ^ Эрл Р.А., Хухзермейер Ф.В., Беннетт Г.Ф., Бросси Дж.Дж. (январь 1993 г.). «Babesia peirceisp. nov. от пингвина-осла». Южноафриканский журнал зоологии . 28 (2): 88–90. дои : 10.1080/02541858.1993.11448298 . ISSN 0254-1858 .
- ^ Перейти обратно: а б Меринос С (апрель 1998 г.). «Babesia bennetti n. sp. от желтоногой чайки (Larus cachinnans, Aves, Laridae) на острове Бенидорм, Средиземное море». Журнал паразитологии . 84 (2): 422–424. дои : 10.2307/3284504 . ISSN 0022-3395 . JSTOR 3284504 . ПМИД 9576519 .
- ^ Хунфельд К., Хильдебрандт А., Грей Дж. (сентябрь 2008 г.). «Бабезиоз: недавнее понимание древней болезни». Международный журнал паразитологии . 38 (11): 1219–1237. дои : 10.1016/j.ijpara.2008.03.001 . ISSN 0020-7519 . ПМИД 18440005 .
- ^ Парсонс, Нью-Джерси, Гоус Т.А., Шефер А.М., Ванстрилс Р.Э. (09 марта 2016 г.). «Оценка здоровья африканских пингвинов ( Spheniscus demersus ) на юге Африки» . Ондерстепоорт J Vet Res . 83 (1): е1–е13. дои : 10.4102/ojvr.v83i1.1147 . ISSN 2219-0635 . ПМК 6238701 . ПМИД 27796116 .
- ^ Краузе П.Дж., Лепор Т., Сиканд В.К. и др. (ноябрь 2000 г.). «Атоваквон и азитромицин для лечения бабезиоза» . Н. англ. Дж. Мед . 343 (20): 1454–1458. дои : 10.1056/NEJM200011163432004 . ПМИД 11078770 .
- ^ Перейти обратно: а б Тийл Ванстрилс Р.Э., Уртадо Р., Снайман А., Робертс Д.Г., Парсонс Н.Дж., Писториус П.А. (9 сентября 2019 г.). «Эмпирическое лечение примахином птичьего бабезиоза у морских птиц». Журнал птичьей медицины и хирургии . 33 (3): 258–264. дои : 10.1647/20178-373 . ISSN 1082-6742 . ПМИД 31893621 . S2CID 201949698 .
Внешние ссылки
[ редактировать ]- Краузе П.Дж. и др. (27 января 2021 г.). «Руководство по клинической практике Американского общества инфекционистов (IDSA): Рекомендации 2020 года по диагностике и лечению бабезиоза» . Клинические инфекционные болезни . 72 (2): e49–e64. дои : 10.1093/cid/ciaa1216 . ПМИД 33252652 .
- Информационный бюллетень Департамента здравоохранения штата Нью-Йорк
- Центры по контролю и профилактике заболеваний: о бабезиозе
- Лабораторная идентификация CDC паразитов, вызывающих обеспокоенность общественного здравоохранения: бабезиоз