Карбоксилирование
Карбоксилирование – это химическая реакция , в которой карбоновая кислота образуется путем обработки субстрата диоксидом углерода . [1] Противоположная реакция – декарбоксилирование . В химии термин карбонизация иногда используется как синоним карбоксилирования, особенно применительно к реакции карбанионных реагентов с CO 2 . В более общем смысле карбонизация обычно описывает производство карбонатов . [2]
Органическая химия
[ редактировать ]Карбоксилирование — стандартное преобразование в органической химии . [3] В частности, карбонизация (т.е. карбоксилирование) реактивов Гриньяра и литийорганических соединений является классическим способом преобразования органических галогенидов в карбоновые кислоты. [4]
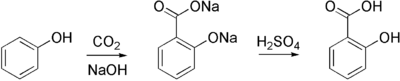
Салицилат натрия , предшественник аспирина , коммерчески получают путем обработки фенолята натрия (натриевой соли фенола ) диоксидом углерода при высоком давлении (100 атм) и высокой температуре (390 К) — метод, известный как реакция Кольбе-Шмитта . Подкисление полученной салицилатной соли дает салициловую кислоту.
Многие подробные процедуры описаны в журнале Organic Syntheses . [5] [6] [7]
Катализаторы карбоксилирования включают N-гетероциклические карбены. [8] и катализаторы на основе серебра. [9]
Карбоксилирование в биохимии
[ редактировать ]Углеродная жизнь возникает в результате карбоксилирования, которое связывает атмосферный углекислый газ с сахаром. Процесс обычно катализируется ферментом RuBisCO . Рибулозо-1,5-бисфосфаткарбоксилаза/оксигеназа , фермент, катализирующий это карбоксилирование, возможно, является самым распространенным белком на Земле. [10] [11] [12]


Многие карбоксилазы, включая ацетил-КоА-карбоксилазу , метилкротонил-КоА-карбоксилазу , пропионил-КоА-карбоксилазу и пируваткарбоксилазу , требуют биотина в качестве кофактора. Эти ферменты участвуют в различных биогенных путях. [13] В схеме EC такие карбоксилазы отнесены к EC 6.3.4 «Другие углерод-азотные лигазы».
Другим примером является посттрансляционная модификация остатков глутамата в γ-карбоксиглутамат в белках. Это происходит главным образом в белках, участвующих в каскаде свертывания крови , в частности в факторах II, VII, IX и X, белке C и белке S, а также в некоторых костных белках. Эта модификация необходима для функционирования этих белков. Карбоксилирование происходит в печени и осуществляется γ-глутамилкарбоксилазой (GGCX). [14] GGCX требует витамина К в качестве кофактора и осуществляет реакцию процессивным образом. [15] γ-карбоксиглутамат связывает кальций, который необходим для его активности. [16] Например, в протромбине связывание кальция позволяет белку связываться с плазматической мембраной тромбоцитов тромбина , приближая его к белкам, которые расщепляют протромбин до активного после повреждения. [17]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ «Карбоксилирование: введение карбоксильной группы в молекулу или соединение с образованием карбоновой кислоты или карбоксилата; пример этого». Оксфордский словарь английского языка . Издательство Оксфордского университета. 2018.
- ^ «Карбонизация: пропитка или обработка углекислым газом; преобразование в карбонат». Оксфордский словарь английского языка . Издательство Оксфордского университета. 2018.
- ^ Браунштейн, Пьер; Мэтт, Доминик; Нобель, Доминик (август 1988 г.). «Реакции углекислого газа с образованием углерод-углеродной связи, катализируемые комплексами переходных металлов». Химические обзоры . 88 (5): 747–764. дои : 10.1021/cr00087a003 .
- ^ А. М. Аппель; и др. (2013). «Границы, возможности и проблемы биохимического и химического катализа фиксации CO 2 » . хим. Преподобный . 113 (8): 6621–6658. дои : 10.1021/cr300463y . ПМЦ 3895110 . ПМИД 23767781 .
- ^ Акира Янагисава; Кацутака Ясуэ; Хисаси Ямамото (1997). «Регио- и стереоселективное карбоксилирование реагентов аллилового бария: (E)-4,8-диметил-3,7-нонадиеновая кислота». Органические синтезы . 74 : 178. дои : 10.15227/orgsyn.074.0178 .
- ^ Х. Кох; В. Хааф (1964). «1-адамантанкарбоновая кислота». Органические синтезы . 44 : 1. дои : 10.15227/orgsyn.044.0001 .
- ^ В. Хааф (1966). «1-Метилциклогексанкарбоновая кислота». Органические синтезы . 46 : 72. дои : 10.15227/orgsyn.046.0072 .
- ^ Чжан Лян (2013). «N-Гетероциклический карбен (NHC) – катализируемые медью превращения диоксида углерода». Химическая наука . 4 (9): 3395. дои : 10.1039/C3SC51070K .
- ^ К. Секин; Т. Ямада (2016). «Карбоксилирование, катализируемое серебром» . хим. Соц. Преподобный . 45 (16): 4524–4532. дои : 10.1039/C5CS00895F . ПМИД 26888406 .
- ^ Дхингра А., Портис А.Р., Дэниел Х. (апрель 2004 г.). «Усиленная трансляция экспрессируемого в хлоропластах гена RbcS восстанавливает уровни малых субъединиц и фотосинтез в ядерных антисмысловых растениях RbcS» . Учеб. Натл. акад. наук. США . 101 (16): 6315–20. Бибкод : 2004PNAS..101.6315D . дои : 10.1073/pnas.0400981101 . ПМК 395966 . ПМИД 15067115 .
(Рубиско) — наиболее распространенный фермент на этой планете, на его долю приходится 30–50% общего растворимого белка в хлоропластах;
- ^ Феллер Ю, Андерс И, Мэй Т (2008). «Рубисколитики: судьба Рубиско после прекращения его ферментативной функции в клетке» (PDF) . Дж. Эксп. Бот . 59 (7): 1615–24. дои : 10.1093/jxb/erm242 . ПМИД 17975207 .
- ^ Рэйвен, Джон А. (апрель 2013 г.). «Рубиско: по-прежнему самый распространенный белок на Земле?» . Новый фитолог . 198 (1): 1–3. дои : 10.1111/nph.12197 . ПМИД 23432200 .
- ^ «Биотин – информационный бюллетень для работников здравоохранения» . Управление пищевых добавок, Национальные институты здравоохранения США . 8 декабря 2017 года . Проверено 25 февраля 2018 г. .
- ^ OMIM - гамма-глутамилкарбоксилаза, предоставлено МакКузиком В.А., последнее обновление в октябре 2004 г. [1]
- ^ Моррис Д.П., Стивенс Р.Д., Райт DJ, Стаффорд Д.В. (1995). «Процессивная посттрансляционная модификация. Витамин К-зависимое карбоксилирование пептидного субстрата» . Ж. Биол. Хим . 270 (51): 30491–8. дои : 10.1074/jbc.270.51.30491 . ПМИД 8530480 .
- ^ Хаушка П.В., Лиан Дж.Б., Галоп П.М. (1975). «Прямая идентификация кальцийсвязывающей аминокислоты гамма-карбоксиглутамата в минерализованных тканях» . Учеб. Натл. акад. наук. США . 72 (10): 3925–9. Бибкод : 1975PNAS...72.3925H . дои : 10.1073/pnas.72.10.3925 . ПМЦ 433109 . ПМИД 1060074 .
- ^ Берг Дж. М., Тимочко Дж. Л., Страйер Л. Биохимия , 5-е изд. Нью-Йорк: WH Freeman and Company, 2002.