Дефицит среднецепочечного ацил-коэнзима А дегидрогеназы
| Дефицит среднецепочечного ацил-коэнзима А-дегидрогеназы (MCAD) | |
|---|---|
| Другие имена | Дефицит карнитина, вторичный по отношению к дефициту ацил-КоА-дегидрогеназы средней цепи , [1] Дефицит MCAD или MCADD |
 | |
| Это состояние наследуется по аутосомно-рецессивному типу. | |
| Специальность | Эндокринология |
Дефицит ацил-КоА-дегидрогеназы средней цепи ( дефицит MCAD или MCADD ) — это нарушение окисления жирных кислот , которое ухудшает способность организма расщеплять жирные кислоты средней цепи до ацетил-КоА . Заболевание характеризуется гипогликемией и внезапной смертью без своевременного вмешательства, чаще всего вызванной периодами голодания или рвоты.
До расширения скрининга новорожденных MCADD был недостаточно диагностируемой причиной внезапной смерти младенцев. Лица, у которых заболевание было выявлено до появления симптомов, имеют отличный прогноз .
MCADD наиболее распространен у лиц североевропейского происхождения, с частотой от 1:4000 до 1:17000 в зависимости от популяции. Лечение MCADD в основном профилактическое, избегая голодания и других ситуаций, когда организм использует окисление жирных кислот для получения энергии.
Признаки и симптомы
[ редактировать ]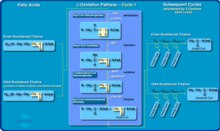
MCADD проявляется в раннем детстве гипокетотической гипогликемией и дисфункцией печени, которым часто предшествуют длительные периоды голодания или инфекция, сопровождающаяся рвотой. Младенцы, находящиеся на исключительно грудном вскармливании, могут проявлять такое состояние вскоре после рождения из-за плохого питания. У некоторых людей первым проявлением MCADD может быть внезапная смерть после незначительного заболевания. [2] У ряда людей с MCADD симптомы могут оставаться совершенно бессимптомными , при условии, что они никогда не столкнутся с ситуацией, которая существенно нагружает их метаболизм. [2] [3] С появлением расширенного скрининга новорожденных у некоторых матерей был выявлен MCADD после того, как их младенцы получили положительные результаты скрининга новорожденных на низкий уровень карнитина. [4]
Фермент ацил-КоА-дегидрогеназа со средней длиной цепи ( MCAD ) отвечает за стадию дегидрирования жирных кислот с длиной цепи от 6 до 12 атомов углерода, когда они подвергаются бета-окислению в митохондриях . жирных кислот Бета-окисление обеспечивает энергию после того, как организм израсходовал запасы глюкозы и гликогена . Это окисление обычно происходит в периоды длительного голодания или болезни, когда потребление калорий снижается, а потребности в энергии увеличиваются. [ нужна ссылка ]
Генетика
[ редактировать ]MCADD наследуется по аутосомно-рецессивному типу, то есть больной человек должен унаследовать мутировавший аллель от обоих родителей. ACADM — это задействованный ген , расположенный в позиции 1p31, имеющий 12 экзонов и кодирующий белок, состоящий из 421 аминокислоты . [3] Среди представителей европеоидной расы Северной Европы распространена мутация — замена аденина в положении 985 на гуанин , что приводит к замене лизина глутаминовой кислотой в положении 304 белка. Другие мутации выявляются чаще, поскольку скрининг новорожденных расширил спектр мутаций. [3] Общая мутация 985A>G присутствует в гомозиготном состоянии у 80% лиц европеоидной расы, у которых клинически выявлен MCADD, и у 60% популяции, выявленной при скрининге. [2]
человека Генотип плохо коррелирует с его клиническим фенотипом MCADD. Клиническая картина человека с MCADD зависит не только от наличия мутаций в гене ACADM , но также от присутствия экологических или физиологических стрессоров, которые требуют, чтобы организм зависел от окисления жирных кислот для получения энергии. Некоторые мутации, выявленные в ходе программ скрининга новорожденных и связанные с более высокой остаточной активностью ферментов, не наблюдались у лиц с клиническими симптомами MCADD. Несмотря на это, лечение с избеганием голодания остается нормой для всех пациентов с диагнозом MCADD. [2]
Диагностика
[ редактировать ]Клинически MCADD или другое нарушение окисления жирных кислот подозревают у лиц с летаргией , судорогами , комой и гипокетотической гипогликемией , особенно если они вызваны легким заболеванием. MCADD может также проявляться острым заболеванием печени и гепатомегалией , что может привести к ошибочному диагнозу синдрома Рея . У некоторых людей единственным проявлением MCADD является внезапная необъяснимая смерть, которой часто предшествует легкое заболевание, которое обычно не приводит к летальному исходу. [3]

В регионах, где проводится расширенный скрининг новорожденных с использованием тандемной масс-спектрометрии (МС/МС), MCADD обычно выявляется вскоре после рождения путем анализа пятен крови, собранных на фильтровальной бумаге. Профили ацилкарнитина с помощью МС/МС покажут очень характерную картину повышенного содержания гексаноилкарнитина (С6), октаноилкарнитина (С8), деканоилкарнитина (С10) или деценоилкарнитина (С10:1), причем уровень С8 превышает уровень С6 и С10. Вторичный дефицит карнитина иногда наблюдается при MCADD, и в этих случаях профили ацилкарнитина могут быть неинформативными. [3] Анализ органических кислот мочи методом газовой хроматографии-масс-спектрометрии (ГХ-МС) покажет картину дикарбоновой ацидурии с низким уровнем кетонов . Также могут быть обнаружены следы видов ацилглицина. У бессимптомных людей могут быть нормальные результаты биохимических лабораторных исследований. Для этих людей диагностическим может быть целенаправленный анализ видов ацилглицина с помощью ГХ-МС, в частности гексаноилглицина и суберилглицина. [3] [5] При биохимическом подозрении на MCADD молекулярно-генетический анализ ACADM . для подтверждения диагноза можно использовать [6] Анализ активности MCAD в культивируемых фибробластах также может быть использован для диагностики. [3]
В случаях внезапной смерти, когда предыдущее заболевание обычно не было фатальным, часто подозревают MCADD. Вскрытие . часто показывает жировые отложения в печени В случаях подозрения на MCADD анализ ацилкарнитина в желчи и крови для диагностики можно провести посмертный . Если образцы недоступны, может оказаться полезным использование остаточной крови, полученной при скрининге новорожденных. Биохимическое тестирование бессимптомных братьев и сестер и родителей также может быть информативным. [7] MCADD и другие нарушения окисления жирных кислот были признаны в последние годы недиагностированными причинами синдрома внезапной детской смерти . [8] [9]
Уход
[ редактировать ]Как и в случае с большинством других нарушений окисления жирных кислот, людям с MCADD необходимо избегать голодания в течение длительных периодов времени. Во время заболеваний они требуют тщательного лечения, чтобы предотвратить метаболическую декомпенсацию , которая может привести к смерти. [2] Добавление простых углеводов или глюкозы во время болезни является ключом к предотвращению катаболизма . [3] Продолжительность голодания у людей с MCADD варьируется в зависимости от возраста; младенцам обычно требуется частое кормление или источник углеводов с медленным высвобождением, такой как сырой кукурузный крахмал . Болезни и другие стрессы могут значительно снизить переносимость голодания у пострадавших людей. [10]
Лица с MCADD должны иметь «экстренное письмо», которое позволит медицинскому персоналу, незнакомому с пациентом и его состоянием, правильно назначить правильное лечение в случае острой декомпенсации. В этом письме должны быть описаны шаги, необходимые для вмешательства в кризисную ситуацию, а также указана контактная информация специалистов, знакомых с уходом за человеком. [3]
Проблемы с ошибочным диагнозом
- принимают расстройство MCADD за синдром Рея Педиатры часто ошибочно . Синдром Рея — это тяжелое заболевание, которое может развиться у детей, когда они выздоравливают от вирусных инфекций, таких как ветряная оспа или грипп.
- Большинство случаев синдрома Рея связаны с применением аспирина во время этих вирусных инфекций.
Прогноз
[ редактировать ]Исследование 1994 года всего населения Нового Южного Уэльса ( Австралия ) выявило 20 пациентов. Из них 5 (25%) умерли в возрасте 30 месяцев или раньше. Из выживших 1 (5%) имел тяжелую инвалидность, а остальные либо страдали легкой формой инвалидности, либо нормально учились в школе. [11] Голландское исследование 2006 года проанализировало 155 случаев и показало, что 27 человек (17%) умерли в раннем возрасте. Из выживших 24 человека (19%) страдали той или иной степенью инвалидности, большинство из которых были легкой степени. Все 18 пациентов с диагнозом неонатально были живы на момент наблюдения. [12]
Заболеваемость
[ редактировать ]MCADD наиболее распространен у лиц североевропейского европеоидного происхождения. Заболеваемость в Северной Германии составляет 1:4000, что в настоящее время является самым высоким в мире. Северная Европа также является источником распространенной мутации MCADD. Для групп населения, не имеющих происхождения из Северной Европы, заболеваемость значительно ниже: 1:51 000 в Японии и 1:700 000 на Тайване . Общая мутация не была выявлена в случаях MCADD, выявленных в азиатских популяциях. [3]
Ссылки
[ редактировать ]- ^ ЗАРЕЗЕРВИРОВАНО, ВСТАВИТЬ US14 -- ВСЕ ПРАВА. «Орфанет: дефицит ацил-КоА-дегидрогеназы средней цепи» . www.orpha.net . Проверено 14 апреля 2019 г. .
{{cite web}}: CS1 maint: числовые имена: список авторов ( ссылка ) - ^ Jump up to: а б с д и Моррис, Эндрю AM; Шпикеркоттер, Юте (2012). «Нарушения митохондриального окисления жирных кислот и связанных с ним метаболических путей». В Содубре, Жан-Мари; ван ден Берге, Жорж; Уолтер, Джон Х. (ред.). Врожденные метаболические заболевания: диагностика и лечение (5-е изд.). Нью-Йорк: Спрингер. стр. 201–216 . ISBN 978-3-642-15719-6 .
- ^ Jump up to: а б с д и ж г час я дж Матерн, Д.; Ринальдо, П.; Пагон, РА; Берд, Т.Д.; Долан, ЧР; Стивенс, К.; Адам, член парламента (1993). «Среднецепочечный ацил-кофермент и дефицит дегидрогеназы». ПМИД 20301597 .
{{cite journal}}: Для цитирования журнала требуется|journal=( помощь ) - ^ Лейдикер, КБ; Нейдич, Дж. А.; Лори, Ф.; Барр, Э.М.; Пакетт, РЛ; Лобо, РМ; Абденур, Дж. Э. (2011). «Дефицит ацил-КоА-дегидрогеназы у матери со средней длиной цепи, выявленный при скрининге новорожденных». Молекулярная генетика и обмен веществ . 103 (1): 92–95. дои : 10.1016/j.ymgme.2011.01.011 . ПМИД 21354840 .
- ^ Ринальдо, П.; О'Ши, Джей-Джей; Коутс, премьер-министр; Хейл, Делавэр; Стэнли, Калифорния; Танака, К. (1988). «Дефицит ацил-КоА-дегидрогеназы средней цепи». Медицинский журнал Новой Англии . 319 (20): 1308–1313. дои : 10.1056/NEJM198811173192003 . ПМИД 3054550 .
- ^ «Повышение C8 + меньшие повышения C6 и C10» (PDF) . Американский колледж медицинской генетики . Проверено 9 июня 2012 г.
- ^ Ринальдо, П.; Матерн, Д.; Беннетт, MJ (2002). «Нарушения окисления жирных кислот». Ежегодный обзор физиологии . 64 : 477–502. doi : 10.1146/annurev.phyol.64.082201.154705 . ПМИД 11826276 .
- ^ Хеги, Т.; Остфельд, Б.; Гарднер, К. (1992). «Среднецепочечный ацил-кофермент дегидрогеназы и СВДС». Медицина Нью-Джерси . 89 (5): 385–392. ПМИД 1635678 .
- ^ Кеппен, LD; Рэндалл, Б. (1999). «Врожденные дефекты окисления жирных кислот: предотвратимая причина СВДС». Медицинский журнал Южной Дакоты . 52 (6): 187–188, обсуждение 188–9. ПМИД 10388343 .
- ^ Уолтер, Дж. Х. (2009). «Толерантность к голоданию: рациональная и практическая оценка у детей с гипокетонемией». Журнал наследственных метаболических заболеваний . 32 (2): 214–217. дои : 10.1007/s10545-009-1087-y . ПМИД 19255872 . S2CID 28507050 .
- ^ Вилкен, Б.; Хаммонд, Дж.; Силинк, М. (1 мая 1994 г.). «Заболеваемость и смертность при дефиците ацил-коэнзима А со средней длиной цепи» . Архив болезней в детстве . 70 (5): 410–412. дои : 10.1136/adc.70.5.410 . ISSN 1468-2044 . ПМЦ 1029830 . ПМИД 8017963 .
- ^ Деркс, Терри Дж.Дж.; Рейнгуд, Дирк-Ян; Уотерхэм, Ханс Р.; Гервер, Виллем-Ян М.; Берг, Мартен П. ван ден; Зауэр, Питер Дж. Дж.; Смит, Г. Питер А. (2006). «Естественная история дефицита ацил-КоА-дегидрогеназы средней цепи в Нидерландах: клиническая картина и исход». Журнал педиатрии . 148 (5): 665–670.е3. дои : 10.1016/j.jpeds.2005.12.028 . ПМИД 16737882 .