Кадмийорганическая химия
Химия органокадмия описывает физические свойства, синтез, реакции и использование кадмийорганических соединений , которые представляют собой металлоорганические соединения, содержащие углерода с кадмием химическую связь . [ 1 ] Кадмий относится к 12-й группе с цинком и ртутью , и их химический состав имеет много общего. Синтетическая применимость кадмийорганических соединений ограничена.
Простейшим кадмийорганическим соединением является диметилкадмий . Это линейная молекула с длиной связи C-Cd 213 пм . [ 2 ] Кадмиорганические соединения обычно чувствительны к воздуху, свету и влаге.
Синтез
[ редактировать ]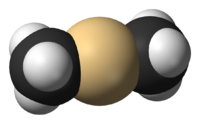
О диметилкадмии и диэтилкадмии сообщил в 1917 году Эрих Краузе. Обычно их получают путем трансметаллирования или реакции обмена между алкилирующим агентом и солью кадмия. [ 3 ]
По одной методике диэтилкадмий получают реакцией бромида кадмия с двумя эквивалентами реактива Гриньяра этилмагнийбромидом в диэтиловом эфире . Диэтилкадмий — бесцветное масло с температурой плавления −21 °С . Дифенилкадмий можно получить реакцией фениллития с бромидом кадмия. Дифенилкадмий — твердое вещество с температурой плавления 174 °С.
Фторалкильные и алкенильные производные
[ редактировать ]Следуя установленным тенденциям, перфторированные алкил- и алкенильные производные кадмия обладают повышенной термической стабильностью. Алкенильные производные получаются присоединением йодтрифторэтилена к металлическому кадмию. [ 4 ]
Реакции
[ редактировать ]Кадморганические соединения менее нуклеофильны , чем цинкорганические соединения . Эта пониженная реакционная способность демонстрируется при превращении ацилхлоридов в кетоны с помощью этих реагентов. [ 5 ] Об этой реакции сообщил Генри Гилман в 1936 году, и она использовалась до тех пор, пока не стали доступны менее токсичные купраты. Соответствующий реактив Гриньяра будет реагировать дальше, давая третичный спирт . Метилкадмий использовался на одной из стадий, ведущих к полному синтезу холестерина : [ 6 ]
Другим синтетическим применением кадмия является реакция диизоамилкадмия с β-карбометоксипропионилхлоридом с образованием метил-4-кето-7-метилоктаноата без дальнейшей реакции с кетоновой группой или сложноэфирной группой. [ 7 ]
Такая селективность наблюдается при условии, что реакцию проводят без соли. [ 8 ] Когда реагент кадмия образуется in situ из соли кадмия, галогенид образует более нуклеофильный кадмиевый органический реагент, ат-комплекс . Тот же солевой эффект можно наблюдать и с цинкорганическими соединениями.
Диметилкадмий использовался для синтеза коллоидных нанокристаллов материалов II-VI, таких как селенид кадмия . Его токсичная и летучая природа побудила исследователей искать в других местах прекурсоры кадмия, такие как оксид кадмия. [ 9 ]
Токсичность
[ редактировать ]Соединения кадмия токсичны. Диметилкадмий токсичен для почек, печени, центральной нервной системы и органов дыхания при вдыхании. [ 10 ] Соединения кадмия в целом рассматриваются как канцерогены для человека МАИР . [ 11 ]
Ссылки
[ редактировать ]- ^ Синтетические методы металлоорганической и неорганической химии, том 5, Медь, серебро, золото, цинк, кадмий и ртуть WA Herrmann Ed. ISBN 3-13-103061-5
- ^ Феликс Ханке; Сара Хиндли; Энтони С. Джонс; Александр Штайнер (2016). «Твердотельные структуры высоко- и низкотемпературных фаз диметилкадмия». Химические коммуникации . 52 (66): 10144–10146. дои : 10.1039/c6cc05851e . ПМИД 27457504 .
- ^ Эрих Краузе (1917). «Простые диалкилы кадмия. (I. Сообщение об органических соединениях кадмия.)» . Отчеты Немецкого химического общества . 50 (2): 1813–1822. дои : 10.1002/cber.19170500292 .
- ^ Бертон, Дональд Дж.; Ян, Чжэнь-Ю; Моркен, Питер А. (1994). «Фторированные металлорганические соединения: винил, алкинил, аллил, бензил, пропаргил и арил». Тетраэдр . 50 (10): 2993–3063. дои : 10.1016/S0040-4020(01)81105-4 .
- ^ Дэвид А. Ширли (2011). «Синтез кетонов из галогенангидридов и металлоорганических соединений магния, цинка и кадмия». Орг. Реакции : 28–58. дои : 10.1002/0471264180.или008.02 . ISBN 9780471264187 .
- ^ Вудворд, РБ; Зондхаймер, Франц; Тауб, Дэвид; Хойслер, Карл; Макламор, WM (1952). «Полный синтез стероидов». Журнал Американского химического общества . 74 (17): 4223–51. дои : 10.1021/ja01137a001 .
- ^ Кейсон, Джеймс; Год проута = 1948, Франклин С. (1948). «Метил 4-кето-7-метилоктаноат». Органические синтезы . 28 : 75. дои : 10.15227/orgsyn.028.0075 .
{{cite journal}}: CS1 maint: числовые имена: список авторов ( ссылка ) - ^ Джонс, Пол Р.; Дезио, Питер Дж. (1978). «Менее знакомые реакции кадмийорганических реагентов». Химические обзоры . 78 (5): 491–516. дои : 10.1021/cr60315a001 .
- ^ Пэн ЗА, Пэн X (2001). «Формирование высококачественных нанокристаллов CdTe, CdSe и CdS с использованием CdO в качестве прекурсора». Журнал Американского химического общества . 123 (1): 183–4. дои : 10.1021/ja003633m . ПМИД 11273619 .
- ^ Спиридонова Е.И.а (1991). «[Экспериментальное изучение токсических свойств диметилкадмия]». Гигиена Труда и Профессиональные заболевания (на русском языке) (6): 14–7. ПМИД 1916391 .
- ^ «Кадмий и соединения кадмия». Мышьяк, металлы, волокна и пыль . Международное агентство по исследованию рака . 2012. стр. 121–145. ISBN 9789283201359 .
