α-глюкозидаза
| α-глюкозидаза | |||
|---|---|---|---|
 α-глюкозидаза Гексамер, Sulfolobus solfataricus | |||
| Идентификаторы | |||
| ЕС №. | 3.2.1.20 | ||
| CAS №. | 9001-42-7 | ||
| Базы данных | |||
| Intenz | Intenz View | ||
| Бренда | Бренда вход | ||
| Расширение | Вид Nicezyme | ||
| Кегг | Кегг вход | ||
| Метатический | Метаболический путь | ||
| Напрямую | профиль | ||
| PDB Структуры | RCSB PDB PDBE PDBSUM | ||
| |||
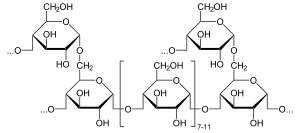

α-глюкозидаза ( EC 3.2.1.20 , (систематическое название α -D -глюкозида глюкогидролаза ) представляет собой глюкозидазу , расположенную на границе кисти мелкой кишки, которая действует на α (1 → 4) связи: [ 1 ] [ 2 ] [ 3 ] [ 4 ] [ 5 ] [ 6 ]
- Гидролиз терминальных, нередуцирующих (1 → 4)-связанных с α- г- глюкозой с высвобождением d -глюкозы
Это в отличие от EC 3.2.1.21 β-глюкозидазы .
Терминология
[ редактировать ]Go: 0090599, широкий смысл
[ редактировать ]Вход гена онтологии GO: 0090599 представляет широкое чувство «альфа-глюкозидазы». Он определяется как «катализ гидролиза терминального, не восстанавливающего альфа-связанного остатка альфа-D-глюкозы с высвобождением альфа-D-глюкозы». В этом смысле «альфа-глюкозидаза» может охватывать широкий диапазон активности ферментов, отличающийся от связи их терминала (1 → 3, 1 → 4 или 1 → 6), специфическая идентичность их субстрата (сахароза, мальтоза. , или крахмал), среди других аспектов. [ 7 ]
EC 3.2.1.20, узкий смысл
[ редактировать ]Определение, связанное с ферментной комиссией № 3.2.1.20, более уже. Это требует, чтобы связь была 1 → 4, а предпочтительным субстратом для меньшего количества олигосахаридов (в отличие от более крупных полисахаридов, таких как крахмал : альфа-амилаза в противном случае будет включена). Человеческие гены, которые производят ферменты с действиями, указанными в этом номере ЕС, включают: [ 8 ]
- MGAM -это «малтаза-глюкоамилаза», найденная на границе кисти кишечника.
- GAA -это «кислотная альфа-глюкозидаза», обнаруженная в лизосоме .
- Ganc , «Нейтральная альфа-глюкозидаза C».
Синонимы, упомянутые Комиссией, включают мальтазу, глюкоинвертазу, глюкозидозукразу, мальтазу-глюкоамилазу, α-глюкопиранозидазу, глюкозидуинвертазу, α - глюкозидазу, α-глюкозид гидролазой, α-1,4-глюкозидаза, α- d -глакозид . [ 9 ] Эти имена не рекомендуются, потому что они могут относиться только к конкретной активности фермента или конкретного белка, обладающего этой активностью.
Механизм
[ редактировать ]α-глюкозидаза гидролизует терминальные нередуцирующие (1 → 4)-связанные остатки α-глюкозы для высвобождения одной молекулы α-глюкозы. [ 10 ] α-глюкозидаза представляет собой углеводу-гидролазу, которая высвобождает α-глюкозу в отличие от β-глюкозы. Остатки β-глюкозы могут высвобождаться глюкоамилазой, функционально сходным ферментом. Селективность субстрата α-глюкозидазы обусловлена дочерней сродством активного сайта фермента. [ 11 ] Два предложенных механизма включают нуклеофильное смещение и промежуточное соединение ионов оксокарбения. [ 11 ]

- Rhodnius prolixus , кровеносное насекомое, образует гемозоин (Гц) во время расщепления гемоглобина-хозяина. Синтез гемозоина зависит от сайта связывания субстрата α-глюкозидазы. [ 12 ]
- Форель печень α-глюкозидазы экстрагировали и охарактеризовали. Было показано, что для одного из α-глюкозидаз печени печени максимальная активность фермента была увеличена на 80% во время физических упражнений по сравнению с форелью покоя. Было показано, что это изменение коррелирует с увеличением активности для гликогеновой фосфорилазы печени. Предполагается, что α-глюкозидаза в глюкозидном пути играет важную роль в дополнении фосфоролитического пути в метаболическом ответе печени на потребности в энергии на физические упражнения. [ 13 ]
- Было показано, что дрожжи и крыса с небольшим кишечником α-глюкозидазы ингибируются несколькими группами флавоноидов. [ 14 ]
Структура
[ редактировать ]
α-глюкозидазы могут быть разделены, согласно первичной структуре на две семьи. [ 11 ] Ген, кодирующий лизосомальную α-глюкозидазу человека, составляет около 20 КБ, и его структура была клонирована и подтверждена. [ 15 ]
- Лизосомальная α-глюкозидаза человека была изучена для значения ASP-518 и других остатков в непосредственной близости от активного сайта фермента. Было обнаружено, что замена ASP-513 на GLU-513 мешает посттрансляционной модификации и внутриклеточному транспорту предшественника α-глюкозидазы. Кроме того, остатки TRP-516 и ASP-518 считались критическими для каталитической функциональности фермента. [ 16 ]
- Было показано, что кинетические изменения в α-глюкозидазе индуцируются денатуринами, такими как растворы гунидиния (GDMCL) и SDS. Эти денатуранты вызывают потерю активности и конформационные изменения. Потеря активности фермента возникает в гораздо более низких концентрациях денатура, чем требуется для конформационных изменений. Это приводит к выводу, что конформация активного сайта фермента является менее стабильной, чем вся конформация фермента в ответ на два денатура. [ 17 ]
Актуальность заболевания
[ редактировать ]- Заболевание гликогена II типа II , также называемое болезнью Помпа : расстройство, при котором α-глюкозидаза является дефицитом. В 2006 году препарат альглюкозидаза Альфа стала первым выпущенным лечением болезни Помпа и действует как аналог с α-глюкозидазой. [ 18 ] Дальнейшие исследования альглюкозидазы Alfa показали, что иминосугары демонстрируют ингибирование фермента. Было обнаружено, что одна молекула соединения связывается с одной молекулой фермента. Было показано, что 1-деоксинодзиримицин (DNJ) связывал бы самый сильный из протестированных сахаров и почти полностью заблокировал активное место фермента. Исследования повысили знание механизма, с помощью которого α-глюкозидаза связывается с сахарами имино. [ 19 ]
- Диабет : акарбоза , ингибитор α-глюкозидазы, конкурентно и обратимо ингибирует α-глюкозидазу в кишечнике. Это ингибирование снижает скорость поглощения глюкозы посредством задержки углеводов и расширенного времени пищеварения. Акарбоза может предотвратить развитие диабетических симптомов. [ 20 ] Следовательно, ингибиторы α-глюкозидазы (например, акарбоза) используются в качестве антидиабетических препаратов в сочетании с другими антидиабетическими препаратами. Было обнаружено, что лютеолин является сильным ингибитором α-глюкозидазы. Соединение может ингибировать фермент до 36% с концентрацией 0,5 мг/мл. [ 21 ] По состоянию на 2016 год это вещество проверяется у крыс, мышей и клеточной культуры . Аналоги флавоноидов были продемонстрированы с ингибирующей активностью. [ 22 ]
- Азооспермия : диагностика азооспермии может способствовать измерению активности α-глюкозидазы в семенной плазме. Активность в семенной плазме соответствует функциональности эпидидимиса. [ 23 ]
- Антивирусные агенты: многие вирусы животных обладают внешней оболочкой, состоящей из вирусных гликопротеинов. Они часто требуются для жизненного цикла вируса и используют клеточный механизм для синтеза. Ингибиторы α -глюкозидазы показывают, что фермент участвует в пути N -гликанов для вирусов, таких как ВИЧ и вирус гепатита В (HBV). Ингибирование α-глюкозидазы может предотвратить слияние ВИЧ и секрецию HBV. [ 24 ]
Смотрите также
[ редактировать ]Некоторые другие глюкозидазы:
Ссылки
[ редактировать ]- ^ Альфа-глюкозидазы в Национальной библиотеке медицины Медицинской библиотеки США (сетка)
- ^ Бруни, CB; SICA, V.; Auricchio, F.; Ковелли И. (1970). «Дальнейшая кинетическая и структурная характеристика лизосомальной α-D-глюкозидной глюкогидролазы из печени крупного рогатого скота». Биохим. Биофиз. Акт . 212 (3): 470–477. doi : 10.1016/0005-2744 (70) 90253-6 . PMID 5466143 .
- ^ Фланаган, PR; Forstner, GG (1978). «Очистка кишечной малтазы/глюкоамилазы крысы и ее аномальной диссоциации либо тепло, либо с помощью низкого pH» . Биохимия. Дж . 173 (2): 553–563. doi : 10.1042/bj1730553 . PMC 1185809 . PMID 29602 .
- ^ Larner, J.; Lardy, H.; Myrback, K. (1960). «Другие глюкозидазы». В Boyer, PD (ред.). Ферменты . Тол. 4 (2 -е изд.). Нью -Йорк: Академическая пресса. С. 369–378.
- ^ Sivikami, S.; Радхакришнан, (1973). «Очистка глюкоамилазы кишечника кролика с помощью аффинной хроматографии на сефадексе G-200». Индиан Дж. Биохим. Биофиз . 10 (4): 283–284. PMID 4792946 .
- ^ Søresen, Sh; Норен, О.; Дизайн, H.; Дэниелс, Эм (1982). «Амфилическая свинья кишечная микровиллы mals/gluco-glucoalsis. Структуры и указанные». Однако. Дж. Бихем . 126 (3): 559–568. doi : 10 1111) /j.1432-1033,1982.tb06817.x . PMID 6814909 .
- ^ «Альфа-глюкозидазная активность гена онтология (GO: 0090599)» . www.informatics.jax.org . См.: Определение, Go Tree View.
- ^ «Фермент - 3.2.1.20 Альфа -глюкозидаза» . Enzyme.expasy.org .
Группа ферментов, чья специфичность направлена главным образом на экзогидролиз 1,4-альфа-глюкозидных связей, и что гидролизовые олигосахариды быстро по сравнению с полисахаридами, которые относительно медленно или нет.
- ^ "Explorenz: EC 3.2.1.20" . www.enzyme-database.org .
- ^ "EC 3.2.1.20" . Расширение . Получено 1 марта 2012 года .
- ^ Jump up to: а беременный в Chiba S (август 1997 г.). «Молекулярный механизм в α-глюкозидазе и глюкоамилазе» . Biosci. Биотехнол. Биохимия . 61 (8): 1233–9. doi : 10.1271/bbb.61.1233 . PMID 9301101 .
- ^ Mury FB, Da Silva JR, Ferreira LS, et al. (2009). «α-глюкозидаза способствует образованию гемозоина в кровеносной ошибке: эволюционная история» . Plos один . 4 (9): E6966. Bibcode : 2009ploso ... 4.6966M . doi : 10.1371/journal.pone.0006966 . PMC 2734994 . PMID 19742319 .
- ^ Mehrani H, Storey KB (октябрь 1993). «Характеристика α-глюкозидаз из печени радужной форели». Архи Биохимия. Биофиз . 306 (1): 188–94. doi : 10.1006/abbi.1993.1499 . PMID 8215402 .
- ^ Тадера К., Минами Ю., Такамацу К., Мацуока Т (апрель 2006 г.). «Ингибирование α-глюкозидазы и α-амилазы флавоноидами» . J. Nutr. Наука Витаминол . 52 (2): 149–53. doi : 10.3177/jnsv.52.149 . PMID 16802696 .
- ^ Hystem L; M Howene-Western Field; AJ SAINT; Ba Asstra (1 декабрь 1990). «Chragerzensation или гоманские тисосоциальные гены α-гумуло-гумуло-гумкодиаста» . Бим. Дж . 272 (2): 493–497. doi : 10,1042/bj2720493 . PMC 1149727 . PMID 2268276 .
- ^ Германс, Моник; Мариан Кроос; Джос Ван Биемен; Бен Оостра; Арнольд Реусер (25 июля 1991 г.). «Человеческая лизосомальная характеристика а-глюкозидазы каталитического сайта» . Журнал биологической химии . 21. 266 (21): 13507–13512. doi : 10.1016/s0021-9258 (18) 92727-4 . Получено 1 марта 2012 года .
- ^ Wu XQ, Xu H, Yue H, Liu KQ, Wang XY (декабрь 2009 г.). «Кинетика ингибирования и агрегация α-глюкозидазы различными денатуру». Белок j . 28 (9–10): 448–56. doi : 10.1007/s10930-009-9213-0 . PMID 19921411 . S2CID 36546023 .
- ^ «FDA одобряет первое лечение болезни Помпа» . FDA . FDA . Получено 1 марта 2012 года .
- ^ Yoshimizu, M.; Таджима, y; Matsuzawa, F; Aikawa, S; Iwamoto, K; Kobayashi, T; Эдмундс, т; Fujishima, K; Цудзи, D; Itoh, k; Ikekita, M; Кавашима, я; Sugawara, K; Ohyanagi, n; Suzuki, T; Тогава, т; Оно, К; Сакураба, ч (май 2008 г.). «Параметры связывания и термодинамика взаимодействия сахаров имино с рекомбинантной α-глюкозидазой человеческой кислотой (альглюкозидаза альфа): понимание механизма сложного образования». Clin Chim Acta . 391 (1–2): 68–73. doi : 10.1016/j.cca.2008.02.014 . PMID 18328816 .
- ^ Бишофф H (август 1995 г.). «Механизм ингибирования α-глюкозидазы при лечении диабета». Clin Invest Med . 18 (4): 303–11. PMID 8549017 .
- ^ Ким Дж.С., Квон К.С., Сон К.Х. (ноябрь 2000 г.). «Ингибирование α-глюкозидазы и амилазы лютеолином, флавоноидом» . Biosci. Биотехнол. Биохимия . 64 (11): 2458–61. doi : 10.1271/bbb.64.2458 . PMID 11193416 . S2CID 5757649 .
- ^ Zhen, et al. (Ноябрь 2017). «Синтез новых флавоноидных алкалоидов в качестве ингибиторов α-глюкозидазы». Биоорганическая и лекарственная химия . 25 (20): 5355–64. doi : 10.1016/j.bmc.2017.07.055 . PMID 28797772 .
- ^ Mahmoud AM, Geslevich J, Kint J, et al. (Март 1998 г.). «Активность α-глюкозидазы в плазме и мужское бесплодие» . Гул Воспроизведение 13 (3): 591–5. doi : 10.1093/Humrep/13.3.591 . PMID 9572418 .
- ^ Мехта, Ананд; Зитцманн, Николь; Радд, Полин М; Блок, Тимоти М; Dwek, Raymond A (23 июня 1998 г.). «Ингибиторы α-глюкозидазы как потенциальные антивирусные агенты на основе широких» . Письма Febs . 430 (1–2): 17–22. doi : 10.1016/s0014-5793 (98) 00525-0 . PMID 9678587 . S2CID 25156942 .