Стрептококк пиогенный
| Стрептококк пиогенный | |
|---|---|
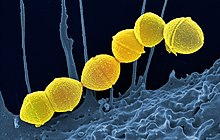 | |
| Сканирующая электронная микрофотография цепочки бактерий Streptococcus pyogenes в искусственных цветах (желтая) | |
| Научная классификация | |
| Домен: | Бактерии |
| Тип: | Бациллота |
| Сорт: | Бациллы |
| Заказ: | лактобактерии |
| Семья: | Стрептококковые |
| Род: | Стрептококк |
| Разновидность: | С. пиогенес |
| Биномиальное имя | |
| Стрептококк пиогенный Розенбах 1884 г. | |
Streptococcus — разновидность грамположительных бактерий аэротолерантных . рода Streptococcus pyogenes Эти бактерии являются внеклеточными и состоят из неподвижных кокков , не образующих спор (круглых клеток), которые имеют тенденцию соединяться в цепочки. Они имеют клиническое значение для человека, так как представляют собой нечастую, но обычно патогенную часть микробиоты кожи , способную вызывать инфекцию группы А. стрептококковую S. pyogenes является преобладающим видом, содержащим Лансфилда группы А антиген , и его часто называют группы А стрептококком ( GAS ). Однако как Streptococcus disgalactiae , так и группа Streptococcus anginosus также могут обладать антигеном группы А. Стрептококки группы А при выращивании на кровяном агаре обычно образуют небольшие (2–3 мм) зоны -гемолиза , полного разрушения эритроцитов бета . название группы А (бета-гемолитический стрептококк ). Таким образом, также используется [1]
Видовое название происходит от греческих слов, означающих «цепочку» ( streptos ) ягод ( coccus [латинизированное от kokkos ]) и гной ( pyo образующих ) ( генов ), поскольку при ряде инфекций, вызванных бактерией, выделяется гной. Основной критерий дифференциации Staphylococcus spp. и виды Streptococcus . это тест на каталазу . Стафилококки являются каталазо-положительными, тогда как стрептококки каталазо-отрицательными. [2] S. pyogenes можно культивировать на чашках со свежей кровью и агаром. Тест PYR позволяет дифференцировать Streptococcus pyogenes от других морфологически сходных бета-гемолитических стрептококков (включая S. disgalactiae subsp. esquismilis ), поскольку S. pyogenes дает положительный результат теста. [3]
Ежегодно во всем мире происходит около 700 миллионов случаев заражения ГАС. Хотя общий уровень смертности от этих инфекций составляет менее 0,1%, более 650 000 случаев являются тяжелыми и инвазивными, а уровень смертности в этих случаях составляет 25%. [4] Раннее выявление и лечение имеют решающее значение; неудачная диагностика может привести к сепсису и смерти. [5] [6] S. pyogenes клинически и исторически значима как причина скарлатины , возникающей в результате воздействия экзотоксина этого вида . [7]
Эпидемиология
[ редактировать ]

В отличие от большинства бактериальных патогенов, S. pyogenes заражает только человека. Таким образом, зоонозная передача от животного (или продуктов животного происхождения) человеку встречается редко. [8]
S. pyogenes обычно колонизирует горло, слизистую оболочку половых органов, прямую кишку и кожу. Среди здоровых взрослых от 1% до 5% имеют горловое, вагинальное или ректальное носительство, причем дети являются более частыми носителями. Чаще всего передача от одного человека к другому происходит при вдыхании воздушно-капельных капель , образующихся при чихании и кашле инфицированного человека. Контакт с кожей, контакт с предметами , содержащими бактерию, и употребление зараженной пищи возможны, но являются редкими способами передачи. В большинстве стран стрептококковый фарингит чаще всего возникает в конце зимы - начале весны, поскольку внутренние помещения используются чаще и, следовательно, более переполнены. Осенью заболеваемость минимальна. [9]
Заражение матери S. pyogenes обычно происходит на поздних сроках беременности, от 30 недель беременности до четырех недель после родов . Материнские инфекции составляют от 2 до 4% всех клинически диагностированных инфекций, вызванных S. pyogenes . [9] Риск сепсиса относительно высок по сравнению с другими бактериальными инфекциями, приобретенными во время беременности, а S. pyogenes является основной причиной септического шока и смертности у беременных и родильниц. [10]
Бактериология
[ редактировать ]
Серотипирование
[ редактировать ]В 1928 году Ребекка Лэнсфилд опубликовала метод серотипирования S. pyogenes на основе его полисахарида клеточной стенки. [11] фактор вирулентности , отображаемый на его поверхности. [12] Позже, в 1946 году, Лэнсфилд описал серологическую классификацию изолятов S. pyogenes на основе компонентов их поверхностных пилей (известных как Т-антиген). [13] которые используются бактериями для прикрепления к клеткам-хозяевам. [14] По состоянию на 2016 год идентифицировано 120 М белков. Эти М-белки кодируются 234 типами генов emm, содержащими более 1200 аллелей. [9]
Лизогения
[ редактировать ]Все штаммы S. pyogenes полилизогенизированы, т. е. несут в своих геномах один или несколько бактериофагов. [15] Некоторые из фагов могут быть дефектными, но в некоторых случаях активный фаг может компенсировать дефекты других. [16] В целом геном штаммов S. pyogenes , выделенных во время заболевания, идентичен более чем на 90%, они различаются переносимым ими фагом. [17]
Факторы вирулентности
[ редактировать ]S. pyogenes обладает несколькими факторами вирулентности , которые позволяют ему прикрепляться к тканям хозяина, уклоняться от иммунного ответа и распространяться, проникая в слои тканей хозяина. [18] на основе углеводов, Бактериальная капсула состоящая из гиалуроновой кислоты окружает бактерию, защищая ее от фагоцитоза нейтрофилов , . [2] Кроме того, капсула и несколько факторов, встроенных в клеточную стенку, включая белок М , липотейхоевую кислоту и белок F (SfbI), облегчают прикрепление к различным клеткам-хозяевам. [19] Белок М также ингибирует опсонизацию по альтернативному пути комплемента путем связывания с регуляторами комплемента хозяина. Белок М, обнаруженный в некоторых серотипах, также способен предотвращать опсонизацию путем связывания с фибриногеном . [2] Однако белок М также является самым слабым местом в защите этого патогена, поскольку антитела, вырабатываемые иммунной системой против белка М, нацелены на бактерии для поглощения фагоцитами . Белки М уникальны для каждого штамма, и их идентификация может быть использована клинически для подтверждения штамма, вызывающего инфекцию. [20]
| Имя | Описание |
|---|---|
| Стрептолизин О | Экзотоксин ; , одна из основ бета-гемолитического свойства организма, стрептолизин О вызывает иммунный ответ и выявление антител к нему антистрептолизин О (АСО) можно клинически использовать для подтверждения недавней инфекции. Он повреждается кислородом. |
| Стрептолизин С | Кардиотоксический экзотоксин, еще один бета-гемолитический компонент, неиммуногенный и стабильный к O 2 . Мощный клеточный яд, поражающий многие типы клеток, включая нейтрофилы, тромбоциты и субклеточные органеллы. |
| Стрептококковый пирогенный экзотоксин А (SpeA) | Суперантигены, секретируемые многими штаммами S. pyogenes . Этот пирогенный экзотоксин ответственен за сыпь при скарлатине и многие симптомы стрептококкового синдрома токсического шока, также известного как синдром, подобный токсическому шоку (TSLS). |
| Стрептококковый пирогенный экзотоксин C (SpeC) | |
| Стрептококковый пирогенный экзотоксин B (SpeB) | Цистеиновая протеаза и преобладающий секретируемый белок. Множественные действия, включая разрушение внеклеточного матрикса, цитокинов, компонентов комплемента и иммуноглобулинов. Также называется стрептопаином. [21] |
| Стрептокиназа | Ферментативно активирует плазминоген , протеолитический фермент, в плазмин , который, в свою очередь, переваривает фибрин и другие белки. |
| Гиалуронидаза | Широко распространено мнение, что гиалуронидаза облегчает распространение бактерий по тканям, расщепляя гиалуроновую кислоту , важный компонент соединительной ткани . Однако очень немногие изоляты S. pyogenes способны секретировать активную гиалуронидазу из-за мутаций в гене, кодирующем этот фермент. Более того, немногим изолятам, способным секретировать гиалуронидазу, по-видимому, не требуется ее распространение через ткани или повреждение кожи. [22] Таким образом, истинная роль гиалуронидазы в патогенезе, если таковая имеется, остается неизвестной. |
| стрептодорназа | Большинство штаммов S. pyogenes секретируют до четырех различных ДНКаз , которые иногда называют стрептодорназой. ДНКазы защищают бактерии от попадания во внеклеточные ловушки нейтрофилов (NET), переваривая сеть ДНК NET, с которой связаны нейтрофилов сериновые протеазы , которые могут убивать бактерии. [23] |
| C5a пептидаза | Пептидаза C5a расщепляет мощный хемотаксин нейтрофилов , называемый C5a , который вырабатывается системой комплемента . [24] Пептидаза C5a необходима для минимизации притока нейтрофилов на ранних стадиях инфекции, когда бактерии пытаются колонизировать ткань хозяина. [25] Пептидаза C5a, хотя и необходима для разрушения нейтрофильного хемотаксина C5a на ранних стадиях инфекции, не требуется S. pyogenes для предотвращения притока нейтрофилов по мере распространения бактерий через фасцию . [26] |
| Стрептококковая хемокиновая протеаза | Пораженные ткани больных тяжелыми формами некротического фасциита лишены нейтрофилов. [27] Сериновая протеаза ScpC, выделяемая S. pyogenes , отвечает за предотвращение миграции нейтрофилов в зону распространения инфекции. ScpC разрушает хемокин IL-8 , который в противном случае привлек бы нейтрофилы к месту инфекции. [25] [26] |
Геном
[ редактировать ]Секвенированы геномы разных штаммов (размер генома 1,8–1,9 МБП). [28] кодирующий около 1700-1900 белков (1700 у штамма NZ131, [29] [30] 1865 г. в штамме MGAS5005 [31] [32] ). Полные последовательности генома типового штамма S. pyogenes ( NCTC 8198 Т = ККУГ 4207 Т ) доступны в Банке данных ДНК Японии , Европейском архиве нуклеотидов и GenBank под номерами доступа LN831034 и CP028841 . [33]
Образование биопленки
[ редактировать ]Биопленки — это способ общения S. pyogenes, как и других бактериальных клеток, друг с другом. В биопленке экспрессия генов для различных целей (например, защита от иммунной системы хозяина) контролируется посредством определения кворума . [34] Одним из путей формирования биопленок при GAS является путь Rgg2/3. Он регулирует SHP (короткие гидрофобные пептиды), которые являются феромонами, чувствительными к кворуму, также известными как аутоиндукторы. SHP транслируются в незрелую форму феромона и должны подвергнуться обработке сначала ферментом металлопротеазой внутри клетки, а затем во внеклеточном пространстве, чтобы достичь своей зрелой активной формы. Способ транспортировки из клетки и факторы внеклеточной обработки до сих пор неизвестны. Зрелый феромон SHP затем может быть перенесен в близлежащие клетки и в клетку, из которой он произошел, через трансмембранный белок, олигопептид-пермеазу. [34] В цитозоле феромоны выполняют две функции в пути Rgg2/3. Во-первых, они ингибируют активность Rgg3, который является регулятором транскрипции, подавляющим выработку SHP. Во-вторых, они связывают другой регулятор транскрипции, Rgg2, который увеличивает продукцию SHP, оказывая антагонистическое действие по отношению к Rgg3. SHP, активирующие свой собственный активатор транскрипции, создают петлю положительной обратной связи, которая является общей для производства пептидов, чувствительных к кворуму. Это позволяет быстро производить феромоны в больших количествах. Производство SHP увеличивает биогенез биопленок. [34] Было высказано предположение, что GAS переключается между образованием и деградацией биопленок, используя пути с противоположными эффектами. В то время как путь Rgg2/3 увеличивает биопленку, путь RopB разрушает ее. RopB — еще один Rgg-подобный белок (Rgg1), который непосредственно активирует SpeB (стрептококковый пирогенный экзотоксин B), цистеиновую протеазу, действующую как фактор вирулентности. В отсутствие этого пути образование биопленок усиливается, возможно, из-за отсутствия феромонов, разрушающих протеазу, или других эффектов, противодействующих пути Rgg2/3. [34]
Болезнь
[ редактировать ]S. pyogenes является причиной многих заболеваний человека, от легких поверхностных кожных инфекций до опасных для жизни системных заболеваний. [2] Наиболее частые проявления заболевания широко известны как скарлатина . Инфекции обычно начинаются в горле или на коже. Самый яркий признак — клубничная сыпь. Примеры легких инфекций, вызванных S. pyogenes, включают фарингит (ангиноз) и локализованную кожную инфекцию ( импетиго ). Рожистое воспаление и целлюлит характеризуются размножением и латеральным распространением S. pyogenes в глубокие слои кожи. Инвазия и размножение S. pyogenes в фасции подкожной может привести к некротизирующему фасцииту , опасному для жизни хирургическому вмешательству. [35] [36] Бактерия также является важной причиной инфекции у новорожденных , которые восприимчивы к некоторым формам инфекции, которые редко наблюдаются у взрослых, включая менингит . [37] [38]
Как и многие патогенные бактерии, S. pyogenes могут колонизировать дыхательную систему здорового человека, не вызывая заболевания. Он обычно встречается в некоторых популяциях как часть смешанного микробиома верхних дыхательных путей. Лица, у которых в организме есть бактерия, но нет признаков заболевания, называются бессимптомными носителями . [39] [40] [41] Бактерии могут начать вызывать заболевание, когда иммунная система хозяина ослабевает, например, во время респираторной вирусной инфекции, что может привести к S. pyogenes суперинфекции . [40] [41]
Инфекции, вызванные S. pyogenes, обычно связаны с выделением одного или нескольких бактериальных токсинов . Выброс эндотоксинов при инфекциях горла связан с развитием скарлатины. [7] Другие токсины, вырабатываемые S. pyogenes, могут привести к синдрому стрептококкового токсического шока , опасному для жизни состоянию. [2]
S. pyogenes также может вызывать заболевание в виде постинфекционных «негнойных» (не связанных с местным размножением бактерий и гноеобразованием) синдромов. Эти аутоиммунные осложнения возникают в небольшом проценте случаев инфекций и включают ревматическую лихорадку и острый постинфекционный гломерулонефрит . Оба состояния появляются через несколько недель после первоначальной стрептококковой инфекции. Ревматическая лихорадка характеризуется воспалением суставов и/или сердца после эпизода стрептококкового фарингита . Острый гломерулонефрит, воспаление почечных клубочков , может развиваться вследствие стрептококкового фарингита или кожной инфекции. [ нужна ссылка ]
Эта бактерия остается очень чувствительной к пенициллину . Неудача лечения пенициллином обычно объясняется другими местными комменсальными организмами, продуцирующими β-лактамазу , или неспособностью достичь адекватных уровней пенициллина в тканях глотки. Некоторые штаммы выработали устойчивость к макролидам , тетрациклинам и клиндамицину . [42]
Вакцина
[ редактировать ]Существует поливалентная инактивированная вакцина против нескольких типов стрептококков , включая S. pyogenes, называемая «vacuna antipiogena poliваленте BIOL». Ее рекомендуется вводить курсами по 5 недель. Два еженедельных применения производятся с интервалом от 2 до 4 дней. Вакцина производится Аргентинским биологическим институтом. [43]
Разрабатывается еще одна потенциальная вакцина; пептид-кандидат в вакцину называется StreptInCor. [44]
Приложения
[ редактировать ]Бионанотехнологии
[ редактировать ]Многие белки S. pyogenes обладают уникальными свойствами, которые в последние годы были использованы для производства высокоспецифичного «суперклея». [45] [46] и путь повышения эффективности терапии антителами . [47]
Редактирование генома
[ редактировать ]Система CRISPR этого организма [48] который используется для распознавания и уничтожения ДНК вторгшихся вирусов, тем самым останавливая инфекцию, был использован в 2012 году для использования в качестве инструмента редактирования генома, который потенциально может изменить любой фрагмент ДНК, а затем и РНК . [49]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ «Streptococcus pyogenes — Паспорта безопасности возбудителя» . Правительство Канады, Агентство общественного здравоохранения Канады. 26 сентября 2001 г.
- ^ Jump up to: а б с д и Райан К.Дж., Рэй К.Г., ред. (2004). Медицинская микробиология Шерриса (4-е изд.). МакГроу Хилл. ISBN 978-0-8385-8529-0 .
- ^ Спеллерберг Б., Брандт С. (9 октября 2022 г.) [Первоначально опубликовано 15 сентября 2022 г.]. «Глава 29: Лабораторная диагностика Streptococcus pyogenes (стрептококки группы А)» . В Ферретти Дж. Дж., Стивенсе Д. Л., Фишетти В. А. (ред.). Streptococcus pyogenes : от фундаментальной биологии до клинических проявлений (2-е изд.). Оклахома-Сити, США: Центр медицинских наук Университета Оклахомы. ПМИД 36479747 . Получено 11 мая 2023 г. - через Национальный центр биотехнологической информации Национальной медицинской библиотеки.
- ^ Азиз Р.К., Кансал Р., Аронов Б.Дж., Тейлор В.Л., Роу С.Л., Кубал М. и др. (апрель 2010 г.). Ахмед Н. (ред.). «Микроэволюция стрептококков группы А in vivo: захват регуляторных сетей, участвующих в социомикробиологии, адаптации ниши и гипервирулентности» . ПЛОС ОДИН . 5 (4): е9798. Бибкод : 2010PLoSO...5.9798A . дои : 10.1371/journal.pone.0009798 . ПМЦ 2854683 . ПМИД 20418946 .
- ^ Джим Дуайер (11 июля 2012 г.). «Инфекция, незамеченная, становится неудержимой» . Нью-Йорк Таймс . Проверено 12 июля 2012 г.
- ^ Джим Дуайер (18 июля 2012 г.). «После смерти мальчика больница изменила порядок выписки» . Нью-Йорк Таймс . Проверено 19 июля 2012 г.
- ^ Jump up to: а б Пардо С., Перера ТБ (2023 г.), «Скарлатина» , StatPearls , Остров сокровищ (Флорида): StatPearls Publishing, PMID 29939666 , получено 14 января 2024 г.
- ^ Гера К., МакИвер К.С. (октябрь 2013 г.). «Лабораторный рост и поддержание Streptococcus pyogenes (стрептококк группы А, ГАЗ)» . Современные протоколы в микробиологии . 30 : 9D.2.1–9D.2.13. дои : 10.1002/9780471729259.mc09d02s30 . ПМК 3920295 . ПМИД 24510893 .
- ^ Jump up to: а б с Андрулла Э., Тереза Л. (10 февраля 2016 г.). «Эпидемиология Streptococcus pyogenes» . Streptococcus pyogenes: от базовой биологии до клинических проявлений . Оклахома-Сити, США: Центр медицинских наук Университета Оклахомы. ПМИД 26866237 . Проверено 24 февраля 2018 г.
- ^ Танака Х., Кацураги С., Хасегава Дж., Танака К., Осато К., Наката М. и др. (январь 2019 г.). «Наиболее распространенными бактериями, вызывающими материнский сепсис, в Японии были стрептококки группы А: общенациональное исследование». Журнал инфекции и химиотерапии . 25 (1): 41–44. дои : 10.1016/j.jiac.2018.10.004 . ПМИД 30377069 .
- ^ Пиньянелли С., Бруса С., Пулькрано Г., Катания М.Р., Кокки Э., Ланари М. (октябрь 2015 г.). «Редкий случай детского сепсиса, вызванный генотипом emm-89 стрептококка группы А в внебольничном кластере». Новая микробиология . 38 (4): 589–592. ПМИД 26485019 .
- ^ Лансфилд RC (январь 1928 г.). «Антигенный комплекс Streptococcus Hæmolyticus» . Журнал экспериментальной медицины . 47 (1): 91–103. дои : 10.1084/jem.47.1.91 . ПМК 2131344 . ПМИД 19869404 .
- ^ Лэнсфилд Р.К., Доул В.П. (октябрь 1946 г.). «Свойства Т-антигенов, выделенных из гемолитических стрептококков группы А» . Журнал экспериментальной медицины . 84 (5): 449–471. дои : 10.1084/jem.84.5.449 . ПМК 2135665 . ПМИД 19871581 .
- ^ Мора М., Бенси Г., Капо С., Фалуги Ф., Зингаретти С., Манетти А.Г. и др. (октябрь 2005 г.). «Стрептококки группы А продуцируют пилообразные структуры, содержащие защитные антигены и Т-антигены Лансфилда» . Труды Национальной академии наук Соединенных Штатов Америки . 102 (43): 15641–15646. Бибкод : 2005PNAS..10215641M . дои : 10.1073/pnas.0507808102 . ПМЦ 1253647 . ПМИД 16223875 .
- ^ Ферретти Дж.Дж., МакШан В.М., Айдич Д., Савич Дж., Савич Дж., Лион К. и др. (апрель 2001 г.). «Полная последовательность генома штамма M1 Streptococcus pyogenes» . Труды Национальной академии наук Соединенных Штатов Америки . 98 (8): 4658–4663. Бибкод : 2001PNAS...98.4658F . дои : 10.1073/pnas.071559398 . ПМК 31890 . ПМИД 11296296 .
- ^ Канчая С., Дезиер Ф., МакШан В.М., Ферретти Дж.Дж., Паркхилл Дж., Брюссов Х. (октябрь 2002 г.). «Анализ генома индуцибельного профага и остатков профага, интегрированных в штамм Streptococcus pyogenes SF370» . Вирусология . 302 (2): 245–258. дои : 10.1006/виро.2002.1570 . ПМИД 12441069 .
- ^ Бэнкс DJ, Порселла С.Ф., Барбиан К.Д., Мартин Дж.М., Массер Дж.М. (декабрь 2003 г.). «Структура и распределение необычного химерного генетического элемента, кодирующего устойчивость к макролидам, в филогенетически разнообразных клонах стрептококка группы А» . Журнал инфекционных болезней . 188 (12): 1898–1908. дои : 10.1086/379897 . ПМИД 14673771 .
- ^ Паттерсон М.Дж. (1996). «Стрептококк» . У барона С; и др. (ред.). Стрептококк. В: Медицинская микробиология Барона (4-е изд.). Университет Техасского медицинского отделения. ISBN 978-0-9631172-1-2 .
- ^ Бисно А.Л., Брито М.О., Коллинз К.М. (апрель 2003 г.). «Молекулярные основы вирулентности стрептококка группы А». «Ланцет». Инфекционные болезни . 3 (4): 191–200. дои : 10.1016/S1473-3099(03)00576-0 . ПМИД 12679262 .
- ^ Энгель М.Э., Мухамед Б., Уайтлоу А.С., Мусвосви М., Майоси Б.М., Дейл Дж.Б. (февраль 2014 г.). «Распространенность стрептококка группы А среди детей с симптомами в Кейптауне и потенциальный охват вакцинацией» . Журнал детских инфекционных заболеваний . 33 (2): 208–210. дои : 10.1097/INF.0b013e3182a5c32a . ПМЦ 3947201 . ПМИД 23934204 .
- ^ Нельсон, округ Колумбия, Гарб Дж., Коллин М. (декабрь 2011 г.). «Цистеиновая протеиназа SpeB из Streptococcus pyogenes - мощный модификатор иммунологически важных белков хозяина и бактерий» . Биологическая химия . 392 (12): 1077–1088. дои : 10.1515/BC.2011.208 . ПМИД 22050223 . S2CID 207441558 .
- ^ Старр ЧР, Энглеберг, Северная Каролина (январь 2006 г.). «Роль гиалуронидазы в подкожном распространении и росте стрептококка группы А» . Инфекция и иммунитет . 74 (1): 40–48. дои : 10.1128/IAI.74.1.40-48.2006 . ПМК 1346594 . ПМИД 16368955 .
- ^ Бьюкенен Дж.Т., Симпсон А.Дж., Азиз Р.К., Лю Г.И., Кристиан С.А., Котб М. и др. (февраль 2006 г.). «Экспрессия ДНКазы позволяет стрептококку группы А избежать уничтожения во внеклеточных ловушках нейтрофилов». Современная биология . 16 (4): 396–400. Бибкод : 2006CBio...16..396B . дои : 10.1016/j.cub.2005.12.039 . ПМИД 16488874 . S2CID 667804 .
- ^ Векслер Д.Э., Ченовет Д.Е., Клири П.П. (декабрь 1985 г.). «Механизм действия стрептококкового инактиватора C5a группы А» . Труды Национальной академии наук Соединенных Штатов Америки . 82 (23): 8144–8148. Бибкод : 1985PNAS...82.8144W . дои : 10.1073/pnas.82.23.8144 . ПМЦ 391459 . ПМИД 3906656 .
- ^ Jump up to: а б Джи Й, МакЛэндсборо Л., Кондагунта А., Клири П.П. (февраль 1996 г.). «Пептидаза C5a изменяет выведение и транспортировку стрептококков группы А инфицированными мышами» . Инфекция и иммунитет . 64 (2): 503–510. дои : 10.1128/IAI.64.2.503-510.1996 . ПМЦ 173793 . ПМИД 8550199 .
- ^ Jump up to: а б Идальго-Грасс С., Мишалян И., Дан-Гур М., Белоцерковский И., Эран Ю., Низет В. и др. (октябрь 2006 г.). «Стрептококковая протеаза, которая разрушает хемокины CXC и ухудшает выведение бактерий из инфицированных тканей» . Журнал ЭМБО . 25 (19): 4628–4637. дои : 10.1038/sj.emboj.7601327 . ПМК 1589981 . ПМИД 16977314 .
- ^ Идальго-Грасс С., Дэн-Гур М., Мали А., Эран Ю., Квинн Л.А., Низет В. и др. (февраль 2004 г.). «Влияние бактериального феромонного пептида на деградацию хемокинов хозяина при стрептококковых некротизирующих инфекциях мягких тканей». Ланцет . 363 (9410): 696–703. дои : 10.1016/S0140-6736(04)15643-2 . ПМИД 15001327 . S2CID 7219898 .
- ^ Берес С.Б., Рихтер Э.В., Нагиек М.Дж., Самби П., Порселла С.Ф., ДеЛео Ф.Р., Массер Дж.М. (май 2006 г.). «Молекулярно-генетическая анатомия меж- и внутрисеротипической изменчивости бактериального возбудителя группы А человека стрептококка» . Труды Национальной академии наук Соединенных Штатов Америки . 103 (18): 7059–7064. Бибкод : 2006PNAS..103.7059B . дои : 10.1073/pnas.0510279103 . ПМК 1459018 . ПМИД 16636287 .
- ^ «Streptococcus pyogenes NZ131» .
- ^ МакШан В.М., Ферретти Дж.Дж., Карасава Т., Суворов А.Н., Лин С., Цинь Б. и др. (декабрь 2008 г.). «Последовательность генома нефритогенного и высокотрансформируемого штамма M49 Streptococcus pyogenes» . Журнал бактериологии . 190 (23): 7773–7785. дои : 10.1128/JB.00672-08 . ПМЦ 2583620 . ПМИД 18820018 .
- ^ Сумби П., Порселла С.Ф., Мадригал А.Г., Барбиан К.Д., Виртанева К., Риклефс С.М. и др. (сентябрь 2005 г.). «Эволюционное происхождение и появление весьма успешного клона стрептококка серотипа М1 группы А включало множественные события горизонтального переноса генов» . Журнал инфекционных болезней . 192 (5): 771–782. дои : 10.1086/432514 . ПМИД 16088826 .
- ^ «Streptococcus pyogenes MGAS5005» .
- ^ Сальва-Серра Ф., Хаэн-Лучоро Д., Якобссон Х.Э., Гонсалес-Силес Л., Карлссон Р., Бускетс А. и др. (июль 2020 г.). «Полные последовательности генома типового штамма Streptococcus pyogenes показывают 100% совпадение между гибридными сборками PacBio-solo и Illumina-Oxford Nanopore» . Научные отчеты . 10 (1): 11656. doi : 10.1038/s41598-020-68249-y . ПМЦ 7363880 . ПМИД 32669560 .
- ^ Jump up to: а б с д Чанг Х.К., ЛаСарр Б., Хименес Х.К., Аггарвал К., Федерле М.Дж. (август 2011 г.). «Два пептидных феромона стрептококка А действуют через противоположные регуляторы Rgg, контролируя развитие биопленки» . ПЛОС Патогены . 7 (8): e1002190. дои : 10.1371/journal.ppat.1002190 . ПМК 3150281 . ПМИД 21829369 .
- ^ Шредер Дж.Л., Стейнке Э.Э. (декабрь 2005 г.). «Некротический фасциит - важность ранней диагностики и хирургической обработки». Журнал АОРН . 82 (6): 1031–1040. дои : 10.1016/s0001-2092(06)60255-x . ПМИД 16478083 .
- ^ «Некротический фасциит» . CDC . Источник контента: Национальный центр иммунизации и респираторных заболеваний, Отдел бактериальных заболеваний. Страница поддерживается: Офисом заместителя директора по коммуникациям, Отдел цифровых медиа, Отдел по связям с общественностью. 26 октября 2017 г. Проверено 6 января 2018 г.
- ^ Бауселс Б.Дж., Меркадаль Халли М., Альварес Санчес А.Т., Фигерас Алой Дж. (ноябрь 2016 г.). в профилактике некротизирующего энтероколита и снижении сепсиса с поздним «Пробиотические ассоциации началом и неонатальной смертности у недоношенных детей с массой тела менее 1500 г: систематический обзор». Анналы педиатрии (на испанском языке). 85 (5): 247–255. дои : 10.1016/j.anpedi.2015.07.038 . ПМИД 26611880 .
- ^ Бернер Р., Хердег С., Горджани Н., Брэндис М. (июль 2000 г.). «Менингит, вызванный Streptococcus pyogenes: отчет о случае и обзор литературы». Европейский журнал педиатрии . 159 (7): 527–529. дои : 10.1007/s004310051325 . ПМИД 10923229 . S2CID 7693087 .
- ^ Хунг Т., Фуонг Л.К., Гроблер А., Тонг С.Ю., Фрит П., Пеленда А., Гибни К.Б., Стир AC (март 2024 г.). «Антибиотики для ликвидации глоточного носительства Streptococcus pyogenes у бессимптомных детей и взрослых: систематический обзор» . Дж. Заразить . 88 (3): 106104. doi : 10.1016/j.jinf.2024.01.003 . ПМИД 38360357 .
- ^ Jump up to: а б Осман А.М., Ассайаги Р.М., Аль-Шами Х.З., Саиф-Али Р. (июнь 2019 г.). «Бессимптомное носительство Streptococcus pyogenes среди школьников города Сана, Йемен» . Исследовательские заметки BMC . 12 (1): 339. doi : 10.1186/s13104-019-4370-5 . ПМК 6570875 . ПМИД 31200755 .
- ^ Jump up to: а б Оливер Дж., Маллия Ваду Э., Пирс Н., Морленд Нью-Джерси, Уильямсон Д.А., Бейкер М.Г. (март 2018 г.). «Фарингит, вызванный стрептококком группы А, и глоточное носительство: метаанализ» . PLOS Забытые тропические болезни . 12 (3): e0006335. дои : 10.1371/journal.pntd.0006335 . ПМЦ 5875889 . ПМИД 29554121 .
- ^ Тадессе, Молла (март 2023 г.). «Распространенность, профиль чувствительности к антибиотикам и связанные факторы стрептококкового фарингита группы А среди педиатрических пациентов с острым фарингитом в Гондаре, северо-запад Эфиопии» . Инфекции и устойчивость к лекарствам . 16 : 1637–1648. дои : 10.2147/IDR.S402292 . ПМК 40342 . ПМИД 36992964 .
- ^ «Информация об упаковке на официальном сайте БИОЛ» (PDF) . Архивировано (PDF) из оригинала 10 октября 2022 г.
- ^ Гильерме Л., Феррейра Ф.М., Кёлер К.Ф., Постол Э., Калил Дж. (февраль 2013 г.). «Вакцина против Streptococcus pyogenes: потенциал предотвращения ревматизма и ревматической болезни сердца» . Американский журнал сердечно-сосудистых препаратов . 13 (1): 1–4. дои : 10.1007/s40256-013-0005-8 . ПМИД 23355360 . S2CID 13071864 .
- ^ Ховарт М. (май 2017 г.). «Умный суперклей в стрептококках? Доказательство — в выдергивании» . Журнал биологической химии . 292 (21): 8998–8999. дои : 10.1074/jbc.H117.777466 . ПМЦ 5448131 . ПМИД 28550142 .
- ^ Закери Б., Фиерер Дж.О., Челик Э., Читток Э.К., Шварц-Линек У., Мой В.Т., Ховарт М. (март 2012 г.). «Пептидная метка, образующая быструю ковалентную связь с белком посредством создания бактериального адгезина» . Труды Национальной академии наук Соединенных Штатов Америки . 109 (12): E690–E697. Бибкод : 2012PNAS..109E.690Z . дои : 10.1073/pnas.1115485109 . ПМК 3311370 . ПМИД 22366317 .
- ^ Баруа К., Боуден Т.А., Кришна Б.А., Двек Р.А., Криспин М., Сканлан К.Н. (июнь 2012 г.). «Селективная дезактивация сывороточных IgG: общая стратегия усиления взаимодействия рецепторов моноклональных антител» . Журнал молекулярной биологии . 420 (1–2): 1–7. дои : 10.1016/j.jmb.2012.04.002 . ПМЦ 3437440 . ПМИД 22484364 .
- ^ Дельчева Е., Чилински К., Шарма С.М., Гонсалес К., Чао Ю., Пирзада З.А. и др. (март 2011 г.). «Созревание РНК CRISPR с помощью транскодируемой малой РНК и фактора хозяина РНКазы III» . Природа . 471 (7340): 602–607. Бибкод : 2011Natur.471..602D . дои : 10.1038/nature09886 . ПМК 3070239 . ПМИД 21455174 .
- ^ Циммер С. (3 июня 2016 г.). «Ученые открывают новые возможности редактирования генов Crispr» . Нью-Йорк Таймс . ISSN 0362-4331 . Проверено 10 июня 2016 г.
Дальнейшее чтение
[ редактировать ]- Фрайберг Дж. А., Макивер К. С., Ширтлифф М. Е. (сентябрь 2014 г.). «Экспрессия in vivo иммуногенных белков Streptococcus pyogenes во время инфекции инородного тела большеберцовой кости» . Инфекция и иммунитет . 82 (9): 3891–3899. дои : 10.1128/IAI.01831-14 . ПМК 4187806 . ПМИД 25001603 .
- Розенбах Ф.Дж. (1884 г.). Микроорганизмы при раневых инфекционных заболеваниях человека (на немецком языке). Дж. Ф. Бергман. ОЛ22886502М .
- Уилсон Л.Г. (октябрь 1987 г.). «Раннее распознавание стрептококков как причин заболеваний» . Медицинская история . 31 (4): 403–414. дои : 10.1017/s0025727300047268 . ПМЦ 1139783 . ПМИД 3316876 .
- Роллстон Дж.Д. (ноябрь 1928 г.). «История скарлатины» . Британский медицинский журнал . 2 (3542): 926–929. дои : 10.1136/bmj.2.3542.926 . ПМК 2456687 . ПМИД 20774279 .
- Всемирная организация здравоохранения (2005). «Современные данные о бремени стрептококковых заболеваний группы А» . Архивировано из оригинала (PDF) 12 марта 2008 г. Проверено 22 августа 2011 г.
- Карапетис-младший, Стир А.К., Малхолланд Э.К., Вебер М. (ноябрь 2005 г.). «Глобальное бремя стрептококковых заболеваний группы А». «Ланцет». Инфекционные болезни . 5 (11): 685–694. дои : 10.1016/S1473-3099(05)70267-X . ПМИД 16253886 . (соответствующая сводная статья)
- Ферретти Дж.Дж., Стивенс Д.Л., Фишетти В.А. (2016). Streptococcus pyogenes: от базовой биологии до клинических проявлений [Интернет] . Оклахома-Сити, Оклахома: Центр медицинских наук Университета Оклахомы. ПМИД 26866208 .
Внешние ссылки
[ редактировать ]- Типовой штамм Streptococcus pyogenes в Bac Dive - база метаданных по бактериальному разнообразию
- Вдохновленные природой открытия фермента CRISPR значительно расширяют возможности редактирования генома . На: SciTechDaily. 16 июня 2020 г. Источник: Медиа-лаборатория Массачусетского технологического института.