Clostridioides difficile
| Clostridioides difficile | |
|---|---|
 | |
| C. difficile Колонии на пластинке с кровяным агаром | |
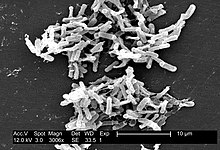 | |
| Электронная микрофотография бактерии | |
| Научная классификация | |
| Домен: | Бактерии |
| Тип: | Бациллота |
| Сорт: | Клостридии |
| Заказ: | Эубактерии |
| Семья: | Пептострептококковые |
| Род: | Клостридиоиды |
| Разновидность: | C. трудный |
| Биномиальное имя | |
| Clostridioides difficile (Холл и О'Тул, 1935 г.) Лоусон и Рейни, 2016 г. | |
| Синонимы | |
Clostridioides difficile ( син. Clostridium difficile ) — бактерия, известная тем, что вызывает серьезные диарейные инфекции, а также может вызывать рак толстой кишки . [4] [5] Он известен также как C. difficile или C. diff ( / s iː d ɪ f / ) и представляет собой грамположительный вид бактерий спорообразующих . [6] Clostridioides spp. являются анаэробными , подвижными бактериями, повсеместно распространенными в природе и особенно распространенными в почве. Вегетативные клетки палочковидные, плеоморфные , встречаются парами или короткими цепочками. Под микроскопом они выглядят как длинные клетки неправильной формы (часто в форме голени или веретена) с выпуклостью на конце (образуют субтерминальные споры). При окрашивании по Граму клетки C. difficile являются грамположительными и демонстрируют оптимальный рост на кровяном агаре при температуре человеческого тела в отсутствие кислорода . C. difficile является каталазо- и супероксиддисмутазо -отрицательным и продуцирует до трех типов токсинов: энтеротоксин А , цитотоксин В и трансферазу Clostridioides difficile. [7] В условиях стресса бактерии производят споры , способные переносить экстремальные условия, которые активные бактерии не переносят. [8]
Clostridioides difficile – важный новый патоген человека ; По данным CDC , в 2017 году в США было зарегистрировано 223 900 случаев госпитализации пациентов и 12 800 смертей. [9] Хотя C. difficile широко известен как больничный и антибиотикоассоциированный патоген, не более трети инфекций можно объяснить передачей инфекции от инфицированного человека в больницах. [10] и лишь небольшое количество антибиотиков напрямую связано с повышенным риском развития C. difficile инфекции (CDI), а именно ванкомицин , клиндамицин , фторхинолоны и цефалоспорины . [11] [12] [13] Большинство инфекций приобретается вне больниц, и большинство антибиотиков имеют такой же повышенный риск заражения, как и многие неантибиотические факторы риска, такие как использование размягчителей стула и установка клизмы . [14]
Clostridioides difficile также может проникать в толстую кишку человека , не вызывая заболевания. [15] Хотя ранние оценки показали, что C. difficile присутствует у 2–5% взрослого населения, [8] более поздние исследования показывают, что колонизация тесно связана с историей несвязанных диарейных заболеваний, таких как пищевое отравление или злоупотребление слабительными . [16] Маловероятно, что лица, у которых в анамнезе не было желудочно-кишечных расстройств, станут бессимптомными носителями. Считается, что эти носители являются основным резервуаром инфекции. [17]
Таксономия
[ редактировать ]Вид был переведен из рода Clostridium в Clostridioides в 2016 году, что дало ему биномиальное название Clostridioides difficile . [18] [19] [20] Это новое название отражает таксономические различия между этим видом и представителями рода Clostridium , сохраняя при этом общее название C. diff . [19] По состоянию на 2018 год [update], единственным другим видом этого нового рода является Clostridioides mangenotii (ранее известный как Clostridium mangenotii ). [21]
Человеческий патоген
[ редактировать ]Патогенные штаммы C. difficile продуцируют множество токсинов . [22] Наиболее изученными являются энтеротоксин ( C. difficile токсин A ) и цитотоксин ( C. difficile токсин B ), оба из которых могут вызывать диарею и воспаление у инфицированных пациентов ( C. difficile колит ), хотя их относительный вклад обсуждается. Диарея может варьироваться от потери кишечной жидкости в течение нескольких дней до опасного для жизни псевдомембранозного колита , который связан с интенсивным воспалением толстой кишки и образованием псевдомембран на поверхности слизистой оболочки кишечника. [8] Это может прогрессировать до токсического мегаколона , тяжелой формы вздутия толстой кишки, которая может подвергнуть пациента риску перфорации толстой кишки, сепсиса и шока. Токсины А и В представляют собой глюкозилтрансферазы, которые нацелены и инактивируют семейство ГТФаз Rho . Токсин B (цитотоксин) индуцирует деполимеризацию актина по механизму, коррелирующему со снижением АДФ-рибозилирования низкомолекулярных GTP-связывающих Rho-белков. [23] Существует также бинарный токсин ( АТ-токсин ), но его роль в заболевании до конца не изучена. [24]
Дополнительные факторы вирулентности включают фактор адгезии, который опосредует связывание с клетками толстой кишки человека, и гиалуронидазу . [25] Бактерия также производит химическое вещество , паракрезол которое подавляет рост других микробов поблизости и позволяет ей вытеснять нормальную кишечную флору человека. [26]
Устойчивость к противомикробным препаратам
[ редактировать ]антибиотиками Лечение инфекций, вызванных C. diff , может быть затруднено как из-за устойчивости к антибиотикам, так и из-за физиологических факторов бактерии (образование спор, защитное действие псевдомембраны). [8] В 2005 году сообщалось о появлении нового высокотоксичного штамма C. difficile , устойчивого к фторхинолоновым антибиотикам, таким как ципрофлоксацин и левофлоксацин , который, как утверждается, вызывает географически рассредоточенные вспышки в Северной Америке. [27] США Центры по контролю заболеваний в Атланте предупредили о появлении эпидемического штамма с повышенной вирулентностью, устойчивостью к антибиотикам или тем и другим. [28] Устойчивость к другим антибиотикам, таким как метронидазол, противомикробный препарат первого выбора при лечении ИКД, наблюдалась у до 12% клинических изолятов, поэтому по мере продолжения лечения различными антибиотиками у C. difficile , что еще больше усложняет попытки эффективного лечения. [29]
Дезинфекция поверхностей в больницах также может быть сложной задачей, поскольку C. difficile споры устойчивы ко многим дезинфицирующим средствам . [30] включая высокие концентрации отбеливателя . [31]
Передача инфекции
[ редактировать ]
Clostridioides difficile передается от человека или животного к человеку фекально-оральным путем , через фекалии. Организм образует термостойкие аэротолерантные споры, которые не уничтожаются чистящими средствами для рук на спиртовой основе или обычной очисткой поверхностей, поэтому эти споры выживают в клинических условиях в течение длительного времени. [32] Любая поверхность, устройство или материал (например, туалеты, ванны и электронные ректальные термометры), загрязненные фекалиями, могут служить резервуаром для спор C. difficile , а споры C. difficile могут жить в течение длительного периода времени на поверхности. [33] Благодаря этому бактерию можно культивировать практически с любой поверхности. После попадания спор в организм их кислотоустойчивость позволяет им пройти через желудок невредимыми. Они прорастают и размножаются в вегетативные клетки толстой кишки под воздействием желчных кислот. Следовательно, Всемирная организация здравоохранения выступает за использование мыла в дополнение к спиртовым растворам, чтобы ограничить распространение спор. [34] Было показано, что споруляция значительно снижается после инактивации C. difficile . ДНК-метилтрансферазы CamA [35] поднимая перспективу разработки препарата, который мог бы ингибировать эту бактерию определенным образом.
Восприимчивость к колонизации, по-видимому, вызвана диарейными заболеваниями, такими как пищевое отравление , болезнь Крона или злоупотребление слабительными; люди, не страдавшие диарейными заболеваниями и подвергшиеся воздействию спор C. difficile, не обязательно станут носителями. [16] После колонизации людей C. difficile они остаются носителями в течение года, но ежедневная численность C. difficile значительно колеблется – от уровня ниже предела обнаружения до высоких уровней выделения от одного дня. к следующему. Нарушения желудочно-кишечного тракта у носителей, по-видимому, вызывают периоды повышенного выделения вируса, что может быть важным фактором передачи вируса. [ нужна ссылка ]
Диапазон хостов
[ редактировать ]Clostridioides difficile инфицирует свиней, телят и людей и обитает в естественных резервуарах почвы, фекалиях домашних животных и людей, сточных водах, кишечном тракте человека и мясной продукции, продаваемой в розничной торговле. [36]
По оценкам исследования CDC 2015 года, C. diff поразил почти полмиллиона американцев и стал причиной 29 000 смертей в 2011 году. По оценкам исследования, 40% случаев начались в домах престарелых или общественных медицинских учреждениях, а 24% - в больницах. [37]
Clostridioides difficile часто встречается в пищеварительной системе человека. Однако это плохой конкурент, и его часто вытесняют другие бактерии пищеварительной системы за питательные вещества. В результате количество C. difficile сохраняется на управляемом уровне. Если внезапное введение антибиотика нарушает микробиом, C. difficile может вырасти в результате уничтожения многих его конкурентов. Инкубационный период после лечения антибиотиками диареи, связанной с антибиотиками, составляет 5–10 дней и варьируется от 1 дня до нескольких недель. Кроме того, у детей раннего возраста часто встречается носительство C. difficile с высоким уровнем токсинов, тогда как заболевание встречается редко. Выработка одного или даже обоих токсинов не всегда достаточна для возникновения симптомов. [38]
Признаки и симптомы
[ редактировать ]Симптомы инфекции C. difficile включают диарею (не менее трех раз в день), обезвоживание, боли в животе , которые могут быть очень сильными, потерю аппетита и тошноту. [39]
Патофизиология
[ редактировать ]C. difficile передается орально-фекальным путем, многие из них размножаются спорами. Прорастание этих спор зависит от способности воспринимать первичные желчные кислоты в печени, такие как таурохолат, которые воспринимаются герминантным рецептором CspC. Вторичные желчные кислоты могут ингибировать эти процессы в толстой кишке. Споры могут расти и колонизировать кишечник в результате вызванных антибиотиками изменений в микробиоте хозяина. C. difficile секретирует муколитические ферменты, такие как CWp84, которые разрушают слизистую оболочку толстой кишки. Эти споры также способны прикрепляться к клеткам толстой кишки. Кроме того, C. difficile — это подвижная бактерия, которая может переключаться между подвижной и сидячей фазами — процесс, регулируемый циклическим ди-ГМФ. Кроме того, C. difficile способен образовывать биопленки и передавать сигналы от клетки к клетке. [40] C. difficile часто передается от других пациентов через руки медицинских работников или из общей больничной среды и приобретается при проглатывании возбудителя. Споры устойчивы к кислотности желудка и прорастают в вегетативную форму в тонком кишечнике. C. difficile может иметь широкий спектр клинических проявлений: от бессимптомного течения до тяжелого колита и смерти. [41] Таким образом, C. difficile является наиболее распространенной инфекцией в здравоохранении США, создавая серьезные риски для здоровья и значительные расходы на лечение. [42]
Иммунный ответ хозяина
[ редактировать ]Секретируемые C. difficile токсины A (TcdA) и B (TcdB) содержат иммуногенные антигены, которые распознаются антителами и Т-клетками. Однако уровни антител IgG против TcdA и -TcdB не позволяют отличить здоровых людей от пациентов с инфекцией C. difficile , а это означает, что они имеют ограниченное клиническое применение. [43] [44] эти токсины также распознаются Т-хелперными клетками CD4+, преимущественно хелперными , Недавние исследования показали, что клетками Th17 которые важны для поддержания здоровой среды кишечника, хотя у пациентов с тяжелой инфекцией эти клетки повреждены. [45] Интересно, что у людей с тяжелой инфекцией C. difficile было значительно больше токсин-специфичных Т-клеток по сравнению с людьми с легкой инфекцией, что указывает на то, что Т-клетки играют ключевую роль в борьбе с этой инфекцией. Этот иммунный ответ может еще больше нарушить регуляцию экспрессии микроРНК . [46] Об этом также свидетельствует восстановление токсин-специфичных клеток Th17 и экспрессия микроРНК после трансплантации фекальной микробиоты пациентов с тяжелым заболеванием. [46] [47] Новые данные показывают, что потеря интерлейкина-10 соответствует более высоким уровням интерлейкина-22, который, как было установлено, играет важную роль в ответе хозяина на инфекцию C.difficile. Таким образом, дефицит IL-10 может повысить защиту хозяина от патогена. Это может представлять особый интерес для будущих исследований методов лечения. [48]
Диагностика
[ редактировать ]Инфекцию C. difficile часто подозревают из-за диареи с неприятным запахом, но это не подтверждает наличие у пациента ИКД. Для подтверждения CDI анализ цитотоксинов выявляет цитотоксичность клеточного токсина B (ToxB) в фекальном элюате. Наличие токсина C. difficile подтверждается нейтрализацией цитотоксического действия антителами к токсину. Штаммы C. difficile также можно культивировать перед проведением анализа цитотоксина. Эти культуры обнаруживают штамм C. difficile, который может продуцировать токсины. [49] Однако эти иммуноферментные анализы используются более широко из-за их быстрого выполнения, низкой стоимости и простоты. Кроме того, они демонстрируют более низкую чувствительность, чем токсигенные культуры кала. ПЦР-анализы имеют более короткое время выполнения и более высокий диапазон чувствительности, чем токсигенный посев кала. Использование анализа на основе ПЦР помогает избежать выявления бессимптомных пациентов. [41]
Уход
[ редактировать ]Пациенты, получающие лечение антибиотиками, при появлении симптомов должны прекратить их прием, если это возможно. Этот перерыв в антибиотикотерапии иногда может привести к спонтанному разрешению симптомов. Пациентов, которые не реагируют на прекращение приема антибиотиков широкого спектра действия, необходимо лечить антибиотиками, способными убивать споры C. difficile . Первичные инфекции обычно лечат ванкомицином в обычной дозе 125 мг каждые 6 часов. [50] Режим ванкомицина заменил традиционное использование метронидазола благодаря его большей эффективности, профилю безопасности и более низкой частоте рецидивов. У пациентов, которые не переносят ванкомицин, фидаксомицин является приемлемым вариантом с такой же эффективностью и даже более низкой частотой рецидивов, чем ванкомицин. [51] В случаях молниеносной ИКД рекомендуется адъювантная терапия парентеральным метронидазолом плюс пероральный ванкомицин или фидаксомицин. [52]
Примерно 15-30% [53] пациентов, успешно завершивших терапию первичной инфекции метронидазолом или ванкомицином, произойдет рецидив . Около 40% этих пациентов будут продолжать болеть рецидивирующей инфекцией C. difficile . Первый рецидив C. difficile обычно лечат тем же антибиотиком, который использовался для лечения первичной инфекции. Любые последующие инфекции не следует лечить метронидазолом. Иногда стандартный 10-дневный курс перорального ванкомицина не помогает. В этих случаях предпочтительным лечением является снижение дозы ванкомицина. Пациенты принимают уменьшающиеся дозы ванкомицина в течение периода до 3 месяцев, в зависимости от тяжести инфекции. [39]
Каждый последующий рецидив C. difficile имеет тенденцию быть более тяжелым, чем предыдущие инфекции. Длительное лечение постепенной дозой ванкомицина с добавлением пробиотиков, особенно Saccharomyces boulardii , связано с более высоким уровнем успеха. [54]
После трех рецидивов пациентов можно лечить пероральным фидаксомицином , антибиотиком узкого спектра действия. Обычная дозировка составляет 200 мг два раза в день перорально в течение 10 дней. Считается, что фидаксомицин превосходит ванкомицин при тяжелой ИКД. [55] Основным недостатком лечения фидаксомицином является стоимость лекарства. 10-дневный курс может стоить до 3500 долларов США. [ нужна ссылка ] Когда состояние пациента ухудшается или прогрессирует до тяжелого осложнения, целесообразно рассмотреть возможность добавления внутривенного тигециклина. [56] [57] Пациентам с высоким риском рецидива также может быть полезно добавление моноклонального антитела безлотоксумаба к стандартному лечению. [58]
Пациенты, которые не реагируют на традиционную антибиотикотерапию, могут иметь право на трансплантацию фекальной микробиоты (ТФМ). Медицинские работники могут перенести кал здорового человека в толстую кишку пациента с рецидивирующей ИКД. Этот процесс является наиболее успешным методом лечения тяжелой ИКД с уровнем излечения около 93%. Трансплантация фекалий также оказалась эффективным и безопасным вариантом лечения для детей и молодых людей. [59] Частота рецидивов ИКД у пациентов, получавших ТФМ, обычно низкая, около 19%, что делает ее очень эффективной при лечении хронических случаев ИКД. Однако в некоторых случаях обострение воспалительного заболевания кишечника является возможным побочным эффектом лечения. [60] Состояние иммунной системы хозяина важно при рассмотрении успеха лечения на основе микробиоты в устранении инфекции. [61] Долгосрочные эффекты ТФМ неизвестны, поскольку эта процедура была одобрена FDA только для лечения рецидивирующей ИКД с 2013 года, и было выполнено относительно мало процедур. Если трансплантация невозможна, удаление инфицированной части толстой кишки может вылечить ИКД. [55] [39]
Прогнозирование рецидива C. difficile представляло большой интерес, но не было единого мнения относительно существенно связанных с ним факторов риска. [62]
Профилактика
[ редактировать ]Инфекция C. difficile распространяется фекально-оральным путем через пищеварение и кислотоустойчивые споры. Соответствующая гигиена рук медицинских работников имеет жизненно важное значение для удаления спор, которая включает тщательное мытье рук с мылом и теплой водой. Кроме того, изоляция пациентов с острой диареей может предотвратить распространение спор внутри больницы. [63] Еще один способ предотвращения ИКД – ношение средств индивидуальной защиты при общении с пациентами, зараженными C. difficile. Кроме того, передачу ИКД можно предотвратить путем ежедневной спорицидной дезинфекции окружающей среды в палатах пациентов. Кроме того, сокращение продолжительности антибиотикотерапии снижает частоту ИКД в больницах. [64]
Штаммы
[ редактировать ]В 2005 году молекулярный анализ привел к идентификации типа штамма C. difficile , охарактеризованного как группа BI с помощью эндонуклеазного анализа рестрикции, как североамериканский NAP1 типа импульсного поля с помощью гель-электрофореза в импульсном поле и как риботип 027; Различная терминология отражает преобладающие методы, используемые для эпидемиологического типирования. Этот штамм называется C. difficile BI/NAP1/027. [49]
По состоянию на 2016 год штамм NAP1 был заменен новыми штаммами в некоторых районах Британской Колумбии. Эти новые штаммы включают NAP2 и NAP4, а также некоторые штаммы, не имеющие обозначения NAP. Частота появления этих новых штаммов увеличилась с 2008 по 2013 год в одном изученном регионе, вытеснив первоначально более распространенные и узнаваемые бактерии NAP1. [65]
Два штамма, риботипы RT078 и RT027, могут жить при низких концентрациях сахарной трегалозы ; Оба штамма стали более распространенными после того, как трегалоза была введена в качестве пищевой добавки в начале 2000-х годов, что привело к увеличению потребления трегалозы с пищей. [66]
Геном
[ редактировать ]| NCBI Идентификатор генома | 535 |
|---|---|
| Плоидность | гаплоидный |
| Размер генома | 4,3 Мб |
| Количество хромосом | 1 |
| Год завершения | 2005 |
Первая полная последовательность генома штамма C. difficile была опубликована в 2005 году Институтом Сэнгера в Великобритании. Это был штамм 630, вирулентный штамм с множественной лекарственной устойчивостью, выделенный в Швейцарии в 1982 году. Ученые из Института Сэнгера секвенировали геномы около 30 изолятов C. difficile нового поколения , используя технологии секвенирования от 454 Life Sciences и Illumina . [67]
Исследователи из Университета Макгилла в Монреале секвенировали геном высоковирулентного квебекского штамма C. difficile в 2005 году, используя технологию сверхвысокопроизводительного секвенирования. Тесты включали проведение 400 000 реакций параллельного секвенирования ДНК генома бактерии, который был фрагментирован для секвенирования. Эти последовательности были собраны с помощью вычислений, чтобы сформировать полную последовательность генома. [27] [68]
В 2012 году ученые Оксфордского университета секвенировали геномы C. difficile из 486 случаев, возникших за четыре года в Оксфордшире, используя технологии секвенирования нового поколения от Illumina. [69]
Эпигеном
[ редактировать ]Clostridioides difficile имеет весьма разнообразный эпигеном: на данный момент зарегистрировано 17 высококачественных мотивов метилирования, большинство из которых относятся к типу 6mA. Было показано, что метилирование одного из этих мотивов - CAAAA A - влияет на споруляцию, ключевой этап передачи заболевания C. difficile , а также на длину клеток, образование биопленок и колонизацию хозяина. [35]
Бактериофаг
[ редактировать ]по меньшей мере восемь преимущественно умеренного климата бактериофагов было выделено Из C. difficile с размером генома от примерно 30 до примерно т.п.н. 60 [70] , полученные как из окружающей среды, так и из клинических источников, Штаммы C. difficile несут разнообразный и распространенный набор профагов . [70]
Этимология и произношение
[ редактировать ]Ссылки
[ редактировать ]- ^ Холл IC, О'Тул Э (1935). «Кишечная флора у новорожденных: с описанием нового патогенного анаэроба Bacillus difficilis ». Американский журнал болезней детей . 49 (2): 390–402. дои : 10.1001/archpedi.1935.01970020105010 .
- ^ Прево А.Р. (1938). «Исследования по бактериальной систематике. IV. Критика современной концепции рода Clostridium » . Анналы Института Пастера . 61 (1): 84. Архивировано из оригинала 28 июля 2020 года . Проверено 15 декабря 2018 г.
- ^ Страница Виды: Clostridioides difficile на «ЛПСН - Список названий прокариот, стоящих в номенклатуре» . Немецкая коллекция микроорганизмов и клеточных культур . Архивировано из оригинала 8 ноября 2022 года . Проверено 8 ноября 2022 г.
- ^ Древес Дж.Л., Чен Дж., Маркхэм Н.О., Книппель Р.Дж., Доминг Дж.К., Тэм А.Дж. и др. (август 2022 г.). «Штаммы Clostridioides difficile, полученные из рака толстой кишки человека, вызывают опухоль толстой кишки у мышей» . Открытие рака . 12 (8): 1873–1885. дои : 10.1158/2159-8290.CD-21-1273 . ПМЦ 9357196 . PMID 35678528 .
- ^ «Врачи Университета Джона Хопкинса обнаружили, что обычная инфекция может вызвать рак» . 24 августа 2022 года. Архивировано из оригинала 26 мая 2023 года . Проверено 29 августа 2022 г.
- ^ Морено М.А., Фуртнер Ф., Ривара Ф.П. (июнь 2013 г.). «Clostridium difficile: причина диареи у детей». JAMA Педиатрия . 167 (6): 592. doi : 10.1001/jamapediatrics.2013.2551 . ПМИД 23733223 .
- ^ Кордус С.Л., Томас А.К., Лейси Д.Б. (май 2022 г.). «Токсины Clostridioides difficile: механизмы действия и антитоксиновая терапия» . Обзоры природы. Микробиология . 20 (5): 285–298. дои : 10.1038/s41579-021-00660-2 . ПМЦ 9018519 . ПМИД 34837014 .
- ^ Перейти обратно: а б с д Райан К.Дж., Рэй К.Г., ред. (2004). Медицинская микробиология Шерриса (4-е изд.). МакГроу Хилл. стр. 322 –4. ISBN 978-0-8385-8529-0 .
- ^ «Инфекция Clostridioides difficile | HAI | CDC» . www.cdc.gov . 2 января 2020 года. Архивировано из оригинала 8 марта 2020 года . Проверено 10 марта 2020 г.
- ^ Эйр Д.В., Кьюл М.Л., Уилсон Д.Д., Гриффитс Д., Воган А., О'Коннор Л. и др. (сентябрь 2013 г.). «Различные источники инфекции C. difficile, выявленные при полногеномном секвенировании» . Медицинский журнал Новой Англии . 369 (13): 1195–1205. дои : 10.1056/NEJMoa1216064 . ПМЦ 3868928 . ПМИД 24066741 .
- ^ Гух А.Ю., Адкинс Ш., Ли К., Буленс С.Н., Фарли М.М., Смит З. и др. (1 октября 2017 г.). «Факторы риска внебольничной инфекции Clostridium difficile у взрослых: исследование случай-контроль» . Открытый форум Инфекционные болезни . 4 (4): офх171. дои : 10.1093/ofid/ofx171 . ПМК 5903408 . ПМИД 29732377 .
- ^ Браун К.А., Ханафер Н., Данеман Н., Фисман Д.Н. (май 2013 г.). «Метаанализ антибиотиков и риск внебольничной инфекции Clostridium difficile» . Антимикробные средства и химиотерапия . 57 (5): 2326–2332. дои : 10.1128/AAC.02176-12 . ПМЦ 3632900 . ПМИД 23478961 .
- ^ Рафей А., Джахан С., Фарук У., Ахтар Ф., Иршад М., Низамуддин С. и др. (май 2023 г.). «Антибиотики, связанные с инфекцией Clostridium difficile» . Куреус . 15 (5): e39029. дои : 10.7759/cureus.39029 . ПМЦ 10266117 . ПМИД 37323360 .
- ^ МакФарланд Л.В., Суравич К.М., Стамм В.Е. (сентябрь 1990 г.). «Факторы риска носительства Clostridium difficile и диареи, связанной с C. difficile, в когорте госпитализированных пациентов». Журнал инфекционных болезней . 162 (3): 678–684. дои : 10.1093/infdis/162.3.678 . ПМИД 2387993 .
- ^ МакФарланд Л.В., Маллиган М.Э., Квок Р.Ю., Стамм МЫ (январь 1989 г.). «Внутрибольничное заражение Clostridium difficile». Медицинский журнал Новой Англии . 320 (4): 204–210. дои : 10.1056/NEJM198901263200402 . ПМИД 2911306 .
- ^ Перейти обратно: а б ВанИнсберге Д., Эльшербини Дж.А., Вариан Б., Путахидис Т., Эрдман С., Польц М.Ф. (апрель 2020 г.). «Диарея может спровоцировать длительную колонизацию Clostridium difficile с периодическим цветением». Природная микробиология . 5 (4): 642–650. дои : 10.1038/s41564-020-0668-2 . ПМИД 32042128 . S2CID 211074075 .
- ^ Эйр Д.В., Гриффитс Д., Воган А., Голубчик Т., Ачарья М., О'Коннор Л. и др. (12 ноября 2013 г.). Чанг Ю.Ф. (ред.). «Бессимптомная колонизация Clostridium difficile и дальнейшая передача» . ПЛОС ОДИН . 8 (11): е78445. Бибкод : 2013PLoSO...878445E . дои : 10.1371/journal.pone.0078445 . ПМЦ 3827041 . ПМИД 24265690 .
- ^ Орен А., генеральный директор Гаррити (сентябрь 2017 г.). «Список новых имен и новых комбинаций, ранее эффективно, но недействительно опубликованный» . Международный журнал систематической и эволюционной микробиологии . 67 (9): 3140–3143. дои : 10.1099/ijsem.0.002278 . ПМЦ 5817221 . ПМИД 28891789 .
- ^ Перейти обратно: а б Лоусон П.А., Цитрон Д.М., Тиррелл К.Л., Файнголд С.М. (август 2016 г.). «Реклассификация Clostridium difficile в Clostridioides difficile (Холл и О'Тул, 1935) Прево, 1938». Анаэроб . 40 : 95–99. дои : 10.1016/j.anaerobe.2016.06.008 . ПМИД 27370902 .
- ^ Чжу Д., Сорг Дж.А., Сунь X (2018). « Биология Clostridioides difficile : спорообразование, прорастание и соответствующие методы лечения инфекции C. difficile » . Границы клеточной и инфекционной микробиологии . 8:29 . дои : 10.3389/fcimb.2018.00029 . ПМК 5809512 . ПМИД 29473021 .
- ^ Гальперин М.Ю., Бровер В., Толстой И., Ютин Н. (декабрь 2016). «Филогеномный анализ семейства Peptostreptococcaceae (кластер Clostridium XI) и предложение по реклассификации Clostridiumlitorale (Fendrich et al. 1991) и Eubacterium acidaminophilum (Zindel et al. 1989) как Peptoclostridiumlitorale gen. nov.com. nov. и Peptoclostridium acidaminophilum гребень. ноя» . Международный журнал систематической и эволюционной микробиологии . 66 (12): 5506–5513. дои : 10.1099/ijsem.0.001548 . ПМК 5244501 . ПМИД 27902180 .
- ^ Ди Белла С., Асенци П., Сиаракас С., Петросильо Н., ди Маси А. (май 2016 г.). «Токсины A и B Clostridium difficile: понимание патогенных свойств и внекишечных эффектов» . Токсины . 8 (5): 134. doi : 10.3390/toxins8050134 . ПМЦ 4885049 . ПМИД 27153087 .
- ^ Просто я, Зельцер Дж., фон Эйхель-Штрайбер С., Актерес К. (март 1995 г.). «Низкомолекулярный ГТФ-связывающий белок Rho подвергается воздействию токсина А Clostridium difficile» . Журнал клинических исследований . 95 (3): 1026–1031. дои : 10.1172/JCI117747 . ПМК 441436 . ПМИД 7883950 .
- ^ Барт Х., Акториес К., Попофф М.Р., Стайлз Б.Г. (сентябрь 2004 г.). «Бинарные бактериальные токсины: биохимия, биология и применение обычных белков Clostridium и Bacillus» . Обзоры микробиологии и молекулярной биологии . 68 (3): 373–402, оглавление. дои : 10.1128/MMBR.68.3.373-402.2004 . ПМК 515256 . ПМИД 15353562 .
- ^ [Медицинская микробиология, пятое издание, Патрик Мюррей, Elsevier Mosby, 2005, стр. 412]
- ^ «Химическое оружие, которое помогает бактериям сеять хаос в кишечнике» . Природа . 561 (7723): 288. 14 сентября 2018 г. Бибкод : 2018Natur.561S.288. . дои : 10.1038/d41586-018-06650-4 . S2CID 52297840 . Архивировано из оригинала 28 июля 2020 года . Проверено 8 октября 2018 г.
- ^ Перейти обратно: а б Лоо В.Г., Пуарье Л., Миллер М.А., Оутон М., Либман М.Д., Мишо С. и др. (декабрь 2005 г.). «Преимущественно клональная мультиинституциональная вспышка диареи, связанной с Clostridium difficile, с высокой заболеваемостью и смертностью» . Медицинский журнал Новой Англии . 353 (23): 2442–2449. doi : 10.1056/NEJMoa051639 . ПМИД 16322602 . S2CID 14818750 .
- ^ McDonald LC (август 2005 г.). «Clostridium difficile: ответ на новую угрозу старого врага» . Инфекционный контроль и госпитальная эпидемиология . 26 (8): 672–675. дои : 10.1086/502600 . ПМИД 16156321 .
- ^ Банавас СС (21 февраля 2018 г.). « Инфекции Clostridium difficile : глобальный обзор чувствительности к лекарствам и механизмов устойчивости» . БиоМед Исследования Интернэшнл . 2018 : 8414257. doi : 10.1155/2018/8414257 . ПМК 5841113 . ПМИД 29682562 .
- ^ Рашид Т., Хагиги Ф., Хасан И., Бассер Э., Алам М.Дж., Шарма С.В. и др. (декабрь 2019 г.). «Активность больничных дезинфицирующих средств против вегетативных клеток и спор Clostridioides difficile, встроенных в биопленки» . Антимикробные средства и химиотерапия . 64 (1). дои : 10.1128/AAC.01031-19 . ПМЦ 7187568 . ПМИД 31611365 .
- ^ «Отбеливатель не убивает распространенных супербактерий, показали исследования» . Новости Би-би-си . 22 ноября 2023 года. Архивировано из оригинала 22 ноября 2023 года . Проверено 22 ноября 2023 г.
- ^ Ди Белла С., Сансон Дж., Монтичелли Дж., Зербато В., Принсипи Л., Джуффре М. и др. (29 февраля 2024 г.). Стейли С. (ред.). «Инфекция Clostridioides difficile: история, эпидемиология, факторы риска, профилактика, клинические проявления, лечение и будущие варианты» . Обзоры клинической микробиологии . 37 (2). Маюреш Абхьянкар: e0013523. дои : 10.1128/cmr.00135-23 . ISSN 0893-8512 . ПМИД 38421181 . Архивировано из оригинала 4 марта 2024 года . Проверено 4 марта 2024 г.
- ^ «Информация для пациентов об инфекции Clostridium difficile» . Инфекции, связанные со здравоохранением (ИСМП) . Центры США по контролю и профилактике заболеваний. Архивировано из оригинала 30 марта 2017 года . Проверено 22 мая 2017 г.
- ^ «Руководство ВОЗ по гигиене рук в здравоохранении: краткое изложение» (PDF) . Всемирная организация здравоохранения . 2009. с. 31. Архивировано (PDF) из оригинала 9 мая 2020 г. Проверено 18 июня 2018 г.
- ^ Перейти обратно: а б Оливейра П.Х., Рибис Дж.В., Гарретт Э.М., Трзилова Д., Ким А., Секулович О. и др. (январь 2020 г.). «Эпигеномная характеристика Clostridioides difficile выявила консервативную ДНК-метилтрансферазу, которая опосредует споруляцию и патогенез» . Природная микробиология . 5 (1): 166–180. дои : 10.1038/s41564-019-0613-4 . ПМЦ 6925328 . ПМИД 31768029 .
- ^ Гулд Л.Х., Лимбаго Б (сентябрь 2010 г.). «Clostridium difficile в продуктах питания и домашних животных: новый патоген пищевого происхождения?» . Клинические инфекционные болезни . 51 (5): 577–582. дои : 10.1086/655692 . ПМИД 20642351 .
- ^ Беллак П. (25 февраля 2015 г.). «Увеличено число погибших от C. Difficile» . Нью-Йорк Таймс . Архивировано из оригинала 29 сентября 2017 года . Проверено 25 февраля 2015 г.
- ^ Мюррей П. (2005). Медицинская микробиология (Пятое изд.). Эльзевир Мосби. п. 412.
- ^ Перейти обратно: а б с «Может ли у вас быть смертельная диарея (К. Дифф)?» . 4 января 2019. Архивировано из оригинала 30 марта 2017 года . Проверено 22 мая 2017 г.
- ^ Смитс В.К., Лирас Д., Лейси Д.Б., Уилкокс М.Х. и Куйпер Э.Дж. (7 апреля 2017 г.). «Инфекция Clostridium difficile» . Обзоры природы. Учебники по болезням . 2 : 16020. дои : 10.1038/nrdp.2016.20 . ПМЦ 5453186 . ПМИД 27158839 .
- ^ Перейти обратно: а б Лесса ФК, Гулд CV, McDonald LC (1 августа 2012 г.). «Текущий статус эпидемиологии инфекции Clostridium difficile» . Клинические инфекционные болезни . 55 (Приложение 2): S65–S70. дои : 10.1093/cid/cis319 . ПМК 3388017 . ПМИД 22752867 .
- ^ Цимбал М., Чаттерджи А., Бэгготт Б., Аурон М. (март 2024 г.). «Лечение инфекции Clostridioides difficile: диагностика, лечение и перспективы на будущее» . Я Джей Мед . 137 (7): 571–576. doi : 10.1016/j.amjmed.2024.03.024 . PMID 38508330 .
- ^ Монаган Т.М., Негм Огайо, Маккензи Б., Хамед М.Р., Шон К.С., Хамфрис Д.П. и др. (июль 2017 г.). «Высокая распространенность подкласс-специфических связывающих и нейтрализующих антител против токсинов Clostridium difficile в сыворотке крови от муковисцидоза взрослых: возможный способ иммунозащиты от симптоматической C. difficile инфекции » . Клиническая и экспериментальная гастроэнтерология . 10 : 169–175. дои : 10.2147/CEG.S133939 . ПМЦ 5525456 . ПМИД 28765714 .
- ^ Вуллт М., Норен Т., Люнг А., Окерлунд Т. (сентябрь 2012 г.). «Реакция антител IgG на токсины А и В у пациентов с инфекцией Clostridium difficile» . Клиническая и вакциноиммунология . 19 (9): 1552–1554. дои : 10.1128/CVI.00210-12 . ПМЦ 3428380 . ПМИД 22787196 .
- ^ Кук Л., Рис В.Д., Вонг М.К., Квок В.В., Левингс М.К., Штайнер Т.С. (март 2021 г.). «Рецидивирующая инфекция Clostridioides difficile связана с нарушением иммунитета T-хелперов типа 17 к токсину B C difficile» . Гастроэнтерология . 160 (4): 1410–1413.e4. дои : 10.1053/J.GASTRO.2020.11.043 . ПМИД 33253683 .
- ^ Перейти обратно: а б Боккетти М., Ферраро М.Г., Мелиси Ф., Грисолия П., Скрима М., Коссу А.М. и др. (июнь 2023 г.). «Обзор современных методов обнаружения и потенциала микроРНК при Clostridioides difficile скрининге инфекции » . Всемирный журнал гастроэнтерологии . 29 (22): 3385–3399. дои : 10.3748/wjg.v29.i22.3385 . ПМЦ 10303512 . ПМИД 37389232 .
- ^ Кук Л., Рис В.Д., Вонг М.К., Питерс Х., Левингс М.К., Штайнер Т.С. (май 2021 г.). «Трансплантация фекальной микробиоты при рецидивирующей инфекции Clostridioides difficile повышает адаптивный иммунитет к токсину B C difficile». Гастроэнтерология . 160 (6): 2155–2158.e4. дои : 10.1053/J.GASTRO.2021.01.009 . hdl : 11343/289863 . PMID 33444574 . S2CID 231611318 .
- ^ Крибас Э.С., Денни Дж.Э., Масланка-младший, Абт MC (16 апреля 2021 г.). «Потеря передачи сигналов интерлейкина-10 (IL-10) способствует IL-22-зависимой защите хозяина от острой инфекции Clostridioides difficile» . Инфекция и иммунитет . 89 (5): e00730–20. дои : 10.1128/IAI.00730-20 . ISSN 1098-5522 . ПМК 8091099 . ПМИД 33649048 .
- ^ Перейти обратно: а б Рупник М., Уилкокс М.Х., Гердинг Д.Н. (июль 2009 г.). «Инфекция Clostridium difficile: новые достижения в эпидемиологии и патогенезе». Обзоры природы. Микробиология . 7 (7): 526–536. дои : 10.1038/nrmicro2164 . ПМИД 19528959 . S2CID 23376891 .
- ^ Макдональд Л.С., Гердинг Д.Н., Джонсон С., Баккен Дж.С., Кэрролл К.С., Коффин С.Е. и др. (март 2018 г.). «Руководство по клинической практике инфекции Clostridium difficile у взрослых и детей: обновление 2017 г., подготовленное Американским обществом инфекционистов (IDSA) и Американским обществом эпидемиологии здравоохранения (SHEA)» . Клинические инфекционные болезни . 66 (7): е1–е48. дои : 10.1093/cid/cix1085 . ПМК 6018983 . ПМИД 29462280 .
- ^ Муллейн К.М., Миллер М.А., Вайс К., Лентнек А., Голан Ю., Сирс П.С. и др. (сентябрь 2011 г.). «Эффективность фидаксомицина по сравнению с ванкомицином в качестве терапии инфекции Clostridium difficile у лиц, одновременно принимающих антибиотики по поводу других сопутствующих инфекций» . Клинические инфекционные болезни . 53 (5): 440–447. дои : 10.1093/cid/cir404 . ПМК 3156139 . ПМИД 21844027 .
- ^ Шейн А.Л., Моди Р.К., Крамп Дж.А., Тарр П.И., Штайнер Т.С., Котлофф К. и др. (ноябрь 2017 г.). «Руководство по клинической практике по диагностике и лечению инфекционной диареи Американского общества инфекционистов, 2017 г.» . Клинические инфекционные болезни . 65 (12): е45–е80. дои : 10.1093/cid/cix669 . ПМЦ 5850553 . ПМИД 29053792 .
- ^ Сон Дж.Х., Ким Ю.С. (январь 2019 г.). «Рецидивирующая инфекция Clostridium difficile : факторы риска, лечение и профилактика» . Кишечник и печень . 13 (1): 16–24. дои : 10.5009/gnl18071 . ПМК 6346998 . ПМИД 30400734 .
- ^ «Лечение рецидивирующего колита Clostridium difficile ванкомицином и Saccharomyces boulardii» (PDF) . Американский журнал гастроэнтерологии . Архивировано из оригинала (PDF) 9 августа 2017 года . Проверено 28 апреля 2018 г.
- ^ Перейти обратно: а б Суравич С.М., Брандт Л.Дж., Биньон Д.Г., Анантакришнан А.Н., Карри С.Р., Гиллиган П.Х. и др. (апрель 2013 г.). «Руководство по диагностике, лечению и профилактике инфекций Clostridium difficile» . Американский журнал гастроэнтерологии . 108 (4): 478–98, викторина 499. doi : 10.1038/ajg.2013.4 . ПМИД 23439232 . S2CID 54629762 .
- ^ ван Прен Дж., Рейгадас Э., Фогельзанг Э.Х., Буза Э., Христеа А., Гери Б. и др. (декабрь 2021 г.). «Европейское общество клинической микробиологии и инфекционных заболеваний: обновленная информация о руководстве по лечению инфекции Clostridioides difficile у взрослых на 2021 год» (PDF) . Клиническая микробиология и инфекции . 27 (Приложение 2): S1–S21. дои : 10.1016/j.cmi.2021.09.038 . ПМИД 34678515 . S2CID 239473944 .
- ^ Ди Белла С., Нисии С., Петросилло Н. (июль 2015 г.). «Является ли тигециклин подходящим вариантом лечения инфекции Clostridium difficile? Данные из литературы». Международный журнал противомикробных средств . 46 (1): 8–12. дои : 10.1016/j.ijantimicag.2015.03.012 . ПМИД 25982915 .
- ^ Джакоббе Д.Р., Деттори С., Ди Белла С., Вена А., Граната Г., Луццати Р. и др. (сентябрь 2020 г.). «Безлотоксумаб для предотвращения рецидивирующей инфекции Clostridioides difficile: описательный обзор от патофизиологии к клиническим исследованиям» . Инфекционные болезни и терапия . 9 (3): 481–494. дои : 10.1007/s40121-020-00314-5 . ПМЦ 7452994 . ПМИД 32632582 .
- ^ АКАГАВА С, АКАГАВА Й, ЯМАНОУТИ С, КИМАТА Т, ЦУДЗИ С, КАНЕКО К (25 августа 2020 г.). «Развитие микробиоты кишечника и дисбиоз у детей» . Национальная медицинская библиотека . 40 (1): 12–18. ПМЦ 7817514 . ПМИД 33520564 .
- ^ Чен Т, Чжоу Ц, Чжан Д, Цзян Ф, Ву Дж, Чжоу Цзюй и др. (май 2018 г.). «Эффект трансплантации фекальной микробиоты для лечения инфекции Clostridium difficile у пациентов с воспалительными заболеваниями кишечника: систематический обзор и метаанализ когортных исследований» . Журнал Крона и колита . 12 (6): 710–717. doi : 10.1093/ecco-jcc/jjy031 . ПМИД 29528385 . S2CID 3841585 .
- ^ Литтманн Э.Р., Ли Дж.Дж., Денни Дж.Э., Алам З., Масланка Дж.Р., Зарин И. и др. (2 февраля 2021 г.). «Иммунитет хозяина модулирует эффективность трансплантации микробиоты для лечения инфекции Clostridioides difficile» . Природные коммуникации . 12 (1): 755. Бибкод : 2021NatCo..12..755L . дои : 10.1038/s41467-020-20793-x . ISSN 2041-1723 . ПМЦ 7854624 . ПМИД 33531483 .
- ^ Стюарт Д.Б., Берг А., Хегарти Дж. (январь 2013 г.). «Прогнозирование рецидива колита, вызванного C. difficile, с использованием факторов бактериальной вирулентности: ключ к успеху – бинарный токсин» . Журнал желудочно-кишечной хирургии . 17 (1): 118–125. дои : 10.1007/s11605-012-2056-6 . ПМИД 23086451 . Архивировано из оригинала 21 марта 2024 года . Проверено 20 марта 2024 г.
- ^ Берк К.Э., Ламонт Дж.Т. (29 января 2014 г.). «Инфекция Clostridium difficile: всемирное заболевание» . Кишечная печень . 8 (1): 1–6. дои : 10.5009/gnl.2014.8.1.1 . ПМЦ 3916678 . ПМИД 24516694 .
- ^ Чудин-Саттер С., Куйпер Э.Дж., Дурович А., Верешильд М.Дж., Барбут Ф., Эккерт С. и др. (октябрь 2018 г.). «Руководство по профилактике инфекции Clostridium difficile в условиях неотложной медицинской помощи» . Клиническая микробиология и инфекции . 24 (10): 1051–1054. дои : 10.1016/j.cmi.2018.02.020 . ПМИД 29505879 .
- ^ Яссем А.Н., Пристаецкий Н. , Марра Ф., Кибси П., Тан К., Умландт П. и др. (29 марта 2016 г.). «Характеристика штаммов Clostridium difficile в Британской Колумбии, Канада: переход от большинства NAP1 (2008 г.) к новым типам штаммов (2013 г.) в одном регионе» . Канадский журнал инфекционных заболеваний и медицинской микробиологии . 2016 : 8207418. doi : 10.1155/2016/8207418 . ПМЦ 4904575 . ПМИД 27366181 .
- ^ Коллинз Дж., Робинсон С., Данхоф Х., Кнетш К.В., ван Леувен Х.К., Лоули Т.Д. и др. (январь 2018 г.). «Диетическая трегалоза повышает вирулентность эпидемии Clostridium difficile» . Природа . 553 (7688): 291–294. Бибкод : 2018Natur.553..291C . дои : 10.1038/nature25178 . ПМЦ 5984069 . ПМИД 29310122 .
- ^ Хе М., Себайхия М., Лоули Т.Д., Стейблер Р.А., Доусон Л.Ф., Мартин М.Дж. и др. (апрель 2010 г.). «Эволюционная динамика Clostridium difficile в краткосрочном и долгосрочном масштабе» . Труды Национальной академии наук Соединенных Штатов Америки . 107 (16): 7527–7532. Бибкод : 2010PNAS..107.7527H . дои : 10.1073/pnas.0914322107 . ПМЦ 2867753 . ПМИД 20368420 .
- ^ Ученые составляют карту C. difficile. штамма Архивировано 22 мая 2022 года в Wayback Machine - Институт по связям с общественностью, Монреаль.
- ^ Дидело X, Эйр Д.В., Кул М., Ип КЛ, Ансари М.А., Гриффитс Д. и др. (декабрь 2012 г.). «Микроэволюционный анализ геномов Clostridium difficile для исследования передачи» . Геномная биология . 13 (12): 118 р. дои : 10.1186/gb-2012-13-12-r118 . ПМК 4056369 . ПМИД 23259504 .
- ^ Перейти обратно: а б Харгривз К.Р., Клоки М.Р. (2014). «Фаги Clostridium difficile: все еще сложно?» . Границы микробиологии . 5 : 184. дои : 10.3389/fmicb.2014.00184 . ПМК 4009436 . ПМИД 24808893 .
Внешние ссылки
[ редактировать ]- Паспорта безопасности патогенов: Инфекционные вещества – Clostridium Difficile [ постоянная мертвая ссылка ] , Агентство общественного здравоохранения, Канада, 10 сентября 2014 г.
- Типовой штамм Clostridium difficile , Bac Dive — база метаданных бактериального разнообразия.