Протеиногенная аминокислота

Протеиногенные аминокислоты представляют собой аминокислоты , которые включены биосинтетически в белки во время трансляции . Слово «протеиногенный» означает «создание белка». На протяжении всей известной жизни существует 22 генетически кодируемых (протеиногенных) аминокислот, 20 в стандартном генетическом коде и дополнительные 2 ( селеноцистеин и пирролизин ), которые могут быть включены с помощью специальных механизмов трансляции. [ 1 ]
Напротив, небелтеногенные аминокислоты представляют собой аминокислоты, которые либо не включены в белки (такие как ГАМК , L -допа или триодотиронин ), неправильно инкорпорированные вместо генетически кодируемой аминокислоты или не продуцируемые непосредственно и в изоляции стандартными клетками. Машины (например, гидроксипролин ). Последний часто является результатом посттрансляционной модификации белков. Некоторые небелкогенные аминокислоты включены в нерибосомные пептиды , которые синтезируются нерибосомными пептид-синтетазами.
Как эукариоты , так и прокариоты могут включать селеноцистеин в свои белки через нуклеотидную последовательность, известную как элемент SECIS , которая направляет клетку для трансляции соседнего UGA Codon в качестве селеноцистеина (UGA, как правило, является стоп -кодоном ). В некоторых метаногенных прокариотах кодон UAG (обычно стоп -кодон) также может быть переведен в пирролизин . [ 2 ]
У эукариот есть только 21 протеиногенный аминокислот, 20 из стандартного генетического кода, а также селеноцистеин . Люди могут синтезировать 12 из них друг от друга или из других молекул промежуточного метаболизма. Остальные девять должны быть потреблены (обычно в качестве производных белка), и поэтому они называются незаменимыми аминокислотами . Основными аминокислотами являются гистидин , изолейцин , лейцин , лизин , метионин , фенилаланин , треонин , триптофан и валин (то есть H, I, L, K, M, F, T, W, V). [ 3 ]
Было обнаружено, что протеиногенные аминокислоты связаны с набором аминокислот , которые могут быть распознаны системами аутоаминоациалирования рибозима . [ 4 ] Таким образом, небелкогенные аминокислоты были бы исключены из-за условного эволюционного успеха нуклеотидных форм жизни. Были предложены другие причины, чтобы объяснить, почему определенные специфические небелкогенные аминокислоты обычно не включены в белки; Например, орнитин и гомосерин циклируются против пептидной основной цепи и фрагментируют белок с относительно коротким периодом полураспада , в то время как другие токсичны, потому что их можно ошибочно включить в белки, такие как аналог аналога аргинина .
отбор эволюционный некоторых протеиногенных аминокислот из первичного супа связан из-за их лучшего включения в полипептидную цепь, а не белокногенные аминокислоты. Предполагалось, что [ 5 ]
Структуры
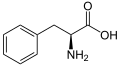
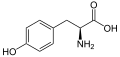
[ редактировать ]Следующее иллюстрирует структуры и аббревиатуры 21 аминокислот, которые непосредственно кодируются для синтеза белка генетическим кодом эукариот. Структуры, приведенные ниже, представляют собой стандартные химические структуры, а не типичные формы Zwitterion , которые существуют в водных растворах.

-
L -аланин
(Путь / А) -
L -Arginine
(Angry / r) -
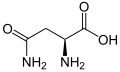
L -ASPARAGINE
(ASN / N) -
L -Asparicic Acid
(ASP / D) -
L -цистеин
(Cys / c) -
L -глютамическая кислота
(Клей) -
L -глютамин
(GLN / Q) -
Глицин
(Gly / g) -
L -Хистидин
(Его / ч) -
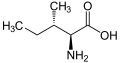
L -изолецин
(Ile / i) -
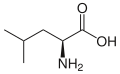
L -Leucine
(Leu / l) -
L -lysine
(Свет / К) -
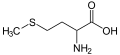
L -метионин
(С / м) -
L -фенилаланин
(Phe / f) -
L -Proline
(Pro / p) -
L -серин
(Be / s) -
L -Threonine
(THR / T) -
L -tryptophan
(Trp / w) -
L -Тирозин
(Терроризировать) -
L -валина
(Val / V)
IUPAC / IUBMB теперь также рекомендует стандартные сокращения для следующих двух аминокислот:
-
L -Selenocysteine
(Sec / u) -
L -пирролизин
(Pyl / O)
Химические свойства
[ редактировать ]Ниже приведена таблица, в которой перечислены однобуквенные символы, трибуктные символы и химические свойства боковых цепей стандартных аминокислот. Перечисленные массы основаны на взвешенных средних значениях элементарных изотопов в их естественной численности . Образование пептидной связи приводит к элиминации молекулы воды . Следовательно, масса белка равен массе аминокислот, белок состоит из минус 18,01524 да на пептидную связь.
Общие химические свойства
[ редактировать ]| Аминокислота | Короткий | Сокращение. | Ав. Масса ( да ) | пик | PK 1 (A-Coo - ) |
PK 2 (A-NH 3 + ) |
|---|---|---|---|---|---|---|
| Аланин | А | Земля | 89.09404 | 6.01 | 2.35 | 9.87 |
| Цистеин | В | Cys | 121.15404 | 5.05 | 1.92 | 10.70 |
| Аспартациновая кислота | Дюймовый | Аспирант | 133.10384 | 2.85 | 1.99 | 9.90 |
| Глутаминовая кислота | И | Глю | 147.13074 | 3.15 | 2.10 | 9.47 |
| Фенилаланин | Фон | Пэ | 165.19184 | 5.49 | 2.20 | 9.31 |
| Глицин | Глин | Гли | 75.06714 | 6.06 | 2.35 | 9.78 |
| Гистидин | ЧАС | Его | 155.15634 | 7.60 | 1.80 | 9.33 |
| Изолецин | я | С | 131.17464 | 6.05 | 2.32 | 9.76 |
| Лизин | K | Свет | 146.18934 | 9.60 | 2.16 | 9.06 |
| Лейцин | Л | Лея | 131.17464 | 6.01 | 2.33 | 9.74 |
| Метионин | М | Из | 149.20784 | 5.74 | 2.13 | 9.28 |
| Аспарагин | Не | ASN | 132.11904 | 5.41 | 2.14 | 8.72 |
| Пирролизин | А | Pyl | 255.31 | ? | ? | ? |
| Пролин | П | Профиль | 115.13194 | 6.30 | 1.95 | 10.64 |
| Глутамин | Q. | Глн | 146.14594 | 5.65 | 2.17 | 9.13 |
| Аргинин | Ведущий | Арг | 174.20274 | 10.76 | 1.82 | 8.99 |
| Серин | С | Быть | 105.09344 | 5.68 | 2.19 | 9.21 |
| Треонин | Т | Тр | 119.12034 | 5.60 | 2.09 | 9.10 |
| Селеноцистеин | В | Раздел | 168.053 | 5.47 | 1.91 | 10 |
| Валин | V | Дольдо | 117.14784 | 6.00 | 2.39 | 9.74 |
| Триптофан | В | TRP | 204.22844 | 5.89 | 2.46 | 9.41 |
| Тирозин | И | Тир | 181.19124 | 5.64 | 2.20 | 9.21 |
Свойства боковой цепи
[ редактировать ]| Аминокислота | Короткий | Сокращение. | Боковая цепь | Гидро- фобический |
ПКА § | Полярный | pH | Маленький | Крошечный | Ароматический или алифатический |
Ван Дер Ваальс том (до 3 ) |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Аланин | А | Земля | -H 3 | - | - | Алифатический | 67 | ||||
| Цистеин | В | Cys | -Ч 2 Ш. | 8.55 | кислый | - | 86 | ||||
| Аспартациновая кислота | Дюймовый | Аспирант | -Ch 2 COOH | 3.67 | кислый | - | 91 | ||||
| Глутаминовая кислота | И | Глю | -Ch 2 ch 2 cooh | 4.25 | кислый | - | 109 | ||||
| Фенилаланин | Фон | Пэ | -Ch 2 C 6 H 5 | - | - | Ароматический | 135 | ||||
| Глицин | Глин | Гли | -ЧАС | - | - | - | 48 | ||||
| Гистидин | ЧАС | Его | -Ch 2 - C 3 H N2 | 6.54 | Слабая базовая | Ароматический | 118 | ||||
| Изолецин | я | С | -C (Ch 3 ) Ch 2 CH 3 | - | - | Алифатический | 124 | ||||
| Лизин | K | Свет | -(Ch 2 ) 4 NH 2 | 10.40 | базовый | - | 135 | ||||
| Лейцин | Л | Лея | -Ch 2 ch (ch 3 ) 2 | - | - | Алифатический | 124 | ||||
| Метионин | М | Из | -Ch 2 CH 2 S CH 3 | - | - | Алифатический | 124 | ||||
| Аспарагин | Не | ASN | -Ч 2 conh 2 | - | - | - | 96 | ||||
| Пирролизин | А | Pyl | -(Ch 2 ) 4 NHCO C 4 H 5 N CH 3 | Н.д. | Слабая базовая | - | ? | ||||
| Пролин | П | Профиль | -Ch 2 ch 2 ch 2 - | - | - | - | 90 | ||||
| Глутамин | Q. | Глн | -Ch 2 ch 2 conh 2 | - | - | - | 114 | ||||
| Аргинин | Ведущий | Арг | -(Ch 2 ) 3 NH-C (NH) NH 2 | 12.3 | сильно простой | - | 148 | ||||
| Серин | С | Быть | -Ч 2 О | - | - | - | 73 | ||||
| Треонин | Т | Тр | -Ch (OH) Ch 3 | - | - | - | 93 | ||||
| Селеноцистеин | В | Раздел | -Ч 2 seh | 5.43 | кислый | - | ? | ||||
| Валин | V | Дольдо | -C (ch 3 ) 2 | - | - | Алифатический | 105 | ||||
| Триптофан | В | TRP | -Ch 2 C 8 H 6 N | - | - | Ароматический | 163 | ||||
| Тирозин | И | Тир | -Ch 2 -c 6 H 4 OH | 9.84 | слабый кислый | Ароматический | 141 |
§: Значения для ASP, Cys, Glu, His, Lys & Tyr были определены с использованием аминокислотного остатка, расположенного централизованно в аланиновом пентапептиде. [ 6 ] Значение для ARG от Pace et al. (2009). [ 7 ] Значение для SEC от Byun & Kang (2011). [ 8 ]
ND: Значение PKA пирролизина не сообщалось.
Примечание. Значение PKA аминокислотного остатка в маленьком пептиде обычно немного отличается, когда он находится внутри белка. Расчеты белка PKA иногда используются для расчета изменения значения PKA аминокислотного остатка в этой ситуации.
Экспрессия гена и биохимия
[ редактировать ]| Аминокислота | Короткий | Сокращение. | Кодон (ы) | Возникновение | Основное ‡ у людей | |||
|---|---|---|---|---|---|---|---|---|
| в архейских белках (%) И |
У бактерий белки (%) И |
В белках эукариот (%) И |
в белках человека (%) И | |||||
| Аланин | А | Земля | Внешний вид, GCC, Cha, GCG | 8.2 | 10.06 | 7.63 | 7.01 | Нет |
| Цистеин | В | Cys | Большинство, UGC | 0.98 | 0.94 | 1.76 | 2.3 | Условно |
| Аспартациновая кислота | Дюймовый | Аспирант | Закрыт, Gac | 6.21 | 5.59 | 5.4 | 4.73 | Нет |
| Глутаминовая кислота | И | Глю | GAA, Gag | 7.69 | 6.15 | 6.42 | 7.09 | Условно |
| Фенилаланин | Фон | Пэ | Uuu, UUC | 3.86 | 3.89 | 3.87 | 3.65 | Да |
| Глицин | Глин | Гли | GGU, GGC, GGA, GGG | 7.58 | 7.76 | 6.33 | 6.58 | Условно |
| Гистидин | ЧАС | Его | Cau, cac | 1.77 | 2.06 | 2.44 | 2.63 | Да |
| Изолецин | я | С | OU, AAC, потому что | 7.03 | 5.89 | 5.1 | 4.33 | Да |
| Лизин | K | Свет | AAA, AAG | 5.27 | 4.68 | 5.64 | 5.72 | Да |
| Лейцин | Л | Лея | Uua, uug, cuu, cuc, cua, cug | 9.31 | 10.09 | 9.29 | 9.97 | Да |
| Метионин | М | Из | Август | 2.35 | 2.38 | 2.25 | 2.13 | Да |
| Аспарагин | Не | ASN | AAU, AAC | 3.68 | 3.58 | 4.28 | 3.58 | Нет |
| Пирролизин | А | Pyl | UAG * | 0 | 0 | 0 | 0 | Нет |
| Пролин | П | Профиль | CCU, CCC, CCA, CCG | 4.26 | 4.61 | 5.41 | 6.31 | Нет |
| Глутамин | Q. | Глн | CAA, CAG | 2.38 | 3.58 | 4.21 | 4.77 | Нет |
| Аргинин | Ведущий | Арг | CGU, CGC, CGA, CGG, AGA, AGG | 5.51 | 5.88 | 5.71 | 5.64 | Условно |
| Серин | С | Быть | UCU, UCC, UCA, UCG, AGU, AGC | 6.17 | 5.85 | 8.34 | 8.33 | Нет |
| Треонин | Т | Тр | ACU, ACC, ACA, ACG | 5.44 | 5.52 | 5.56 | 5.36 | Да |
| Селеноцистеин | В | Раздел | От ** | 0 | 0 | 0 | > 0 | Нет |
| Валин | V | Дольдо | Guu, Guc, Gua, Gug | 7.8 | 7.27 | 6.2 | 5.96 | Да |
| Триптофан | В | TRP | Угг | 1.03 | 1.27 | 1.24 | 1.22 | Да |
| Тирозин | И | Тир | Uau, uac | 3.35 | 2.94 | 2.87 | 2.66 | Условно |
| Стоп -кодон † | - | Срок | Uaa, собака, uga † | ? | ? | ? | — | — |
* UAG, как правило, является янтарным стоп -кодоном , но у организмов, содержащих биологический механизм, кодируемый кластером генов PyltsBCD, аминокислотный пирролизин будет включен. [ 9 ]
** UGA, как правило, является стоп -кодоном опала (или UMBER), но кодирует селеноцистеин, если элемент SECIS . присутствует
† Стоп -кодон не является аминокислотой, но включен для полноты.
†† UAG и UGA не всегда действуют как стоп -кодоны (см. Выше).
‡ Основная аминокислота не может быть синтезирована у людей и, следовательно, должна быть поставлена в рационе. Условные незаменимые аминокислоты обычно не требуются в рационе, но должны поставляться экзогенно для конкретных популяций, которые не синтезируют их в достаточных количествах.
И появление аминокислот основано на 135 Archaea, 3775 бактериях, 614 протеомах эукариоты и протеоме человека (21 006 белка) соответственно. [ 10 ]
Масс -спектрометрия
[ редактировать ]В масс -спектрометрии пептидов и белков полезны знания о массах остатков. Масса пептида или белка представляет собой сумму остаточных масс плюс масса воды ( моноизотопная масса = 18,01056 да; средняя масса = 18,0153 Да). Массы остатков рассчитываются по табличным химическим формулам и атомным весам. [ 11 ] В масс -спектрометрии ионы могут также включать один или несколько протонов ( моноизотопная масса = 1,00728 Да; средняя масса* = 1,0074 Да). *Протоны не могут иметь среднюю массу, это смущающе не позволяет Второнам в качестве действительного изотопа, но они должны быть другим видом (см. Hydron (химия) )
| Аминокислота | Короткий | Сокращение. | Формула | Мой. Масса § ( da ) | Ав. Масса ( да ) |
|---|---|---|---|---|---|
| Аланин | А | Земля | 100 3 ч 5 нет | 71.03711 | 71.0779 |
| Цистеин | В | Cys | C 3 H 5 № | 103.00919 | 103.1429 |
| Аспартациновая кислота | Дюймовый | Аспирант | C 4 H 5 Нет 3 | 115.02694 | 115.0874 |
| Глутаминовая кислота | И | Глю | C 5 H 7 Нет 3 | 129.04259 | 129.1140 |
| Фенилаланин | Фон | Пэ | C 9 H 9 Нет | 147.06841 | 147.1739 |
| Глицин | Глин | Гли | C 2 H 3 нет | 57.02146 | 57.0513 |
| Гистидин | ЧАС | Его | C 6 H 7 N O O | 137.05891 | 137.1393 |
| Изолецин | я | С | C 6 H 11 Нет | 113.08406 | 113.1576 |
| Лизин | K | Свет | C 6 H 12 N 2 O | 128.09496 | 128.1723 |
| Лейцин | Л | Лея | C 6 H 11 Нет | 113.08406 | 113.1576 |
| Метионин | М | Из | C 5 H 9 № | 131.04049 | 131.1961 |
| Аспарагин | Не | ASN | C 4 H 6 N 2 O 2 | 114.04293 | 114.1026 |
| Пирролизин | А | Pyl | C 12 H 19 N 3 2 | 237.14773 | 237.2982 |
| Пролин | П | Профиль | C 5 H 7 Нет | 97.05276 | 97.1152 |
| Глутамин | Q. | Глн | C 5 H 8 N 2 O 2 | 128.05858 | 128.1292 |
| Аргинин | Ведущий | Арг | C 6 H 12 N 4 O | 156.10111 | 156.1857 |
| Серин | С | Быть | C 3 H 5 № 2 | 87.03203 | 87.0773 |
| Треонин | Т | Тр | C 4 H 7 Нет 2 | 101.04768 | 101.1039 |
| Селеноцистеин | В | Раздел | C 3 H 5 нос | 150.95364 | 150.0489 |
| Валин | V | Дольдо | C 5 H 9 Нет | 99.06841 | 99.1311 |
| Триптофан | В | TRP | C 11 H 10 N 2 O | 186.07931 | 186.2099 |
| Тирозин | И | Тир | C 9 H 9 № 2 | 163.06333 | 163.1733 |
Стехиометрия и метаболическая стоимость в клетке
[ редактировать ]В таблице ниже перечислены численность аминокислот в клетках E.Coli и метаболические затраты (АТФ) для синтеза аминокислот. Отрицательные числа показывают, что метаболические процессы являются энергией благоприятны и не стоят чистых АТФ клетки. [ 12 ] Обилие аминокислот включает аминокислоты в свободной форме и в форме полимеризации (белки).
| Аминокислота | Короткий | Сокращение. | Избыток (# молекул (× 10 8 ) Для ячейки кишечной палочки ) |
Стоимость АТФ по синтезу | |
|---|---|---|---|---|---|
| Аэробный условия |
Анаэробный условия | ||||
| Аланин | А | Земля | 2.9 | -1 | 1 |
| Цистеин | В | Cys | 0.52 | 11 | 15 |
| Аспартациновая кислота | Дюймовый | Аспирант | 1.4 | 0 | 2 |
| Глутаминовая кислота | И | Глю | 1.5 | -7 | -1 |
| Фенилаланин | Фон | Пэ | 1.1 | -6 | 2 |
| Глицин | Глин | Гли | 3.5 | -2 | 2 |
| Гистидин | ЧАС | Его | 0.54 | 1 | 7 |
| Изолецин | я | С | 1.7 | 7 | 11 |
| Лизин | K | Свет | 2.0 | 5 | 9 |
| Лейцин | Л | Лея | 2.6 | -9 | 1 |
| Метионин | М | Из | 0.88 | 21 | 23 |
| Аспарагин | Не | ASN | 1.4 | 3 | 5 |
| Пирролизин | А | Pyl | - | - | - |
| Пролин | П | Профиль | 1.3 | -2 | 4 |
| Глутамин | Q. | Глн | 1.5 | -6 | 0 |
| Аргинин | Ведущий | Арг | 1.7 | 5 | 13 |
| Серин | С | Быть | 1.2 | -2 | 2 |
| Треонин | Т | Тр | 1.5 | 6 | 8 |
| Селеноцистеин | В | Раздел | - | - | - |
| Валин | V | Дольдо | 2.4 | -2 | 2 |
| Триптофан | В | TRP | 0.33 | -7 | 7 |
| Тирозин | И | Тир | 0.79 | -8 | 2 |
Замечания
[ редактировать ]| Аминокислота | Сокращение. | Замечания | |
|---|---|---|---|
| Аланин | А | Земля | Очень обильный и очень универсальный, он более жесткий, чем глицин, но достаточно маленький, чтобы позировать только небольшие стерические ограничения для конформации белка. Он ведет себя довольно нейтрально и может быть расположен в обеих гидрофильных областях на белке снаружи, так и на гидрофобных областях внутри. |
| Аспарагин или аспарагиновая кислота | Беременный | Ас | Заполнитель, когда любая аминокислота может занимать позицию |
| Цистеин | В | Cys | Атом серы легко связывается с ионами тяжелых металлов . В условиях окисления два цистеина могут присоединиться к дисульфидной связи с образованием аминокислотной цистины . Когда кисти являются частью белка, , инсулин например , третичная структура стабилизируется, что делает белок более устойчивым к денатурации ; Следовательно, дисульфидные связи распространены в белках, которые должны функционировать в суровых средах, включая пищеварительные ферменты (например, пепсин и химотрипсин ) и структурные белки (например, кератин ). Дисульфиды также обнаруживаются в пептидах, слишком маленьких, чтобы самостоятельно удерживать стабильную форму (например, инсулин ). |
| Аспартациновая кислота | Дюймовый | Аспирант | ASP ведет себя аналогично глутаминовой кислоте и несет гидрофильную кислотую группу с сильным отрицательным зарядом. Обычно он расположен на внешней поверхности белка, что делает его водорастворимым. Он связывается с положительно заряженными молекулами и ионами, и часто используется в ферментах для исправления иона металла. Находясь внутри белка, аспартат и глутамат обычно в паре с аргинином и лизином. |
| Глутаминовая кислота | И | Глю | GLU ведет себя так же, как аспартациновая кислота и имеет более длинную, немного более гибкую боковую цепь. |
| Фенилаланин | Фон | Пэ | Необходимый для людей, фенилаланин, тирозин и триптофан содержат большую жесткую ароматическую группу на боковой цепи. Это самые большие аминокислоты. Как и изолейцин, лейцин и валин, они гидрофобные и имеют тенденцию ориентироваться на внутреннюю часть молекулы сложенного белка. Фенилаланин может быть превращен в тирозин. |
| Глицин | Глин | Гли | Из -за двух атомов водорода при α углерод глицин не является оптически активным . Это наименьшая аминокислота, легко вращается и добавляет гибкость к белковой цепи. Он способен вписаться в самые жесткие пространства, например, тройную спираль коллагена . Поскольку слишком большая гибкость обычно не желательна, как структурный компонент, он встречается реже, чем аланин. |
| Гистидин | ЧАС | Его | Это необходимо для людей. Даже в слегка кислотных условиях происходит протонирование азота, изменяя свойства гистидина и полипептида в целом. Он используется многими белками в качестве регуляторного механизма, изменяя конформацию и поведение полипептида в кислых областях, таких как поздняя эндосома или лизосома , обеспечивая соблюдение изменений конформации в ферментах. Тем не менее, для этого необходимо лишь несколько гистидинов, так что это сравнительно скудно. |
| Изолецин | я | С | Иль необходим для людей. Изолейцин, лейцин и валин имеют большие алифатические гидрофобные боковые цепи. Их молекулы жесткие, и их взаимные гидрофобные взаимодействия важны для правильного складывания белков, так как эти цепи, как правило, расположены внутри молекулы белка. |
| Лейцин или изолейцин | Дж | Xle | Заполнитель, когда любая аминокислота может занимать позицию |
| Лизин | K | Свет | Лис необходим для людей и ведет себя аналогично аргинину. Он содержит длинную гибкую боковую цепь с положительно заряженным концом. Гибкость цепи делает лизин и аргинин подходящим для связывания с молекулами со многими отрицательными зарядами на их поверхностях. Например, ДНК -связывающие белки имеют свои активные области, богатые аргинином и лизином. Сильный заряд делает эти две аминокислоты, подверженные расположенным на внешних гидрофильных поверхностях белков; Когда они находятся внутри, они обычно сочетаются с соответствующей отрицательно заряженной аминокислотой, например, аспартатом или глутаматом. |
| Лейцин | Л | Лея | Леу необходим для людей и ведет себя аналогично изолецину и валину. |
| Метионин | М | Из | МЕТ ТЕРИЧЕСКИЕ для людей. Всегда первая аминокислота, которая была включена в белок, иногда она удаляется после трансляции. Как цистеин, он содержит серу, но с метильной группой вместо водорода. Эта метильная группа может быть активирована и используется во многих реакциях, где к другой молекуле добавляется новый атом углерода. |
| Аспарагин | Не | ASN | Подобно аспарагиновой кислоте, ASN содержит амидную группу, где ASP имеет карбоксил . |
| Пирролизин | А | Pyl | Подобно лизину , но у него прикреплено пирролиновое кольцо. |
| Пролин | П | Профиль | Pro содержит необычное кольцо для группы амин N-концов, которая заставляет амидную последовательность ко-NH в фиксированную конформацию. Он может нарушать структуры складывания белка, такие как α -спираль или β -лист , заставляя желаемый перевод в белковой цепи. Распространенный в коллагене он часто подвергается посттрансляционной модификации гидроксипролина , . |
| Глутамин | Q. | Глн | Подобно глутаминовой кислоте, GLN содержит амидную группу, где Glu имеет карбоксил . Используемый в белках и в качестве хранения аммиака , это самая распространенная аминокислота в организме. |
| Аргинин | Ведущий | Арг | Функционально похож на лизин. |
| Серин | С | Быть | Серин и треонин имеют короткую группу, закончившуюся гидроксильной группой. Его водород легко удалить, поэтому серин и треонин часто действуют как доноры водорода в ферментах. Оба очень гидрофильные, поэтому внешние области растворимых белков, как правило, богаты с ними. |
| Треонин | Т | Тр | Необходимый для людей, TH ведет себя аналогично серину. |
| Селеноцистеин | В | Раздел | Аналог селена цистеина, в котором селен заменяет атом серы . |
| Валин | V | Дольдо | Важ, необходимый для людей, ведет себя аналогично изолецину и лейцине. |
| Триптофан | В | TRP | Необходимый для людей, TRP ведет себя аналогично фенилаланину и тирозину. Это предшественник серотонина и естественно флуоресцентен . |
| Неизвестный | Х | Газету | Заполнитель, когда аминокислота неизвестна или не важна. |
| Тирозин | И | Тир | Тир ведет себя аналогично фенилаланину (предшественник тирозина) и триптофан и является предшественником меланина , адреналина и гормонов щитовидной железы . Естественно флуоресцентный , его флуоресценция обычно гасит переносом энергии в триптофаны. |
| Глутаминовая кислота или глутамин | С | Glx | Заполнитель, когда любая аминокислота может занимать позицию |

Катаболизм
[ редактировать ]Аминокислоты могут быть классифицированы в соответствии с свойствами их основных продуктов: [ 13 ]
- Глюкогенный, с продуктами, способными образовывать глюкозу путем глюконеогенеза
- Кетогенный, с продуктами, не имеющими способности образовывать глюкозу: эти продукты все еще могут использоваться для кетогенеза или синтеза липидов .
- Аминокислоты катаболизируются как в глюкогенные, так и кетогенные продукты
Смотрите также
[ редактировать ]Ссылки
[ редактировать ]- ^ Ambrogelly A, Palioura S, Söll D (январь 2007 г.). «Естественное расширение генетического кода». Природная химическая биология . 3 (1): 29–35. doi : 10.1038/nchembio847 . PMID 17173027 .
- ^ Лобанов А.В., Туранов А.А., Хэтфилд Д.Л., Гладишев Вн (август 2010 г.). «Двойные функции кодонов в генетическом коде» . Критические обзоры биохимии и молекулярной биологии . 45 (4): 257–65. doi : 10.3109/10409231003786094 . PMC 3311535 . PMID 20446809 .
- ^ Young VR (август 1994 г.). «Требования к аминокислотам для взрослых: случай серьезного пересмотра в текущих рекомендациях» (PDF) . Журнал питания . 124 (8 Suppl): 1517S - 1523S. doi : 10.1093/jn/124.suppl_8.1517s . PMID 8064412 .
- ^ Эйвс А (август 2011 г.). «Модель протоанти-кодонских РНК-ферментов, требующих гомохиральности L-аминокислот» . Журнал молекулярной эволюции . 73 (1–2): 10–22. Bibcode : 2011jmole..73 ... 10e . doi : 10.1007/s00239-011-9453-4 . PMC 3223571 . PMID 21779963 .
- ^ Френкель-Пинтер, Моран; Хейнс, Джей У.; С, Мартин; Петров, Антон с.; Burcar, Bradley T.; Кришнамурти, Раманараянан; HUD, Nicholas v.; Леман, Люк Дж.; Уильямс, Лорен Дин (2019-08-13). «Селективное включение белков по сравнению с непротеинационными катионными аминокислотами в модельные пребиотические реакции олигомеризации» . Труды Национальной академии наук . 116 (33): 16338–16346. BIBCODE : 2019PNAS..11616338F . doi : 10.1073/pnas.1904849116 . ISSN 0027-8424 . PMC 6697887 . PMID 31358633 .
- ^ Thurlkill RL, Grimsley GR, Scholtz JM, Pace CN (май 2006 г.). «Значения PK ионизируемых групп белков» . Белковая наука . 15 (5): 1214–8. doi : 10.1110/ps.051840806 . PMC 2242523 . PMID 16597822 .
- ^ Пейс CN, Grimsley GR, Scholtz JM (май 2009 г.). «Белковые ионизируемые группы: значения PK и их вклад в стабильность и растворимость белка» . Журнал биологической химии . 284 (20): 13285–9. doi : 10.1074/jbc.r800080200 . PMC 2679426 . PMID 19164280 .
- ^ Byun BJ, Kang YK (май 2011 г.). «Конформационные предпочтения и значение PK (A) остатка селеноцистеина». Биополимеры . 95 (5): 345–53. doi : 10.1002/bip.21581 . PMID 21213257 . S2CID 11002236 .
- ^ Rother M, Krzycki JA (август 2010 г.). «Селеноцистеин, пирролизин и уникальный энергетический метаболизм метаногенной археи» . Археи . 2010 : 1–14. doi : 10.1155/2010/453642 . PMC 2933860 . PMID 20847933 .
- ^ Kozlowski LP (январь 2017 г.). «Протеом-PI: Протеоемная изоэлектрическая база данных точек» . Исследование нуклеиновых кислот . 45 (D1): D1112 - D1116. doi : 10.1093/nar/gkw978 . PMC 5210655 . PMID 27789699 .
- ^ «Атомные веса и изотопные композиции для всех элементов» . Нист . Получено 2016-12-12 .
- ^ Phillips R, Kondev J, Theriot J, Garcia HG, Orme N (2013). Физическая биология клетки (второе изд.). Гарлендская наука. п. 178. ISBN 978-0-8153-4450-6 .
- ^ Ferier DR (2005). «Глава 20: деградация и синтез аминокислот». В ПК Champe, Harvey RA, Ferrier Dr (Eds.). Иллюстрированные отзывы Липпинкотта: Биохимия (иллюстрированные обзоры Липпинкотта) . Hagerstwon, MD: Lippincott Williams & Wilkins. ISBN 978-0-7817-2265-0 .
Общие ссылки
[ редактировать ]- Нельсон, Дэвид Л.; Кокс, Майкл М. (2000). Лехнингер Принципы биохимии (3 -е изд.). Стоит издатели. ISBN 978-1-57259-153-0 .
- Kyte J, Doolittle RF (май 1982). «Простой метод отображения гидропатического характера белка». Журнал молекулярной биологии . 157 (1): 105–32. Citeseerx 10.1.1.458.454 . doi : 10.1016/0022-2836 (82) 90515-0 . PMID 7108955 .
- Meierhenrich, Uwe J. (2008). Аминокислоты и асимметрия жизни (1 -е изд.). Спрингер. ISBN 978-3-540-76885-2 .
- Биохимия, Harpers (2015). Арперс иллюстрировал биохимию (30 -е изд.). Ланге ISBN 978-0-07-182534-4 .