Пост-транскрипционная модификация
Это отсутствует информация о разделах для РНК, отличной от мРНК. ( Октябрь 2020 г. ) |
| Часть серии на |
| Генетика |
|---|
 |
Транскрипционная модификация или модификация совместной транскрипции представляют собой набор биологических процессов, общих для большинства эукариотических клеток, с помощью которых РНК первичная транскрипт химически изменяется после транскрипции из гена для получения зрелой, функциональной молекулы РНК, которая затем может покинуть ядро и выполнить любой из различные различные функции в ячейке. [ 1 ] Существует много типов посттранскрипционных модификаций, достигнутых с помощью разнообразного класса молекулярных механизмов.
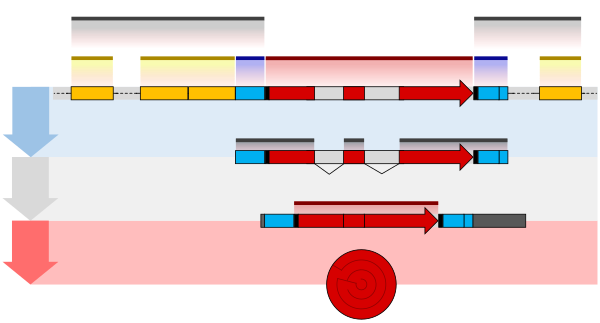
Одним из примеров является преобразование транскриптов РНК -предшественника Мессенджера в зрелую РНКсенджера, которая впоследствии способна транслироваться в белок . Этот процесс включает в себя три основных этапа, которые значительно модифицируют химическую структуру молекулы РНК: добавление 5 'CAP , добавление 3' полиаденилированного хвоста и сплайсинг РНК . Такая обработка жизненно важна для правильной трансляции эукариотических геномов , поскольку начальная мРНК-предшественника, продуцируемая транскрипцией, часто содержит как экзоны (кодирующие последовательности), так и интронов (некодирующие последовательности); Сплайсинг удаляет интроны и напрямую связывает экзоны, в то время как крышка и хвост облегчают транспорт мРНК в рибосому и защищают ее от молекулярной деградации. [ 2 ]
Посттранскрипционные модификации также могут происходить при обработке других транскриптов, которые в конечном итоге становятся переносными РНК , рибосомальной РНК или любым другим типам РНК, используемой клеткой.
Обработка мРНК
[ редактировать ]|
|
5 'Обработка
[ редактировать ]Задержка
[ редактировать ]Закрытие пре-мРНК включает в себя добавление 7-метилгуанозина (M 7 Г) до 5 'конец. Чтобы достичь этого, терминальный 5 'фосфат требует удаления, что выполняется с помощью ферментной РНК -трифосфатазы . Фермент гуанозилтрансфераза затем катализирует реакцию, которая продуцирует конец дифосфата 5 '. Конец дифхосфата 5 'затем атакует атом альфа -фосфора молекулы GTP , чтобы добавить остаток гуанина в 5'5 -' трифосфатном звене. Фермент (гуанин- n 7 -)-Метилтрансфераза («Cap MTase») передает метильную группу от S-аденозилметионина в гуаниновое кольцо. [ 4 ] Этот тип крышки, только с (м 7 G) в положении называется структура CAP 0. Рибоза также может быть метилирована , соседнего нуклеотида чтобы получить крышку 1. Метилирование нуклеотидов ниже по течению от молекулы РНК продуцирует CAP 2, структуры CAP 3 и так далее. В этих случаях метильные группы добавляются к 2 'ОН -группам рибозного сахара. Крышка защищает 5 'конец первичного транскрипта РНК от атаки рибонуклеазами , которые имеют специфичность до 3'5' фосфодиэфирных связей . [ 5 ]
3 'обработка
[ редактировать ]Расщепление и полиаденилирование
[ редактировать ]Процедура до мРНК на 3 'конце молекулы РНК включает расщепление его 3' конца, а затем добавление около 250 остатков аденина с образованием поли (а) хвоста . Реакции расщепления и аденилирования происходят главным образом, если сигнала полиаденилирования (5'-аааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааааа последовательность -3 ') и является местом расщепления. Богатая последовательность GU также обычно присутствует вниз по течению на молекуле пре-мРНК. Совсем недавно было продемонстрировано, что альтернативные сигнальные последовательности, такие как Ugua вверх по течению от сайта расщепления, также могут направлять расщепление и полиаденилирование в отсутствие сигнала Aauaaa. Эти два сигнала не являются взаимно независимыми и часто сосуществуют. После синтеза элементов последовательности несколько мульти-субъединичных белков переносятся в молекулу РНК. Передача этих специфических для последовательности белков расщепления белков и фактора специфичности полиаденилирования (CPSF), коэффициента расщепления I (CF I) и Коэффициент стимуляции расщепления (CSTF) происходит из РНК -полимеразы II . Три фактора связываются с элементами последовательности. Сигнал AAUAAA напрямую связан CPSF. Для Угуа -зависимых сайтов обработки связывание мульти белкового комплекса осуществляется с помощью фактора расщепления I (ср. I). Результирующий белковой комплекс содержит дополнительные коэффициенты расщепления и полиаденилат -полимеразу фермента (PAP). Этот комплекс расщепляет РНК между последовательности полиаденилирования и богатой последовательности ГУ в месте расщепления, отмеченной последовательностями (5'-CA-3 '). Поли (а) полимераза затем добавляет около 200 адденских единиц к новому 3 'конец молекулы РНК с использованием АТФ в качестве предшественника. По мере синтезируемого поли (а) хвоста он связывает несколько копий поли (a)-связывающего белка , что защищает 3'end от расщепления рибонуклеазы ферментами, включая комплекс CCR4-NOT . [ 5 ]
Интрон сплайсинг
[ редактировать ]Сплайсинг РНК-это процесс, посредством которого интроны , области РНК не кодируют белки, удаляются из пре-мРНК и оставшиеся экзоны, соединенные для повторной формы одной непрерывной молекулы. Экзоны представляют собой секции мРНК, которые становятся «экспрессируемыми» или переводятся в белок. Они являются кодирующими частями молекулы мРНК. [ 6 ] Хотя большая часть сплайсинга РНК происходит после полного синтеза и конечной капитализации пре-мРНК, транскрипты со многими экзонами могут быть сплайсированы совместно. [ 7 ] Реакция сплайсинга катализируется большим белковым комплексом, называемой сплайсосомой, собранной из белков, и малых молекул ядерной РНК , которые распознают сайты сплайсинга в последовательности пре-мРНК. Многие пре-мРНК, в том числе те, которые кодируют антитела , могут быть сплайсированы несколькими способами для получения различных зрелых мРНК, которые кодируют различные последовательности белка . Этот процесс известен как альтернативный сплайсинг и обеспечивает производство большого разнообразия белков из ограниченного количества ДНК.
Обработка мРНК гистона
[ редактировать ]Гистоны H2A, H2B, H3 и H4 образуют ядро нуклеосомы и , следовательно, называются основными гистонами . Обработка основных гистонов осуществляется по -разному, потому что в типичной мРНК гистонов отсутствует несколько признаков других эукариотических мРНК, таких как поли (а) хвост и интроны. Таким образом, такие мРНК не подвергаются сплайсингу, и их 3 'обработка осуществляется независимо от большинства факторов расщепления и полиаденилирования. МРНК основных гистонов имеют особую структуру стволовых петли на 3-х пострадавшем конце, которая распознается белком , связывающим стволовой , и нисходящей последовательности, называемой гистоновым нижним элементом (HDE), который рекрутирует SnRNA U7 . Фактор специфичности расщепления и полиаденилирования фактор 73 сокращает мРНК между петлей стебля и HDE [ 8 ]
Однако варианты гистонов, такие как H2A.Z или H3.3, имеют интроны и обрабатываются как нормальные мРНК, включая сплайсинг и полиаденилирование. [ 8 ]
Смотрите также
[ редактировать ]Ссылки
[ редактировать ]- ^ KISS T (июль 2001 г.). «Небольшая нуклеолярная РНК-подведенная посттранскрипционная модификация клеточных РНК» . Embo Journal . 20 (14): 3617–22. doi : 10.1093/emboj/20.14.3617 . PMC 125535 . PMID 11447102 .
- ^ Berg, Tymoczko & Stryer 2007 , p. 836
- ^ Jump up to: а беременный Шафи, Томас; Лоу, Рохан (2017). «Эукариотическая и прокариотическая структура генов» . Викиджурнал медицины . 4 (1). doi : 10.15347/wjm/2017.002 . ISSN 2002-4436 .
- ^ Yamada-Okabe T, Mio T, Kashima Y, Matsui M, Arisawa M, Yamada-Okabe H (ноябрь 1999 г.). «Ген Candida albicans для мРНК 5-Cap метилтрансферазы: идентификация дополнительных остатков, необходимых для катализа» . Микробиология . 145 (Pt 11) (11): 3023–33. doi : 10.1099/00221287-145-11-3023 . PMID 10589710 .
- ^ Jump up to: а беременный Hames & Hooper 2006 , p. 221
- ^ Биология . Mgraw Hill Education. 2014. С. 241–242. ISBN 978-981-4581-85-1 .
- ^ Lodish HF, Berk A, Kaiser C, Krieger M, Scott MP, Bretscher A, Ploegh H, Matsudaira PT (2007). «Глава 8: Пост-транскрипционный контроль генов». Молекулярная клетка. Биология . Сан -Франциско: WH Freeman. ISBN 978-0-7167-7601-7 .
- ^ Jump up to: а беременный Marzluff WF, Wagner EJ, Duronio RJ (ноябрь 2008 г.). «Метаболизм и регуляция мРНК канонических гистонов: жизнь без поли (а) хвоста» . Природные обзоры. Генетика . 9 (11): 843–54. doi : 10.1038/nrg2438 . PMC 2715827 . PMID 18927579 .
Дальнейшее чтение
[ редактировать ]- Berg JM, Tymoczko JL, Stryer L (2007). Биохимия (6 изд.). Нью -Йорк : WH Freeman & Co. ISBN 978-0-7167-6766-4 .
- Hames D, Hooper N (2006). Мгновенные заметки Биохимия . Тол. 58 (3 изд.). Лидс : Тейлор и Фрэнсис. п. 767. ISBN 978-0-415-36778-3 Полем PMID 11098183 .
{{cite book}}:|journal=игнорируется ( помощь ) - Sun WJ, Li JH, Liu S, Wu J, Zhou H, Qu LH, Yang JH (январь 2016 г.). «RMBase: ресурс для декодирования ландшафта модификаций РНК из высокопроизводительных данных секвенирования» . Исследование нуклеиновых кислот . 44 (D1): D259-65. doi : 10.1093/nar/gkv1036 . PMC 4702777 . PMID 26464443 .
- Machnicka MA, Milanowska K, Osman Oglou O, Purta E, Kurkowska M, Olchowik A, Januszewski W, Kalinowski S, Dunin-Horkawicz S, Rother KM, Helm M, Bujnicki JM, Grosjean H (январь 2013 г.). «MODOMICS: база данных путей модификации РНК-обновление 2013» . Исследование нуклеиновых кислот . 41 (проблема базы данных): D262-7. doi : 10.1093/nar/gks1007 . PMC 3531130 . PMID 23118484 .
- Cantara WA, Crain PF, Rozenski J, McCloskey JA, Harris KA, Zhang X, Vendeix FA, Fabris D, Agris PF (январь 2011 г.). «База данных модификации РНК, RNAMDB: 2011 Обновление» . Исследование нуклеиновых кислот . 39 (выпуск базы данных): D195-201. doi : 10.1093/nar/gkq1028 . PMC 3013656 . PMID 21071406 .
- Пост-транскрипция+РНК+модификация в Национальной библиотеке Медицинской библиотеки Медицинской библиотеки (Mesh)