оксалат железа
 | |
| Имена | |
|---|---|
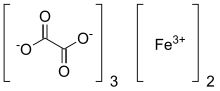
| Систематическое название ИЮПАК этандиоат железа(3+) (2:3) | |
| Другие имена Оксалат железа(III) | |
| Идентификаторы | |
| |
3D model ( JSmol ) | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.019.047 |
| Номер ЕС |
|
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| С 6 Fe 2 О 12 | |
| Молярная масса | 375.747 g/mol |
| Появление | Бледно-желтое твердое вещество (безводное) Лаймово-зеленое твердое вещество (гексагидрат) |
| Запах | без запаха |
| Температура плавления | 365,1 ° С (689,2 ° F) |
| слабо растворим | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Оксалат железа , также известный как оксалат железа(III) , относится к неорганическим соединениям с формулой Fe 2 (C 2 O 4 ) 3 (H 2 O) x , но также может относиться к солям [Fe(C 2 O 4 ) 3 ] 3- . Fe 2 (C 2 O 4 ) 3 (H 2 O) x являются координационными полимерами различной степени гидратации. Координационный комплекс по формуле [Fe(C 2 O 4 ) 3 ] 3- образует множество солей, хорошо известным примером является ферриоксалат калия . В этой статье особое внимание уделяется координации полимеров.
Структура
[ редактировать ]Тетрагидрат
[ редактировать ]

По данным рентгеноструктурного анализа тетрагидрата Fe 2 (C 2 O 4 ) 3 · 4 H 2 O , железо октаэдрическое. Оксалатные лиганды являются мостиковыми . Некоторые через все четыре атома кислорода, некоторые через два атома кислорода. Половина воды представляет собой решетчатую воду , расположенную между цепочками оксалатов железа. Мессбауэровский спектр Fe 2 (C 2 O 4 ) 3 · 4 H 2 O демонстрирует изомерный сдвиг 0,38 мм/с и квадрупольное расщепление 0,40 мм/с, что указывает на высокий спин Фе 3+ в октаэдрической координации. [1] [2]
Производство
[ редактировать ]Оксалат железа можно получить реакцией гидроксида железа (III) и раствора щавелевой кислоты :
- 2Fe(OH) 3 + 3H 2 C 2 O 4 → Fe 2 (C 2 O 4 ) 3 + 6H 2 O
Использование
[ редактировать ]Стоматология
[ редактировать ]Как и многие оксалаты, оксалат железа исследовался в качестве краткосрочного средства лечения гиперчувствительности дентина . [3] Он используется в некоторых составах зубных паст; однако его эффективность подвергается сомнению. [4]
Фотография
[ редактировать ]Оксалат железа используется в качестве светочувствительного элемента в Kallitype процессе фотопечати ; и процесс платинотипии «Платиновая/палладиевая печать».
Батареи
[ редактировать ]Тетрагидрат оксалата железа был исследован как возможный дешевый материал для положительного электрода литий-железных батарей . Он может интеркалировать ионы лития при среднем потенциале 3,35 В и показал устойчивую емкость 98 мАч/г. [1]
Органический синтез
[ редактировать ]Гексагидрат оксалата железа используется с боргидридом натрия для радикальных Марковникова реакций гидрофункционализации алкенов. [5]
См. также
[ редактировать ]Известен ряд других оксалатов железа:
Ссылки
[ редактировать ]- ^ Jump up to: а б Ауари, Ханья; Русе, Гвеналь; Родригес-Карвахаль, Хуан; Суграти, Мулай-Тахар; Собаньер, Матье; Корти, Матье; Рехам, Надир; Тараскон, Жан-Мари (2015). «Раскрытие структуры тетрагидрата оксалата железа (III) и его способности к обратимому внедрению лития». Химия материалов . 27 (5): 1631–1639. дои : 10.1021/см5043149 .
- ^ Русе, Г.; Родригес-Карвахаль, Дж. (2016). «Опосредованный оксалатами дальний антиферромагнетизм в Fe 2 (C 2 O 4 ) 3 ·4H 2 O». Транзакции Далтона . 45 (36): 14311–14319. дои : 10.1039/C6DT02740G . ПМИД 27539964 .
- ^ Гиллам, генеральный директор; Ньюман, Х.Н.; Дэвис, Э.Х.; Булман, Дж.С.; Труллос, ES; Курро, ФА (2004). «Клиническая оценка оксалата железа в снижении гиперчувствительности дентина». Журнал реабилитации полости рта . 31 (3): 245–250. дои : 10.1046/j.0305-182X.2003.01230.x . ПМИД 15025657 .
- ^ Кунья-Круз, Дж.; Стаут, младший; Хитон, LJ; Ватаха, JC (29 декабря 2010 г.). «Гиперчувствительность дентина и оксалаты: систематический обзор» . Журнал стоматологических исследований . 90 (3): 304–310. дои : 10.1177/0022034510389179 . ПМК 3144108 . ПМИД 21191127 .
- ^ Баркер, Тимоти (15 апреля 2001 г.). «Гексагидрат оксалата железа». Энциклопедия реагентов для органического синтеза (1-е изд.). Уайли. стр. 1–4. дои : 10.1002/047084289X.rn02346 . ISBN 978-0-471-93623-7 . S2CID 225482606 .