гликопептид
Гликопептиды — это пептиды , которые содержат углеводные фрагменты ( гликаны ), ковалентно присоединенные к боковым цепям аминокислотных остатков , составляющих пептид.
За последние несколько десятилетий было признано, что гликаны на поверхности клеток (прикрепленные к мембранным белкам или липидам ) и те, которые связаны с белками ( гликопротеины ), играют решающую роль в биологии. Например, было показано, что эти конструкции играют важную роль в оплодотворении . [ 1 ] система иммунная , [ 2 ] развитие мозга , [ 3 ] система эндокринная , [ 3 ] и воспаление . [ 3 ] [ 4 ] [ 5 ]
Синтез . гликопептидов предоставляет исследователям биологические зонды для выяснения функции гликанов в природе и продукты, которые имеют полезные терапевтические и биотехнологические применения [ нужны разъяснения ] [ нужна ссылка ]
Разнообразие гликопептидных связей
[ редактировать ]N- связанные гликаны
[ редактировать ]N -связанные гликаны получили свое название из-за того, что гликан присоединен к остатку аспарагина (Asn, N), и являются одними из наиболее распространенных связей, встречающихся в природе. Хотя большинство N-связанных гликанов имеют форму GlcNAc-β-Asn [ 6 ] другие менее распространенные структурные связи, такие как GlcNac-α-Asn [ 7 ] и Глк-Асн [ 8 ] наблюдались. В дополнение к своей функции в сворачивании белка и прикреплении клеток, N-подобные гликаны белка могут модулировать функцию белка, в некоторых случаях действуя как выключатель. [ 5 ]

О- связанные гликаны
[ редактировать ]О -связанные гликаны образуются путем связи между боковой цепью аминокислоты гидроксильной (обычно серина или треонина ) с гликаном. Большинство O -связанных гликанов имеют форму GlcNac-β-Ser/Thr или GalNac-α-Ser/Thr. [ 6 ]

С- связанные гликаны
[ редактировать ]Из трех связей наименее распространенными и наименее изученными являются С -связанные гликаны. С-связь относится к ковалентному присоединению маннозы к остатку триптофана . Примером С-связанного гликана является α-маннозилтриптофан. [ 9 ] [ 10 ]
Синтез гликопептидов
[ редактировать ]В литературе описано несколько методов синтеза гликопептидов. Из этих методов наиболее распространенные стратегии перечислены ниже.
Твердофазный синтез пептидов
[ редактировать ]В рамках твердофазного пептидного синтеза (SPPS) существуют две стратегии синтеза гликопептидов: линейная и конвергентная сборка. Линейная сборка основана на синтезе строительных блоков, а затем использовании SPPS для соединения строительных блоков вместе. Схема этого подхода проиллюстрирована ниже.
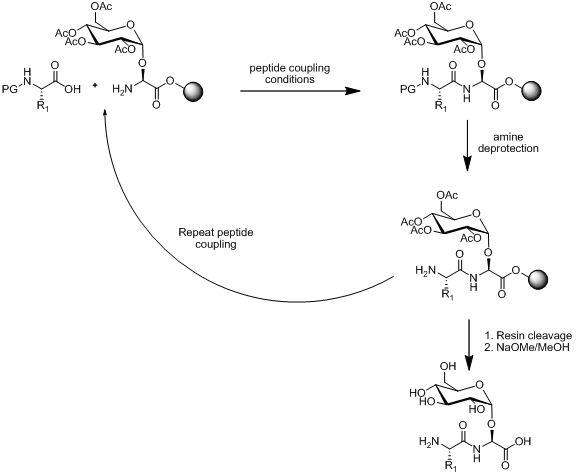
Существует несколько методов синтеза моносахаридного аминокислотного строительного блока, как показано ниже.
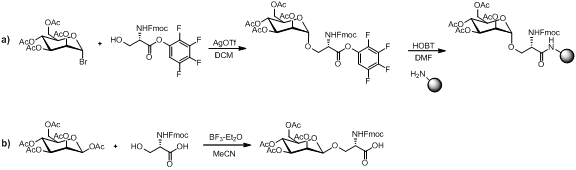
При условии, что моносахаридный аминокислотный строительный блок стабилен в условиях пептидного связывания, условий снятия защитной группы амина и расщепления смолы. Линейная сборка остается популярной стратегией синтеза гликопептидов, и в литературе имеется множество примеров. [ 13 ] [ 14 ] [ 15 ]
В стратегии конвергентной сборки пептидная цепь и остаток гликана сначала синтезируются отдельно. Затем гликан гликозилируется по определенному остатку пептидной цепи. Этот подход не так популярен, как линейная стратегия, из-за плохих выходов реакции на стадии гликозилирования . [ 16 ]
Другая стратегия создания библиотек гликопептидов — использование метода синтеза Glyco-SPOT. [ 17 ] Методика расширяет существующий метод SPOT-синтеза. [ 18 ] В этом методе библиотеки гликопептидов создаются на поверхности целлюлозы (например, фильтровальной бумаги), которая действует как твердая фаза. Гликопептиды производятся путем обнаружения аминокислот, защищенных FMOC, что позволяет осуществлять синтез в масштабе микрограммов (наномолей) с использованием очень небольших количеств гликоаминокислот. Масштаб этого метода может быть преимуществом для создания библиотек для скрининга за счет использования меньшего количества гликоаминокислот на пептид. Однако для производства большего количества гликопептидов лучше использовать традиционные твердофазные методы на основе смол.
Нативное химическое лигирование
[ редактировать ]Нативное химическое лигирование (NCL) представляет собой конвергентную синтетическую стратегию, основанную на линейном соединении гликопептидных фрагментов. В этом методе используется хемоселективная реакция между N-концевым остатком цистеина одного пептидного фрагмента и тиоэфиром на С-конце другого пептидного фрагмента. [ 19 ] как показано ниже.
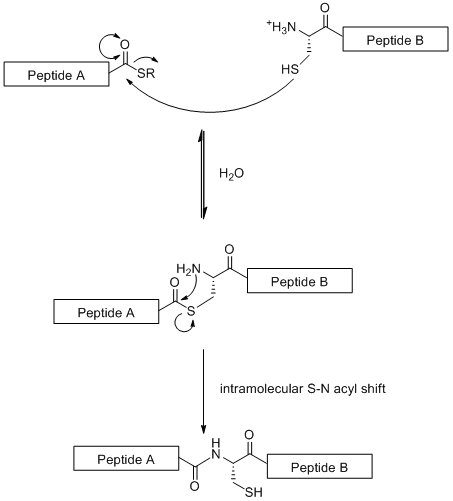
В отличие от стандартного SPPS (который ограничен 50 аминокислотными остатками), NCL позволяет строить большие гликопептиды. Однако эта стратегия ограничена тем фактом, что для нее требуется остаток цистеина на N-конце , аминокислотный остаток, который редко встречается в природе. [ 19 ] Однако эта проблема частично была решена путем селективной десульфурации остатка цистеина до аланина . [ 20 ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Талбот П.; Шур Б.Д.; Майлз Д.Г. (2003). «Адгезия клеток и оплодотворение: этапы транспортировки ооцитов, взаимодействие спермия-пеллюцида и слияние спермия-яйцеклетки» . Биология размножения . 68 (1): 1–9. дои : 10.1095/biolreprod.102.007856 . ПМИД 12493688 . S2CID 10166894 .
- ^ Радд П.М.; Эллиотт Т.; Крессвелл П.; Уилсон И.А.; Двек РА (2001). «Гликозилирование и иммунная система». Наука . 291 (5512): 2370–2376. Бибкод : 2001Sci...291.2370R . дои : 10.1126/science.291.5512.2370 . ПМИД 11269318 .
- ^ Jump up to: а б с Варки А (1993). «Биологическая роль олигосахаридов – все теории верны» . Гликобиология . 3 (2): 97–130. дои : 10.1093/гликоб/3.2.97 . ПМЦ 7108619 . ПМИД 8490246 .
- ^ Бертоцци ЧР; Кисслинг Л.Л. (2001). «Химическая гликобиология». Наука . 291 (5512): 2357–2364. Бибкод : 2001Sci...291.2357B . дои : 10.1126/science.1059820 . ПМИД 11269316 . S2CID 9585674 .
- ^ Jump up to: а б Маверакис Э., Ким К., Шимода М., Гершвин М., Патель Ф., Уилкен Р., Райчаудхури С., Рухаак Л.Р., Лебрилла CB (2015). «Гликаны в иммунной системе и теория аутоиммунитета с измененными гликанами» . Дж. Аутоиммун . 57 (6): 1–13. дои : 10.1016/j.jaut.2014.12.002 . ПМЦ 4340844 . ПМИД 25578468 .
- ^ Jump up to: а б Влигентхарт Дж.Ф.Г.; Кассет Ф. (1998). «Новые формы гликозилирования белков». Современное мнение в области структурной биологии . 8 (5): 565–571. дои : 10.1016/s0959-440x(98)80145-0 . hdl : 1874/5477 . ПМИД 9818259 . S2CID 9360182 .
- ^ Шибата С.; Такеда Т.; Натори Ю. (1988). «Структура нефритогенозида — нефритогенного гликопептида с альфа-N-гликозидной связью» . Журнал биологической химии . 263 (25): 12483–12485. дои : 10.1016/S0021-9258(18)37780-9 . ПМИД 3410849 .
- ^ Виланд Ф.; Хейцер Р.; Шефер В. (1983). «Аспарагинилглюкоза — новый тип углеводной связи» . Труды Национальной академии наук Соединенных Штатов Америки . 80 (18): 5470–5474. Бибкод : 1983PNAS...80,5470W . дои : 10.1073/pnas.80.18.5470 . ПМЦ 384279 . ПМИД 16593364 .
- ^ Дебир Т.; Влигентхарт Дж.Ф.Г.; Лоффлер А.; Хофстендж Дж. (1995). «Гексопиранозильный остаток, который C-гликозидно связан с боковой цепью триптофана-7 в человеческой РНКазе США, представляет собой альфа-мармопиранозу». Биохимия . 34 (37): 11785–11789. дои : 10.1021/bi00037a016 . hdl : 1874/5760 . ПМИД 7547911 . S2CID 22324479 .
- ^ Ихара, Ёсито; Инай, Йоко; Икезаки, Мидори; Мацуи, Ин-Сук Л.; Манабе, Сино; Ито, Юкисиге (2014). «C-маннозилирование: модификация триптофана в клеточных белках». Гликосаука: биология и медицина : 1–8. дои : 10.1007/978-4-431-54836-2_67-1 . ISBN 978-4-431-54836-2 . S2CID 82050024 .
- ^ Янссон А.М.; Мелдал М.; Бок К. (1990). «Активный эфир N-Fmoc-3-O-[Ac4-Alpha-D-Manp-(1-]2)-Ac3-Alpha-D-Manp-1-]-Треонин-O-Pfp как строительный блок в Твердофазный синтез О-связанного диманнозилгликопептида». Буквы тетраэдра . 31 (48): 6991–6994. дои : 10.1016/s0040-4039(00)97224-1 .
- ^ Элофссон М.; Уолс Б.; Кильберг Дж. (1991). «Строительные блоки для синтеза гликопептидов - гликозилирование 3-меркаптопропионовой кислоты и Fmoc-аминокислот с незащищенными карбоксильными группами». Буквы тетраэдра . 32 (51): 7613–7616. дои : 10.1016/0040-4039(91)80548-к .
- ^ Ли Х.Г.; Ли Б.; Сон HJ; Брейдо Л.; Баскаков И.В.; Ван LX (2005). «Хемоферментативный синтез гликопептидов ВИЧ-1V3, несущих два N-гликана, и эффекты гликозилирования на пептидный домен». Журнал органической химии . 70 (24): 9990–9996. дои : 10.1021/jo051729z . ПМИД 16292832 .
- ^ Ямамото Н.; Такаянаги Ю.; Ёсино А.; Сакакибара Т.; Кадзихара Ю. (2007). «Подход к синтезу сиалилгликопептидов, связанных с аспарагином, имеющих интактные и гомогенные ундекадисиалилолигосахариды сложного типа». Химия: Европейский журнал . 13 (2): 613–625. дои : 10.1002/chem.200600179 . ПМИД 16977655 .
- ^ Шао Н.; Сюэ Дж.; Го ZW (2003). «Химический синтез гликопептидов CD52, содержащих кислотолабильную фукозильную связь». Журнал органической химии . 68 (23): 9003–9011. дои : 10.1021/jo034773s . PMID 14604374 .
- ^ Гамблин Д.П.; Сканлан ЭМ; Дэвис Б.Г. (2009). «Синтез гликопротеинов: обновление». Химические обзоры . 109 (1): 131–163. дои : 10.1021/cr078291i . ПМИД 19093879 .
- ^ Мехта, AY; Вирайя, РХ; Дутта, С; Гот, СК; Ханес, М.С.; Гао, К; Ставенхаген, К; Кардиш, Р; Мацумото, Ю; Хаймбург-Молинаро, Дж; Бойс, М; Пол, НЛБ; Каммингс, РД (29 июня 2020 г.). «Параллельный синтез гликопептидных библиотек Glyco-SPOT» . Клеточная химическая биология . 27 (9): 1207–1219.e9. doi : 10.1016/j.chembiol.2020.06.007 . ПМЦ 7556346 . ПМИД 32610041 .
- ^ Хильперт, К; Винклер, Д.Ф.; Хэнкок, Р.Э. (2007). «Пептидные массивы на целлюлозной основе: SPOT-синтез, эффективный по времени и затратам метод синтеза большого количества пептидов параллельным и адресуемым способом». Протоколы природы . 2 (6): 1333–49. дои : 10.1038/nprot.2007.160 . ПМИД 17545971 . S2CID 32143600 .
- ^ Jump up to: а б Нильссон Б.Л.; Зёлльнер МБ; Рейнс РТ (2005). «Химический синтез белков» . Ежегодный обзор биофизики и биомолекулярной структуры . 34 : 91–118. doi : 10.1146/annurev.biophys.34.040204.144700 . ПМЦ 2845543 . ПМИД 15869385 .
- ^ Ван Ц.; Данишефский С.Дж. (2007). «Специфическая десульфурация цистеина на основе свободных радикалов: мощный прогресс в синтезе полипептидов и гликополипептидов». Энджью. Хим . 119 (48): 9408–9412. Бибкод : 2007AngCh.119.9408W . дои : 10.1002/ange.200704195 . ПМИД 18046687 .
Дальнейшее чтение
[ редактировать ]- Эмануал Маверакис; и др. «Гликаны в иммунной системе и теория аутоиммунитета с измененными гликанами» (PDF) .
Внешние ссылки
[ редактировать ] СМИ, связанные с гликопептидами, на Викискладе?
СМИ, связанные с гликопептидами, на Викискладе?