Гальваника

Гальваника известная как электрохимическое осаждение или электроосаждение , представляет собой процесс создания металлического покрытия на твердой подложке путем восстановления катионов , также этого металла с помощью постоянного электрического тока . Часть, на которую будет нанесено покрытие, действует как катод (отрицательный электрод ) электролитической ячейки ; электролит представляет собой раствор соли ( покрываемого металла, а анод положительный электрод) обычно представляет собой либо блок этого металла, либо какой-либо инертный проводящий материал. Ток обеспечивается внешним источником питания .
Гальваника широко используется в промышленности и декоративном искусстве для улучшения качества поверхности предметов, например устойчивости к истиранию и коррозии , смазывающей способности , отражательной способности , электропроводности или внешнего вида. Он используется для увеличения толщины деталей меньшего размера или изношенных, а также для изготовления металлических пластин сложной формы (процесс, называемый гальванопластикой) . Он используется для нанесения меди и других проводников при формировании печатных плат и медных межсоединений в интегральных схемах. Он также используется для очистки металлов, таких как медь .
Вышеупомянутая гальваника металлов использует процесс электровосстановления (то есть отрицательный или катодный на рабочем электроде протекает ток). Термин «гальваника» также иногда используется для обозначения процессов, которые происходят при электроокислении (т.е. положительный или анодный ток на рабочем электроде), хотя такие процессы чаще называют анодированием, а не гальванопокрытием. Одним из таких примеров является образование хлорида серебра на серебряной проволоке в растворах хлоридов для изготовления электродов из серебра/хлорида серебра (AgCl) .
Электрополировка — процесс, в котором электрический ток используется для избирательного удаления внешнего слоя с поверхности металлического предмета, является обратным процессу гальваники. [1]
Мощность броска является важным параметром, который обеспечивает меру однородности гальванического тока и, следовательно, однородности толщины гальванического металла на участках детали, находящихся рядом с анодом, по сравнению с областями, удаленными от него. Это зависит главным образом от состава и температуры гальванического раствора, а также от плотности рабочего тока . [2] Более высокая рассеивающая способность гальванической ванны приводит к более равномерному покрытию. [3]
Процесс
[ редактировать ]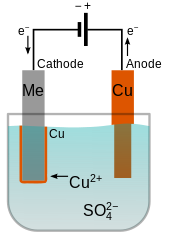
4 в серной кислоте . Медный анод используется для пополнения электролита катионами меди Cu. 2+
поскольку они осаждаются на катоде.
Электролит в гальванической ячейке должен содержать положительные ионы (катионы) осаждаемого металла. Эти катионы восстанавливаются на катоде до металла в состоянии нулевой валентности. Например, электролитом для гальваники меди может служить раствор сульфата меди(II) , который диссоциирует на Cu. 2+ катионы и SO 2−
4 аниона. На катоде Cu 2+ восстанавливается до металлической меди путем присоединения двух электронов.
Когда анод изготовлен из металла, предназначенного для нанесения покрытия на катод, на аноде может протекать противоположная реакция, превращающая его в растворенные катионы. Например, медь окисляется на аноде до Cu. 2+ потеряв два электрона. В этом случае скорость растворения анода будет равна скорости покрытия катода, и, таким образом, ионы в электролитной ванне постоянно пополняются анодом. Конечным результатом является эффективный перенос металла от анода к катоду. [4]
Вместо этого анод может быть изготовлен из материала, устойчивого к электрохимическому окислению, такого как свинец или углерод . кислород , перекись водорода Вместо этого на аноде образуются и некоторые другие побочные продукты. В этом случае ионы плакируемого металла необходимо пополнять (постоянно или периодически) в ванне по мере их вытягивания из раствора. [5]
Покрытие чаще всего представляет собой один металлический элемент , а не сплав . Однако некоторые сплавы можно подвергать электроосаждению, особенно латунь и припой . Покрытые «сплавы» не являются «настоящими сплавами» (твердыми растворами), а представляют собой крошечные кристаллы покрываемых элементарных металлов. В случае припоя с покрытием иногда считается необходимым иметь настоящий сплав, и припой с покрытием плавят, чтобы олово и свинец соединились в настоящий сплав. Настоящий сплав более устойчив к коррозии, чем смесь в исходном состоянии.
Многие гальванические ванны содержат цианиды других металлов (например, цианид калия ) в дополнение к цианидам осаждаемого металла. Эти свободные цианиды способствуют анодной коррозии, помогают поддерживать постоянный уровень ионов металлов и способствуют повышению проводимости. неметаллические химические вещества, такие как карбонаты и фосфаты Кроме того, для повышения проводимости могут быть добавлены .
Если нанесение покрытия на определенные участки основания нежелательно, применяются ограничители , предотвращающие контакт ванны с основанием. Типичные средства защиты включают ленту, фольгу, лаки и воски . [6]
Ударять
[ редактировать ]Первоначально можно использовать специальный слой покрытия, называемый ударом или вспышкой, для формирования очень тонкого (обычно толщиной менее 0,1 мкм) покрытия высокого качества и хорошего сцепления с подложкой. Это служит основой для последующих процессов нанесения покрытия. При ударе используется высокая плотность тока и ванна с низкой концентрацией ионов. Этот процесс медленный, поэтому после достижения желаемой толщины удара используются более эффективные процессы нанесения покрытия.
Метод чеканки также применяется в сочетании с гальванопокрытием различных металлов. Если желательно нанести на металл один тип покрытия для улучшения коррозионной стойкости, но этот металл по своей природе имеет плохую адгезию к подложке, то сначала можно нанести слой, совместимый с обоими. Одним из примеров такой ситуации является плохая адгезия электролитического никеля к цинковым сплавам, и в этом случае используется медная накладка, которая имеет хорошее сцепление с обоими. [5]
Импульсная гальваника
[ редактировать ]Процесс импульсного гальванического покрытия или импульсного электроосаждения (PED) включает в себя быстрое изменение электрического потенциала или тока между двумя разными значениями, в результате чего образуется серия импульсов одинаковой амплитуды, длительности и полярности, разделенных нулевым током. Изменяя амплитуду и ширину импульса, можно изменять состав и толщину наносимой пленки. [7]
Экспериментальные параметры импульсного гальванического покрытия обычно состоят из пикового тока/потенциала, рабочего цикла, частоты и эффективного тока/потенциала. Пиковый ток/потенциал — это максимальное значение гальванического тока или потенциала. Рабочий цикл — это эффективная часть времени в определенном периоде гальваники с приложенным током или потенциалом. Эффективный ток/потенциал рассчитывается путем умножения рабочего цикла и пикового значения тока или потенциала. Импульсное гальванопокрытие может помочь улучшить качество гальванической пленки и снять внутреннее напряжение, возникающее во время быстрого осаждения. Сочетание короткого рабочего цикла и высокой частоты может уменьшить образование поверхностных трещин. Однако для поддержания постоянного эффективного тока или потенциала может потребоваться высокопроизводительный источник питания, обеспечивающий высокий ток/потенциал и быстрое переключение. Другая распространенная проблема импульсной гальваники заключается в том, что материал анода может быть покрыт металлом и загрязнен во время обратного гальванопокрытия, особенно для дорогих инертных электродов, таких как платина .
Другие факторы, влияющие на импульсное гальванопокрытие, включают температуру, зазор между анодом и катодом и перемешивание. Иногда импульсное гальванопокрытие можно проводить в нагретой гальванической ванне для увеличения скорости осаждения, поскольку скорость большинства химических реакций увеличивается экспоненциально с температурой по закону Аррениуса . Зазор между анодом и катодом связан с распределением тока между анодом и катодом. Небольшое соотношение площади зазора к площади образца может привести к неравномерному распределению тока и повлиять на топологию поверхности покрытого образца. Перемешивание может увеличить скорость переноса/диффузии ионов металлов из основного раствора на поверхность электрода. Идеальные настройки перемешивания различаются для разных процессов гальванопокрытия металлов.
Щеточная гальваника
[ редактировать ]Близким процессом является щеточная гальваника, при которой на отдельные участки или целые изделия наносят покрытие с помощью щетки, пропитанной гальваническим раствором. Щетка, обычно представляющая собой корпус из нержавеющей стали , обернутый впитывающим тканевым материалом, который одновременно удерживает раствор для покрытия и предотвращает прямой контакт с покрываемым предметом, подключается к аноду низковольтного источника питания постоянного тока , а предмет - к быть покрытым, соединен с катодом . Оператор погружает кисть в раствор для покрытия, а затем наносит его на изделие, постоянно перемещая кисть, чтобы добиться равномерного распределения материала покрытия.
Щеточная гальваника имеет несколько преимуществ перед обшивкой резервуаров, включая портативность, возможность покрытия предметов, которые по какой-либо причине не могут быть покрыты резервуарами (одним из применений было покрытие частей очень больших декоративных опорных колонн при реставрации здания), низкие требования к маскировке или отсутствие их. и сравнительно низкие требования к объему гальванического раствора. К недостаткам по сравнению с обшивкой резервуаров можно отнести более активное участие оператора (покрытие резервуаров часто может выполняться с минимальным вниманием) и невозможность добиться такой же большой толщины листа.
Обшивка ствола
[ редактировать ]Этот метод гальванического покрытия является одним из наиболее распространенных в промышленности для обработки большого количества небольших объектов. Объекты помещаются в непроводящую клетку бочкообразной формы, а затем погружаются в химическую ванну, содержащую растворенные ионы металла, который должен быть на них нанесен. Затем ствол вращается, и электрические токи проходят через различные части ствола, которые замыкают цепи, когда они соприкасаются друг с другом. В результате получается очень равномерный и эффективный процесс нанесения покрытия, хотя отделка конечного продукта, вероятно, пострадает от истирания во время процесса нанесения покрытия. Он не подходит для декоративных или точно спроектированных изделий. [8]
Чистота
[ редактировать ]Чистота необходима для успешной гальванизации, поскольку молекулярные слои масла могут препятствовать прилипанию покрытия. ASTM B322 — это стандартное руководство по очистке металлов перед гальванопокрытием. Очистка включает очистку растворителем, очистку горячими щелочными моющими средствами, электроочистку, ультразвуковую очистку и кислотную обработку. Наиболее распространенным промышленным испытанием на чистоту является испытание на водонепроницаемость, при котором поверхность тщательно промывают и удерживают вертикально. Гидрофобные загрязнения, такие как масла, заставляют воду скапливаться и распадаться, позволяя воде быстро стекать. Идеально чистые металлические поверхности гидрофильны и сохраняют непрерывный слой воды, который не скапливается и не стекает. ASTM F22 описывает версию этого теста. Этот тест не обнаруживает гидрофильных загрязнений, но гальваника может легко их вытеснить, поскольку растворы основаны на воде. Поверхностно-активные вещества, такие как мыло, снижают чувствительность теста, и их необходимо тщательно смывать.
Тестовые ячейки и характеристика
[ редактировать ]Бросоковая мощность
[ редактировать ]Бросательная мощность (или макрокинетическая мощность ) является важным параметром, который обеспечивает меру однородности гальванического тока и, следовательно, однородности толщины гальванического металла на участках детали, находящихся вблизи анода, по сравнению с областями, удаленными от него. это. Это зависит главным образом от состава и температуры гальванического раствора. [2] Микрорассеивающая способность означает степень, в которой процесс может заполнить или покрыть небольшие углубления, такие как сквозные отверстия . [9] Метательную силу можно охарактеризовать безразмерным числом Вагнера :
где R — универсальная газовая постоянная , T — рабочая температура , κ — ионная проводимость раствора для нанесения покрытия, F — постоянная Фарадея , L — эквивалентный размер объекта с покрытием, α — коэффициент переноса , а i — поверхность -средняя общая (с учетом выделения водорода ) плотность тока. Число Вагнера количественно определяет соотношение кинетического и омического сопротивлений. Более высокое число Вагнера обеспечивает более равномерное осаждение. На практике этого можно добиться, уменьшив размер ( L ) объекта покрытия, уменьшив плотность тока | i |, добавление химикатов, которые снижают α (делают электрический ток менее чувствительным к напряжению), и повышают проводимость раствора (например, путем добавления кислоты ). Параллельное выделение водорода обычно улучшает однородность гальванического покрытия за счет увеличения | я |; однако этот эффект можно компенсировать закупоркой из-за пузырьков водорода и отложений гидроксидов. [10]
Число Вагнера довольно сложно точно измерить; поэтому вместо этого обычно используются другие связанные параметры, которые легче получить экспериментально с использованием стандартных ячеек. Эти параметры получаются из двух соотношений: отношения M = m 1 / m 2 толщины покрытия заданной области катода, «близкой» к аноду, к толщине области, «далекой» от катода и отношения L = x 2 / x 1 расстояний этих участков через электролит до анода. Например, в ячейке Харинга-Блюма L = 5 для ее двух независимых катодов, а соотношение толщины покрытия ячейки M = 6 имеет рассеивающую способность Харринга-Блюма 100% × ( L - M ) / L = -20%. . [9] Другие условные обозначения включают метательную мощность Хитли 100% × ( L − M ) / ( L − 1) и метательную силу Филда 100% × ( L − M ) / ( L + M − 2) . [11] Более однородная толщина достигается за счет увеличения метательной способности (менее отрицательной) в соответствии с любым из этих определений.
Параметры, описывающие рабочие характеристики ячейки, такие как бросающая способность, измеряются в небольших испытательных ячейках различной конструкции, целью которых является воспроизведение условий, аналогичных тем, которые наблюдаются в производственной гальванической ванне. [9]
Ячейка Харинга – Блюма
[ редактировать ]
Ячейка Харинга-Блюма используется для определения макрорассеивающей способности гальванической ванны. Ячейка состоит из двух параллельных катодов с неподвижным анодом посередине. Катоды располагаются на расстояниях от анода в соотношении 1:5. Макросбрасывающая способность рассчитывается по толщине покрытия на двух катодах при постоянного тока пропускании в течение определенного периода времени. Ячейка изготавливается из плексигласа или стекла. [12] [13]
Корпусная ячейка
[ редактировать ]
Ячейка Халла — это тип испытательной камеры, используемой для полуколичественной проверки состояния гальванической ванны. Он измеряет полезный диапазон плотности тока, оптимизирует концентрацию добавок, распознает эффекты примесей и указывает на способность макроизлучения. [14] Ячейка Халла повторяет гальваническую ванну в лабораторном масштабе. Он заполнен образцом гальванического раствора и соответствующим анодом, подключенным к выпрямителю . «Работа» заменяется испытательной панелью для ячеек Халла, на которую будет нанесено покрытие, чтобы показать «здоровье» ванны.
Ячейка Халла представляет собой контейнер трапециевидной формы, вмещающий 267 миллилитров раствора гальванической ванны. Такая форма позволяет расположить тестовую панель под углом к аноду. В результате на осадок наносится покрытие с диапазоном плотности тока по его длине, который можно измерить с помощью линейки ячеек Халла. Объем раствора позволяет провести полуколичественное измерение концентрации добавки: 1 грамм добавки к 267 мл эквивалентен 0,5 унции/галлона в гальваническом резервуаре. [15]
Эффекты
[ редактировать ]Гальваника изменяет химические, физические и механические свойства заготовки. Примером химического изменения является улучшение коррозионной стойкости никелированием . Примером физического изменения является изменение внешнего вида. Примером механического изменения является изменение прочности на разрыв или твердости поверхности , что является обязательным атрибутом в инструментальной промышленности. [16] Гальваническое покрытие кислотным золотом нижележащих цепей с медным или никелированным покрытием снижает контактное сопротивление, а также твердость поверхности. Участки из мягкой стали с медным покрытием действуют как маска, если цементация таких участков нежелательна. Луженую сталь хромируют для предотвращения потускнения поверхности из-за окисления олова.
Конкретные металлы
[ редактировать ]Альтернативы гальванике
[ редактировать ]Существует ряд альтернативных процессов получения металлических покрытий на твердых подложках, не предполагающих электролитического восстановления:
- Для химического осаждения используется ванна, содержащая ионы металлов и химические вещества, которые восстанавливают их до металла посредством окислительно-восстановительных реакций . Реакция должна быть автокаталитической , чтобы новый металл осаждался на растущем покрытии, а не осаждался в виде порошка сразу по всей ванне. Химический процесс широко используется для нанесения никель-фосфорных или никель-борных сплавов для обеспечения износостойкости и коррозионной стойкости, серебра для изготовления зеркал , меди для печатных плат и многих других. Основным преимуществом этих процессов перед гальванопокрытием является то, что они позволяют создавать покрытия одинаковой толщины на поверхностях произвольной формы, даже внутри отверстий, при этом подложка не обязательно должна быть электропроводной. Еще одним важным преимуществом является то, что им не нужны источники питания или аноды специальной формы. К недостаткам относятся более низкая скорость осаждения, расход относительно дорогих химикатов и ограниченный выбор металлов покрытия.
- В процессах нанесения иммерсионного покрытия используются реакции замещения , в которых металл подложки окисляется до растворимых ионов, в то время как ионы металла покрытия восстанавливаются и осаждаются на его месте. Этот процесс ограничен очень тонкими покрытиями, поскольку реакция прекращается после полного покрытия подложки. Тем не менее, он имеет некоторые важные применения, такие как процесс химического иммерсионного никелирования золота (ENIG), используемый для получения позолоченных электрических контактов на печатных платах.
- При распылении используется электронный луч или плазма для выброса микроскопических частиц металла на подложку в вакууме.
- Физическое осаждение из паровой фазы переносит металл на подложку путем его испарения.
- При химическом осаждении из паровой фазы используется газ, содержащий летучие соединения металла, которые осаждаются на подложку в результате химической реакции.
- Золочение – это традиционный способ прикрепить слой золота к металлу путем нанесения очень тонкого листа золота, удерживаемого клеем .

История
[ редактировать ]
Было высказано предположение, что первая гальваника была сделана в эпоху Парфянской империи . Вильгельм Кёниг , будучи ассистентом Национального музея Ирака в 1930-х годах, наблюдал ряд очень прекрасных серебряных предметов из древнего Ирака, покрытых очень тонкими слоями золота, и предположил, что они были гальванопокрыты. [17] [ циклическая ссылка ] . Он подтвердил свою идею, сославшись на возможную парфянскую батарею, обнаруженную в 1938 году недалеко от метрополии Ктесифон , столицы Парфянской ( 150 г. до н. э. — 223 г. н. э.) и Сасанидской (224–650 гг. н. э.) империй Персии . Однако это мнение было широко опровергнуто исследователями. Современные археологи теперь в целом согласны с тем, что предметы, увиденные Кенигом, на самом деле были вовсе не гальваническими, а скорее позолоченными с помощью ртути. Поэтому нет известных примеров предметов из древней Месопотамии, которые можно было бы достоверно описать как имеющие признаки гальваники. [18]
Гальваническое покрытие было изобретено итальянским химиком Луиджи Валентино Бругнателли в 1805 году. Бругнателли использовал своего коллеги Алессандро Вольты изобретение , сделанное пятью годами ранее, гальваническую батарею , чтобы облегчить первое электроосаждение. Изобретения Бругнателли были запрещены Французской академией наук и не использовались в общей промышленности в течение следующих тридцати лет. К 1839 году учёные из Великобритании и России независимо друг от друга разработали процессы осаждения металлов, аналогичные методам Бруньятелли, для гальванопокрытия медью пластин печатных машин .

Борис Якоби в России не только заново открыл гальванопластику, но разработал гальванопластику и гальванопластическую скульптуру . Гальванопластика быстро вошла в моду в России, и такие люди, как изобретатель Петр Багратион , ученый Генрих Ленц и писатель-фантаст Владимир Одоевский, внесли свой вклад в дальнейшее развитие технологии. Среди наиболее громких случаев использования гальваники в России середины XIX века были гигантские гальванопластические скульптуры Исаакиевского собора в Санкт-Петербурге и позолоченный купол храма Христа Спасителя в Москве , третьего по высоте православного храма в мире. . [19]

Вскоре после этого Джон Райт из Бирмингема , Англия, обнаружил, что цианид калия является подходящим электролитом для гальваники золота и серебра. Соратники Райта, Джордж Элкингтон и Генри Элкингтон, получили первые патенты на гальванику в 1840 году. Эти двое затем основали гальваническую промышленность в Бирмингеме, откуда она распространилась по всему миру. 1844 Электрический генератор Вулрича года, который сейчас находится в аналитическом центре Бирмингемского музея науки , является первым электрическим генератором, используемым в промышленности. [20] Его использовали Элкингтоны . [21] [22] [23]
Norddeutsche Affinerie в Гамбурге была первым современным гальваническим заводом, начавшим свое производство в 1876 году. [24]
По мере развития науки электрохимии стала понятна ее связь с гальванопокрытием, и были разработаны другие виды недекоративной гальванизации металлов. Коммерческое гальванопокрытие никеля , латуни , олова и цинка было разработано к 1850-м годам. Гальванические ванны и оборудование, основанные на патентах Элкингтонов, были адаптированы для нанесения покрытий на многочисленные крупномасштабные объекты, а также для конкретных производственных и инженерных применений.
Гальваническая промышленность получила большой импульс с появлением электрических генераторов в конце 19 века. Благодаря более высоким токам металлические детали машин, метизы и автомобильные можно обрабатывать детали, требующие защиты от коррозии и повышенных износостойких свойств, а также лучшего внешнего вида.
Две мировые войны и растущая авиационная промышленность дали толчок дальнейшим разработкам и усовершенствованиям, включая такие процессы, как твердое хромирование , покрытие бронзовыми сплавами, сульфаматное никелирование и множество других процессов покрытия. с ручным управлением Гальваническое оборудование превратилось из деревянных резервуаров, покрытых смолой, в автоматизированное оборудование, способное обрабатывать тысячи килограммов деталей в час.
Одним из первых проектов американского физика Ричарда Фейнмана была разработка технологии гальванопокрытия металла на пластик . Фейнман развил первоначальную идею своего друга в успешное изобретение, позволив его работодателю (и другу) сдержать коммерческие обещания, которые он дал, но не смог бы выполнить иначе. [25]
См. также
[ редактировать ]- Анодирование
- Электрохимическая инженерия
- Электрогальванизация
- Электрополировка
- Наноламинирование
- Электроформовка
- Электродобыча
Ссылки
[ редактировать ]- ^ «Часто задаваемые вопросы | Часто задаваемые вопросы | Электрополировка || Electro-Glo» . Архивировано из оригинала 28 ноября 2020 г. Проверено 1 мая 2019 г.
- ^ Перейти обратно: а б Фарбер, Х.Л. (1930). «Энергия хромирования» (PDF) . Журнал исследований Бюро стандартов . 3:27 . Проверено 6 августа 2023 г.
- ^ «Профиль технологии предотвращения загрязнения» Замены трехвалентного хрома для покрытия шестивалентным хромом» (PDF) . Северо-восточная ассоциация чиновников по управлению отходами. 18 октября 2003 г. Архивировано из оригинала (PDF) 20 июля 2011 г.
- ^ Дюфур 2006 , с. IX-1.
- ^ Перейти обратно: а б Дюфур 2006 , с. IX-2
- ^ Дюфур 2006 , с. IX-3
- ^ кунджи дурай, MS; Чаала, Мэти (2008). «Импульсное и импульсное обратное покрытие - концепция, преимущества и применение». Электрохимика Акта . 53 (8): 3313–3322. дои : 10.1016/j.electacta.2007.11.054 .
- ^ А.С. Тан (30 ноября 1992 г.). Лужение и пайка в полупроводниковой промышленности . Springer Science & Business Media. п. 122. ИСБН 978-0-412-48240-3 . Архивировано из оригинала 1 августа 2020 года . Проверено 16 мая 2019 г.
- ^ Перейти обратно: а б с Маккормик, М.; Кун, AT (1993). «Ячейка Харинга-Блюма». Операции МВФ . 71 (2): 74–76. дои : 10.1080/00202967.1993.11870992 . ISSN 0020-2967 .
- ^ Фуллер, Т.Ф.; Харб, Дж. Н. Электрохимическая инженерия; Джон Уайли и сыновья, 2018. ISBN 9781119446583.
- ^ Гейб, Дэвид Р. (2002). «Испытательные ячейки для гальваники». Металлическая отделка . 100 : 579–586. дои : 10.1016/s0026-0576(02)82059-1 . ISSN 0026-0576 .
- ^ Бард, Аллан; Инзельт, Дьёрдь; Шольц, Фриц (2012). «Ячейка Харинга – Блюма». Электрохимический словарь . Спрингер. п. 444. дои : 10.1007/978-3-642-29551-5_8 . ISBN 978-3-642-29551-5 .
- ^ Вендт, Хартмут; Герхард, Крейзе (1999). Электрохимическая инженерия: наука и технологии в химической и других отраслях промышленности . Спрингер. п. 122. ИСБН 3540643869 .
- ^ Отделка металлов: Путеводитель и справочник. Выпуск 98 . Том. 95. 1998. с. 588.
- ^ Кушнер, Артур С. (1 декабря 2006 г.). «Корпусная ячейка 101» . Отделка изделий . Архивировано из оригинала 13 марта 2010 года.
- ^ Тодд, Роберт Х.; Аллен, Делл К.; Альтинг, Лео (1994). «Поверхностное покрытие». Справочное руководство по производственным процессам . Промышленная пресса. стр. 454–458. ISBN 0-8311-3049-0 . Архивировано из оригинала 9 октября 2013 г.
- ^ Гальванический элемент парфянского периода.
- ^ «Разоблачение так называемой «Багдадской батареи» » . Сказки о забытых временах . 08.03.2020 . Проверено 10 октября 2021 г.
- ^ «История гальванотехнологии в России» . Архивировано из оригинала 5 марта 2012 года.
- ^ Каталог фонда музеев Бирмингема, инвентарный номер: 1889S00044.
- ^ Томас, Джон Мейриг (1991). Майкл Фарадей и Королевское учреждение: гений человека и места . Бристоль: Хильгер. п. 51. ИСБН 0750301457 .
- ^ Бошан, КГ (1997). Выставка электричества . ИЭПП. п. 90. ИСБН 9780852968956 .
- ^ Хант, LB (март 1973 г.). «Ранняя история позолоты» . Золотой бюллетень . 6 (1): 16–27. дои : 10.1007/BF03215178 .
- ^ Стелтер, М.; Бомбах, Х. (2004). «Оптимизация процесса электрорафинирования меди». Передовые инженерные материалы . 6 (7): 558. doi : 10.1002/adem.200400403 . S2CID 138550311 .
- ^ Фейнман, Ричард (1985). «Глава 6: Главный химик-исследователь корпорации Метапласт». Вы, конечно, шутите, мистер Фейнман! .
Библиография
[ редактировать ]- Дюфур, Джим (2006). Введение в металлургию (5-е изд.). Кэмерон. [ ISBN отсутствует ]
