Азотный цикл

Азотный цикл — это биогеохимический цикл, в ходе которого азот преобразуется во множество химических форм по мере его циркуляции в атмосфере , наземных и морских экосистемах . Преобразование азота может осуществляться как биологическими, так и физическими процессами. Важнейшие процессы круговорота азота включают фиксацию , аммонификацию , нитрификацию и денитрификацию . Большую часть атмосферы Земли (78%) составляет атмосферный азот . [16] что делает его крупнейшим источником азота. Однако доступность атмосферного азота для биологического использования ограничена, что приводит к нехватке пригодного для использования азота во многих типах экосистем .
Азотный цикл представляет особый интерес для экологов , поскольку доступность азота может влиять на скорость ключевых экосистемных процессов, включая первичное производство и разложение . Деятельность человека, такая как сжигание ископаемого топлива, использование искусственных азотных удобрений и выбросы азота в сточные воды, резко изменила глобальный цикл азота . [17] [18] [19] Изменение человеком глобального цикла азота может негативно повлиять на природную систему окружающей среды, а также на здоровье человека. [20] [21]
Процессы
| Часть серии о |
| Биогеохимические циклы |
|---|
 |
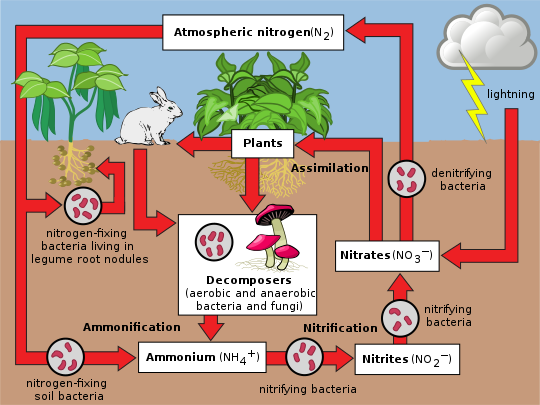
Азот присутствует в окружающей среде в самых разных химических формах, включая органический азот, аммоний ( NH + 4 ), нитрит ( NO - 2 ), нитрат ( NO - 3 ), закись азота ( N 2 O ), оксид азота (NO) или неорганический газообразный азот ( № 2 ). Органический азот может находиться в виде живого организма, гумуса или в виде промежуточных продуктов разложения органического вещества. Процессы круговорота азота заключаются в преобразовании азота из одной формы в другую. Многие из этих процессов осуществляются микробами либо в попытке собрать энергию, либо накопить азот в форме, необходимой для их роста. Например, азотистые отходы животных в моче расщепляются нитрифицирующими бактериями в почве, которые используются растениями. На диаграмме рядом показано, как эти процессы объединяются, образуя азотный цикл.
Фиксация азота
Конверсия газообразного азота ( N 2 ) в нитраты и нитриты в результате атмосферных, промышленных и биологических процессов называется азотфиксацией. Атмосферный азот должен быть переработан или « фиксирован » в пригодную для использования в растениях форму. От 5 до 10 миллиардов кг в год фиксируется ударами молний , но большая часть фиксации осуществляется свободноживущими или симбиотическими бактериями, известными как диазотрофы . Эти бактерии обладают нитрогеназой ферментом , который соединяет газообразный азот с водородом с образованием аммиака , который бактерии преобразуют в другие органические соединения . Большая часть биологической фиксации азота происходит за счет активности молибден (Мо)-нитрогеназы, обнаруженной у самых разных бактерий и некоторых архей . Мо-нитрогеназа представляет собой сложный двухкомпонентный фермент , имеющий несколько металлсодержащих простетических групп. [22] Примером свободноживущих бактерий является Azotobacter . Симбиотические азотфиксирующие бактерии, такие как Rhizobium, обычно живут в корневых клубеньках бобовых (например, гороха, люцерны и акации). Здесь они образуют мутуалистические отношения с растением, производя аммиак в обмен на углеводы . Из-за этой взаимосвязи бобовые часто увеличивают содержание азота в бедных азотом почвах. Некоторые виды, не относящиеся к бобовым, также могут образовывать такие симбиозы . Сегодня около 30% общего количества фиксированного азота производится промышленным способом с использованием процесса Габера-Боша . [23] который использует высокие температуры и давления для преобразования газообразного азота и источника водорода (природного газа или нефти) в аммиак. [24]
Ассимиляция
Растения могут поглощать нитраты или аммоний из почвы своими корневыми волосками. Если нитрат абсорбируется, он сначала восстанавливается до ионов нитрита, а затем ионов аммония для включения в аминокислоты, нуклеиновые кислоты и хлорофилл. У растений, находящихся в симбиотических отношениях с ризобиями, часть азота усваивается в виде ионов аммония непосредственно из клубеньков. существует более сложный круговорот аминокислот Сейчас известно, что между бактероидами ризобий и растениями . Растение снабжает бактероиды аминокислотами, поэтому ассимиляция аммиака не требуется, и бактероиды передают аминокислоты (с новым фиксированным азотом) обратно растению, образуя таким образом взаимозависимые отношения. [25] В то время как многие животные, грибы и другие гетеротрофные организмы получают азот, потребляя аминокислоты , нуклеотиды и другие небольшие органические молекулы, другие гетеротрофы (включая многие бактерии ) способны использовать неорганические соединения, такие как аммоний, в качестве единственного источника азота. Использование различных источников азота тщательно регулируется у всех организмов.
Аммонификация
Когда растение или животное умирает или животное выделяет отходы, первоначальная форма азота является органической . Бактерии или грибы превращают органический азот в останках обратно в аммоний ( NH + 4 ), процесс, называемый аммонификацией или минерализацией . Участвующие ферменты:
- GS: Gln-синтетаза (цитозольная и пластиковая)
- GOGAT: Глю-2-оксоглутарат-аминотрансфераза ( ферредоксин и НАДН-зависимая)
- GDH: глюдегидрогеназа:
- Незначительная роль в ассимиляции аммония.
- Важен в катаболизме аминокислот.

Нитрификация
Превращение аммония в нитрат осуществляется преимущественно почвенными бактериями и другими нитрифицирующими бактериями. На первичной стадии нитрификации происходит окисление аммония ( NH + 4 ) осуществляется такими бактериями, как виды Nitrosomonas , которые превращают аммиак в нитриты ( НЕТ - 2 ). Другие виды бактерий, такие как Nitrobacter , ответственны за окисление нитритов. NO − 2 ) в нитраты ( НЕТ - 3 ). Это важно для аммиака ( NH 3 ) необходимо преобразовать в нитраты или нитриты, поскольку газообразный аммиак токсичен для растений.
Из-за очень высокой растворимости и неспособности почв удерживать анионы нитраты могут попадать в грунтовые воды . Повышенное содержание нитратов в грунтовых водах вызывает обеспокоенность при использовании питьевой воды, поскольку нитраты могут влиять на уровень кислорода в крови у младенцев и вызывать метгемоглобинемию или синдром голубого ребенка. [28] Там, где грунтовые воды пополняют речной сток, обогащенные нитратами грунтовые воды могут способствовать эвтрофикации – процессу, который приводит к высокой популяции и росту водорослей, особенно популяций сине-зеленых водорослей. Хотя нитраты не токсичны напрямую для рыб, как аммиак, они могут оказывать косвенное воздействие на рыбу, если способствуют эвтрофикации. Азот способствовал возникновению серьезных проблем эвтрофикации в некоторых водоемах. С 2006 года применение азотных удобрений все больше контролируется в Великобритании и США. Это происходит по той же схеме, что и контроль над фосфорными удобрениями, ограничение которых обычно считается необходимым для восстановления эвтрофированных водоемов.
Денитрификация
Денитрификация — это восстановление нитратов обратно в газообразный азот ( N
2 ), завершая азотный цикл. Этот процесс осуществляется бактериальными видами, такими как Pseudomonas и Paracoccus , в анаэробных условиях. Они используют нитрат в качестве акцептора электронов вместо кислорода во время дыхания. Эти факультативно (то есть факультативно) анаэробные бактерии могут жить и в аэробных условиях. Денитрификация происходит в анаэробных условиях, например, в заболоченных почвах. Денитрифицирующие бактерии используют нитраты в почве для дыхания и, следовательно, производят газообразный азот, который инертен и недоступен для растений. Денитрификация происходит как у свободноживущих микроорганизмов, так и у облигатных симбионтов анаэробных инфузорий. [29]
- Классическое представление азотного цикла
- Поток азота через экосистему. Бактерии являются ключевым элементом в цикле, обеспечивая различные формы соединений азота, которые могут усваиваться высшими организмами.
- Простое представление круговорота азота. Синий цвет обозначает хранение азота, зеленый — процессы перемещения азота из одного места в другое, а красный — участвующие в нем бактерии.
Диссимиляционное восстановление нитратов до аммония
Диссимиляционное восстановление нитратов до аммония (ДНРА), или аммонификация нитратов/нитритов, представляет собой дыхания анаэробный процесс . Микробы, осуществляющие ДНКРА, окисляют органическое вещество и используют нитрат в качестве акцептора электронов, восстанавливая его до нитрита , а затем до аммония ( НЕТ - 3 → НЕТ - 2 → NH + 4 ). [30] И денитрифицирующие, и нитратаммонифицирующие бактерии будут конкурировать за нитраты в окружающей среде, хотя DNRA действует для сохранения биодоступного азота в виде растворимого аммония, а не для производства газообразного динитрога. [31]
Анаэробное окисление аммиака
процесс идации AN Аэробный AMM onia OX также известен как процесс ANAMMOX — аббревиатура, образованная путем соединения первых слогов каждого из этих трех слов. Этот биологический процесс представляет собой окислительно-восстановительную реакцию сопропорционирования , в которой аммиак ( восстановитель, отдающий электроны) и нитрит ( окислитель, принимающий электроны) переносят три электрона и превращаются в одну молекулу двухатомного азота ( N
2 ) газ и две молекулы воды. Этот процесс составляет основную часть преобразования азота в океанах . Стехиометрически сбалансированную формулу химической реакции АНАММОКС можно записать следующим образом, где аммония ион включает в себя молекулу аммиака, ее сопряженное основание :
- NH + 4 + NO − 2 → N 2 + 2 H 2 O (Δ G ° = −357 кДж⋅моль −1 ). [32]
Это экзергонический процесс (здесь также экзотермическая реакция ), высвобождающий энергию, на что указывает отрицательное значение ΔG ° , разница в свободной энергии Гиббса между продуктами реакции и реагентами.
Другие процессы
Хотя фиксация азота является основным источником доступного для растений азота в большинстве экосистем , в районах с богатой азотом коренной породой разрушение этой породы также служит источником азота. [33] [34] [35] Восстановление нитратов также является частью цикла железа : в бескислородных условиях Fe(II) может отдавать электрон NO − 3 и окисляется до Fe(III), а NO − 3 снижается до NO - 2 , N 2 O, N 2 и NH + 4 в зависимости от условий и вида микробов. [36] Фекальные шлейфы китообразных также действуют как связующее звено в морском азотном цикле, концентрируя азот в эпипелагических зонах океанской среды перед его рассеиванием через различные морские слои, что в конечном итоге повышает первичную продуктивность океана. [37]
Морской азотный цикл


2 фиксация (красный), нитрификация (голубой), восстановление нитратов (фиолетовый), ДНКРА (пурпурный), денитрификация (аквамарин), N-дамо (зеленый) и анаммокс (оранжевый). Черные изогнутые стрелки обозначают физические процессы, такие как адвекция и диффузия. [38]
Круговорот азота также является важным процессом в океане. Хотя общий цикл аналогичен, есть разные игроки. [40] и способы переноса азота в океане. Азот попадает в воду с осадками, стоками или в виде N.
2 из атмосферы. Азот не может быть использован фитопланктоном в виде N
2 , поэтому он должен подвергаться азотфиксации, которая осуществляется преимущественно цианобактериями . [41] Без поставок фиксированного азота в морской цикл фиксированный азот будет израсходован примерно за 2000 лет. [42] Фитопланктону необходим азот в биологически доступных формах для первоначального синтеза органического вещества. Аммиак и мочевина попадают в воду при выделении планктона. Источники азота удаляются из эвфотической зоны за счет движения органического вещества вниз. Это может произойти в результате затопления фитопланктона, вертикального перемешивания или затопления отходов вертикальных мигрантов. В результате погружения аммиак попадает на меньшие глубины ниже эвфотической зоны. Бактерии способны превращать аммиак в нитрит и нитрат, но они ингибируются светом, поэтому это должно происходить ниже эвфотической зоны. [43] Аммонификация или минерализация осуществляется бактериями для преобразования органического азота в аммиак. Затем может произойти нитрификация с преобразованием аммония в нитрит и нитрат. [44] Нитрат может быть возвращен в эвфотическую зону путем вертикального перемешивания и апвеллинга, где он может быть поглощен фитопланктоном для продолжения цикла. Н
2 могут быть возвращены в атмосферу посредством денитрификации .
Считается, что аммоний является предпочтительным источником фиксированного азота для фитопланктона, поскольку его ассимиляция не включает окислительно-восстановительную реакцию и, следовательно, требует мало энергии. Для ассимиляции нитрата требуется окислительно-восстановительная реакция, но он более распространен, поэтому большинство фитопланктона адаптировались к ферментам, необходимым для такого восстановления ( нитратредуктаза ). Есть несколько примечательных и хорошо известных исключений, к которым относятся большинство прохлорококков и некоторые синехококки , которые могут поглощать азот только в виде аммония. [42]
Питательные вещества в океане распределены неравномерно. Области апвеллинга обеспечивают поступление азота из-под эвфотической зоны. Прибрежные зоны обеспечивают азот из стока, и вдоль побережья легко происходит апвеллинг. Однако скорость поглощения азота фитопланктоном снижается в олиготрофных водах круглый год и в водах умеренного пояса летом, что приводит к снижению первичной продукции. [45] Распределение различных форм азота также варьируется в океанах.
Нитраты обеднены в приповерхностных водах, за исключением районов апвеллинга. Прибрежные регионы апвеллинга обычно имеют высокие уровни нитратов и хлорофиллов в результате увеличения производства. Однако существуют области с высоким содержанием нитратов на поверхности, но низким содержанием хлорофилла, которые называются областями HNLC (высокий азот, низкий хлорофилл). Лучшее объяснение регионов HNLC связано с нехваткой железа в океане, которое может играть важную роль в динамике океана и круговороте питательных веществ. Поступление железа варьируется в зависимости от региона и попадает в океан с пылью ( пылевыми бурями ) и вымывается из горных пород. Железо рассматривается как настоящий элемент, ограничивающий продуктивность экосистемы океана.
Максимальные концентрации аммония и нитрита наблюдаются на глубине 50–80 м (нижний конец эвфотической зоны ) с уменьшением концентрации ниже этой глубины. Такое распределение можно объяснить тем, что нитрит и аммоний являются промежуточными соединениями. Они быстро производятся и потребляются через толщу воды. [42] Количество аммония в океане примерно на 3 порядка меньше, чем нитратов. [42] Среди аммония, нитрита и нитрата нитрит имеет самую высокую скорость оборота. Он может образовываться при ассимиляции нитратов, нитрификации и денитрификации; однако он немедленно снова потребляется.
Новый и регенерированный азот
Азот, поступающий в эвфотическую зону, называется новым азотом, поскольку он вновь поступает из-за пределов продуктивного слоя. [41] Новый азот может поступать из-под эвфотической зоны или из внешних источников. Внешние источники — это апвеллинг из глубокой воды и фиксация азота. Если органическое вещество съедается, выдыхается, попадает в воду в виде аммиака и повторно включается в органическое вещество фитопланктоном, это считается переработанным/регенерированным производством.
Новая продукция является важным компонентом морской среды. Одна из причин заключается в том, что только постоянный приток нового азота может определить общую способность океана производить устойчивый улов рыбы. [45] Вылов рыбы на участках с регенерированным азотом приведет к снижению содержания азота и, следовательно, к снижению первичной продукции. Это окажет негативное влияние на систему. Однако, если рыбу вылавливать в районах с новым азотом, азот будет пополняться.
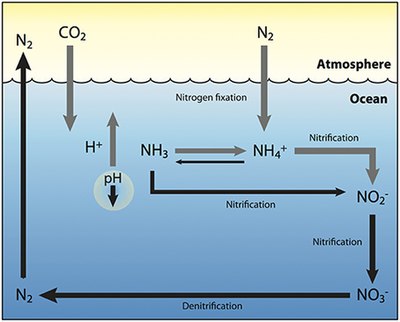
Будущее подкисление
Как показано на диаграмме справа, дополнительный углекислый газ (CO 2 ) поглощается океаном и реагирует с водой, углекислотой ( H
2 СО
3 ) образуется и распадается как на бикарбонат ( HCO - 3 ) и водород ( H +
) ионы (серая стрелка), что снижает биодоступность карбоната ( CO 2− 3 океана ) и снижает pH (черная стрелка). Это, вероятно, усилит фиксацию азота диазотрофами (серая стрелка), которые используют H +
ионы для преобразования азота в биодоступные формы, такие как аммиак ( NH
3 ) и ионы аммония ( НХ + 4 ). Однако по мере снижения pH и большего количества аммиака в ионы аммония (серая стрелка) происходит меньше окисления аммиака в нитрит (NO –
2 ), что приводит к общему снижению нитрификации и денитрификации (черные стрелки). Это, в свою очередь, приведет к дальнейшему накоплению фиксированного азота в океане, что может привести к эвтрофикации . Серые стрелки обозначают увеличение, а черные стрелки — уменьшение соответствующего процесса. [39]
Влияние человека на круговорот азота


В результате широкого выращивания бобовых культур (особенно сои , люцерны и клевера ), растущего использования процесса Габера-Боша в производстве химических удобрений и загрязнения окружающей среды, выбрасываемого транспортными средствами и промышленными предприятиями, человечество более чем вдвое увеличило ежегодные выбросы. перевод азота в биологически доступные формы. [28] Кроме того, люди внесли значительный вклад в перенос азотных примесей с Земли в атмосферу и с суши в водные системы. Антропогенные изменения глобального азотного цикла наиболее интенсивны в развитых странах и в Азии, где выбросы транспортных средств и промышленное сельское хозяйство являются самыми высокими. [46]
Производство Nr, реактивного азота , за последнее столетие увеличилось более чем в 10 раз из-за глобальной индустриализации . [2] [47] Эта форма азота каскадно проходит через биосферу с помощью различных механизмов и накапливается, поскольку скорость его образования превышает скорость денитрификации . [48]
Закись азота ( N
2 O ) поднялся в атмосферу в результате сельскохозяйственных удобрений, сжигания биомассы, скота и откормочных площадок, а также промышленных источников. [49] Н
2 O оказывает вредное воздействие на стратосферу , где он распадается и действует как катализатор разрушения атмосферного озона . Закись азота также является парниковым газом и в настоящее время является третьим по величине фактором глобального потепления после углекислого газа и метана . Хотя он не так распространен в атмосфере, как углекислый газ, при эквивалентной массе он почти в 300 раз более эффективен по своей способности согревать планету. [50]
Аммиак ( NH
3 ) в атмосфере утроилось в результате деятельности человека. Это реагент в атмосфере, где он действует как аэрозоль , ухудшая качество воздуха и прилипая к каплям воды, что в конечном итоге приводит к образованию азотной кислоты ( H NO 3 ), вызывающей кислотные дожди . Атмосферный аммиак и азотная кислота также повреждают дыхательные системы.
Очень высокая температура молнии естественным образом производит небольшое количество NO.
х , Нью-Хэмпшир
3 и ХНО
3 , но высокотемпературное горение способствовало увеличению потока NO в 6 или 7 раз.
х в атмосферу. Его производство зависит от температуры сгорания: чем выше температура, тем больше NO.
х производится. Сжигание ископаемого топлива вносит основной вклад, но также и биотопливо, и даже сжигание водорода. Однако скорость, с которой водород впрыскивается непосредственно в камеры сгорания двигателей внутреннего сгорания, можно контролировать, чтобы предотвратить более высокие температуры сгорания, приводящие к образованию NO.
х .
Аммиак и оксиды азота активно изменяют химический состав атмосферы . Они являются предшественниками образования тропосферного (нижних слоев атмосферы) озона, который способствует образованию смога и кислотных дождей , наносит ущерб растениям и увеличивает поступление азота в экосистемы. Экосистемные процессы могут усиливаться при внесении азотных удобрений , но антропогенное воздействие также может привести к насыщению азотом, что снижает продуктивность и может нанести вред здоровью растений, животных, рыб и людей. [28]
Снижение биоразнообразия может также произойти, если более высокая доступность азота приведет к увеличению количества трав, требовательных к азоту, что приведет к деградации бедных азотом пустошей с большим видовым разнообразием . [51]
Последствия модификации азотистого цикла человеком

Воздействие на природные системы
Показано, что повышение уровня отложений азота оказывает ряд негативных последствий как на наземные, так и на водные экосистемы . [52] [53] Азотные газы и аэрозоли могут быть непосредственно токсичными для некоторых видов растений, влияя на надземную физиологию и рост растений вблизи крупных точечных источников загрязнения азотом. Могут также произойти изменения в видах растений, поскольку накопление соединений азота увеличивает его доступность в данной экосистеме, что в конечном итоге приводит к изменению видового состава, разнообразия растений и круговорота азота. Аммиак и аммоний – две восстановленные формы азота – могут со временем нанести вред из-за повышенной токсичности для чувствительных видов растений. [54] особенно те, которые привыкли использовать нитраты в качестве источника азота, что приводит к плохому развитию их корней и побегов. Повышенное отложение азота также приводит к подкислению почвы, что увеличивает выщелачивание основных катионов в почве и количество алюминия и других потенциально токсичных металлов, а также уменьшает количество происходящей нитрификации и увеличивает количество растительного мусора. Из-за продолжающихся изменений, вызванных высокими отложениями азота, восприимчивость окружающей среды к экологическому стрессу и нарушениям, таким как вредители и патогены , может увеличиться, что делает ее менее устойчивой к ситуациям, которые в противном случае мало повлияли бы на ее долгосрочную жизнеспособность.
Дополнительные риски, связанные с увеличением доступности неорганического азота в водных экосистемах, включают закисление воды; эвтрофикация систем пресной и соленой воды; и проблемы токсичности для животных, включая человека. [55] Эвтрофикация часто приводит к снижению уровня растворенного кислорода в толще воды, включая гипоксические и бескислородные условия, что может привести к гибели водной фауны. Относительно сидячие бентосы, или обитающие на дне существа, особенно уязвимы из-за отсутствия подвижности, хотя гибель крупных рыб не является редкостью. Океанические мертвые зоны возле устья Миссисипи в Мексиканском заливе являются хорошо известным примером цветением водорослей , вызванной гипоксии . [56] [57] Озера Нью-Йорка Адирондак , Катскиллс , Гудзонское нагорье , плато Ренсселер и некоторые части Лонг-Айленда демонстрируют воздействие осадков азотной кислоты , что приводит к гибели рыбы и многих других водных видов. [58]
Аммиак ( NH
3 уровень аммиака, сбрасываемого очистными сооружениями ) очень токсичен для рыб, поэтому необходимо тщательно контролировать . Чтобы предотвратить гибель рыбы, часто желательно проводить нитрификацию посредством аэрации перед сбросом. Внесение земли может быть привлекательной альтернативой аэрации.
Влияние на здоровье человека: накопление нитратов в питьевой воде
Утечка Nr (реактивного азота) в результате деятельности человека может вызвать накопление нитратов в природной водной среде, что может оказать вредное воздействие на здоровье человека. Чрезмерное использование азотных удобрений в сельском хозяйстве было одним из основных источников загрязнения нитратами грунтовых и поверхностных вод. [59] [60] Благодаря высокой растворимости и низкой удерживаемости почвой нитраты могут легко выходить из подпочвенного слоя в грунтовые воды, вызывая нитратное загрязнение. Некоторые другие неточечные источники загрязнения нитратами подземных вод связаны с кормлением скота, загрязнением животных и людей, а также бытовыми и промышленными отходами. Поскольку грунтовые воды часто служат основным источником бытового водоснабжения, загрязнение нитратами может распространяться из грунтовых вод в поверхностные и питьевые воды в процессе производства питьевой воды , особенно для небольших общинных систем водоснабжения, где используются плохо регулируемые и антисанитарные воды. [61]
Стандарт ВОЗ для питьевой воды составляет 50 мг. НЕТ − 3 л −1 для кратковременного воздействия и для 3 мг НЕТ − 3 л −1 хронические эффекты. [62] Попадая в организм человека, нитрат может вступать в реакцию с органическими соединениями посредством нитрозирования реакций в желудке с образованием нитрозаминов и нитрозамидов , которые участвуют в некоторых типах рака (например, раке полости рта и раке желудка ). [63]
Воздействие на здоровье человека: качество воздуха
Деятельность человека также радикально изменила глобальный цикл азота за счет производства азотистых газов, что связано с глобальным загрязнением атмосферы азотом. Существует множество источников атмосферных потоков реактивного азота (Nr). Сельскохозяйственные источники реактивного азота могут производить выбросы аммиака в атмосферу ( NH 3 ), оксиды азота ( NO
x ) и закись азота ( N
2 О ). Процессы сгорания в производстве энергии, на транспорте и в промышленности также могут приводить к образованию нового химически активного азота за счет выбросов NO.
x , непреднамеренный ненужный продукт. Когда эти химически активные азоты выбрасываются в нижние слои атмосферы, они могут вызвать образование смога, твердых частиц и аэрозолей, которые вносят основной вклад в неблагоприятное воздействие загрязнения воздуха на здоровье человека. [64] В атмосфере НЕТ
2 можно окислить до азотной кислоты ( HNO
3 ) и далее может реагировать с NH
3 с образованием нитрата аммония ( NH 4 NO 3 ), что способствует образованию твердых частиц нитрата. Более того, НХ
3 может реагировать с другими кислыми газами ( серной и соляной кислотами ) с образованием аммонийсодержащих частиц, которые являются предшественниками вторичных органических аэрозольных частиц в фотохимическом смоге . [65]
См. также
- Планетарные границы – пределы, которые нельзя превышать, если человечество хочет выжить в безопасной экосистеме
- Цикл фосфора - Биогеохимическое движение
Ссылки
- ^ Фаулер, Дэвид ; Койл, Мхайри; Скиба, Уте; Саттон, Марк А.; Кейп, Дж. Нил; Рейс, Стефан; Шеппард, Люси Дж.; Дженкинс, Алан; Гриззетти, Бруна; Галлоуэй, JN; Витоусек, П; Лич, А; Бауман, А.Ф.; Баттербах-Баль, К.; Дентенер, Ф; Стивенсон, Д; Аманн, М; Восс, М. (5 июля 2013 г.). «Глобальный азотный цикл в XXI веке» . Философские труды Лондонского королевского общества. Серия Б, Биологические науки . 368 (1621): 20130164. doi : 10.1098/rstb.2013.0164 . ПМЦ 3682748 . ПМИД 23713126 .
- ^ Перейти обратно: а б Галлоуэй, JN; Таунсенд, Арканзас; Эрисман, Дж.В.; Бекунда, М.; Кай, З.; Френи-младший; Мартинелли, Луизиана; Зейтцингер, СП; Саттон, Массачусетс (2008). «Трансформация азотного цикла: последние тенденции, вопросы и потенциальные решения» (PDF) . Наука . 320 (5878): 889–892. Бибкод : 2008Sci...320..889G . дои : 10.1126/science.1136674 . ISSN 0036-8075 . ПМИД 18487183 . S2CID 16547816 . Архивировано (PDF) из оригинала 8 ноября 2011 г. Проверено 23 сентября 2019 г.
- ^ Витоусек, премьер-министр; Менге, DNL; Рид, Южная Каролина; Кливленд, CC (2013). «Биологическая фиксация азота: темпы, закономерности и экологический контроль в наземных экосистемах» . Философские труды Королевского общества B: Биологические науки . 368 (1621): 20130119. doi : 10.1098/rstb.2013.0119 . ПМЦ 3682739 . ПМИД 23713117 .
- ^ Перейти обратно: а б Восс, М.; Банге, Х.В.; Диппнер, Дж.В.; Мидделбург, Джей-Джей; Монтойя, Япония; Уорд, Б. (2013). «Цикл морского азота: недавние открытия, неопределенности и потенциальная значимость изменения климата» . Философские труды Королевского общества B: Биологические науки . 368 (1621): 20130121. doi : 10.1098/rstb.2013.0121 . ПМЦ 3682741 . ПМИД 23713119 .
- ^ Перейти обратно: а б Фаулер, Дэвид ; Койл, Мхайри; Скиба, Уте; Саттон, Марк А.; Кейп, Дж. Нил; Рейс, Стефан; Шеппард, Люси Дж.; Дженкинс, Алан; Гриззетти, Бруна; Галлоуэй, JN; Витоусек, П; Лич, А; Бауман, А.Ф.; Баттербах-Баль, К.; Дентенер, Ф; Стивенсон, Д; Аманн, М; Восс, М. (5 июля 2013 г.). «Глобальный азотный цикл в XXI веке» . Философские труды Лондонского королевского общества. Серия Б, Биологические науки . 368 (1621): 20130164. doi : 10.1098/rstb.2013.0164 . ПМЦ 3682748 . ПМИД 23713126 .
- ^ Вуурен, Детлеф П. Ван; Бауман, Лекс Ф; Смит, Стивен Дж; Дентенер, Фрэнк (2011). «Глобальные прогнозы антропогенных выбросов реактивного азота в атмосферу: оценка сценариев в научной литературе». Текущее мнение об экологической устойчивости . 3 (5): 359–369. Бибкод : 2011COES....3..359В . дои : 10.1016/j.cosust.2011.08.014 . hdl : 1874/314192 . ISSN 1877-3435 . S2CID 154935568 .
- ^ Пилегаард, К. (2013). «Процессы регулирования выбросов оксида азота из почв» . Философские труды Королевского общества B: Биологические науки . 368 (1621): 20130126. doi : 10.1098/rstb.2013.0126 . ПМЦ 3682746 . ПМИД 23713124 .
- ^ Леви, Х.; Моксим, WJ; Касибхатла, PS (1996). «Глобальный трехмерный, зависящий от времени источник молний тропосферных NOx». Журнал геофизических исследований: Атмосфера . 101 (Д17): 22911–22922. Бибкод : 1996JGR...10122911L . дои : 10.1029/96jd02341 . ISSN 0148-0227 .
- ^ Саттон, Массачусетс; Рейс, С.; Риддик, С.Н.; Драгосиц, У.; Немиц, Э.; Теобальд, MR; Тан, Ю.С.; Брабан, CF; Вьено, М. (2013). «На пути к климатозависимой парадигме выбросов и отложений аммиака» . Философские труды Королевского общества B: Биологические науки . 368 (1621): 20130166. doi : 10.1098/rstb.2013.0166 . ПМК 3682750 . ПМИД 23713128 .
- ^ Дентенер, Ф.; Древет, Дж.; Ламарк, Дж. Ф.; Бей, И.; Эйкхаут, Б.; Фиоре, AM; Хоглустейн, Д.; Горовиц, Л.В.; Крол, М. (2006). «Отложения азота и серы в региональном и глобальном масштабах: мультимодельная оценка» (PDF) . Глобальные биогеохимические циклы . 20 (4): н/д. Бибкод : 2006GBioC..20.4003D . дои : 10.1029/2005GB002672 . S2CID 839759 .
- ^ Перейти обратно: а б с Дуче, РА; Ларош, Дж.; Альтьери, К.; Арриго, КР; Бейкер, Арканзас; Капоне, генеральный директор; Корнелл, С.; Дентенер, Ф.; Галлоуэй, Дж. (2008). «Воздействие атмосферного антропогенного азота на открытый океан». Наука . 320 (5878): 893–7. Бибкод : 2008Sci...320..893D . дои : 10.1126/science.1150369 . hdl : 21.11116/0000-0001-CD7A-0 . ПМИД 18487184 . S2CID 11204131 .
- ^ Бауман, Л.; Гольдевейк, КК; Ван дер Хук, KW; Бойзен, AHW; Ван Вуурен, ДП; Виллемс, Дж.; Руфино, MC; Стефест, Э. (16 мая 2011 г.). «Изучение глобальных изменений в циклах азота и фосфора в сельском хозяйстве, вызванных животноводством в период 1900-2050 годов» . Труды Национальной академии наук . 110 (52): 20882–7. дои : 10.1073/pnas.1012878108 . ПМК 3876211 . ПМИД 21576477 .
- ^ Соломон, Сьюзен (2007). Изменение климата 2007: основы физической науки . Опубликовано для Межправительственной группы экспертов по изменению климата [издательством Cambridge University Press]. ISBN 9780521880091 . OCLC 228429704 .
- ^ Саттон, Марк А., изд. (14 апреля 2011 г.). Европейская оценка азота: источники, последствия и политические перспективы . Издательство Кембриджского университета. ISBN 9781107006126 . ОСЛК 690090202 .
- ^ Дойч, Кертис; Сармьенто, Хорхе Л.; Сигман, Дэниел М.; Грубер, Николас; Данн, Джон П. (2007). «Пространственная связь поступления и потерь азота в океане». Природа . 445 (7124): 163–167. Бибкод : 2007Natur.445..163D . дои : 10.1038/nature05392 . ISSN 0028-0836 . ПМИД 17215838 . S2CID 10804715 .
- ^ Стивен Б. Кэрролл; Стивен Д. Солт (2004). Экология для садоводов . Лесной пресс. п. 93. ИСБН 978-0-88192-611-8 .
- ^ Кайперс, МММ; Марчант, Гонконг; Картал, Б (2011). «Микробная сеть круговорота азота». Обзоры природы Микробиология . 1 (1): 1–14. дои : 10.1038/nrmicro.2018.9 . hdl : 21.11116/0000-0003-B828-1 . ПМИД 29398704 . S2CID 3948918 .
- ^ Галлоуэй, JN; и др. (2004). «Азотные циклы: прошлое, настоящее и будущие поколения». Биогеохимия . 70 (2): 153–226. дои : 10.1007/s10533-004-0370-0 . S2CID 98109580 .
- ^ Рейс, Стефан; Бекунда, Матетете; Ховард, Клэр М; Каранджа, Нэнси; Винивартер, Уилфрид; Ян, Сяоюань; Бликер, Альберт; Саттон, Марк А. (1 декабря 2016 г.). «Синтез и обзор: Решение проблемы управления азотом: от глобального до местного масштаба» . Письма об экологических исследованиях . 11 (12): 120205. Бибкод : 2016ERL....11l0205R . дои : 10.1088/1748-9326/11/12/120205 . ISSN 1748-9326 .
- ^ Гу, Баоцзин; Ге, Ин; Рен, Юань; Сюй, Бин; Ло, Вэйдун; Цзян, Хун; Гу, Биньхэ; Чанг, Цзе (17 августа 2012 г.). «Атмосферный химически активный азот в Китае: источники, последние тенденции и стоимость ущерба». Экологические науки и технологии . 46 (17): 9420–9427. Бибкод : 2012EnST...46.9420G . дои : 10.1021/es301446g . ISSN 0013-936X . ПМИД 22852755 .
- ^ Ким, Харюн; Ли, Китак; Лим, Донг-Иль; Нам, Сын Иль; Ким, Тэ Ук; Ян, Джин-Ю Т.; Ко, Ён Хо; Шин, Кён Хун; Ли, Юнил (11 мая 2017 г.). «Распространенный антропогенный азот в отложениях северо-западной части Тихого океана». Экологические науки и технологии . 51 (11): 6044–52. Бибкод : 2017EnST...51.6044K . doi : 10.1021/acs.est.6b05316 . ISSN 0013-936X . ПМИД 28462990 .
- ^ Мойр, JWB, изд. (2011). Круговорот азота в бактериях: молекулярный анализ . Кайстер Академик Пресс . ISBN 978-1-904455-86-8 .
- ^ Смит, Б.; Ричардс, РЛ; Ньютон, МЫ (2013) [2004]. Катализаторы азотфиксации: нитрогеназы, соответствующие химические модели и коммерческие процессы . Клювер. ISBN 9781402036118 .
- ^ Смиль, В (1997). Циклы жизни . Научная американская библиотека. ISBN 9780716750796 .
- ^ Уилли, Джоан М. (2011). Микробиология Прескотта (8-е изд.). МакГроу Хилл. п. 705. ИСБН 978-0-07-337526-7 .
- ^ Спарачино-Уоткинс, Кортни; Штольц, Джон Ф.; Басу, Парта (16 декабря 2013 г.). «Нитрат и периплазматические нитратредуктазы» . хим. Соц. Преподобный . 43 (2): 676–706. дои : 10.1039/c3cs60249d . ПМК 4080430 . ПМИД 24141308 .
- ^ Саймон, Йорг; Клотц, Мартин Г. (2013). «Разнообразие и эволюция биоэнергетических систем, участвующих в превращениях микробных соединений азота» . Biochimica et Biophysica Acta (BBA) — Биоэнергетика . 1827 (2): 114–135. дои : 10.1016/j.bbabio.2012.07.005 . ПМИД 22842521 .
- ^ Перейти обратно: а б с Витоусек, премьер-министр; Абер, Дж; Ховарт, RW; Лайкенс, GE; Мэтсон, Пенсильвания; Шиндлер, Д.В.; Шлезингер, штат Вашингтон; Тилман, Джорджия (1997). «Изменение человеком глобального цикла азота: источники и последствия» (PDF) . Экологические приложения . 1 (3): 1–17. doi : 10.1890/1051-0761(1997)007[0737:HAOTGN]2.0.CO;2 . hdl : 1813/60830 . ISSN 1051-0761 .
- ^ Граф, Джон С.; Шорн, Сина; Китцингер, Катарина; Ахмеркамп, Серен; Вёле, Кристиан; Хюттель, Бруно; Шуберт, Карстен Дж.; Кайперс, Марсель ММ; Милучка, Яна (3 марта 2021 г.). «Анаэробный эндосимбионт генерирует энергию для инфузорий-хозяев путем денитрификации» . Природа . 591 (7850): 445–450. Бибкод : 2021Natur.591..445G . дои : 10.1038/s41586-021-03297-6 . ISSN 0028-0836 . ПМЦ 7969357 . ПМИД 33658719 .
- ^ Лам, Филлис; Кайперс, Марсель М.М. (2011). «Микробные азотные процессы в зонах минимума кислорода». Ежегодный обзор морской науки . 3 : 317–345. Бибкод : 2011ARMS....3..317L . doi : 10.1146/annurev-marine-120709-142814 . hdl : 21.11116/0000-0001-CA25-2 . ПМИД 21329208 .
- ^ Марчант, Гонконг; Лавик, Г.; Холтаппельс, М.; Кайперс, МММ (2014). «Судьба нитратов в проницаемых отложениях приливной зоны» . ПЛОС ОДИН . 9 (8): е104517. Бибкод : 2014PLoSO...9j4517M . дои : 10.1371/journal.pone.0104517 . ПМК 4134218 . ПМИД 25127459 .
- ^ «Анаммокс» . Анаммокс — MicrobeWiki . МикробВики. Архивировано из оригинала 27 сентября 2015 г. Проверено 5 июля 2015 г.
- ^ «Исследование азота может «перевернуть» мир растений» . NPR.org . 06 сентября 2011 г. Архивировано из оригинала 5 декабря 2011 г. Проверено 22 октября 2011 г.
- ^ Шур, ЕАГ (2011). «Экология: Азот из глубин» . Природа . 477 (7362): 39–40. Бибкод : 2011Natur.477...39S . дои : 10.1038/477039а . ПМИД 21886152 . S2CID 2946571 .
- ^ Морфорд, СЛ; Хоултон, БЗ; Дальгрен, РА (2011). «Увеличение запасов углерода и азота в лесных экосистемах из богатой азотом коренной породы». Природа . 477 (7362): 78–81. Бибкод : 2011Природа.477...78М . дои : 10.1038/nature10415 . ПМИД 21886160 . S2CID 4352571 .
- ^ Бургин, Эми Дж.; Ян, Венди Х.; Гамильтон, Стивен К.; Сильвер, Уэнди Л. (2011). «Помимо углерода и азота: как микробная энергетическая экономика объединяет элементарные циклы в различных экосистемах». Границы в экологии и окружающей среде . 9 (1): 44–52. Бибкод : 2011FrEE....9...44B . дои : 10.1890/090227 . hdl : 1808/21008 . ISSN 1540-9309 .
- ^ Роман, Дж.; Маккарти, Джей-Джей (2010). «Китовый насос: морские млекопитающие повышают первичную продуктивность в прибрежном бассейне» . ПЛОС ОДИН . 5 (10): е13255. Бибкод : 2010PLoSO...513255R . дои : 10.1371/journal.pone.0013255 . ПМЦ 2952594 . ПМИД 20949007 .
- ^ Пахарес Морено, С.; Рамос, Р. (2019). «Процессы и микроорганизмы, участвующие в морском азотном цикле: знания и пробелы» . Границы морской науки . 6 : 739. дои : 10.3389/fmars.2019.00739 .
 Материал был скопирован из этого источника, который доступен по международной лицензии Creative Commons Attribution 4.0 .
Материал был скопирован из этого источника, который доступен по международной лицензии Creative Commons Attribution 4.0 . - ^ Перейти обратно: а б О'Брайен, Пол А.; Морроу, Кэтлин М.; Уиллис, Бетт Л.; Борн, Дэвид Г. (2016). «Последствия закисления океана для морских микроорганизмов, от свободноживущих до ассоциированных с хозяином» . Границы морской науки . 3 . дои : 10.3389/fmars.2016.00047 .
 Материал был скопирован из этого источника, который доступен по международной лицензии Creative Commons Attribution 4.0 .
Материал был скопирован из этого источника, который доступен по международной лицензии Creative Commons Attribution 4.0 . - ^ Моултон, Орисса М; Альтабет, Марк А; Беман, Дж. Майкл; Диган, Линда А; Льорет, Хавьер; Лайонс, Миган К; Нельсон, Джеймс А; Пфистер, Кэтрин А. (май 2016 г.). «Микробные ассоциации с макробиотой в прибрежных экосистемах: закономерности и последствия для круговорота азота». Границы в экологии и окружающей среде . 14 (4): 200–8. Бибкод : 2016FrEE...14..200M . дои : 10.1002/плата.1262 . hdl : 1912/8083 . ISSN 1540-9295 .
- ^ Перейти обратно: а б Миллер, Чарльз (2008). Биологическая океанография . Блэквелл. стр. 60–62. ISBN 978-0-632-05536-4 .
- ^ Перейти обратно: а б с д Грубер, Николас (2008). Азот в морской среде . Эльзевир. стр. 1–35. ISBN 978-0-12-372522-6 .
- ^ Миллер, Чарльз (2008). Биологическая океанография . Блэквелл. стр. 60–62. ISBN 978-0-632-05536-4 .
- ^ Бойс, Эллиот, Сьюзен, Майкл. «Учебный раздел: Морская среда азотного цикла» . Архивировано из оригинала 15 апреля 2012 года . Проверено 22 октября 2011 г.
{{cite web}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Перейти обратно: а б Лалли, Парсонс, Кэрол, Тимоти (1997). Биологическая океанография: Введение . Баттерворт-Хайнеманн. ISBN 978-0-7506-3384-0 .
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Холланд, Элизабет А.; Дентенер, Фрэнк Дж.; Брасвелл, Бобби Х.; Сульцман, Джеймс М. (1999). «Современные и доиндустриальные глобальные балансы реактивного азота». Биогеохимия . 46 (1–3): 7. Бибкод : 1999Biogc..46....7H . дои : 10.1007/BF01007572 . S2CID 189917368 .
- ^ Гу, Баоцзин; Ге, Ин; Рен, Юань; Сюй, Бин; Ло, Вэйдун; Цзян, Хун; Гу, Биньхэ; Чанг, Цзе (4 сентября 2012 г.). «Атмосферный химически активный азот в Китае: источники, последние тенденции и стоимость ущерба». Экологические науки и технологии . 46 (17): 9420–7. Бибкод : 2012EnST...46.9420G . дои : 10.1021/es301446g . ISSN 0013-936X . ПМИД 22852755 .
- ^ Косби, Б. Джек; Коулинг, Эллис Б.; Ховарт, Роберт В.; Зейцингер, Сибил П.; Эрисман, Ян Виллем; Абер, Джон Д.; Галлоуэй, Джеймс Н. (1 апреля 2003 г.). «Азотный каскад» . Бионаука . 53 (4): 341–356. doi : 10.1641/0006-3568(2003)053[0341:TNC]2.0.CO;2 . ISSN 0006-3568 . S2CID 3356400 .
- ^ Чапин, Сан-Франциско; Мэтсон, Пенсильвания; Муни, ХА (2002). Принципы экологии наземных экосистем . Спрингер. п. 345. ИСБН 0-387-95443-0 .
- ^ Труды Научного комитета по проблемам окружающей среды (SCOPE), Быстрая оценка международного проекта по биотопливу, 22–25 сентября 2008 г., Гуммерсбах, Германия, Р. В. Ховарт и С. Брингезу, редакторы. 2009 г. Краткое изложение , стр. 3. Архивировано 6 июня 2009 г. в Wayback Machine.
- ^ Аэртс, Риен и Берендсе, Франк (1988). «Влияние повышенной доступности питательных веществ на динамику растительности во влажных пустоши». Растительность . 76 (1/2): 63–69. дои : 10.1007/BF00047389 . JSTOR 20038308 . S2CID 34882407 .
- ^ Боббинк, Р.; Хикс, К.; Галлоуэй, Дж.; Спрангер, Т.; Алкемаде, Р.; Эшмор, М.; Бустаманте, М.; Синдерби, С.; Дэвидсон, Э. (1 января 2010 г.). «Глобальная оценка воздействия отложений азота на разнообразие наземных растений: синтез» (PDF) . Экологические приложения . 20 (1): 30–59. Бибкод : 2010EcoAp..20...30B . дои : 10.1890/08-1140.1 . ISSN 1939-5582 . ПМИД 20349829 . S2CID 4792945 . Архивировано (PDF) из оригинала 30 сентября 2019 г. Проверено 30 сентября 2019 г.
- ^ Лю, Сюэцзюнь, Лэй; Ду, Энцай; Лу, Сянькай; Чжоу, Сяобин; «Отложение азота и его экологическое воздействие: Ан». «Обзор». Загрязнение окружающей среды . 159 10): 2251–2264. 2011EPoll.159.2251L . doi : 10.1016 / j.envpol.2010.08.002 . : ( Бибкод
- ^ Бритто, Дев Т.; Кронцукер, Герберт Дж. (2002). «Токсичность NH4+ у высших растений: критический обзор». Журнал физиологии растений . 159 (6): 567–584. дои : 10.1078/0176-1617-0774 .
- ^ Камаргоа, Хулио А.; Алонсо, Альваро (2006). «Экологические и токсикологические последствия загрязнения неорганическим азотом в водных экосистемах: глобальная оценка». Интернационал окружающей среды . 32 (6): 831–849. Бибкод : 2006EnInt..32..831C . дои : 10.1016/j.envint.2006.05.002 . hdl : 10261/294824 . ПМИД 16781774 .
- ^ Рабале, Нэнси Н .; Тернер, Р. Юджин; Уайзман, Уильям младший (2002). «Гипоксия Мексиканского залива, она же «Мертвая зона» ». Анну. Преподобный Экол. Сист . 33 : 235–63. doi : 10.1146/annurev.ecolsys.33.010802.150513 . JSTOR 3069262 .
- ^ Дайбас, Шерил Лин. (2005). «Мертвые зоны, распространяющиеся в Мировом океане» . Бионаука . 55 (7): 552–557. doi : 10.1641/0006-3568(2005)055[0552:DZSIWO]2.0.CO;2 .
- ^ Охрана окружающей среды штата Нью-Йорк, Воздействие кислотных отложений на окружающую среду: озера [1]. Архивировано 24 ноября 2010 г. в Wayback Machine.
- ^ Пауэр, Дж. Ф.; Шеперс, Дж. С. (1989). «Загрязнение нитратами подземных вод в Северной Америке». Сельское хозяйство, экосистемы и окружающая среда . 26 (3–4): 165–187. Бибкод : 1989AgEE...26..165P . дои : 10.1016/0167-8809(89)90012-1 . ISSN 0167-8809 .
- ^ Штребель, О.; Дуйнисвелд, WHM; Бетчер, Дж. (1989). «Нитратное загрязнение подземных вод в Западной Европе». Сельское хозяйство, экосистемы и окружающая среда . 26 (3–4): 189–214. Бибкод : 1989AgEE...26..189S . дои : 10.1016/0167-8809(89)90013-3 . ISSN 0167-8809 .
- ^ Фьютрелл, Лорна (2004). «Нитраты в питьевой воде, метгемоглобинемия и глобальное бремя болезней: обсуждение» . Перспективы гигиены окружающей среды . 112 (14): 1371–4. дои : 10.1289/ehp.7216 . ПМЦ 1247562 . ПМИД 15471727 .
- ^ Глобальная обсерватория здравоохранения: (GHO) . Всемирная организация здравоохранения. OCLC 50144984 .
- ^ Кантер, Ларри В. (22 января 2019 г.), «Иллюстрации загрязнения подземных вод нитратами», Нитраты в подземных водах , Routledge, стр. 39–71, doi : 10.1201/9780203745793-3 , ISBN 9780203745793 , S2CID 133944481
- ^ Кампа, Марилена; Кастанас, Элиас (2008). «Влияние загрязнения воздуха на здоровье человека». Загрязнение окружающей среды . 151 (2): 362–367. Бибкод : 2008EPoll.151..362K . дои : 10.1016/j.envpol.2007.06.012 . ПМИД 17646040 . S2CID 38513536 .
- ^ Эрисман, Дж.В.; Галлоуэй, JN; Зейтцингер, С.; Бликер, А.; Диз, Северная Каролина; Петреску, АМР; Лич, AM; де Врис, В. (27 мая 2013 г.). «Последствия человеческой модификации глобального азотного цикла» . Философские труды Королевского общества B: Биологические науки . 368 (1621): 20130116. doi : 10.1098/rstb.2013.0116 . ПМЦ 3682738 . ПМИД 23713116 .