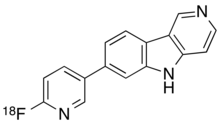
Флортаучипир ( 18 Ф)
 | |
| Клинические данные | |
|---|---|
| Произношение | флор тау' и пир 18 F |
| Торговые названия | Таувид |
| Другие имена | 18Ф-АВ-1451, 18 Ф-АВ-1451, 18 F-T807, Флортауципир F-18, Флортауципир F 18 ( США , США ) |
| Данные лицензии |
|
| Маршруты администрация | внутривенный |
| код АТС | |
| Юридический статус | |
| Юридический статус | |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| ХЭМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Химические и физические данные | |
| Формула | С 16 Ч 10 18 ФН 3 |
| Молярная масса | 262.27 g·mol −1 |
| 3D model ( JSmol ) | |
Флортаучипир ( 18 F) , продаваемый под торговой маркой Tauvid , представляет собой радиоактивный диагностический агент, предназначенный для использования при позитронно-эмиссионной томографии (ПЭТ) для визуализации мозга. [1] [2] [3]
Наиболее частые побочные реакции включают головную боль, боль в месте инъекции и повышение артериального давления. [1] [2]
Два белка – тау и амилоид – признаны признаками болезни Альцгеймера . [2] У людей с болезнью Альцгеймера патологические формы тау-белков развиваются внутри нейронов головного мозга, создавая нейрофибриллярные клубки . [2] После флортауципира ( 18 F) вводится внутривенно, он связывается с участками мозга, связанными с неправильным сворачиванием тау-белка. [2] Затем мозг можно визуализировать с помощью ПЭТ, чтобы выявить наличие тау-патологии. [2]
Это первый препарат, используемый для визуализации отличительной характеристики болезни Альцгеймера в мозге, называемой тау-патологией. [2] США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) считает его первым в своем классе лекарством . [4]
Медицинское использование
[ редактировать ]Флортаучипир ( 18 F) является радиоактивным диагностическим средством для взрослых с когнитивными нарушениями, проходящих обследование на болезнь Альцгеймера. [1] Он показан для позитронно-эмиссионной томографии (ПЭТ) головного мозга для оценки плотности и распределения агрегированных тау-нейрофибриллярных клубков (NFT), основного маркера болезни Альцгеймера. [2] [1] [3]
Флортаучипир ( 18 F) не показан для использования при обследовании людей на хроническую травматическую энцефалопатию (ХТЭ). [2] [1]
Химия
[ редактировать ]По химическому составу флортауципир F 18 представляет собой 7-(6-[F-18]фторпиридин-3-ил)-5H-пиридо[4,3b]индол. [1]
История
[ редактировать ]Флортаучипир (он же 18 F-T807) был обнаружен исследовательской группой биомаркеров Siemens, возглавляемой Хартмутом Кольбом и Катрин Сзарденингс, [5] который также первым провел испытания на людях. [6] Флортаучипир ( 18 F) был одобрен для медицинского использования в США в мае 2020 года. [2] [7] [8]
Безопасность и эффективность флортауципира ( 18 F) визуализация оценивалась в двух клинических исследованиях. [2] В каждом исследовании пять экспертов читали и интерпретировали флортауципир ( 18 Е) визуализация. [2] Оценщики не знали клинической информации и интерпретировали изображение как положительное или отрицательное. [2]
В первом исследовании приняли участие 156 неизлечимо больных участников, согласившихся пройти курс лечения флортауципиром. 18 F) визуализация и участие в программе посмертного донорства мозга. [2] У 64 участников, умерших в течение девяти месяцев от флортауципира ( 18 F) сканирование мозга, чтение оценщиками флортауципира ( 18 F) сканирование сравнивали с посмертными показаниями независимых патологов, которые оценивали плотность и распределение нейрофибриллярных клубков (НФТ) в том же мозге. [2] Исследование показало, что эксперты читают флортауципир ( 18 F) изображения имели высокую вероятность правильной оценки участников с тау-патологией и имели среднюю и высокую вероятность правильной оценки участников без тау-патологии. [2]
Во второе исследование вошли те же участники с неизлечимой болезнью, что и в первое исследование, плюс 18 дополнительных участников с неизлечимой болезнью и 159 участников с когнитивными нарушениями, проходивших обследование на болезнь Альцгеймера (указанная популяция пациентов). [2] В ходе исследования оценивалось, насколько хорошо флортауципир ( 18 F) показания оценщиков соответствовали оценкам друг друга. [2] Идеальное читательское согласие будет равно 1, а отсутствие читательского согласия — 0. [2] В этом исследовании согласие читателей составило 0,87 среди всех 241 участника. [2] В отдельном анализе подгрупп, включавшем 82 неизлечимо больных участника, диагностированных после смерти, и 159 участников с когнитивными нарушениями, согласие читателей составило 0,90 для участников из указанной популяции и 0,82 для неизлечимо больных участников. [2]
США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) одобрило флортауципир. 18 F) на основе показаний 1921 участника 19 исследований, проведенных в 322 центрах в США, Австралии, Бельгии, Канаде, Франции, Японии, Нидерландах и Польше. [3]
Способность флортауципира ( 18 F) выявление тау-патологии оценивалось у участников с тяжелой стадией деменции и может быть ниже у участников на более ранних стадиях когнитивного снижения, чем у участников с неизлечимым заболеванием, которые участвовали в исследовании. [2]
Общество и культура
[ редактировать ]Юридический статус
[ редактировать ]США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) удовлетворило заявку на флортауципир. 18 F) приоритетная проверка , и компания Avid Radiopharmaceuticals, Inc. одобрила препарат Таувид. [2]
В июне 2024 года Комитет по лекарственным средствам для применения человеком (CHMP) Европейского агентства по лекарственным средствам принял положительное заключение, рекомендовав выдачу регистрационного удостоверения на лекарственный препарат Таувид, предназначенный для диагностики болезни Альцгеймера. [9] [10] Заявителем данного лекарственного препарата является компания Eli Lilly Nederland BV. [9]
Имена
[ редактировать ]Флортаучипир ( 18 F) – международное непатентованное наименование (МНН). [11]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с д и ж г «Таувид-флортаучипир ф-18 инъекционный, раствор» . ДейлиМед . 22 июля 2020 г. Проверено 28 мая 2022 г.
- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п д р с т в v В «FDA одобрило первый препарат для визуализации тау-патологии у пациентов, проходящих обследование на болезнь Альцгеймера» . США Управление по контролю за продуктами и лекарствами (FDA) (пресс-релиз). 28 мая 2020 г. Проверено 28 мая 2020 г.
 В данную статью включен текст из этого источника, находящегося в свободном доступе .
В данную статью включен текст из этого источника, находящегося в свободном доступе .
- ^ Перейти обратно: а б с «Снимок судебного процесса над наркотиками: Таувид» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . 28 мая 2020 г. Проверено 10 июня 2020 г.
 В данную статью включен текст из этого источника, находящегося в свободном доступе .
В данную статью включен текст из этого источника, находящегося в свободном доступе .
- ^ «Новые разрешения на лекарственную терапию 2020» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . 31 декабря 2020 г. Проверено 17 января 2021 г.
 В данную статью включен текст из этого источника, находящегося в свободном доступе .
В данную статью включен текст из этого источника, находящегося в свободном доступе .
- ^ Ся К.Ф., Артеага Дж., Чен Г., Гангадхармат У., Гомес Л.Ф., Каси Д. и др. (ноябрь 2013 г.). «[(18)F]T807, новый агент тау-позитронно-эмиссионной томографии для лечения болезни Альцгеймера». Болезнь Альцгеймера и деменция . 9 (6): 666–676. дои : 10.1016/j.jalz.2012.11.008 . ПМИД 23411393 . S2CID 1079628 .
{{cite journal}}: CS1 maint: переопределенная настройка ( ссылка ) - ^ Чиен Д.Т., Бахри С., Сзарденингс А.К., Уолш Дж.К., Му Ф., Су М.И. и др. (20 июня 2013 г.). «Ранние клинические результаты ПЭТ с использованием нового радиолиганда PHF-тау [F-18]-T807» (PDF) . Журнал болезни Альцгеймера . 34 (2): 457–468. дои : 10.3233/JAD-122059 . ПМИД 23234879 . S2CID 46044539 .
{{cite journal}}: CS1 maint: переопределенная настройка ( ссылка ) - ^ «Лилли получает одобрение FDA США на препарат Таувид (инъекция флортауципира F 18) для использования у пациентов, проходящих обследование на болезнь Альцгеймера» (пресс-релиз). Эли Лилли. 28 мая 2020 г. Проверено 28 мая 2020 г. - через PR Newswire.
- ^ «Пакет одобрения лекарств: Таувид» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . 16 июля 2020 г. Проверено 28 мая 2022 г.
- ^ Перейти обратно: а б «Таувид ЭПАР» . Европейское агентство по лекарственным средствам . 27 июня 2024 г. Проверено 12 июля 2024 г. Текст скопирован из источника, права на который принадлежат Европейскому агентству по лекарственным средствам. Воспроизведение разрешено при условии указания источника.
- ^ «Основные сведения о заседании Комитета по лекарственным препаратам для человеческого применения (CHMP) 24–27 июня 2024 г.» . Европейское агентство по лекарственным средствам . 28 июня 2024 года. Архивировано из оригинала 12 июля 2024 года . Проверено 12 июля 2024 г.
- ^ Всемирная организация здравоохранения (2016). «Международные непатентованные наименования фармацевтических субстанций (МНН): рекомендуемое МНН: список 76». Информация ВОЗ о лекарствах . 30 (3). HDL : 10665/331020 .
Дальнейшее чтение
[ редактировать ]- Понтекорво М.Д., Девус М.Д., Кеннеди И., Навицкий М., Лу М., Галанте Н. и др. (июнь 2019 г.). «Многоцентровое продольное исследование флортауципира (18F) при нормальном старении, легких когнитивных нарушениях и деменции при болезни Альцгеймера» . Мозг . 142 (6): 1723–1735. дои : 10.1093/brain/awz090 . ПМК 6536847 . ПМИД 31009046 .
{{cite journal}}: CS1 maint: переопределенная настройка ( ссылка ) - Шонхаут Д.Р., Макмиллан К.Т., Спина С., Дикерсон Б.С., Сидеровф А., Девоус М.Д. и др. (октябрь 2017 г.). " 18 и болезни Паркинсона: многоцентровое исследование» . Annals of Neurology . 82 (4): 622–634. doi : 10.1002/ana.25060 . PMC 5665658. . PMID 28980714 Позитронно-эмиссионная томография F-флортауципир-тау отличает установленный прогрессирующий надъядерный паралич от контрольной группы
{{cite journal}}: CS1 maint: переопределенная настройка ( ссылка )
Внешние ссылки
[ редактировать ]- Номер клинического исследования NCT03507257 «Протокол продольного исследования болезни Альцгеймера с ранним началом (LEADS)» на сайте ClinicalTrials.gov.
- Номер клинического исследования NCT02278367 «Клиническая оценка 18F-AV-1451» на сайте ClinicalTrials.gov.
- Номер клинического испытания NCT02516046 для «Исследования аутопсии 18F-AV-1451» на сайте ClinicalTrials.gov.
- Номер клинического испытания NCT03901092 «Читательское исследование по оценке точности и надежности интерпретации ПЭТ-сканирования Флортауципира F 18» на сайте ClinicalTrials.gov.