Биомаркер рака
Биомаркер рака относится к веществу или процессу, который указывает на наличие рака в организме. Биомаркером , может быть молекула, секретируемая опухолью или специфическая реакция организма на наличие рака. Генетический , [1] эпигенетический , [2] протеомный , [3] гликомный , [4] а визуализирующие биомаркеры можно использовать для диагностики рака, прогноза и эпидемиологии. В идеале такие биомаркеры можно анализировать в биожидкостях, собранных неинвазивным путем, таких как кровь или сыворотка. [5]

Несмотря на то, что существуют многочисленные проблемы с внедрением исследований биомаркеров в клиническую сферу; ряд биомаркеров на основе генов и белков уже использовался в какой-то момент при лечении пациентов; в том числе, AFP ( рак печени ), BCR-ABL ( хронический миелолейкоз ), BRCA1 / BRCA2 ( рак молочной железы / яичников ), BRAF V600E ( меланома / колоректальный рак ), CA-125 (рак яичников), CA19.9 ( рак поджелудочной железы ). ), CEA (колоректальный рак), EGFR ( немелкоклеточный рак легких ), HER-2 (рак молочной железы), KIT ( стромальная опухоль желудочно -кишечного тракта ), PSA (специфический антиген простаты) ( рак простаты ), S100 (меланома), и многие другие. [6] [7] [8] [9] [10] [11] [12] [13] [14] [15] сами мутантные белки, обнаруженные с помощью мониторинга выбранных реакций (SRM), являются наиболее специфичными биомаркерами рака, поскольку они могут происходить только из существующей опухоли. Сообщается, что [16] Около 40% раковых заболеваний можно вылечить, если их обнаружить на ранней стадии при обследовании. [17]
Определения биомаркеров рака
[ редактировать ]Организации и публикации различаются в своих определениях биомаркера . Во многих областях медицины биомаркеры ограничиваются белками, которые можно идентифицировать или измерить в крови или моче . Однако этот термин часто используется для обозначения любого молекулярного, биохимического, физиологического или анатомического свойства, которое можно определить количественно или измерить.
Национальный институт рака (NCI), в частности, определяет биомаркер как: «Биологическая молекула, обнаруженная в крови, других жидкостях организма или тканях, которая является признаком нормального или аномального процесса, состояния или заболевания. Биомаркер можно использовать, чтобы увидеть, насколько хорошо организм реагирует на лечение заболевания или состояния. Также называется молекулярным маркером и сигнатурной молекулой». [18]
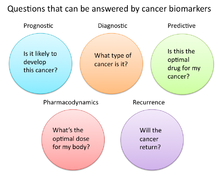
В исследованиях рака и медицине биомаркеры используются тремя основными способами: [19]
- Чтобы помочь диагностировать состояния, как в случае выявления рака на ранней стадии (диагностика).
- Чтобы спрогнозировать, насколько агрессивным является состояние, например, в случае определения способности пациента жить в отсутствие лечения (прогностический).
- Чтобы предсказать, насколько хорошо пациент отреагирует на лечение (прогностический)
Роль биомаркеров в исследованиях рака и медицине
[ редактировать ]Использование биомаркеров в медицине рака
[ редактировать ]Оценка риска
[ редактировать ]Биомаркеры рака, особенно те, которые связаны с генетическими мутациями или эпигенетическими изменениями, часто предлагают количественный способ определить, предрасположены ли люди к определенным типам рака. Яркие примеры потенциально прогностических биомаркеров рака включают мутации в генах KRAS , p53 , EGFR , erbB2 при колоректальном раке , раке пищевода , печени и поджелудочной железы ; мутации генов BRCA1 и BRCA2 при молочной железы и яичников раке ; аномальное метилирование генов -супрессоров опухолей p16 , CDKN2B и p14ARF при раке головного мозга ; гиперметилирование MYOD1 , CDH1 и CDH13 при раке шейки матки ; и гиперметилирование p16 , p14 и RB1 при раке полости рта . [20]
Диагностика
[ редактировать ]Биомаркеры рака также могут быть полезны при установлении конкретного диагноза. Это особенно актуально, когда необходимо определить, имеют ли опухоли первичное или метастатическое происхождение. Чтобы провести это различие, исследователи могут сравнить хромосомные изменения, обнаруженные в клетках, расположенных в первичном участке опухоли, с изменениями, обнаруженными во вторичном участке. Если изменения совпадают, вторичную опухоль можно идентифицировать как метастатическую; тогда как, если изменения различаются, вторичную опухоль можно идентифицировать как отдельную первичную опухоль. [21] Например, люди с опухолями имеют высокий уровень циркулирующей опухолевой ДНК (кДНК) из-за опухолевых клеток, прошедших апоптоз. [22] Этот опухолевый маркер можно обнаружить в крови, слюне или моче. [17] Возможность идентификации эффективного биомаркера для ранней диагностики рака недавно была поставлена под сомнение в свете высокой молекулярной гетерогенности опухолей, наблюдаемой в исследованиях секвенирования следующего поколения. [23]
Прогноз и прогнозы лечения
[ редактировать ]Другое использование биомаркеров в медицине рака — прогнозирование заболеваний , которое происходит после того, как у человека был диагностирован рак. Здесь биомаркеры могут быть полезны для определения агрессивности выявленного рака, а также вероятности его ответа на определенное лечение. Частично это связано с тем, что опухоли, демонстрирующие определенные биомаркеры, могут реагировать на лечение, связанное с экспрессией или присутствием этого биомаркера. Примеры таких прогностических биомаркеров включают повышенные уровни ингибитора металлопептидазы 1 (TIMP1) , маркера, связанного с более агрессивными формами множественной миеломы . [24] повышенная экспрессия рецептора эстрогена (ER) и/или рецептора прогестерона (PR) , маркеров, связанных с лучшей общей выживаемостью у пациенток с раком молочной железы; [25] [26] HER2/neu Амплификация гена , маркера, указывающего на рак молочной железы, вероятно, ответит на трастузумабом ; лечение [27] [28] мутация в экзоне 11 протоонкогена c -KIT , маркера, указывающего на стромальную опухоль желудочно-кишечного тракта (GIST) , вероятно, будет реагировать на иматинибом ; лечение [29] [30] и мутации в тирозинкиназном домене EGFR1 , маркере, указывающем на то, что у пациента немелкоклеточная карцинома легкого (НМРЛ), вероятно, будет реагировать на гефитинибом или эрлотинибом . лечение [31] [32]
Фармакодинамика и фармакокинетика
[ редактировать ]Биомаркеры рака также можно использовать для определения наиболее эффективного режима лечения рака у конкретного человека. [33] Из-за различий в генетической структуре каждого человека некоторые люди по-разному метаболизируют или изменяют химическую структуру наркотиков. В некоторых случаях снижение метаболизма некоторых лекарств может создать опасные условия, при которых в организме накапливаются высокие уровни лекарств. Таким образом, скрининг таких биомаркеров может помочь в принятии решений о дозировке лекарств в конкретных методах лечения рака. Примером может служить ген, кодирующий фермент тиопуринметилтрансферазу (TPMPT) . [34] Лица с мутациями в гене TPMT не способны метаболизировать большие количества препарата от лейкемии , меркаптопурина , который потенциально вызывает фатальное падение количества лейкоцитов у таких пациентов. Таким образом, пациентам с мутациями ТПМТ из соображений безопасности рекомендуется назначать более низкую дозу меркаптопурина. [35]
Мониторинг ответа на лечение
[ редактировать ]Биомаркеры рака также показали свою полезность при мониторинге эффективности лечения с течением времени. В этой конкретной области проводится много исследований, поскольку успешные биомаркеры потенциально могут обеспечить значительное снижение затрат на уход за пациентами, поскольку текущие тесты на основе изображений, такие как КТ и МРТ, для мониторинга состояния опухоли, очень дорогостоящие. [36]
Одним из примечательных биомаркеров, привлекающих значительное внимание, является белковый биомаркер S100 -бета при мониторинге реакции злокачественной меланомы . При таких меланомах меланоциты , клетки, вырабатывающие пигмент в нашей коже, производят белок S100-бета в высоких концентрациях, зависящих от количества раковых клеток. Таким образом, ответ на лечение связан со снижением уровня S100-бета в крови таких людей. [37] [38]
Аналогичным образом, дополнительные лабораторные исследования показали, что опухолевые клетки, подвергающиеся апоптозу, могут высвобождать клеточные компоненты, такие как цитохром С , нуклеосомы , расщепленный цитокератин-18 и Е-кадгерин . Исследования показали, что эти и другие макромолекулы можно обнаружить в кровообращении во время терапии рака, что является потенциальным источником клинических показателей для мониторинга лечения. [36]
Повторение
[ редактировать ]Биомаркеры рака также могут оказаться полезными для прогнозирования или мониторинга рецидивов рака . Анализ рака молочной железы Oncotype DX® является одним из таких тестов, используемых для прогнозирования вероятности рецидива рака молочной железы. Этот тест предназначен для женщин с ранней стадией (стадии I или II), инвазивным раком молочной железы с отрицательными узлами и положительным по рецепторам эстрогена (ER+), которым будет назначена гормональная терапия . Oncotype DX анализирует панель из 21 гена в клетках, взятых во время биопсии опухоли . Результаты теста представлены в виде шкалы рецидивов, которая указывает на вероятность рецидива через 10 лет. [39] [40]
Использование биомаркеров в исследованиях рака
[ редактировать ]Разработка целей по борьбе с наркотиками
[ редактировать ]Помимо использования в медицине рака, биомаркеры часто используются в процессе разработки лекарств от рака. Например, в 1960-х годах исследователи обнаружили, что большинство пациентов с хроническим миелогенным лейкозом обладают определенной генетической аномалией в хромосомах 9 и 22, получившей название « Филадельфийская хромосома» . Когда эти две хромосомы объединяются, они создают ген, вызывающий рак, известный как BCR-ABL . У таких больных этот ген выступает в качестве основной исходной точки всех физиологических проявлений лейкоза. В течение многих лет BCR-ABL просто использовался в качестве биомаркера для стратификации определенного подтипа лейкемии. Однако разработчикам лекарства в конечном итоге удалось разработать иматиниб — мощный препарат, который эффективно ингибирует этот белок и значительно снижает выработку клеток, содержащих филадельфийскую хромосому. [41] [42]
Суррогатные конечные точки
[ редактировать ]Другая многообещающая область применения биомаркеров – это суррогатные конечные точки . В этом приложении биомаркеры выступают в роли заменителей воздействия лекарства на прогрессирование и выживаемость рака. В идеале использование проверенных биомаркеров избавило бы пациентов от необходимости проходить биопсию опухоли и длительные клинические испытания, чтобы определить, работает ли новый препарат. В текущих стандартах лечения критерием определения эффективности препарата является проверка того, замедляет ли оно прогрессирование рака у людей и, в конечном итоге, продлевает ли оно выживаемость. Однако успешные суррогаты биомаркеров могли бы сэкономить значительное время, усилия и деньги, если бы неудачные лекарства можно было исключить из разработки до того, как они будут доведены до клинических испытаний.
Некоторые идеальные характеристики суррогатных биомаркеров конечной точки включают: [43] [44]
- Биомаркер должен быть вовлечен в процесс, вызывающий рак
- Изменения биомаркера должны коррелировать с изменениями в заболевании.
- Уровни биомаркеров должны быть достаточно высокими, чтобы их можно было легко и надежно измерить.
- Уровни или наличие биомаркера должны легко различать нормальную, раковую и предраковую ткань.
- Эффективное лечение рака должно изменить уровень биомаркера
- Уровень биомаркера не должен меняться спонтанно или в ответ на другие факторы, не связанные с успешным лечением рака.
В частности, две области, которым уделяется внимание в качестве суррогатных маркеров, включают циркулирующие опухолевые клетки (ЦОК). [45] [46] и циркулирующие микроРНК . [47] [48] Оба этих маркера связаны с количеством опухолевых клеток, присутствующих в крови, и поэтому есть надежда, что они станут заменой прогрессирования и метастазирования опухоли . Однако существенными препятствиями на пути их внедрения являются трудности обогащения, идентификации и измерения уровней ЦОК и микроРНК в крови. Для их внедрения в клиническую помощь, вероятно, необходимы новые технологии и исследования. [49] [50] [51]
Типы биомаркеров рака
[ редактировать ]Молекулярные биомаркеры рака
[ редактировать ]| Тип опухоли | Биомаркер |
|---|---|
| Грудь | ER / PR (рецептор эстрогена/рецептор прогестерона) [52] [53] |
| HER-2/новый [52] [53] | |
| Колоректальный | РЭФР [52] [53] |
| КРАС [52] [54] | |
| УГТ1А1 [52] [54] | |
| Желудочный | HER-2/новый [52] |
| СУТЬ | c-KIT [52] [55] |
| Лейкемия/лимфома | CD20 [52] [56] |
| CD30 [52] [57] | |
| FIP1L1 — PDGFRальфа [52] [58] | |
| ПДГФР [52] [59] | |
| Филадельфийская хромосома ( BCR / ABL ) [52] [60] [61] | |
| PML / RAR-альфа [52] [62] | |
| ТПМТ [52] [63] | |
| УГТ1А1 [52] [64] | |
| Легкое | ЕМЛ4 / АЛК [52] [65] [66] |
| РЭФР [52] [53] | |
| КРАС [52] [53] | |
| Меланома | БРАФ [52] [66] |
| поджелудочная железа | Повышенный уровень лейцина , изолейцина и валина. [67] |
| Яичники | СА-125 [68] |
Другие примеры биомаркеров:
- Супрессоры опухоли теряются при раке
- РНК
- Белки, обнаруженные в жидкостях или тканях организма.
- Примеры: простатический специфический антиген и CA-125.
- Антитела к раковым антигенам
- Примеры: полиомавирус клеток Меркеля. [70]
- ДНК
Биомаркеры рака без специфичности
[ редактировать ]Не все биомаркеры рака должны быть специфичными для типов рака. Некоторые биомаркеры, обнаруженные в системе кровообращения, можно использовать для определения аномального роста клеток, присутствующих в организме. Все эти типы биомаркеров можно выявить с помощью диагностических анализов крови, что является одной из основных причин регулярно проходить медицинское обследование. Регулярно проходя тестирование, многие проблемы со здоровьем, такие как рак, можно обнаружить на ранней стадии, что предотвращает множество смертей.
Было показано, что соотношение нейтрофилов и лимфоцитов является неспецифическим определяющим фактором многих видов рака. Это соотношение фокусируется на активности двух компонентов иммунной системы, участвующих в воспалительной реакции, которая, как показано, выше при наличии злокачественных опухолей. [71] Кроме того, основной фактор роста фибробластов ( bFGF ) представляет собой белок, который участвует в пролиферации клеток. К сожалению, было показано, что при наличии опухолей он очень активен, что привело к выводу, что он может способствовать более быстрому размножению злокачественных клеток. [72] Исследования показали, что антитела против bFGF можно использовать для лечения опухолей различного происхождения. [72] Более того, инсулиноподобный фактор роста (IGF-R) участвует в пролиферации и росте клеток. Возможно, он участвует в ингибировании апоптоза, запрограммированной гибели клеток из-за какого-то дефекта. [73] В связи с этим уровни IGF-R могут повышаться при наличии рака молочной железы, простаты, легких и прямой кишки. [74]
| Биомаркер | Описание | Используемый биосенсор |
|---|---|---|
| NLR (соотношение нейтрофилов и лимфоцитов) | Повышается при воспалении, вызванном раком [75] | Нет |
| Основной фактор роста фибробластов (bFGF) | Этот уровень увеличивается при наличии опухоли, способствует быстрому воспроизводству опухолевых клеток. [76] | Электрохимический [77] |
| Инсулиноподобный фактор роста (IGF-R) | Высокая активность в раковых клетках, помогает размножению [78] | Датчик электрохимической импедансной спектроскопии [79] |
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Кальцоне К.А. (май 2012 г.). «Генетические биомаркеры риска рака» . Семинары по сестринскому делу в онкологии . 28 (2): 122–128. дои : 10.1016/j.soncn.2012.03.007 . ПМЦ 10433658 . ПМИД 22542320 .
- ^ Герцег З., Эно П. (июнь 2007 г.). «Генетические и эпигенетические изменения как биомаркеры обнаружения, диагностики и прогноза рака» . Молекулярная онкология . 1 (1): 26–41. дои : 10.1016/j.molonc.2007.01.004 . ПМЦ 5543860 . ПМИД 19383285 .
- ^ Ли Д., Чан Д.В. (апрель 2014 г.). «Протеомные биомаркеры рака от открытия до одобрения: усилия того стоят» . Экспертное обозрение по протеомике . 11 (2): 135–136. дои : 10.1586/14789450.2014.897614 . ПМК 4079106 . ПМИД 24646122 .
- ^ Айспуруа-Олайсола О, Тораньо Х.С., Фалькон-Перес Х.М., Уильямс С., Райхардт Н., Бунс Г.Дж. (2018). «Масс-спектрометрия для открытия биомаркеров гликанов». TrAC Тенденции в аналитической химии . 100 : 7–14. дои : 10.1016/j.trac.2017.12.015 .
- ^ Мишра А., Верма М. (март 2010 г.). «Биомаркеры рака: готовы ли мы к прайм-тайму?» . Раки . 2 (1): 190–208. дои : 10.3390/cancers2010190 . ПМЦ 3827599 . ПМИД 24281040 .
- ^ Рея Дж., Молинаро Р.Дж. (март 2011 г.). «Биомаркеры рака: пережить путь от скамьи до постели» . Наблюдатель медицинской лаборатории. Архивировано из оригинала 14 октября 2013 года . Проверено 26 апреля 2013 г.
- ^ Бене Т., Копур М.С. (1 января 2012 г.). «Биомаркеры гепатоцеллюлярной карциномы» . Международный журнал гепатологии . 2012 : 859076. doi : 10.1155/2012/859076 . ПМЦ 3357951 . ПМИД 22655201 .
- ^ Мусолино А., Белла М.А., Бортези Б., Мичиара М., Налди Н., Занелли П. и др. (июнь 2007 г.). «Мутации BRCA, молекулярные маркеры и клинические переменные при раке молочной железы с ранним началом: популяционное исследование». Грудь . 16 (3): 280–292. дои : 10.1016/j.breast.2006.12.003 . hdl : 11381/1629553 . ПМИД 17257844 .
- ^ Динстманн Р., Табернеро Дж. (март 2011 г.). «BRAF как мишень для терапии рака». Противораковые агенты в медицинской химии . 11 (3): 285–295. дои : 10.2174/187152011795347469 . ПМИД 21426297 .
- ^ Лампарелла Н., Барочия А., Альмокадем С. (2013). «Влияние генетических маркеров на лечение немелкоклеточного рака легких». Влияние генетических мишеней на терапию рака . Достижения экспериментальной медицины и биологии. Том. 779. стр. 145–164. дои : 10.1007/978-1-4614-6176-0_6 . ISBN 978-1-4614-6175-3 . ПМИД 23288638 .
- ^ Орфанос Г., Кунтуракис П. (2012). «Нацеливание на рецептор HER2 при метастатическом раке молочной железы» . Гематология/онкология и терапия стволовыми клетками . 5 (3): 127–137. дои : 10.5144/1658-3876.2012.127 . ПМИД 23095788 .
- ^ Депримо С.Е., Хуанг Х., Блэкстайн М.Е., Гарретт С.Р., Хармон К.С., Шеффски П. и др. (сентябрь 2009 г.). «Циркулирующие уровни растворимого KIT служат биомаркером клинического исхода у пациентов со стромальными опухолями желудочно-кишечного тракта, получающих сунитиниб после неэффективности иматиниба» . Клинические исследования рака . 15 (18): 5869–5877. дои : 10.1158/1078-0432.CCR-08-2480 . ПМЦ 3500590 . ПМИД 19737953 .
- ^ Бантис А, Грамматикос П (сентябрь – декабрь 2012 г.). «Простатический специфический антиген и сканирование костей в диагностике и наблюдении за раком простаты. Можно ли повысить диагностическую значимость ПСА?». Греческий журнал ядерной медицины . 15 (3): 241–246. ПМИД 23227460 .
- ^ Круйфф С., Хоекстра Х.Дж. (апрель 2012 г.). «Текущий статус S-100B как биомаркера меланомы». Европейский журнал хирургической онкологии . 38 (4): 281–285. дои : 10.1016/j.ejso.2011.12.005 . ПМИД 22240030 .
- ^ Людвиг Дж. А., Вайнштейн Дж. Н. (ноябрь 2005 г.). «Биомаркеры в определении стадии рака, прогнозе и выборе лечения» . Обзоры природы. Рак . 5 (11): 845–856. дои : 10.1038/nrc1739 . ПМИД 16239904 . S2CID 25540232 .
- ^ Ван Кью, Чаеркади Р., Ву Дж., Хван Х.Дж., Пападопулос Н., Копелович Л. и др. (февраль 2011 г.). «Мутантные белки как рак-специфические биомаркеры» . Труды Национальной академии наук Соединенных Штатов Америки . 108 (6): 2444–2449. Бибкод : 2011PNAS..108.2444W . дои : 10.1073/pnas.1019203108 . ПМЦ 3038743 . ПМИД 21248225 .
- ^ Перейти обратно: а б с Ли Х, Е М, Чжан В, Тан Д, Джафрезик-Рено Н, Ян Х, Го Цз (февраль 2019 г.). «Жидкостная биопсия циркулирующей опухолевой ДНК и применение биосенсоров». Биосенсоры и биоэлектроника . 126 : 596–607. дои : 10.1016/j.bios.2018.11.037 . ПМИД 30502682 . S2CID 56479882 .
- ^ «биомаркер» . Словарь терминов, посвященных раку, NCI . Национальный институт рака. 2 февраля 2011 г.
- ^ «Биомаркеры рака: вводное руководство для адвокатов» (PDF) . Исследовательская пропагандистская сеть. 2010. Архивировано из оригинала (PDF) 29 октября 2013 г. Проверено 26 апреля 2013 г.
- ^ Верма М., Манне У. (октябрь 2006 г.). «Генетические и эпигенетические биомаркеры в диагностике рака и выявлении групп высокого риска» . Критические обзоры по онкологии/гематологии . 60 (1): 9–18. doi : 10.1016/j.critrevonc.2006.04.002 . ПМИД 16829121 .
- ^ Леонг П.П., Резай Б., Кох В.М., Рид А., Эйзель Д., Ли DJ и др. (июль 1998 г.). «Отличие вторичных первичных опухолей от метастазов в легких у пациентов с плоскоклеточным раком головы и шеи» . Журнал Национального института рака . 90 (13): 972–977. дои : 10.1093/jnci/90.13.972 . ПМИД 9665144 .
- ^ Лапин М., Олтедал С., Тьенсволл К., Буль Т., Смааланд Р., Гарресори Х. и др. (ноябрь 2018 г.). «Размер фрагмента и уровень внеклеточной ДНК предоставляют прогностическую информацию у пациентов с распространенным раком поджелудочной железы» . Журнал трансляционной медицины . 16 (1): 300. дои : 10.1186/s12967-018-1677-2 . ПМК 6218961 . ПМИД 30400802 .
- ^ Драгани Т.А., Матарезе В., Коломбо Ф. (апрель 2020 г.). «Биомаркеры ранней диагностики рака: перспективы успеха через призму генетики опухолей». Биоэссе . 42 (4): e1900122. doi : 10.1002/bies.201900122 . ПМИД 32128843 . S2CID 212406467 .
- ^ Терпос Э., Димопулос М.А., Шривастава В., Лейтцель К., Кристулас Д., Мигку М. и др. (март 2010 г.). «Высокие уровни ТИМП-1 в сыворотке коррелируют с прогрессирующим заболеванием и предсказывают плохую выживаемость у пациентов с множественной миеломой, получающих новые препараты». Исследования лейкемии . 34 (3): 399–402. doi : 10.1016/j.leukres.2009.08.035 . ПМИД 19781774 .
- ^ Куукасъярви Т., Кононен Дж., Хелин Х., Холли К., Изола Дж. (сентябрь 1996 г.). «Потеря рецептора эстрогена при рецидиве рака молочной железы связана с плохой реакцией на эндокринную терапию». Журнал клинической онкологии . 14 (9): 2584–2589. дои : 10.1200/jco.1996.14.9.2584 . ПМИД 8823339 .
- ^ Харрис Л., Фриче Х., Меннел Р., Нортон Л., Равдин П., Таубе С. и др. (ноябрь 2007 г.). «Обновленные рекомендации Американского общества клинической онкологии, 2007 г. по использованию онкомаркеров при раке молочной железы». Журнал клинической онкологии . 25 (33): 5287–5312. дои : 10.1200/JCO.2007.14.2364 . ПМИД 17954709 .
- ^ Крегер Н., Милде-Лангош К., Ритдорф С., Шмур С., Шумахер М., Зандер А.Р., Лёнинг Т. (январь 2006 г.). «Прогностические и прогностические эффекты иммуногистохимических факторов у больных первичным раком молочной железы высокого риска» . Клинические исследования рака . 12 (1): 159–168. дои : 10.1158/1078-0432.CCR-05-1340 . ПМИД 16397038 .
- ^ Врбич С., Пейчич И., Филипович С., Кочич Б., Врбич М. (январь–март 2013 г.). «Текущая и будущая анти-HER2-терапия при раке молочной железы». Журнал БУОн . 18 (1): 4–16. ПМИД 23613383 .
- ^ Ю С., Рю М.Х., Рю Б.И., Бек М.И., Кан Ю.К. (октябрь 2013 г.). «Эффективность, безопасность и фармакокинетика повышения дозы иматиниба до 800 мг/день у пациентов с распространенными стромальными опухолями желудочно-кишечного тракта». Исследуемые новые лекарства . 31 (5): 1367–1374. дои : 10.1007/s10637-013-9961-8 . ПМИД 23591629 . S2CID 29477955 .
- ^ Деметри Г.Д., ван Остером А.Т., Гарретт С.Р., Блэкстайн М.Е., Шах М.Х., Вервей Дж. и др. (октябрь 2006 г.). «Эффективность и безопасность сунитиниба у пациентов с распространенной стромальной опухолью желудочно-кишечного тракта после неэффективности иматиниба: рандомизированное контролируемое исследование». Ланцет . 368 (9544): 1329–1338. дои : 10.1016/S0140-6736(06)69446-4 . ПМИД 17046465 . S2CID 25931515 .
- ^ Хербст Р.С., Прагер Д., Герман Р., Ференбахер Л., Джонсон Б.Е., Сэндлер А. и др. (сентябрь 2005 г.). «ДАНЬ: исследование III фазы эрлотиниба гидрохлорида (OSI-774) в сочетании с химиотерапией карбоплатином и паклитакселом при распространенном немелкоклеточном раке легких» . Журнал клинической онкологии . 23 (25): 5892–5899. дои : 10.1200/JCO.2005.02.840 . ПМИД 16043829 .
- ^ Линч Т.Дж., Белл Д.В., Сорделла Р., Гурубхагаватула С., Окимото Р.А., Брэнниган Б.В. и др. (май 2004 г.). «Активирующие мутации в рецепторе эпидермального фактора роста, лежащие в основе реакции немелкоклеточного рака легких на гефитиниб» (PDF) . Медицинский журнал Новой Англии . 350 (21): 2129–2139. doi : 10.1056/NEJMoa040938 . ПМИД 15118073 .
- ^ Сойерс CL (апрель 2008 г.). «Проблема биомаркеров рака». Природа . 452 (7187): 548–552. Бибкод : 2008Natur.452..548S . дои : 10.1038/nature06913 . ПМИД 18385728 . S2CID 205213083 .
- ^ Карась-Кузелицкий Н., Млинарик-Раскан I (август 2009 г.). «Индивидуализация тиопуриновой терапии: тиопурин-S-метилтрансфераза и не только». Фармакогеномика . 10 (8): 1309–1322. дои : 10.2217/стр.09.78 . ПМИД 19663675 .
- ^ Реллинг М.В., Хэнкок М.Л., Ривера Г.К., Сандлунд Дж.Т., Рибейро Р.К., Кринецки Е.Ю. и др. (декабрь 1999 г.). «Непереносимость меркаптопуриновой терапии и гетерозиготность по локусу гена тиопурин-S-метилтрансферазы» . Журнал Национального института рака . 91 (23): 2001–2008. дои : 10.1093/jnci/23.91.2001 . ПМИД 10580024 .
- ^ Перейти обратно: а б Шнайдер Дж.Э., Сидху М.К., Дусе С., Кисс Н., Осфельдт Р.Л., Чалфин Д. (ноябрь 2012 г.). «Экономика раковых биомаркеров». Персонализированная медицина . 9 (8): 829–837. дои : 10.2217/pm.12.87 . ПМИД 29776231 .
- ^ Хенце Г., Даммер Р., Йоллер-Джемелька Х.И., Бони Р., Бург Г. (1997). «Сыворотка S100 - маркер для мониторинга заболеваний при метастатической меланоме». Дерматология . 194 (3): 208–212. дои : 10.1159/000246103 . ПМИД 9187834 .
- ^ Харпио Р., Эйнарссон Р. (июль 2004 г.). «Белки S100 как биомаркеры рака с акцентом на S100B при злокачественной меланоме». Клиническая биохимия . 37 (7): 512–518. doi : 10.1016/j.clinbiochem.2004.05.012 . ПМИД 15234232 .
- ^ Ламонд Н.В., Скеджел С., Юнис Т. (апрель 2013 г.). «Является ли оценка рецидива по 21 гену экономически эффективным анализом при раке молочной железы с отрицательным уровнем эндокринно-чувствительных узлов?». Экспертный обзор фармакоэкономических исследований и результатов исследований . 13 (2): 243–250. дои : 10.1586/erp.13.4 . ПМИД 23570435 . S2CID 33661439 .
- ^ Бирошак-младший, Шварц Г.Ф., Палаццо Дж.П., Толл А.Д., Брилл К.Л., Яслоу Р.Дж., Ли С.Ю. (май 2013 г.). «Влияние Oncotype DX на решения о лечении ER-положительного и безузлового рака молочной железы с гистологической корреляцией» . Журнал груди . 19 (3): 269–275. дои : 10.1111/tbj.12099 . ПМИД 23614365 . S2CID 30895945 .
- ^ Моен, доктор медицинских наук, Маккидж К., Плоскер Г.Л., Сиддики М.А. (2007). «Иматиниб: обзор его применения при хроническом миелолейкозе». Наркотики . 67 (2): 299–320. дои : 10.2165/00003495-200767020-00010 . ПМИД 17284091 .
- ^ Лемоник М., Парк А (28 мая 2001 г.). «Новая надежда на рак» . Время . Архивировано из оригинала 15 октября 2007 года . Проверено 26 апреля 2013 г.
- ^ Прайс К., Макдоннелл Д. (февраль 1991 г.). «Влияние ниобиевой фильтрации и постоянного потенциала на сенситометрические реакции стоматологических рентгенографических пленок». Денто-челюстно-лицевая радиология . 20 (1): 11–16. дои : 10.1259/dmfr.20.1.1884846 . ПМИД 1884846 .
- ^ Коэн В., Хури Ф.Р. (2003). «Прогресс в химиопрофилактике рака легких» . Контроль рака . 10 (4): 315–324. дои : 10.1177/107327480301000406 . ПМИД 12915810 .
- ^ Лу С.И., Цай Х.Л., Уэн Ю.Х., Ху Х.М., Чен С.В., Ченг Т.Л. и др. (март 2013 г.). «Циркулирующие опухолевые клетки как суррогатный маркер для определения клинического результата химиотерапии mFOLFOX у пациентов с раком толстой кишки III стадии» . Британский журнал рака . 108 (4): 791–797. дои : 10.1038/bjc.2012.595 . ПМК 3590657 . ПМИД 23422758 .
- ^ Балик М., Уильямс А., Лин Х., Датар Р., Кот Р.Дж. (2013). «Циркулирующие опухолевые клетки: от скамьи до постели» . Ежегодный обзор медицины . 64 : 31–44. doi : 10.1146/annurev-med-050311-163404 . ПМК 3809995 . ПМИД 23092385 .
- ^ Мадхаван Д., Цукник М., Валлвинер М., Кук К., Модуньо С., Шарпфф М. и др. (ноябрь 2012 г.). «Циркулирующие микроРНК как суррогатные маркеры циркулирующих опухолевых клеток и прогностические маркеры при метастатическом раке молочной железы» . Клинические исследования рака . 18 (21): 5972–5982. дои : 10.1158/1078-0432.CCR-12-1407 . ПМИД 22952344 .
- ^ Редова М., Сана Дж., Слаби О. (март 2013 г.). «Циркулирующие микроРНК как новые биомаркеры солидного рака в крови». Будущая онкология . 9 (3): 387–402. дои : 10.2217/фон.12.192 . ПМИД 23469974 .
- ^ Йоссе С.А., Пантель К. (январь 2013 г.). «Биологические проблемы обнаружения циркулирующих опухолевых клеток» . Исследования рака . 73 (1): 8–11. дои : 10.1158/0008-5472.CAN-12-3422 . ПМИД 23271724 .
- ^ Хоу Х.В., Варкиани М.Э., Ху Б.Л., Ли З.Р., Су Р.А., Тан Д.С. и др. (2013). «Выделение и извлечение циркулирующих опухолевых клеток с помощью центробежных сил» . Научные отчеты . 3 : 1259. Бибкод : 2013NatSR...3E1259H . дои : 10.1038/srep01259 . ПМЦ 3569917 . ПМИД 23405273 .
- ^ Дондт Б., Де Блезер Э., Клейс Т., Бьюленс С., Люмен Н., Вандесомпель Дж. и др. (декабрь 2019 г.). «Открытие и проверка сигнатуры микроРНК сыворотки для характеристики олиго- и полиметастатического рака простаты: не готово к прайм-тайму». Всемирный журнал урологии . 37 (12): 2557–2564. дои : 10.1007/s00345-018-2609-8 . hdl : 1854/LU-8586484 . ПМИД 30578441 . S2CID 58594673 .
- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п д р с «Таблица фармакогеномных биомаркеров на этикетках лекарственных средств» . Управление по контролю за продуктами и лекарствами США.
- ^ Перейти обратно: а б с д и «Информационный бюллетень об опухолевых маркерах» (PDF) . Американское онкологическое общество.
- ^ Перейти обратно: а б Хайнц-Йозеф Ленц (18 сентября 2012 г.). Биомаркеры в онкологии: прогноз и прогноз . Springer Science & Business Media. п. 263. ИСБН 978-1-4419-9754-8 .
- ^ Гонсалес Р.С., Карлсон Дж., Пейдж А.Дж., Коэн С. (июль 2011 г.). «Маркеры желудочно-кишечных стромальных опухолей при меланомах кожи: связь с прогностическими факторами и исходом» . Американский журнал клинической патологии . 136 (1): 74–80. дои : 10.1309/AJCP9KHD7DCHWLMO . ПМИД 21685034 .
- ^ Там К.С., Отеро-Паласиос Дж., Абруццо Л.В., Йоргенсен Дж.Л., Ферраджоли А., Виерда В.Г. и др. (апрель 2008 г.). «Экспрессия CD20 при хроническом лимфоцитарном лейкозе зависит от генетического подтипа: исследование количественной проточной цитометрии и флуоресцентной гибридизации in-situ у 510 пациентов» . Британский журнал гематологии . 141 (1): 36–40. дои : 10.1111/j.1365-2141.2008.07012.x . ПМИД 18324964 .
- ^ Чжан М., Яо З., Патель Х., Гарместани К., Чжан З., Таланов В.С. и др. (май 2007 г.). «Эффективная терапия мышиных моделей лейкемии и лимфомы человека с помощью меченого антитела против CD30, HeFi-1» . Труды Национальной академии наук Соединенных Штатов Америки . 104 (20): 8444–8448. Бибкод : 2007PNAS..104.8444Z . дои : 10.1073/pnas.0702496104 . ЧВК 1895969 . ПМИД 17488826 .
- ^ Ямада Ю., Санчес-Агилера А., Брандт Э.Б., МакБрайд М., Аль-Моамен Н.Дж., Финкельман Ф.Д. и др. (сентябрь 2008 г.). «FIP1L1/PDGFRalpha взаимодействует с SCF, вызывая системный мастоцитоз на мышиной модели хронического эозинофильного лейкоза/гиперэозинофильного синдрома» . Кровь . 112 (6): 2500–2507. дои : 10.1182/кровь-2007-11-126268 . ПМИД 18539901 .
- ^ Нимер С.Д. (май 2008 г.). «Миелодиспластические синдромы» . Кровь . 111 (10): 4841–4851. дои : 10.1182/blood-2007-08-078139 . ПМИД 18467609 . S2CID 6802096 .
- ^ Оттманн О, Домбре Х, Мартинелли Г, Симонссон Б, Гийо Ф, Ларсон Р.А. и др. (октябрь 2007 г.). «Дазатиниб вызывает быстрые гематологические и цитогенетические реакции у взрослых пациентов с острым лимфобластным лейкозом с положительной филадельфийской хромосомой и резистентностью или непереносимостью иматиниба: промежуточные результаты исследования фазы 2» . Кровь . 110 (7): 2309–2315. doi : 10.1182/blood-2007-02-073528 . ПМИД 17496201 .
- ^ Булос Н., Малдер Х.Л., Калабрезе С.Р., Моррисон Дж.Б., Рег Дж.Э., Реллинг М.В. и др. (март 2011 г.). «Химиотерапевтические средства предотвращают возникновение устойчивых к дазатинибу мутаций киназы BCR-ABL в точной мышиной модели острого лимфобластного лейкоза с положительной филадельфийской хромосомой» . Кровь . 117 (13): 3585–3595. дои : 10.1182/blood-2010-08-301267 . ПМК 3072880 . ПМИД 21263154 .
- ^ О'Коннелл, Пенсильвания, Мадурейра, Пенсильвания, Берман Дж. Н., Ливски Р. С., Вайсман Д. М. (апрель 2011 г.). «Регуляция S100A10 онкобелком PML-RAR-α» . Кровь . 117 (15): 4095–4105. дои : 10.1182/blood-2010-07-298851 . ПМИД 21310922 .
- ^ Даффи MJ, Crown J (ноябрь 2008 г.). «Персонализированный подход к лечению рака: как биомаркеры могут помочь» . Клиническая химия . 54 (11): 1770–1779. дои : 10.1373/clinchem.2008.110056 . ПМИД 18801934 .
- ^ Рибраг В., Косельни С., Казановас О., Казенев С., Брис П., Моршхаузер Ф. и др. (апрель 2009 г.). «Фармакогенетическое исследование лимфом Ходжкина выявило влияние полиморфизма UGT1A1 на прогноз пациента» . Кровь . 113 (14): 3307–3313. дои : 10.1182/blood-2008-03-148874 . ПМИД 18768784 .
- ^ Ли Ю, Йе Х, Лю Дж, Чжа Дж, Пей Л (январь 2011 г.). «Оценка слитых белков EML4-ALK при немелкоклеточном раке легкого с использованием низкомолекулярных ингибиторов» . Неоплазия . 13 (1): 1–11. дои : 10.1593/neo.101120 . ПМК 3022423 . ПМИД 21245935 .
- ^ Перейти обратно: а б Пао В., Жирар Н. (февраль 2011 г.). «Новые драйверные мутации при немелкоклеточном раке легких». «Ланцет». Онкология . 12 (2): 175–180. дои : 10.1016/S1470-2045(10)70087-5 . ПМИД 21277552 .
- ^ Хьюс А. (2 октября 2014 г.). «Многообещающий метод обнаружения рака поджелудочной железы за годы до традиционной диагностики» . Центр Сингулярности . Проверено 22 апреля 2016 г.
- ^ Гупта Д., Лис К.Г. (октябрь 2009 г.). «Роль CA125 в прогнозировании выживаемости при раке яичников - обзор эпидемиологической литературы» . Журнал исследований яичников . 2 (1): 13. дои : 10.1186/1757-2215-2-13 . ПМЦ 2764643 . ПМИД 19818123 .
- ^ Бартельс К.Л., Цонгалис Г.Дж. (апрель 2009 г.). «МикроРНК: новые биомаркеры рака человека» . Клиническая химия . 55 (4): 623–631. дои : 10.1373/clinchem.2008.112805 . ПМИД 19246618 .
- ^ Полсон К.Г., Льюис К.В., Редман М.В., Саймонсон В.Т., Лисберг А., Риттер Д. и др. (апрель 2017 г.). «Антитела к вирусным онкопротеинам как маркер рецидива карциномы Меркеля: проспективное проверочное исследование» . Рак . 123 (8): 1464–1474. дои : 10.1002/cncr.30475 . ПМЦ 5384867 . ПМИД 27925665 .
- ^ Проктор М.Дж., Макмиллан, округ Колумбия, Моррисон Д.С., Флетчер К.Д., Хорган П.Г., Кларк С.Дж. (август 2012 г.). «Производное соотношение нейтрофилов и лимфоцитов предсказывает выживаемость пациентов с раком» . Британский журнал рака . 107 (4): 695–699. дои : 10.1038/bjc.2012.292 . ПМК 3419948 . ПМИД 22828611 .
- ^ Перейти обратно: а б Лю М, Син LQ (август 2017 г.). «Основной фактор роста фибробластов как потенциальный биомаркер диагностики метастазирования злокачественных опухолей у женщин» . Письма об онкологии . 14 (2): 1561–1567. дои : 10.3892/ol.2017.6335 . ПМЦ 5529833 . ПМИД 28789380 .
- ^ Фюрстенбергер Г., Сенн Х.Дж. (май 2002 г.). «Инсулиноподобные факторы роста и рак». «Ланцет». Онкология . 3 (5): 298–302. дои : 10.1016/s1470-2045(02)00731-3 . ПМИД 12067807 .
- ^ Ю Х, Рохан Т (сентябрь 2000 г.). «Роль семейства инсулиноподобных факторов роста в развитии и прогрессировании рака» . Журнал Национального института рака . 92 (18): 1472–1489. дои : 10.1093/jnci/92.18.1472 . ПМИД 10995803 .
- ^ Вано Я., Удар С., М.А., Тету П., Тибо С., Абудагга Х. и др. (06 апреля 2018 г.). «Оптимальное пороговое значение соотношения нейтрофилов и лимфоцитов: факт или фантазия? Проспективное когортное исследование у пациентов с метастатическим раком» . ПЛОС ОДИН . 13 (4): e0195042. Бибкод : 2018PLoSO..1395042V . дои : 10.1371/journal.pone.0195042 . ПМЦ 5889159 . ПМИД 29624591 .
- ^ Лю М, Син LQ (август 2017 г.). «Основной фактор роста фибробластов как потенциальный биомаркер диагностики метастазирования злокачественных опухолей у женщин» . Письма об онкологии . 14 (2): 1561–1567. дои : 10.3892/ol.2017.6335 . ПМЦ 5529833 . ПМИД 28789380 .
- ^ Торренте-Родригес Р.М., Руис-Вальдепеньяс Монтьель В., Кампусано С., Педреро М., Фарчадо М., Варгас Е. и др. (04.04.2017). «Электрохимический сенсор для быстрого определения рецептора фактора роста фибробластов 4 в сырых лизатах раковых клеток» . ПЛОС ОДИН . 12 (4): e0175056. Бибкод : 2017PLoSO..1275056T . дои : 10.1371/journal.pone.0175056 . ПМК 5380347 . ПМИД 28376106 .
- ^ Дендулури С.К., Идову О., Ван З., Ляо З., Ян З., Мохаммед М.К. и др. (март 2015 г.). «Передача сигналов инсулиноподобного фактора роста (IGF) в онкогенезе и развитии устойчивости рака к лекарствам» . Гены и болезни . 2 (1): 13–25. дои : 10.1016/j.gendis.2014.10.004 . ПМЦ 4431759 . ПМИД 25984556 .
- ^ Резаи, Бехзад; Маджиди, Наджме; Рахмани, Хамидреза; Хаямян, Таги (2011). «Электрохимический импедиметрический иммуносенсор для инсулиноподобного фактора роста-1 с использованием электрода, модифицированного специфическими моноклональными антителами и нанозолотом». Биосенсоры и биоэлектроника . 26 (5). Эльзевир Б.В.: 2130–2134. дои : 10.1016/j.bios.2010.09.020 . ISSN 0956-5663 .