Хронический миелогенный лейкоз
| Хронический миелогенный лейкоз | |
|---|---|
| Другие имена | Хронический миелолейкоз, хронический гранулоцитарный лейкоз (ХГЛ) |
 | |
| Филадельфийская хромосома , как видно с помощью флуоресцентной гибридизации in situ (FISH). | |
| Специальность | Гематология и онкология |
| Частота | 298,000 (2015) [1] |
| Летальные исходы | 32,200 (2015) [2] |
Хронический миелолейкоз ( ХМЛ ), также известный как хронический миелолейкоз , представляет собой рак лейкоцитов . Это форма лейкемии, характеризующаяся повышенным и нерегулируемым ростом миелоидных клеток в костном мозге и накоплением этих клеток в крови. ХМЛ представляет собой клональное заболевание стволовых клеток пролиферация зрелых гранулоцитов ( нейтрофилов , эозинофилов и базофилов костного мозга, при котором обнаруживается ) и их предшественников; характерное увеличение базофилов клинически значимо. Это тип миелопролиферативного новообразования, связанного с характерной хромосомной транслокацией, называемой Филадельфийской хромосомой .
ХМЛ в основном лечат таргетными препаратами, называемыми ингибиторами тирозинкиназы (ИТК), которые с 2001 года привели к значительному улучшению показателей долгосрочной выживаемости. Эти препараты произвели революцию в лечении этого заболевания и позволяют большинству пациентов иметь хорошее качество жизни по сравнению с другими. к бывшим химиотерапевтическим препаратам. В западных странах ХМЛ составляет 15–25% всех лейкозов взрослых и 14% лейкозов в целом (включая педиатрическую популяцию, где ХМЛ встречается реже). [3]
Признаки и симптомы [ править ]
Проявление ХМЛ зависит от стадии заболевания на момент постановки диагноза, поскольку известно, что в некоторых случаях стадии пропускаются. [4]
У большинства пациентов (~90%) диагноз диагностируется на хронической стадии, которая чаще всего протекает бессимптомно. В этих случаях его можно диагностировать случайно по повышенному количеству лейкоцитов при обычном лабораторном тесте. Он также может проявляться симптомами, указывающими на гепатоспленомегалию и вызываемую этим боль в левом подреберье. Увеличенная селезенка может оказывать давление на желудок, вызывая потерю аппетита и, как следствие, потерю веса. Он также может проявляться легкой лихорадкой и ночной потливостью из-за повышенного базального уровня метаболизма. [4]
Некоторые (<10%) диагностируются на ускоренной стадии, которая чаще всего проявляется кровотечением, петехиями и экхимозами . [4] У этих пациентов лихорадка чаще всего является результатом оппортунистических инфекций. [4]
У некоторых пациентов первоначально диагноз диагностируется на бластной фазе, симптомами которой, скорее всего, являются лихорадка, боль в костях и увеличение фиброза костного мозга. [4]
Причина [ править ]
В большинстве случаев не удается выделить очевидную причину ХМЛ. [5]
риска Факторы
ХМЛ чаще встречается у мужчин, чем у женщин (соотношение мужчин и женщин 1,4:1) и чаще встречается у пожилых людей со средним возрастом на момент постановки диагноза 65 лет. [5] Воздействие ионизирующей радиации, по-видимому, является фактором риска, исходя из 50-кратного увеличения заболеваемости ХМЛ среди людей, переживших ядерную бомбардировку Хиросимы и Нагасаки. [5] Частота ХМЛ у этих людей достигает пика примерно через 10 лет после заражения. [5]
Патофизиология [ править ]

ХМЛ был первым раком, который был связан с явной генетической аномалией — хромосомной транслокацией , известной как Филадельфийская хромосома . Эта хромосомная аномалия названа так потому, что впервые была обнаружена и описана в 1960 году двумя учеными из Филадельфии, штат Пенсильвания , США: Питером Ноуэллом из Пенсильванского университета и Дэвидом Хангерфордом из онкологического центра Фокса Чейза . [6]
При этой транслокации части двух хромосом (9-й и 22-й) меняются местами. В результате часть гена BCR («область кластера точки разрыва») из хромосомы 22 сливается с геном ABL на хромосоме 9. Этот аномальный «слитый» ген генерирует белок весом p210 или иногда p185 (p210 — сокращение от 210). кДа- белок (сокращение, используемое для характеристики белков исключительно по размеру). Поскольку abl несет домен, который может добавлять фосфатные группы к остаткам тирозина ( тирозинкиназа ), продукт слитого гена bcr-abl также является тирозинкиназой. [7] [8]

Слитый белок BCR-ABL взаимодействует с субъединицей рецептора интерлейкина 3бета(с) . Транскрипт BCR-ABL постоянно активен и не требует активации другими белками клеточной передачи сообщений. В свою очередь, BCR-ABL активирует каскад белков, контролирующих клеточный цикл , ускоряя деление клеток. Более того, белок BCR-ABL ингибирует репарацию ДНК , вызывая геномную нестабильность и делая клетку более восприимчивой к развитию дальнейших генетических аномалий. Действие белка BCR-ABL является патофизиологической причиной хронического миелогенного лейкоза. С улучшением понимания природы белка BCR-ABL и его действия в качестве тирозинкиназы были разработаны таргетные методы лечения (первым из которых был иматиниб ), которые специфически ингибируют активность белка BCR-ABL. Эти ингибиторы тирозинкиназы могут вызывать полную ремиссию ХМЛ, подтверждая центральное значение bcr-abl как причины ХМЛ. [8]
Диагностика [ править ]

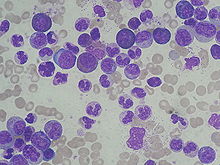

ХМЛ часто подозревают на основании общего анализа крови , который показывает увеличение количества гранулоцитов всех типов, обычно включая зрелые миелоидные клетки . Базофилы и эозинофилы почти всегда повышены; эта особенность может помочь отличить ХМЛ от лейкемоидной реакции . Биопсия костного мозга часто проводится в рамках оценки ХМЛ, а ХМЛ диагностируется с помощью цитогенетики, которая обнаруживает транслокацию t(9;22)(q34;q11.2), которая включает ген ABL1 в хромосоме 9 и ген BCR. в хромосоме 22. [9] В результате этой транслокации хромосома выглядит меньше, чем ее гомологическая хромосома, и это явление известно как хромосомная аномалия Филадельфийской хромосомы . Таким образом, эта аномалия может быть обнаружена с помощью рутинной цитогенетики , а вовлеченные гены BCR-ABL1 могут быть обнаружены с помощью флуоресцентной гибридизации in situ , а также с помощью ПЦР . [10]
Разногласия существуют по поводу так называемого Ph-отрицательного ХМЛ или случаев подозрения на ХМЛ, при которых филадельфийская хромосома не может быть обнаружена. Многие такие пациенты на самом деле имеют сложные хромосомные аномалии, которые маскируют транслокацию (9;22) или имеют доказательства транслокации с помощью FISH или RT-PCR, несмотря на обычное рутинное кариотипирование. [11] Небольшую подгруппу пациентов без обнаруживаемых молекулярных признаков слияния BCR-ABL1 лучше классифицировать как имеющих недифференцированное миелодиспластическое/миелопролиферативное заболевание , поскольку их клиническое течение имеет тенденцию отличаться от пациентов с ХМЛ. [12]
ХМЛ следует отличать от лейкемоидной реакции, которая может иметь аналогичный вид в мазке крови . [10]
Классификация [ править ]
ХМЛ часто делят на три фазы на основании клинических характеристик и лабораторных данных. При отсутствии вмешательства ХМЛ обычно начинается в хронической фазе и в течение нескольких лет переходит в ускоренную фазу и, в конечном итоге, в бластный криз . Бластный криз является терминальной фазой ХМЛ и клинически ведет себя как острый лейкоз . Медикаментозное лечение обычно останавливает это прогрессирование, если оно происходит на ранней стадии. Одним из драйверов перехода от хронической фазы через акселерацию и бластный криз является приобретение новых хромосомных аномалий (помимо филадельфийской хромосомы). [7] К моменту постановки диагноза некоторые пациенты уже могут находиться в ускоренной фазе или бластном кризе. [10]
Хроническая фаза [ править ]
Примерно 85% пациентов с ХМЛ на момент постановки диагноза находятся в хронической фазе. На этом этапе у пациентов обычно нет симптомов или наблюдаются только легкие симптомы усталости, боли в левом боку, боли в суставах и/или бедрах или переполнения живота. Продолжительность хронической фазы варьируется и зависит от того, насколько рано было диагностировано заболевание, а также от используемого лечения. При отсутствии лечения заболевание переходит в ускоренную фазу. [10] Точное определение стадии заболевания на основе клинических маркеров и личного геномного профиля, вероятно, окажется полезным при оценке истории болезни с точки зрения риска прогрессирования. [13]
фаза Ускоренная
Критерии диагностики перехода в ускоренную фазу несколько вариабельны; наиболее широко используемые критерии выдвинуты исследователями Онкологического центра М.Д. Андерсона , [14] by Sokal et al., [15] и Всемирная организация здравоохранения . [12] [16] Критерии ВОЗ [17] возможно, наиболее широко используются и определяют ускоренную фазу по наличию ≥1 из следующих гематологических/цитогенетических критериев или предварительных критериев, касающихся ответа на терапию ингибитором тирозинкиназы (ИТК).
- Гематологические/цитогенетические критерии
- Стойкое или увеличивающееся высокое количество лейкоцитов (> 10 × 10 9 /L), не реагирует на терапию
- Стойкая или нарастающая спленомегалия, не поддающаяся лечению.
- Стойкий тромбоцитоз (> 1000 × 10 9 /L), не реагирует на терапию
- Стойкая тромбоцитопения (< 100 × 10 9 /л), не связанный с терапией
- ≥ 20% базофилов в периферической крови
- 10–19% бластов в периферической крови и/или костном мозге
- Дополнительные клональные хромосомные аномалии в клетках с филадельфийской (Ph) хромосомой (Ph+) на момент постановки диагноза, включая так называемые аномалии основного пути (вторая Ph-хромосома, трисомия 8, изохромосома 17q, трисомия 19), сложный кариотип и аномалии 3q26. 2
- Любая новая клональная хромосомная аномалия в клетках Ph+, возникающая во время терапии.
- Предварительные критерии ответа на ИТК
- Гематологическая резистентность (или неспособность достичь полного гематологического ответа d) к первому ИТК.
- Любые гематологические, цитогенетические или молекулярные признаки устойчивости к двум последовательным ИТК.
- Возникновение двух или более мутаций в слитом гене BCR-ABL1 во время терапии ИТК.
Считается, что пациент находится в ускоренной фазе, если присутствует что-либо из вышеперечисленного. Ускоренная фаза важна, поскольку она сигнализирует о прогрессировании заболевания и неизбежности перехода в бластный кризис. На поздних стадиях медикаментозное лечение часто становится менее эффективным. [12]
Взрывной кризис [ править ]
Бластный криз является заключительной фазой развития ХМЛ и ведет себя как острый лейкоз , с быстрым прогрессированием и короткой выживаемостью. [10] Бластный криз диагностируется, если у пациента с ХМЛ присутствует любой из следующих признаков: [18]
- >20% бластов в крови или костном мозге
- Наличие экстрамедуллярной пролиферации бластов.
Лечение [ править ]
Единственным методом лечения ХМЛ является трансплантация костного мозга или трансплантация аллогенных стволовых клеток. [19] Помимо этого, существует четыре основных направления лечения ХМЛ: лечение ингибиторами тирозинкиназы, миелосупрессивная терапия или лейкаферезная терапия (для противодействия лейкоцитозу на ранних стадиях лечения), спленэктомия и лечение интерфероном альфа-2b . [19] Из-за высокого среднего возраста пациентов с ХМЛ ХМЛ сравнительно редко встречается у беременных женщин, несмотря на это, однако хронический миелогенный лейкоз можно лечить с относительной безопасностью в любое время во время беременности с помощью цитокина интерферона -альфа . [20]
Хроническая фаза [ править ]
В прошлом для лечения ХМЛ в хронической фазе использовались антиметаболиты (например, цитарабин , гидроксимочевина ), алкилирующие агенты , интерферон альфа-2b и стероиды , но с 2000-х годов их заменили ингибиторы тирозинкиназы Bcr-Abl. [21] препараты, специфически нацеленные на BCR-ABL, конститутивно активированный слитый белок тирозинкиназы, вызванный транслокацией филадельфийской хромосомы . Несмотря на переход к замене цитотоксических противоопухолевых препаратов (стандартных противораковых препаратов) ингибиторами тирозинкиназы, иногда гидроксимочевина все еще используется для противодействия высокому количеству лейкоцитов, возникающему во время лечения ингибиторами тирозинкиназы, такими как иматиниб; в этих ситуациях он может быть предпочтительным миелосупрессивным средством из-за его относительного отсутствия лейкемогенного действия и, следовательно, относительного отсутствия возможности возникновения вторичных гематологических злокачественных новообразований в результате лечения. [22] IRIS, международное исследование, в котором сравнивалась комбинация интерферона/цитарабина и первого из этих новых препаратов иматиниба, при долгосрочном наблюдении, продемонстрировало явное превосходство ингибирования тирозинкиназы над существующими методами лечения. [23]
Иматиниб [ править ]
Первым препаратом этого нового класса был мезилат иматиниба (продаваемый как Гливек или Гливек), одобренный Управлением по контролю за продуктами и лекарствами США (FDA) в 2001 году. Было обнаружено, что иматиниб ингибирует прогрессирование ХМЛ у большинства пациентов (65–65–65). 75%) достаточно для достижения возобновления роста нормальной популяции стволовых клеток костного мозга (цитогенетический ответ) со стабильной пропорцией созревающих лейкоцитов. Поскольку некоторые лейкозные клетки (по данным RT-PCR ) персистируют почти у всех пациентов, лечение необходимо продолжать неопределенно долго. С момента появления иматиниба ХМЛ стал первым раком, при котором стандартное лечение может обеспечить пациенту нормальную продолжительность жизни. [24]
Дазатиниб, нилотиниб, радотиниб, аскиминиб и босутиниб
Чтобы преодолеть резистентность к иматинибу и повысить чувствительность к ингибиторам ТК, позже были разработаны четыре новых препарата. Первый, дазатиниб , блокирует несколько других онкогенных белков в дополнение к более мощному ингибированию белка BCR-ABL и был одобрен в 2007 году Управлением по контролю за продуктами и лекарствами США (FDA) для лечения ХМЛ у людей, которые были либо резистентны к или непереносимость иматиниба. Второй ингибитор ТК, нилотиниб , был одобрен FDA по тому же показанию. В 2010 году нилотиниб и дазатиниб были также одобрены в качестве терапии первой линии, что сделало три препарата этого класса доступными для лечения впервые диагностированного ХМЛ. В 2012 году радотиниб присоединился к классу новых средств, ингибирующих белок BCR-ABL, и был одобрен в Южной Корее для людей, резистентных к иматинибу или непереносимых к нему. Босутиниб получил одобрение FDA США и Европейского агентства по лекарственным средствам ЕС 4 сентября 2012 г. и 27 марта 2013 г. соответственно для лечения взрослых с хроническим миелогенным лейкозом (ХМЛ) с филадельфийской хромосомой (Ph+) и резистентностью или непереносимостью предшествующей терапии. [ нужна ссылка ]
Ациминиб (Сцембликс) был одобрен для медицинского применения в США в октябре 2021 года. [25]
к Устойчивый лечению ХМЛ
Хотя дазатиниб и нилотиниб способны вызывать значительно улучшенные ответы по сравнению с действием иматиниба, они не смогли преодолеть лекарственную устойчивость, вызванную одной конкретной мутацией, обнаруженной в структуре BCR-ABL1, известной как мутация T315I (другими словами, где 315-я мутация аминокислота мутирует с остатка треонина на остаток изолейцина ). [ нужна ссылка ] В результате были разработаны два подхода к лечению ХМЛ:
В 2007 году компания Chemgenex опубликовала результаты открытого исследования фазы 2/3 (CGX-635-CML-202), в котором изучалось использование препарата, не нацеленного на BCR-ABL , омацетаксина , вводимого подкожно (под кожу) пациентам с не удалось применить иматиниб, и была обнаружена мутация киназного домена T315I. [26] [27] Это исследование будет продолжаться до 2014 года. [28] В сентябре 2012 года FDA одобрило омацетаксин для лечения ХМЛ в случае резистентности к другим химиотерапевтическим препаратам. [29] [30]
Независимо от этого фармацевтические препараты ARIAD, адаптировав химические структуры ингибиторов ТК первого и второго поколения, пришли к новому ингибитору pan-BCR-ABL1, который показал (впервые) эффективность против T315I, а также всех других известных мутаций онкопротеина. . Препарат понатиниб получил одобрение FDA в декабре 2012 года для лечения пациентов с резистентным или непереносимым ХМЛ. Как и в случае с ингибиторами ТК второго поколения, ведется поиск скорейшего одобрения для распространения использования понатиниба также на впервые диагностированный ХМЛ. [ нужна ссылка ]
Вакцинация [ править ]
обнадеживающие, но неоднозначные результаты вакцинации В 2005 году были получены слитым белком BCR/ABL1 p210 у пациентов со стабильным заболеванием с использованием GM-CSF в качестве адъюванта. [31]
Прогноз [ править ]
До появления ингибиторов тирозинкиназы медиана выживаемости пациентов с ХМЛ составляла около 3–5 лет с момента постановки диагноза. [3]
Благодаря использованию ингибиторов тирозинкиназы показатели выживаемости значительно улучшились. Наблюдение в 2006 году 553 пациентов, принимавших иматиниб (Гливек), показало, что общая выживаемость через пять лет составила 89%. [32]
Наблюдение в 2011 году за 832 пациентами, принимавшими иматиниб и достигшими стабильного цитогенетического ответа, выявило общую выживаемость 95,2% через 8 лет, что аналогично показателю в общей популяции. Менее 1% пациентов умерли из-за прогрессирования лейкемии. [24]
Эпидемиология [ править ]
Соединенное Королевство [ править ]
На ХМЛ приходится 8% всех лейкозов в Великобритании, и в 2011 году это заболевание было диагностировано у 680 человек. [33]
США [ править ]
По оценкам Американского онкологического общества, в 2014 году было диагностировано около 5980 новых случаев хронического миелолейкоза и около 810 человек умерли от этого заболевания. Это означает, что чуть более 10% всех впервые диагностированных случаев лейкоза будут представлять собой хронический миелолейкоз. Средний риск заболевания этим заболеванием у человека составляет 1 из 588. Заболевание чаще встречается у мужчин, чем у женщин, и чаще встречается у белых, чем у афроамериканцев. Средний возраст на момент постановки диагноза составляет 64 года, и это заболевание редко наблюдается у детей. [34]
Ссылки [ править ]
- ^ Вос Т., Аллен С., Арора М., Барбер Р.М., Бхутта З.А., Браун А. и др. (Сотрудники ГББ, 2015 г. по заболеваемости и распространенности заболеваний и травм) (октябрь 2016 г.). «Глобальная, региональная и национальная заболеваемость, распространенность и продолжительность жизни с инвалидностью по 310 заболеваниям и травмам, 1990-2015 гг.: систематический анализ для исследования глобального бремени болезней 2015 г.» . Ланцет . 388 (10053): 1545–1602. дои : 10.1016/S0140-6736(16)31678-6 . ПМК 5055577 . ПМИД 27733282 .
- ^ Ван Х., Нагави М., Аллен С., Барбер Р.М., Бхутта З.А., Картер А. и др. (ГББ, 2015 г. Смертность и причины смерти, сотрудники) (октябрь 2016 г.). «Глобальная, региональная и национальная продолжительность жизни, смертность от всех причин и смертность от конкретных причин по 249 причинам смерти, 1980-2015 гг.: систематический анализ для исследования глобального бремени болезней 2015 г.» . Ланцет . 388 (10053): 1459–1544. дои : 10.1016/s0140-6736(16)31012-1 . ПМК 5388903 . ПМИД 27733281 .
- ↑ Перейти обратно: Перейти обратно: а б Беса Э.К., Бюлер Б., Маркман М., Захер Р.А. (27 декабря 2013 г.). Кришнан К. (ред.). «Хронический миелогенный лейкоз» . Справочник Медскейп . ВебМД . Проверено 3 января 2014 г.
- ↑ Перейти обратно: Перейти обратно: а б с д и Беса Э.К., Бюлер Б., Маркман М., Захер Р.А. (27 декабря 2013 г.). Кришнан К. (ред.). «Клиническая картина хронического миелогенного лейкоза» . Справочник Медскейп . ВебМД . Проверено 3 января 2014 г.
- ↑ Перейти обратно: Перейти обратно: а б с д Прован Д., Гриббен Дж.Г. (2010). «Глава 7 Хронический миелогенный лейкоз» . Молекулярная гематология (3-е изд.). Сингапур: Уайли-Блэквелл. п. 76. ИСБН 9781444318548 .
- ^ Nowell PC (август 2007 г.). «Открытие Филадельфийской хромосомы: личный взгляд» . Журнал клинических исследований . 117 (8): 2033–5. дои : 10.1172/JCI31771 . ЧВК 1934591 . ПМИД 17671636 .
- ↑ Перейти обратно: Перейти обратно: а б Фадерл С., Талпаз М., Эстров З., Кантарджян Х.М. (август 1999 г.). «Хронический миелогенный лейкоз: биология и терапия». Анналы внутренней медицины . 131 (3): 207–19. дои : 10.7326/0003-4819-131-3-199908030-00008 . ПМИД 10428738 . S2CID 46260906 .
- ↑ Перейти обратно: Перейти обратно: а б Хельманн Р., Хоххаус А., Баккарани М. (июль 2007 г.). «Хронический миелолейкоз». Ланцет . 370 (9584): 342–50. дои : 10.1016/S0140-6736(07)61165-9 . ПМИД 17662883 . S2CID 1420863 .
- ^ Роули Джей Ди (июнь 2013 г.). «Генетика. История поменявшихся концов». Наука . 340 (6139): 1412–3. Бибкод : 2013Sci...340.1412R . дои : 10.1126/science.1241318 . ПМИД 23788787 . S2CID 206550237 .
- ↑ Перейти обратно: Перейти обратно: а б с д и Теффери А (2006). «Классификация, диагностика и лечение миелопролиферативных заболеваний в эпоху JAK2V617F» . Гематология. Американское общество гематологии. Образовательная программа . 2006 : 240–5. doi : 10.1182/asheducation-2006.1.240 . ПМИД 17124067 .
- ^ Сэвидж Д.Г., Шидло Р.М., Голдман Дж.М. (январь 1997 г.). «Клинические особенности при постановке диагноза у 430 пациентов с хроническим миелолейкозом, наблюдавшихся в специализированном центре за 16-летний период» . Британский журнал гематологии . 96 (1): 111–6. дои : 10.1046/j.1365-2141.1997.d01-1982.x . ПМИД 9012696 . S2CID 41243342 .
- ↑ Перейти обратно: Перейти обратно: а б с Теффери А., Тиле Дж., Орази А., Квасницка Х.М., Барбуи Т., Хансон К.А. и др. (август 2007 г.). «Предложения и обоснование пересмотра диагностических критериев Всемирной организации здравоохранения для истинной полицитемии, эссенциальной тромбоцитемии и первичного миелофиброза: рекомендации специальной международной экспертной группы» . Кровь . 110 (4): 1092–7. дои : 10.1182/blood-2007-04-083501 . ПМИД 17488875 . S2CID 7086172 .
- ^ Бреме М., Кошмидер С., Монтазери М., Копланд М., Олер В.Г., Радич Дж.П. и др. (апрель 2016 г.). «Комбинированное моделирование демографической динамики и энтропии поддерживает стратификацию пациентов при хроническом миелолейкозе» . Научные отчеты . 6 : 24057. Бибкод : 2016NatSR...624057B . дои : 10.1038/srep24057 . ПМЦ 4822142 . ПМИД 27048866 .
- ^ Кантарджян Х.М., Диксон Д., Китинг М.Дж., Талпаз М., Уолтерс Р.С., МакКреди К.Б., Фрейрих Э.Дж. (апрель 1988 г.). «Особенности ускоренного течения заболевания при хроническом миелогенном лейкозе» . Рак . 61 (7): 1441–6. doi : 10.1002/1097-0142(19880401)61:7<1441::AID-CNCR2820610727>3.0.CO;2-C . ПМИД 3162181 .
- ^ Сокал Дж. Э., Баккарани М., Руссо Д., Тура С. (январь 1988 г.). «Стадирование и прогноз при хроническом миелогенном лейкозе». Семинары по гематологии . 25 (1): 49–61. ПМИД 3279515 .
- ^ Вардиман Дж.В., Харрис Н.Л., Браннинг Р.Д. (октябрь 2002 г.). «Классификация миелоидных новообразований Всемирной организации здравоохранения (ВОЗ)» . Кровь . 100 (7): 2292–302. дои : 10.1182/blood-2002-04-1199 . ПМИД 12239137 . S2CID 9413654 .
- ^ Арбер Д.А., Орази А., Хассерджян Р., Тиле Дж., Боровиц М.Дж., Ле Бо М.М. и др. (май 2016 г.). «Пересмотр классификации миелоидных новообразований и острого лейкоза Всемирной организации здравоохранения 2016 года» . Кровь . 127 (20): 2391–405. дои : 10.1182/blood-2016-03-643544 . ПМИД 27069254 . S2CID 18338178 .
- ^ Карбасян Исфахани М., Моррис Э.Л., Датчер Дж.П., Верник П.Х. (май 2006 г.). «Бластическая фаза хронического миелогенного лейкоза». Современные возможности лечения онкологии . 7 (3): 189–99. дои : 10.1007/s11864-006-0012-y . ПМИД 16615875 . S2CID 21092684 .
- ↑ Перейти обратно: Перейти обратно: а б Беса Э.К., Бюлер Б., Маркман М., Захер Р.А. (27 декабря 2013 г.). Кришнан К. (ред.). «Лечение и лечение хронического миелогенного лейкоза» . Справочник Медскейп . ВебМД . Проверено 4 января 2014 г.
- ^ Шапира Т., Перег Д., Лишнер М. (сентябрь 2008 г.). «Как я лечу острый и хронический лейкоз во время беременности». Обзоры крови . 22 (5): 247–59. дои : 10.1016/j.blre.2008.03.006 . ПМИД 18472198 .
- ^ Куфе Д.В.; Поллак Р.Э.; Вайхзельбаум РР; и др., ред. (2003). «Ингибиторы тирозинкиназы: соображения по таргетированию» . Holland-Frei Cancer Medicine ( книжная полка NCBI ) (6-е изд.). Гамильтон, Онтарио : BC Декер. ISBN 978-1-55009-213-4 . Проверено 27 октября 2012 г.
- ^ Беса Э.К., Бюлер Б., Маркман М., Захер Р.А. (27 декабря 2013 г.). Кришнан К. (ред.). «Хронический миелогенный лейкоз» . Справочник Медскейп . ВебМД . Проверено 3 января 2014 г.
- ^ ДеАнджело DJ, Ritz J (январь 2004 г.). «Терапия иматинибом у пациентов с хроническим миелогенным лейкозом: живут ли пациенты дольше?» (PDF) . Клинические исследования рака . 10 (1 Пт 1): 1–3. дои : 10.1158/1078-0432.CCR-1218-3 . ПМИД 14734443 . S2CID 1761631 .
- ↑ Перейти обратно: Перейти обратно: а б Гамбакорти-Пассерини С., Антолини Л., Махон FX, Гильо Ф., Дейнингер М., Фава С. и др. (апрель 2011 г.). «Многоцентровая независимая оценка результатов лечения пациентов с хроническим миелолейкозом, получавших иматиниб» . Журнал Национального института рака . 103 (7): 553–61. дои : 10.1093/jnci/djr060 . ПМИД 21422402 .
- ^ «FDA одобрило Novartis Schemblix (асциминиб) с новым механизмом действия для лечения хронического миелолейкоза» . Новартис (Пресс-релиз) . Проверено 29 октября 2021 г.
- ^ Джаббур Э., Кортес Дж. Э., Джайлз Ф. Дж., О'Брайен С., Кантарджян Х. М. (июнь 2007 г.). «Текущие и новые варианты лечения хронического миелолейкоза». Рак . 109 (11): 2171–81. CiteSeerX 10.1.1.605.7683 . дои : 10.1002/cncr.22661 . ПМИД 17431887 . S2CID 46509746 .
- ^ Кимура С., Ашихара Э., Маэкава Т. (октябрь 2006 г.). «Новые ингибиторы тирозинкиназы в лечении хронического миелолейкоза». Современная фармацевтическая биотехнология . 7 (5): 371–9. дои : 10.2174/138920106778521532 . ПМИД 17076652 .
- ^ «Гомохаррингтонин (омацетаксин мепесукцинат) при лечении пациентов с хроническим миелолейкозом (ХМЛ) с мутацией гена T315I BCR-ABL» . ClinicalTrial.gov (запись в базе данных) . Проверено 27 октября 2012 г.
- ^ «FDA одобрило препарат Синрибо для лечения хронического миелогенного лейкоза» (пресс-релиз). США Управление по контролю за продуктами и лекарствами . 26 октября 2012 года . Проверено 27 октября 2012 г.
- ^ «FDA одобрило новый орфанный препарат для лечения хронического миелогенного лейкоза» (Пресс-релиз). Управление по контролю за продуктами и лекарствами США. 4 сентября 2012 года . Проверено 27 октября 2012 г.
- ^ Боккиа М., Джентили С., Абруццезе Е., Фанелли А., Юлиано Ф., Табилио А. и др. (2005). «Эффект мультипептидной вакцины p210, связанной с иматинибом или интерфероном, у пациентов с хроническим миелолейкозом и персистирующим остаточным заболеванием: многоцентровое наблюдательное исследование» (PDF) . Ланцет . 365 (9460): 657–62. дои : 10.1016/S0140-6736(05)17945-8 . hdl : 2108/41872 . ПМИД 15721470 . S2CID 26816784 .
- ^ Друкер Б.Дж., Гилхо Ф., О'Брайен С.Г., Гатманн И., Кантарджян Х., Гаттерманн Н. и др. (декабрь 2006 г.). «Пятилетнее наблюдение за пациентами, получавшими иматиниб по поводу хронического миелолейкоза» . Медицинский журнал Новой Англии . 355 (23): 2408–17. doi : 10.1056/NEJMoa062867 . ПМИД 17151364 . S2CID 21772851 .
- ^ «Статистика хронического миелолейкоза (ХМЛ)» . Исследования рака Великобритании . Проверено 28 октября 2014 г.
- ^ «Каковы основные статистические данные о хроническом миелолейкозе?» . сайт рака . Американское онкологическое общество . Архивировано из оригинала 9 февраля 2015 года . Проверено 6 января 2015 г.