Острый промиелоцитарный лейкоз
Эту статью необходимо обновить . ( май 2015 г. ) |
| Острый промиелоцитарный лейкоз | |
|---|---|
 | |
| Мазок костного мозга пациента с острым промиелоцитарным лейкозом, показывающий характерные аномальные промиелоциты . [1] | |
| Специальность | Гематология и онкология |
| Обычное начало | ~40 лет [2] |
| Причины | Неконтролируемая пролиферация промиелоцитов [2] |
| Частота | Развивается примерно у 600–800 человек в год (США) [2] |
Острый промиелоцитарный лейкоз ( ОПМЛ , ОПЛ ) — подтип острого миелолейкоза ОМЛ), рака лейкоцитов ( . [3] При ОПЛ наблюдается аномальное накопление незрелых гранулоцитов, называемых промиелоцитами . Заболевание характеризуется хромосомной транслокацией с участием гена рецептора альфа-ретиноевой кислоты ( RARA ) и отличается от других форм ОМЛ своей чувствительностью к терапии полностью транс -ретиноевой кислотой (ATRA; также известной как третиноин). Острый промиелоцитарный лейкоз впервые был описан в 1957 году. [4] [5] французскими и норвежскими врачами как острое смертельное заболевание, [3] со средним временем выживания менее недели. [6] Сегодня прогнозы резко улучшились; Согласно одному исследованию, 10-летняя выживаемость оценивается примерно в 80-90%. [7] [6] [8]
Признаки и симптомы
[ редактировать ]Симптомы, как правило, аналогичны ОМЛ, при этом возможны следующие симптомы: [9]
- Анемия
- Усталость
- Слабость
- Озноб
- Депрессия
- Затрудненное дыхание ( одышка )
- Низкий уровень тромбоцитов ( тромбоцитопения ), приводящий к легкому кровотечению.
- Высокая температура
- Инфекция в результате низкого уровня нейтрофилов ( нейтропения )
- Повышенные лейкоциты ( лейкоцитоз )
- Коагулопатия (включая диссеминированное внутрисосудистое свертывание крови )
- Бицитопения
Легкое кровотечение из-за низкого уровня тромбоцитов может включать:
- Синяки ( экхимозы )
- Кровоточивость десен
- Носовые кровотечения ( носовое кровотечение )
- Кровотечение из десен
- Усиление менструальных кровотечений ( меноррагия ).
- Кровоизлияние в мозг (внутримозговое кровоизлияние)
Патогенез
[ редактировать ]Острый промиелоцитарный лейкоз характеризуется хромосомной транслокацией, включающей ген рецептора ретиноевой кислоты альфа ( RARA ) на хромосоме 17 . [3] В 95% случаев APL ген RARA на хромосоме 17 участвует во реципрокной транслокации с геном промиелоцитарного лейкоза ( PML ) на хромосоме 15 , транслокация, обозначаемая как t(15;17)(q22;q21). [3] Рецептор RAR зависит от ретиноевой кислоты в регуляции транскрипции. [3]
Восемь других редких перестроек генов были описаны при APL, объединяющем RARA с промиелоцитарным лейкозом «цинковый палец» ( PLZF ). [10] нуклеофосмин , ассоциированный с ядерным матриксом, преобразователь сигнала и активатор транскрипции 5b ( STAT5B ), регуляторная субъединица протеинкиназы A 1α ( PRKAR1A ), фактор, взаимодействующий с PAPOLA и CPSF1 ( FIP1L1 ), корепрессор BCL-6 или олигонуклеотид / олигосахарид -связывающая складка, содержащая 2A ( NABP1 ) гены. Некоторые из этих перегруппировок чувствительны к ATRA или имеют неизвестную чувствительность к ATRA, поскольку они очень редки; Известно, что STAT5B/RARA и PLZF/RARA устойчивы к ATRA. [3]
Слияние PML и RARA приводит к экспрессии гибридного белка с измененными функциями. Этот слитый белок с повышенным сродством связывается с участками клеточной ДНК, блокируя транскрипцию и дифференцировку гранулоцитов. Это происходит за счет усиления взаимодействия молекулы ядерного корепрессора (NCOR) и деацетилазы гистонов (HDAC). Хотя хромосомная транслокация с участием RARA считается инициирующим событием, для развития лейкемии необходимы дополнительные мутации . [3]
RARA/PLZF Слияние генов приводит к возникновению подтипа APL, который не реагирует на терапию третиноином и менее реагирует на стандартную химиотерапию антрациклинами , что приводит к худшим долгосрочным результатам у этой подгруппы пациентов. [3]
Диагностика
[ редактировать ]
Острый промиелоцитарный лейкоз можно отличить от других типов ОМЛ на основании микроскопического исследования мазка крови , аспирата или биопсии костного мозга, а также выявления характерных перестроек. Присутствие промиелоцитов, содержащих множество палочек Ауэра (называемых фагот-клетками ), в мазке периферической крови весьма указывает на острый промиелоцитарный лейкоз. Для окончательного диагноза необходимо тестирование на слитый ген PML/RARA. Это можно сделать с помощью полимеразной цепной реакции (ПЦР), флуоресцентной in situ гибридизации или традиционной цитогенетики периферической крови или костного мозга. Эта мутация включает транслокацию длинных плеч хромосом 15 и 17. В редких случаях может возникнуть скрытая транслокация, которую невозможно обнаружить с помощью цитогенетического тестирования ; в этих случаях для подтверждения диагноза необходимо ПЦР-тестирование. [3]

Уход
[ редактировать ]Первичное лечение
[ редактировать ]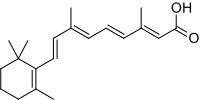
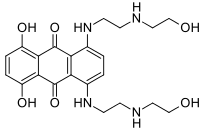
APL уникален среди лейкозов из-за его чувствительности к транс - ретиноевой кислоте (ATRA; третиноин), кислотной форме витамина А. полностью [3] Лечение ATRA диссоциирует комплекс NCOR-HDAC от RAR и позволяет транскрипцию ДНК и дифференцировку незрелых лейкемических промиелоцитов в зрелые гранулоциты путем воздействия на онкогенный фактор транскрипции и его аберрантное действие. [3] В отличие от других химиотерапевтических препаратов, ATRA не убивает непосредственно злокачественные клетки . [3] ATRA индуцирует терминальную дифференцировку лейкозных промиелоцитов, после чего эти дифференцированные злокачественные клетки самостоятельно подвергаются спонтанному апоптозу. ATRA сама по себе способна вызвать ремиссию , но она кратковременна при отсутствии одновременной «традиционной» химиотерапии. [3] С 2013 года стандартом лечения одновременной химиотерапии стал триоксид мышьяка , который в сочетании с ATRA называется ATRA-ATO; [12] [13] до 2013 года стандартом лечения была химиотерапия на основе антрациклинов (например , даунорубицина , доксорубицина , идарубицина или митоксантрона ). Обе химиотерапии приводят к клинической ремиссии примерно у 90% пациентов с триоксидом мышьяка, имеющим более благоприятный профиль побочных эффектов. [7]
Терапия ATRA связана с уникальным побочным эффектом синдрома дифференциации . [14] Это связано с развитием одышки , лихорадки, увеличения массы тела, периферических отеков и лечится дексаметазоном . [15] Этиологию синдрома ретиноевой кислоты связывают с синдромом утечки капилляров из-за высвобождения цитокинов из дифференцирующихся промиелоцитов. [15]
Моноклональное антитело успешно гемтузумаб озогамицин применяется для лечения ОПЛ. [16] хотя он был отозван с рынка США из-за опасений по поводу потенциальной токсичности препарата, и в настоящее время он не продается в Австралии, Канаде или Великобритании. [16] [17] При применении в сочетании с ATRA он дает ответ примерно у 84% пациентов с ОПЛ, что сопоставимо с частотой, наблюдаемой у пациентов, получавших ATRA и терапию на основе антрациклинов. [16] Он вызывает меньшую кардиотоксичность , чем лечение на основе антрациклинов, и, следовательно, может быть предпочтительнее для этих пациентов. [16]
Согласно последним данным, комбинация ATRA и триоксида мышьяка (ATO) в настоящее время во многих случаях предпочтительна для индукционной терапии, предлагая, по крайней мере, столь же эффективные результаты с меньшим количеством побочных эффектов по сравнению с традиционной химиотерапией. [18] В случае рецидива варианты включают повторное лечение АТО или таргетным препаратом гемтузумаб озогамицин (Милотарг). [19]
Поддерживающая терапия
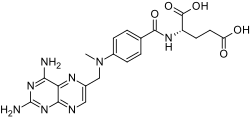
[ редактировать ]После достижения стабильной ремиссии стандартом лечения ранее было проведение 2-летней поддерживающей химиотерапии метотрексатом , меркаптопурином и ATRA. [20] У значительной части пациентов возник рецидив без консолидационной терапии . [15] В европейском исследовании APL 2000 года частота рецидивов в течение двух лет среди тех, кто не получал консолидирующую химиотерапию (без учета ATRA), составляла 27% по сравнению с 11% у тех, кто получал консолидирующую терапию (p<0,01). [21] Аналогичным образом, в исследовании APL в США в 2000 году уровень выживаемости у тех, кто получал поддерживающую терапию ATRA, составил 61% по сравнению с 36% без поддержки ATRA. [22]
Однако недавнее исследование консолидационной терапии после ATRA-ATO, которое стало стандартным лечением в 2013 году, показало, что поддерживающая терапия у пациентов с низким риском после этой терапии может быть ненужной, хотя это и спорно. [13]
Рецидивирующее или рефрактерное заболевание
[ редактировать ]Триоксид мышьяка (As 2 O 3 ) в настоящее время оценивается для лечения рецидивирующих/рефрактерных заболеваний. Сообщалось о ремиссии при применении триоксида мышьяка. [23] Исследования показали, что мышьяк реорганизует ядерные тельца и разрушает мутантный слитый белок PML-RAR. [23] Мышьяк также увеличивает активность каспаз, что затем вызывает апоптоз . [23] Это действительно снижает частоту рецидивов у пациентов с высоким риском. [24] В Японии синтетический ретиноид тамибаротен лицензирован для лечения APL, устойчивого к ATRA. [25]
Следственные агенты
[ редактировать ]Некоторые данные подтверждают потенциальную терапевтическую полезность ингибиторов гистондеацетилазы , таких как вальпроевая кислота или вориностат, при лечении ОПЛ. [26] [27] [28] По данным одного исследования, экстракт корицы влияет на процесс апоптоза в острого миелолейкоза HL-60 . клетках [29]
Прогноз
[ редактировать ]Прогноз обычно хороший по сравнению с другими лейкозами. Из-за остроты начала по сравнению с другими лейкозами ранняя смерть встречается сравнительно чаще. При отсутствии лечения средняя выживаемость составляет менее месяца. Из смертельной болезни она превратилась в излечимую. Причиной ранней смерти чаще всего является сильное кровотечение, чаще внутричерепное кровоизлияние . Ранняя смерть от кровотечения встречается у 5–10% пациентов в странах с адекватным доступом к медицинской помощи и у 20–30% пациентов в менее развитых странах. Факторы риска ранней смерти из-за кровотечения включают позднюю диагностику, позднее начало лечения и высокое количество лейкоцитов при поступлении. [30] Несмотря на успехи в лечении, уровень ранней смертности остается относительно постоянным, как описывают несколько групп, включая Скотта Макклеллана, Бруно Медейроса и Эша Ализаде из Стэнфордского университета . [31]
Частота рецидивов чрезвычайно низка. Большинство смертей после ремиссии происходит по другим причинам, например, от вторичных злокачественных новообразований, которые, по данным одного исследования, произошли у 8% пациентов. В этом исследовании на долю вторичных злокачественных новообразований приходилось 41% смертей, а на болезни сердца — 29%. Выживаемость составила 88% через 6,3 года и 82% через 7,9 года. [32]
В другом исследовании 10-летняя выживаемость оценивалась примерно в 77%. [7]
Эпидемиология
[ редактировать ]Острый промиелоцитарный лейкоз составляет 10–12% случаев ОМЛ. [16] Средний возраст составляет примерно 30–40 лет, [33] который значительно моложе других подтипов ОМЛ (70 лет), однако у пожилых людей ОПЛ имеет свои особенности. [34] Заболеваемость выше среди лиц латиноамериканского или южноевропейского происхождения. [35] Он также может возникать как вторичное злокачественное новообразование у тех, кто получает лечение ингибиторами топоизомеразы II (такими как антрациклины и этопозид ) из-за канцерогенного действия этих агентов, причем пациенты с раком молочной железы . большинство таких пациентов составляют [36] [37] [38] Около 40% пациентов с ОПЛ также имеют хромосомные аномалии , такие как трисомия 8 или изохромосома 17, которые, по-видимому, не влияют на долгосрочные результаты. [3]
Ссылки
[ редактировать ]- ^ Изображение Микаэля Хэггстрема, доктора медицинских наук. Ссылка на выводы: Сайед Заиди, доктор медицинских наук «APL с PML-RARA» . APL с PML-RARA . Последнее обновление автора: 1 февраля 2013 г.
Исходное изображение: Файл: Клетка Faggot в AML-M3.jpg из цифровой библиотеки PEIR (база данных изображений патологии). Архивировано 1 марта 2009 г. в Wayback Machine (общественное достояние). - ^ Jump up to: а б с «Острый промиелоцитарный лейкоз» . Национальная организация редких заболеваний . Проверено 9 марта 2023 г.
- ^ Jump up to: а б с д и ж г час я дж к л м н Котия, SD; Беса, ЕС (3 июня 2013 г.). Саркоди-Аду, К; Талавера, Ф; Захер, РА; Маккенна, Р.; Беса, ЕС (ред.). «Острый промиелоцитарный лейкоз» . Справочник Медскейп . ВебМД . Проверено 14 января 2014 г.
- ^ Таллман М.С., Альтман Дж.К. (2008). «Стратегии лечения острого промиелоцитарного лейкоза» . Программа обучения гематологии Am Soc Hematol . 2008 : 391–9. doi : 10.1182/asheducation-2008.1.391 . ПМИД 19074116 .
- ^ Хиллестад, ЛК (ноябрь 1957 г.). «Острый промиелоцитарный лейкоз». Акта Мед Сканд . 159 (3): 189–94. дои : 10.1111/j.0954-6820.1957.tb00124.x . ПМИД 13508085 .
- ^ Jump up to: а б Кумбс, CC; Тавакколи, М.; Таллман, М.С. (17 апреля 2015 г.). «Острый промиелоцитарный лейкоз: с чего мы начали, где мы находимся сейчас и будущее» . Журнал рака крови . 5 (4): е304. дои : 10.1038/bcj.2015.25 . ПМЦ 4450325 . ПМИД 25885425 .
- ^ Jump up to: а б с Адес, Л; Герчи, А; Раффу, Э; Санс, М; Шевалье, П; Лапусан, С; Речер, К; Томас, X; Район, С; Кастань, С; Турнильяк, О; де Боттон, С; Ифра, Н; Кан Дж.Й.; Солнечная Е; Гарден, К; Фежо, Н.; Бордессуль, Д; Феррант, А; Мейер-Монард, С; Вей, Н; Домбрет, Х; Дегос, Л; Шеврет, С; Фено, П; Европейская группа APL (март 2010 г.). «Очень отдаленные результаты острого промиелоцитарного лейкоза после лечения полностью транс-ретиноевой кислотой и химиотерапии: опыт европейской группы APL» . Кровь . 115 (9): 1690–1696. дои : 10.1182/blood-2009-07-233387 . ПМИД 20018913 . S2CID 18553186 .
- ^ CC, Кумбс (17 апреля 2015 г.). «Острый промиелоцитарный лейкоз: с чего мы начали, где мы находимся сейчас и будущее» . Журнал рака крови . 5 (4): 304. doi : 10.1038/bcj.2015.25 . ПМЦ 4450325 . ПМИД 25885425 .
- ^ Котия, SD; Беса, ЕС (3 июня 2013 г.). Саркоди-Аду, К; Талавера, Ф; Захер, РА; Маккенна, Р.; Беса, ЕС (ред.). «Клиническая картина острого промиелоцитарного лейкоза» . Справочник Медскейп . ВебМД . Проверено 14 января 2014 г.
- ^ Чен З., Брэнд, Нью-Джерси, и др. (март 1993 г.). «Слияние нового круппелеподобного гена цинкового пальца и альфа-локуса рецептора ретиноевой кислоты вследствие варианта транслокации t(11;17), связанного с острым промиелоцитарным лейкозом» . ЭМБО Дж . 12 (3): 1161–7. дои : 10.1002/j.1460-2075.1993.tb05757.x . ПМК 413318 . ПМИД 8384553 .
- ^ Изображение Микаэля Хэггстрема, доктора медицинских наук. Источник выводов: Сайед Заиди, доктор медицинских наук «Неопластика костного мозга, APL с PML-RARA» . Очертания патологии . Последнее обновление автора: 1 февраля 2013 г. Последнее обновление персонала: 29 ноября 2022 г.
- ^ Франческо Ло-Коко, доктор медицины; и др. (июль 2013 г.). «Ретиноевая кислота и триоксид мышьяка при остром промиелоцитарном лейкозе» . Медицинский журнал Новой Англии . 369 (2): 111–121. дои : 10.1056/NEJMoa1300874 . hdl : 11380/980318 . ПМИД 23841729 .
- ^ Jump up to: а б Чингам, Шашанк Р.; Коши, Небу В. (2018), «Рак, лейкемия, промиелоцитарная, острая форма (APL, APML)» , StatPearls , StatPearls Publishing, PMID 29083825 , получено 11 декабря 2018 г. .
Таким образом, появился ATRA-ATO для индукции и консолидации в качестве нового стандарта лечения пациентов с острым промиелоцитарным лейкозом низкого (среднего) риска. Терапия ATRA-ATO также является разумным выбором для пациентов с тяжелыми сопутствующими заболеваниями, пожилых людей, пациентов с сердечной дисфункцией, которые не переносят схемы лечения на основе антрациклинов или общий плохой функциональный статус. Поддерживающая терапия после первоначальной консолидации широко обсуждается. Поддержание может не потребоваться пациентам, получающим интенсивную индукцию/консолидацию, включая АТО.
- ^ Брекча, М; Латальята, Р; Кармозино, я; Каннелла, Л; Диверио, Д; Гуарини, А; Де Пропри, MS; Петти, MC; Аввисати, Г; Чимино, Дж; Манделли, Ф; Ло-Коко, Ф (декабрь 2008 г.). «Клинические и биологические особенности пациентов с острым промиелоцитарным лейкозом, у которых развивается синдром ретиноевой кислоты во время индукционного лечения полностью транс-ретиноевой кислотой и идарубицином» . Гематологическая . 93 (12): 1918–20. дои : 10.3324/гематол.13510 . ПМИД 18945746 .
- ^ Jump up to: а б с Котия, SD; Беса, ЕС (3 июня 2013 г.). Саркоди-Аду, К; Талавера, Ф; Захер, РА; Маккенна, Р.; Беса, ЕС (ред.). «Лечение и лечение острого промиелоцитарного лейкоза» . Справочник Медскейп . ВебМД . Проверено 14 января 2014 г.
- ^ Jump up to: а б с д и Раванди, Ф; Эсти, ЭХ; Аппельбаум, Франция; Ло-Коко, Ф; Шиффер, Калифорния; Ларсон, РА; Бернетт, АК; Кантарджян, HM (ноябрь 2012 г.). «Гемтузумаб озогамицин: время воскреснуть?» . Журнал клинической онкологии . 30 (32): 3921–3923. дои : 10.1200/JCO.2012.43.0132 . ПМЦ 4874205 . ПМИД 22987091 .
- ^ Мартиндейл: Полный справочник лекарств . Фармацевтическая пресса. 23 сентября 2011 г.
- ^ https://www.cancer.org/cancer/types/acute-myeloid-leukemia/treating/m3-leukemia.html
- ^ https://www.fda.gov/news-events/press-announcements/fda-approves-mylotarg-treatment-acute-myeloid-leukemia
- ^ Котия, SD (28 октября 2013 г.). Ананд, Дж; Брейден, CD; Харрис, Дж. Э. (ред.). «Протоколы лечения острого промиелоцитарного лейкоза» . Справочник Медскейп . ВебМД . Проверено 14 января 2014 г.
- ^ Фено, П; Частанг, К; Шеврет, С; Санс, М; Домбрет, Х; Архимбо, Э; Фей, М; Район, С; Юге, Ф; Сотто, Джей-Джей; Гарден, К; Махул, ПК; Траваде, П; Солари, Э; Феге, Н.; Бордессуль, Д; Мигель, Дж.С.; Линк, Х; Десабленс, Б; Стаматуллас, А; Деконинк, Э; Малоизель, Ф; Кастань, С; Преюдомм, К; Дегос, Л. (август 1999 г.). «Рандомизированное сравнение всех трансретиноевых кислот (ATRA) с последующей химиотерапией и ATRA плюс химиотерапия, а также роль поддерживающей терапии при впервые диагностированном остром промиелоцитарном лейкозе». Кровь . 94 (4): 1192–1200. дои : 10.1182/blood.V94.4.1192 . ПМИД 10438706 .
- ^ Таллман, М.С.; Андерсен, Дж.В.; Шиффер, Калифорния; Аппельбаум, Франция; Фойснер, Дж. Х.; Вудс, В.Г.; Огден, А; Вайнштейн, Х; Шепард, Л; Уиллман, К; Блумфилд, CD; Роу, Дж. М.; Верник, PH (декабрь 2002 г.). «Все-трансретиноевая кислота при остром промиелоцитарном лейкозе: долгосрочный результат и анализ прогностических факторов на основе протокола North American Intergroup» . Кровь . 100 (13): 4298–4302. дои : 10.1182/кровь-2002-02-0632 . ПМИД 12393590 .
- ^ Jump up to: а б с Суанье С.Л., Маслак П., Ван З.Г. и др. (ноябрь 1998 г.). «Полная ремиссия после лечения острого промиелоцитарного лейкоза триоксидом мышьяка» . Н. англ. Дж. Мед . 339 (19): 1341–8. дои : 10.1056/NEJM199811053391901 . ПМИД 9801394 .
- ^ «Соединения мышьяка улучшают выживаемость пациентов с острым промиелоцитарным лейкозом» . Онкология . 21 (10). 2007.
- ^ Здания, я; Кагечика, Х. (август 2007 г.). "Тамибаротене" Наркотики сегодня 43 (8): 563–568. дои : 10.1358/точка.2007.43.8.1072615 . ПМИД 17925887 .
- ^ Мартенс, Дж. Х.; Бринкман, AB; Симмер, Ф; Франкойс, К.Дж.; Неббиозо, А; Феррара, Ф; Альтуччи, Л; Стунненберг, Х.Г. (февраль 2010 г.). «PML-RARa/RXR изменяет эпигенетический ландшафт при остром промиелоцитарном лейкозе» . Раковая клетка . 17 (2): 173–185. дои : 10.1016/j.ccr.2009.12.042 . hdl : 2066/84175 . ПМИД 20159609 .
- ^ Лейва, М; Моретти, С; Соилихи, Х; Паллавичини, я; Перес, Л; Меркурио, К; Даль Зуффо, Р; Минуччи, С; де Те, Х. (июль 2012 г.). «Вальпроевая кислота индуцирует дифференцировку и транзиторную регрессию опухоли, но сохраняет активность, инициирующую лейкемию, на мышиных моделях APL» . Лейкемия . 26 (7): 1630–1637. дои : 10.1038/leu.2012.39 . ПМИД 22333881 .
- ^ Он ЛЗ; Толентино Т; Грейсон П; и др. (ноябрь 2001 г.). «Ингибиторы гистондеацетилазы вызывают ремиссию в трансгенных моделях резистентного к терапии острого промиелоцитарного лейкоза» . Журнал клинических исследований . 108 (9): 1321–1330. дои : 10.1172/JCI11537 . ПМК 209432 . ПМИД 11696577 .
- ^ Асадоллахи В., Паривар К., Рудбари Н.Х., Халатбари А.Р., Мотамеди М., Эзатпур Б., Дашти Г.Р. (2013). «Влияние водного экстракта корицы на апоптотический процесс в клетках острого миелолейкоза HL-60» . Adv Biomed Res . 2:25 . дои : 10.4103/2277-9175.108001 . ПМЦ 3748636 . ПМИД 23977653 .
- ^ Брекча, Массимо; Латальята, Роберто; Каннелла, Лаура; Минотти, Клара; Мелони, Джованна; Ло-Коко, Франческо (01 мая 2010 г.). «Ранняя геморрагическая смерть до начала терапии острого промиелоцитарного лейкоза: связь с высоким количеством лейкоцитов, поздней диагностикой и отсроченным началом лечения» . Гематологическая . 95 (5): 853–854. дои : 10.3324/haematol.2009.017962 . ISSN 0390-6078 . ПМЦ 2864399 . ПМИД 20015875 .
- ^ Макклеллан, Джеймс Скотт; Корт, Холбрук Э.; Кутре, Стивен; Готлиб, Джейсон Р.; Маджети, Равиндра; Ализаде, Эш А.; Медейрос, Бруно К. (1 января 2012 г.). «Достижения в области лечения не улучшили уровень ранней смертности при остром промиелоцитарном лейкозе» . Гематологическая . 97 (1): 133–136. дои : 10.3324/haematol.2011.046490 . ISSN 0390-6078 . ПМЦ 3248942 . ПМИД 21993679 .
- ^ Шетти, Адитья Виттал; Раванди, Фархад; Алапати, Нага; Бортакур, Гаутам; Гарсия-Манеро, Гильермо; Кадия, Тапан М.; Виерда, Уильям; Эстров, Зеев; Пирс, Шерри (6 декабря 2014 г.). «Выживаемость при ОПЛ - исходы пациентов с острым промиелоцитарным лейкозом (ОПЛ) (части) после поддержания полной ремиссии (ПР) в течение как минимум 3 лет». Кровь . 124 (21): 954. дои : 10.1182/кровь.V124.21.954.954 . ISSN 0006-4971 .
- ^ Шиффер, Калифорния; Стоун, РМ (2000). «Глава 124: Острый миелолейкоз у взрослых» . В Басте, ЖК; Куфе, Д.В.; Поллок, Р.Э. (ред.). Медицина рака Холланд-Фрай (5-е изд.). Гамильтон, Онтарио: BC Decker . Проверено 15 января 2014 г.
- ^ Розати, Серена; Гурнари, Кармело; Брекча, Массимо; Кармозино, Ида; Скальцулли, Эмилия; Монтефуско, Энрико; Перроне, Сальваторе; Аннибали, Омбретта; Мартини, Винченца; Трапе, Джулио; Колафигли, Джоя (2 ноября 2021 г.). «Острый промиелоцитарный лейкоз (ОПЛ) у очень старых пациентов: протоколы из реальной жизни» . Акта Онкологика . 60 (11): 1520–1526. дои : 10.1080/0284186X.2021.1971291 . hdl : 2108/278430 . ISSN 0284-186X . ПМИД 34461798 . S2CID 238748395 .
- ^ Дауэр, Д; Сантильяна, С; Рамезани, Л; Саманес, К; Словак, МЛ; Ли, MS; Уоткинс, К; Уильямс, Т; Вальехос, К. (август 2003 г.). «Острый промиелоцитарный лейкоз у пациентов, происходящих из Латинской Америки, связан с повышенной частотой подтипа bcr1 слитого гена PML/RARalpha» . Британский журнал гематологии . 122 (4): 563–70. дои : 10.1046/j.1365-2141.2003.04480.x . ПМИД 12899711 . S2CID 20065990 .
- ^ Раванди, Ф (апрель 2011 г.). «Острый промиелоцитарный лейкоз, связанный с терапией» . Гематологическая . 96 (4): 493–495. doi : 10.3324/haematol.2011.041970 . ПМК 3069223 . ПМИД 21454880 .
- ^ Эллиотт, Массачусетс; Летендре, Л; Теффери, А; Хоган, WJ; Крюк, С; Кауфманн, SH; Прути, РК; Парданани, А; Бегна, КХ; Ашрани, А.А.; Воланский, А.П.; Аль-Кали, А; Литцов, MR (март 2012 г.). «Острый промиелоцитарный лейкоз, связанный с терапией: наблюдения, касающиеся патогенеза и терапии ОПЛ». Европейский журнал гематологии . 88 (3): 237–243. дои : 10.1111/j.1600-0609.2011.01727.x . ПМИД 22023492 . S2CID 42345682 .
- ^ Рашиди, А; Фишер, С.И. (2013). «Острый промиелоцитарный лейкоз, связанный с терапией: систематический обзор». Медицинская онкология . 30 (3): 625. doi : 10.1007/s12032-013-0625-5 . ПМИД 23771799 . S2CID 5454988 .
Внешние ссылки
[ редактировать ]- Санс, Мигель А.; Гримуэйд, Дэвид; Таллман, Мартин С.; Ловенберг, Боб; Фено, Пьер; Эсти, Элиху Х.; Наоэ, Томоки; Ленгфельдер, Ева; Бюхнер, Томас; Дёнер, Хартмут; Бернетт, Алан К.; Ло-Коко, Франческо (2009). «Лечение острого промиелоцитарного лейкоза: Рекомендации группы экспертов от имени Европейской сети лейкемии » . Кровь . 113 (9): 1875–1891. doi : 10.1182/blood-2008-04-150250 . hdl : 1765/18239 . ПМИД 18812465 .
- Редакционный совет PDQ по лечению взрослых (2002–2020 гг.). «Лечение острого миелолейкоза у взрослых (PDQ®): версия для пациентов». Лечение острого миелоидного лейкоза у взрослых (PDQ®) . Национальный институт рака (США). ПМИД 26389377 .