Мик
| Протоонкоген MYC, фактор транскрипции bHLH | |||
|---|---|---|---|
| Идентификаторы | |||
| Символ | МИК | ||
| Альт. символы | c-Myc, v-myc | ||
| ген NCBI | 4609 | ||
| HGNC | 7553 | ||
| МОЙ БОГ | 190080 | ||
| RefSeq | НМ_001354870.1 | ||
| ЮниПрот | P01106 | ||
| Другие данные | |||
| Локус | 8 q24.21 | ||
| Викиданные | Q20969939 | ||
| |||
| Протоонкоген MYCL, фактор транскрипции bHLH | |||
|---|---|---|---|
| Идентификаторы | |||
| Символ | МИКЛ | ||
| Альт. символы | LMYC, MYCL1, bHLHe38, L-Myc, v-myc | ||
| ген NCBI | 4610 | ||
| HGNC | 7555 | ||
| МОЙ БОГ | 164850 | ||
| RefSeq | НМ_005376 | ||
| ЮниПрот | P12524 | ||
| Другие данные | |||
| Локус | Хр. 1 п34.2 | ||
| Викиданные | Q18029714 | ||
| |||
| Протоонкоген MYCN, фактор транскрипции bHLH | |||
|---|---|---|---|
| Идентификаторы | |||
| Символ | МИКН | ||
| ген NCBI | 4613 | ||
| HGNC | 7559 | ||
| МОЙ БОГ | 164840 | ||
| RefSeq | НМ_005378 | ||
| ЮниПрот | V | ||
| Другие данные | |||
| Локус | Хр. 2 п24.3 | ||
| Викиданные | Q14906753 | ||
| |||
Myc — это семейство генов-регуляторов и протоонкогенов кодирующих , транскрипции факторы . Семейство Myc состоит из трех родственных человеческих генов: c-myc ( MYC ), l-myc ( MYCL ) и n-myc ( MYCN ). c-myc (также иногда называемый MYC ) был первым геном, обнаруженным в этом семействе из-за гомологии с вирусным геном v-myc .
При раке c - myc часто экспрессируется конститутивно (постоянно). Это приводит к усилению экспрессии многих генов, некоторые из которых участвуют в пролиферации клеток , способствуя образованию рака. [1] Распространенная у человека транслокация с участием c-myc имеет решающее значение для развития большинства случаев лимфомы Беркитта . [2] Конститутивная активация генов Myc также наблюдалась при карциноме шейки матки, толстой кишки, молочной железы, легких и желудка. [1]
Таким образом, Myc рассматривается как многообещающая мишень для противораковых препаратов. [3] К сожалению, Myc обладает несколькими особенностями, которые на сегодняшний день затрудняют лекарственное лечение, например, любые противораковые препараты, направленные на ингибирование Myc, могут продолжать требовать косвенного воздействия на белок, например, путем нацеливания на мРНК белка, а не через небольшой молекула , которая нацелена на сам белок. [4] [5]
c-Myc также играет важную роль в биологии стволовых клеток и был одним из первых факторов Яманаки, используемых для перепрограммирования соматических клеток в индуцированные плюрипотентные стволовые клетки . [6]
В геноме человека и , C-myc расположен на хромосоме 8 как полагают, регулирует экспрессию 15% всех генов. [7] посредством связывания с последовательностями энхансерных боксов ( E-боксы ).
Помимо своей роли классического транскрипционного фактора, N-myc может рекрутировать гистон-ацетилтрансферазы (HAT). Это позволяет ему регулировать глобальную структуру хроматина посредством ацетилирования гистонов. [8]
Открытие
[ редактировать ]Семейство Myc было впервые установлено после открытия гомологии между онкогеном ( , переносимым птичьим вирусом v Myelocytomatosis ) , - myc ; P10395 и человеческим геном, сверхэкспрессируемым при различных видах рака, клеточным Myc ( c-Myc ). . [ нужна ссылка ] Позже открытие других гомологичных генов у человека привело к добавлению n-Myc и l-Myc к семейству генов. [9]
Наиболее часто обсуждаемым примером c-Myc как протоонкогена является его роль в лимфоме Беркитта . При лимфоме Беркитта раковые клетки обнаруживают хромосомные транслокации , чаще всего между хромосомой 8 и хромосомой 14 [t(8;14)]. Это приводит к тому, что c-Myc располагается ниже высокоактивной промоторной области иммуноглобулина (Ig), что приводит к сверхэкспрессии Myc .
Структура
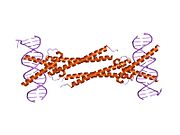
[ редактировать ]Все белковые продукты генов семейства Myc принадлежат к семейству транскрипционных факторов Myc, которые содержат bHLH (базовая спираль-петля-спираль) и LZ ( лейциновая застежка-молния структурные мотивы ). Мотив bHLH позволяет белкам Myc связываться с ДНК , в то время как мотив связывания TF с лейциновой застежкой обеспечивает димеризацию с Max , другим фактором транскрипции bHLH.
Myc МРНК содержит IRES (внутренний сайт входа в рибосому), который позволяет транслировать РНК в белок, когда 5'-кэп -зависимая трансляция ингибируется, например, во время вирусной инфекции.
Функция
[ редактировать ]Белки Myc являются факторами транскрипции , которые активируют экспрессию многих пролиферативных генов посредством связывания последовательностей энхансерных боксов ( E-боксов ) и рекрутирования гистон-ацетилтрансфераз (HAT). Считается, что Myc действует путем усиления элонгации транскрипции активно транскрибируемых генов посредством рекрутирования факторов элонгации транскрипции . [10] Он также может действовать как репрессор транскрипции. Связывая фактор транскрипции Miz-1 и замещая p300 коактиватор , он ингибирует экспрессию генов-мишеней Miz-1. Кроме того, myc играет непосредственную роль в контроле репликации ДНК. [11] Эта активность может способствовать амплификации ДНК в раковых клетках. [12]
Myc активируется различными митогенными сигналами , такими как стимуляция сыворотки или Wnt , Shh и EGF (через путь MAPK/ERK ). [13] Модифицируя экспрессию генов-мишеней, активация Myc приводит к многочисленным биологическим эффектам. Первым, что было обнаружено, была его способность стимулировать пролиферацию клеток (активирует циклины, подавляет р21), но он также играет очень важную роль в регуляции роста клеток (активирует рибосомальные РНК и белки), апоптозе (снижает уровень Bcl-2 ), дифференцировке, и стволовых клеток самообновление . Гены нуклеотидного метаболизма активируются Myc, [14] которые необходимы для Myc-индуцированной пролиферации [15] или рост клеток. [16]
Было проведено несколько исследований, которые ясно указали на роль Myc в клеточной конкуренции. [17]
Основным эффектом c-myc является пролиферация В-клеток , а усиление MYC связано со злокачественными новообразованиями В-клеток и их повышенной агрессивностью, включая гистологическую трансформацию. [18] В В-клетках Myc действует как классический онкоген, регулируя ряд пролиферативных и антиапоптотических путей, это также включает настройку передачи сигналов BCR и передачи сигналов CD40 в регуляции микроРНК (миР-29, миР-150, миР-17 -92). [19]
c-Myc индуцирует экспрессию гена MTDH (AEG-1) и, в свою очередь, сам требует для своей экспрессии онкоген AEG-1.
Myc-ник
[ редактировать ]
Myc-nick представляет собой цитоплазматическую форму Myc, продуцируемую частичным протеолитическим расщеплением полноразмерных c-Myc и N-Myc. [20] Расщепление Myc опосредуется семейством кальпаиновых кальций-зависимых цитозольных протеаз.
Расщепление Myc кальпаинами является конститутивным процессом, но усиливается в условиях, которые требуют быстрого снижения уровней Myc, например, во время терминальной дифференцировки. При расщеплении С-конец Myc (содержащий ДНК-связывающий домен ) разрушается, тогда как Myc-nick, N-концевой сегмент из 298 остатков, остается в цитоплазме . Myc-nick содержит связывающие домены для гистон-ацетилтрансфераз и убиквитинлигаз .
Функции Myc-nick в настоящее время исследуются, но было обнаружено, что этот новый член семейства Myc регулирует морфологию клеток, по крайней мере частично, путем взаимодействия с ацетилтрансферазами, способствуя ацетилированию α-тубулина . Эктопическая экспрессия Myc-nick ускоряет дифференцировку коммитированных миобластов в мышечные клетки.
Клиническое значение
[ редактировать ]Большой объем данных показывает, что гены и белки Myc очень важны для лечения опухолей. [9] За исключением генов раннего ответа, Myc повсеместно усиливает экспрессию генов. Более того, повышение регуляции является нелинейным. Гены, экспрессия которых уже значительно повышена в отсутствие Myc, сильно усиливаются в присутствии Myc, тогда как гены, экспрессия которых низкая в отсутствие Myc, получают лишь небольшое усиление в присутствии Myc. [6]
Инактивация SUMO-активирующего фермента ( SAE1 / SAE2 ) в присутствии гиперактивации Myc приводит к митотической катастрофе и гибели раковых клеток. Следовательно, ингибиторы сумоилирования могут быть возможным средством лечения рака. [21]
Амплификация гена MYC была обнаружена в значительном количестве случаев эпителиального рака яичников . [22] В наборах данных TCGA амплификация Myc происходит при нескольких типах рака, включая рак молочной железы, колоректальный рак, рак поджелудочной железы, желудка и матки. [23]
В экспериментальном процессе трансформации нормальных клеток в раковые ген MYC может сотрудничать с геном RAS. [24] [25]
Экспрессия Myc сильно зависит от функции BRD4 при некоторых видах рака. [26] [27] Ингибиторы BET использовались для успешного блокирования функции Myc на доклинических моделях рака и в настоящее время проходят оценку в клинических испытаниях. [28]
Экспрессия MYC контролируется широким спектром некодирующих РНК, включая микроРНК , днРНК и циркРНК . Было показано, что некоторые из этих РНК специфичны для определенных типов тканей и опухолей человека. [29] Изменения в экспрессии таких РНК потенциально могут быть использованы для разработки таргетной терапии опухолей.
Модели животных
[ редактировать ]У дрозофилы Myc кодируется уменьшительным локусом (который был известен генетикам до 1935 г.). [30] Классические миниатюрные аллели привели к появлению жизнеспособного животного с небольшим размером тела. Впоследствии дрозофилу использовали для вовлечения Myc в клеточную конкуренцию. [31] эндорепликация, [32] и рост клеток. [33]
Во время открытия гена Myc стало понятно, что хромосомы, которые реципрокно транслоцируются в хромосому 8, содержат гены иммуноглобулина в точке разрыва. Чтобы изучить механизм онкогенеза при лимфоме Беркитта путем имитации характера экспрессии Myc в этих раковых клетках, были разработаны модели трансгенных мышей. Ген Myc, помещенный под контроль энхансера тяжелой цепи IgM у трансгенных мышей, вызывает преимущественно лимфомы. Позже, чтобы изучить влияние Myc на другие виды рака, были также созданы трансгенные мыши, которые сверхэкспрессируют Myc в различных тканях (печень, грудь). Во всех этих мышиных моделях сверхэкспрессия Myc вызывает онкогенез, иллюстрируя эффективность онкогена Myc.В исследовании на мышах было показано, что снижение экспрессии Myc приводит к долголетию со значительным увеличением средней и максимальной продолжительности жизни у обоих полов и снижением уровня смертности во всех возрастах, улучшению здоровья, замедлению прогрессирования рака, улучшению метаболизма и меньшим размерам тела. . Кроме того, меньше TOR, AKT, S6K и других изменений в энергетических и метаболических путях (таких как AMPK, большее потребление кислорода, больше движений тела и т. д.). В исследовании Джона М. Седиви и других использовалась Cre-Loxp-рекомбиназа для нокаута одной копии Myc, что привело к появлению «гаплонедостаточного» генотипа, отмеченного как Myc+/-. Наблюдаемые фенотипы противостоят эффектам нормального старения и являются общими со многими другими моделями долгоживущих мышей, такими как CR (ограничение калорий), карлик Эймса, рапамицин, метформин и ресвератрол. Одно исследование показало, что Myc и Гены p53 сыграли ключевую роль в выживании клеток хронического миелолейкоза (ХМЛ). Воздействие лекарств на белки Myc и p53 дало положительные результаты на мышах с ХМЛ. [34] [35]
Связь со стволовыми клетками
[ редактировать ]Гены Myc играют ряд нормальных ролей в стволовых клетках, включая плюрипотентные стволовые клетки. В нервных стволовых клетках N-Myc способствует быстрой пролиферации стволовых клеток и состоянию, подобному предшественнику, в развивающемся мозге, одновременно ингибируя дифференцировку. [36] В гемопоэтических стволовых клетках Myc контролирует баланс между самообновлением и дифференцировкой. [37] В частности, долговременные гемопоэтические стволовые клетки (LT-HSC) экспрессируют низкие уровни c-Myc, обеспечивая самообновление. Усиленная экспрессия c-Myc в LT-HSC способствует дифференцировке за счет самообновления, что приводит к истощению стволовых клеток. [38] При патологических состояниях, особенно при остром миелоидном лейкозе, окислительный стресс может вызывать более высокие уровни экспрессии Myc, что влияет на поведение стволовых клеток лейкемии. [39]
c-Myc играет важную роль в генерации индуцированных плюрипотентных стволовых клеток (ИПСК). Это один из первоначальных факторов, открытых Яманакой и др. стимулировать клетки вернуться в состояние, подобное стеблю, наряду с факторами транскрипции Oct4 , Sox2 и Klf4 . С тех пор было показано, что можно генерировать ИПСК без c-Myc . [40]
Взаимодействия
[ редактировать ]Было показано, что Myc взаимодействует с:
- ACTL6A [41]
- БРЦА1 [42] [43] [44] [45]
- Бкл-2 [46]
- Циклин Т1 [47]
- CHD8 [48]
- ДНМТ3А [49]
- ЭП400 [50]
- GTF2I [51]
- ХТАТИП [52]
- пусть-7 [53] [54] [55]
- МАПК1 [46] [56] [57]
- МАПК8 [58]
- МАКС [59] [60] [61] [62] [63] [64] [65] [66] [67] [68] [69] [70] [71]
- МЛХ1 [63]
- МYCBP2 [72]
- МИКБП [73]
- НМИ [42]
- НФЮБ [74]
- НФИК [75]
- P73 [76]
- ПКАФ [77]
- ПФДН5 [78] [79]
- RuvB-подобный 1 [41] [50]
- SAP130 [77]
- SMAD2 [80]
- SMAD3 [80]
- SMARCA4 [41] [59]
- SMARCB1 [62]
- СУПТ3H [77]
- КОМАНДА1 [81]
- ТАДА2Л [77]
- ТАФ9 [77]
- ТФАП2А [82]
- ЛОВУШКА [41] [60] [61] [77]
- WDR5 [83]
- ГГ1 [84] и
- ЗБТБ17 . [85] [86]
- C2orf16 [87]

См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Перейти обратно: а б «Мик» . НКБИ.
- ^ Финвер С.Н., Нисикура К., Фингер Л.Р., Халуска Ф.Г., Финан Дж., Ноуэлл ПК, Кроче СМ (май 1988 г.). «Анализ последовательности онкогена Myc , участвующего в транслокации хромосомы t(8;14)(q24;q11) в линии Т-клеток лейкемии человека, показывает, что предполагаемые регуляторные области не изменяются» . Труды Национальной академии наук Соединенных Штатов Америки . 85 (9): 3052–6. Бибкод : 1988PNAS...85.3052F . дои : 10.1073/pnas.85.9.3052 . ПМК 280141 . ПМИД 2834731 .
- ^ Бегли С (9 января 2013 г.). «Пионер ДНК Джеймс Уотсон нацелился на онкологические учреждения» . Рейтер.
- ^ Карабет Л.А., Ренни П.С., Черкасов А. (декабрь 2018 г.). «Терапевтическое ингибирование Myc при раке. Структурные основы и компьютерные подходы к открытию лекарств» . Международный журнал молекулярных наук . 20 (1): 120. дои : 10.3390/ijms20010120 . ПМК 6337544 . ПМИД 30597997 .
- ^ Данг К.В., Редди Э.П., Шокат К.М., Соучек Л. (август 2017 г.). «Лекарственное воздействие на «неизлечимые» цели рака» . Обзоры природы. Рак . 17 (8): 502–508. дои : 10.1038/nrc.2017.36 . ПМЦ 5945194 . ПМИД 28643779 .
- ^ Перейти обратно: а б Ни З, Ху Г, Вэй Г, Цуй К, Ямане А, Реш В, Ван Р, Грин Д. Р., Тессаролло Л., Каселлас Р., Чжао К., Левенс Д. (сентябрь 2012 г.). «c-Myc — универсальный усилитель экспрессируемых генов в лимфоцитах и эмбриональных стволовых клетках» . Клетка . 151 (1): 68–79. дои : 10.1016/j.cell.2012.08.033 . ПМЦ 3471363 . ПМИД 23021216 .
- ^ Геархарт Дж., Пашос Э.Э., Прасад М.К. (октябрь 2007 г.). «Редукт плюрипотентности - достижения в исследованиях стволовых клеток». Медицинский журнал Новой Англии . 357 (15): 1469–72. дои : 10.1056/NEJMp078126 . ПМИД 17928593 .
- ^ Коттерман Р., Джин В.Х., Криг С.Р., Лемен Дж.М., Вей А., Фарнхэм П.Дж., Нопфлер П.С. (декабрь 2008 г.). «N-Myc регулирует широко распространенную эухроматическую программу в геноме человека, частично независимо от его роли классического фактора транскрипции» . Исследования рака . 68 (23): 9654–62. doi : 10.1158/0008-5472.CAN-08-1961 . ПМЦ 2637654 . ПМИД 19047142 .
- ^ Перейти обратно: а б Вольф Э., Эйлерс М. (2020). «Нацеливание на белки MYC для терапии опухолей» . Ежегодный обзор биологии рака . 4 : 61–75. doi : 10.1146/annurev-cancerbio-030518-055826 .
- ^ Рал П.Б., Молодой РА (январь 2014 г.). «MYC и элонгация транскрипции» . Перспективы Колд-Спринг-Харбора в медицине . 4 (1): а020990. doi : 10.1101/cshperspect.a020990 . ПМЦ 3869279 . ПМИД 24384817 .
- ^ Домингес-Сола Д., Ин С.И., Грандори С., Руджеро Л., Чен Б., Ли М., Галлоуэй Д.А., Гу В., Готье Дж., Далла-Фавера Р. (июль 2007 г.). «Нетранскрипционный контроль репликации ДНК с помощью c-Myc». Природа . 448 (7152): 445–51. Бибкод : 2007Natur.448..445D . дои : 10.1038/nature05953 . ПМИД 17597761 . S2CID 4422771 .
- ^ Денис Н., Китзис А., Кру Дж., Даутри Ф., Коркос Д. (август 1991 г.). «Стимуляция устойчивости к метотрексату и амплификация гена дигидрофолатредуктазы с помощью c-myc». Онкоген . 6 (8): 1453–7. ПМИД 1886715 .
- ^ Кампизи Дж., Грей Х.Э., Парди А.Б., Дин М., Соненшейн Г.Е. (1984). «Контроль клеточного цикла над экспрессией c-myc, но не c-ras, теряется после химической трансформации». Клетка . 36 (2): 241–7. дои : 10.1016/0092-8674(84)90217-4 . ПМИД 6692471 . S2CID 29661004 .
- ^ Лю Ю.К., Ли Ф., Хэндлер Дж., Хуан Ч.Р., Сян Ю., Неретти Н., Седиви Дж.М., Зеллер К.И., Данг К.В. (июль 2008 г.). «Глобальная регуляция генов биосинтеза нуклеотидов с помощью c-Myc» . ПЛОС ОДИН . 3 (7): e2722. Бибкод : 2008PLoSO...3.2722L . дои : 10.1371/journal.pone.0002722 . ПМК 2444028 . ПМИД 18628958 .
- ^ Маннава С., Гращук В., Уилер Л.Дж., Им М., Чжуан Д., Славина Е.Г., Мэтьюз К.К., Шевах Д.С., Никифоров М.А. (август 2008 г.). «Прямая роль метаболизма нуклеотидов в C-MYC-зависимой пролиферации клеток меланомы» . Клеточный цикл . 7 (15): 2392–400. дои : 10.4161/cc.6390 . ПМЦ 3744895 . ПМИД 18677108 .
- ^ Оги Дж.Н., Грайс С.Дж., Лю Дж.Л. (февраль 2016 г.). «Взаимодействие между Myc и CTP-синтазой у дрозофилы» . ПЛОС Генетика . 12 (2): e1005867. дои : 10.1371/journal.pgen.1005867 . ПМЦ 4759343 . ПМИД 26889675 .
- ^ Клаверия К., Джовинаццо Дж., Сьерра Р., Торрес М. (август 2013 г.). «Конкуренция эндогенных клеток, управляемая Myc, у ранних эмбрионов млекопитающих». Природа . 500 (7460): 39–44. Бибкод : 2013Природа.500...39C . дои : 10.1038/nature12389 . ПМИД 23842495 . S2CID 4414411 .
- ^ де Альборан ИМ, О'Хаган Р.К., Гертнер Ф., Малинн Б., Дэвидсон Л., Рикерт Р., Раевски К., ДеПиньо Р.А., Альт Ф.В. (январь 2001 г.). «Анализ функции C-MYC в нормальных клетках посредством условной мутации, нацеленной на ген» . Иммунитет . 14 (1): 45–55. дои : 10.1016/S1074-7613(01)00088-7 . ПМИД 11163229 .
- ^ Менделл Дж. Т. (апрель 2008 г.). «Роль miRiad для кластера miR-17-92 в развитии и заболевании» . Клетка . 133 (2): 217–22. дои : 10.1016/j.cell.2008.04.001 . ПМЦ 2732113 . ПМИД 18423194 .
- ^ Коначчи-Соррелл М., Нгуэнет С., Эйзенман Р.Н. (август 2010 г.). «Myc-nick: продукт цитоплазматического расщепления Myc, который способствует ацетилированию альфа-тубулина и дифференцировке клеток» . Клетка . 142 (3): 480–93. дои : 10.1016/j.cell.2010.06.037 . ПМЦ 2923036 . ПМИД 20691906 .
- ^ Кесслер Дж.Д., Кале К.Т., Сан Т., Мирбрей К.Л., Шлабах М.Р., Шмитт Э.М., Скиннер С.О., Сюй Кью, Ли М.З., Хартман З.К., Рао М., Ю П., Домингес-Видана Р., Лян А.С., Солимини Н.Л., Бернарди Р.Дж., Ю Б, Сюй Т, Голдинг И, Луо Дж, Осборн С.К., Крейтон С.Дж., Хильзенбек С.Г. , Шифф Р., Шоу К.А., Элледж С.Дж., Вестбрук Т.Ф. (январь 2012 г.). «Для Myc-зависимого онкогенеза необходима транскрипционная подпрограмма, зависимая от SUMOylation» . Наука . 335 (6066): 348–53. Бибкод : 2012Sci...335..348K . дои : 10.1126/science.1212728 . ПМК 4059214 . ПМИД 22157079 .
- ^ Росс Дж.С., Али С.М., Ван К., Палмер Г., Еленский Р., Липсон Д., Миллер В.А., Зайчовски Д., Шоувер Л.К., Стивенс П.Дж. (сентябрь 2013 г.). «Комплексное геномное профилирование эпителиального рака яичников с помощью диагностического анализа нового поколения, основанного на секвенировании, открывает новые пути к таргетной терапии» . Гинекологическая онкология . 130 (3): 554–9. дои : 10.1016/j.ygyno.2013.06.019 . ПМИД 23791828 .
- ^ Чен Ю, МакГи Дж, Чен Х, Доман ТН, Гонг Х, Чжан Ю, Хамм Н, Ма Х, Хиггс Р.Э., Бхагват С.В., Бьюкенен С., Пэн С.Б., Сташке К.А., Ядав В., Юэ Ю, Курос-Мехр Х ( 2014). «Идентификация генов, вызывающих рак, амплифицированных в наборах данных TCGA» . ПЛОС ОДИН . 9 (5): e98293. Бибкод : 2014PLoSO...998293C . дои : 10.1371/journal.pone.0098293 . ПМК 4038530 . ПМИД 24874471 .
- ^ Земля H, Парада LF, Вайнберг РА (1983). «Туморогенная конверсия первичных фибробластов эмбриона требует как минимум двух взаимодействующих онкогенов». Природа . 304 (5927): 596–602. Бибкод : 1983Natur.304..596L . дои : 10.1038/304596a0 . ПМИД 6308472 . S2CID 2338865 .
- ^ Раднер Х., Эль-Шабрави Ю., Эйбл Р.Х., Брюстле О., Кеннер Л., Клейхуэс П., Вистлер О.Д. (1993). «Индукция опухоли онкогенами ras и myc в мозге плода и новорожденного: модулирующее влияние стадии развития и дозы ретровируса». Акта Нейропатологика . 86 (5): 456–65. дои : 10.1007/bf00228580 . ПМИД 8310796 . S2CID 2972931 .
- ^ Фаулер Т., Гатак П., Прайс Д.Х., Конэвей Р., Конэвей Дж., Чианг СМ, Брэднер Дж.Э., Шилатифард А., Рой А.Л. (2014). «Регуляция экспрессии MYC и дифференциальная чувствительность JQ1 в раковых клетках» . ПЛОС ОДИН . 9 (1): e87003. Бибкод : 2014PLoSO...987003F . дои : 10.1371/journal.pone.0087003 . ПМЦ 3900694 . ПМИД 24466310 .
- ^ Ши Дж., Вакоч Ч.Р. (июнь 2014 г.). «Механизмы терапевтической активности ингибирования бромодомена BET» . Молекулярная клетка . 54 (5): 728–36. doi : 10.1016/j.molcel.2014.05.016 . ПМЦ 4236231 . ПМИД 24905006 .
- ^ Делмор Дж.Э., Исса Г.К., Лемье М.Э., Рал П.Б., Ши Дж., Джейкобс Х.М., Кастритис Э., Гилпатрик Т., Паранал Р.М., Ци Дж., Чези М., Шинзель А.С., Маккеун М.Р., Хеффернан Т.П., Вакок Ч.Р., Бергсагель П.Л., Гобриал И.М. , Ричардсон П.Г., Янг Р.А., Хан В.К., Андерсон К.К., Кунг А.Л., Брэднер Дж.Е., Мициадес К.С. (сентябрь 2011 г.). «Ингибирование бромодомена BET как терапевтическая стратегия воздействия на c-Myc» . Клетка . 146 (6): 904–17. дои : 10.1016/j.cell.2011.08.017 . ПМК 3187920 . ПМИД 21889194 .
- ^ Стасевич Е.М., Мурашко М.М., Зиневич Л.С., Демин Д.Е., Шварц А.М. (июль 2021). «Роль некодирующих РНК в регуляции протоонкогена MYC при различных типах рака» . Биомедицины . 9 (8): 921. doi : 10.3390/biomedicines9080921 . ПМЦ 8389562 . ПМИД 34440124 .
- ^ Слизинская Х (май 1938 г.). «Анализ слюнных хромосом белогранной области дрозофилы Melanogaster» . Генетика . 23 (3): 291–9. дои : 10.1093/генетика/23.3.291 . ПМК 1209013 . ПМИД 17246888 .
- ^ де ла Кова С., Абриль М., Беллоста П., Галлант П., Джонстон Л.А. (апрель 2004 г.). «Drosophila myc регулирует размер органов, вызывая конкуренцию клеток» . Клетка . 117 (1): 107–16. дои : 10.1016/S0092-8674(04)00214-4 . ПМИД 15066286 . S2CID 18357397 .
- ^ Мэйнс Дж. З., Стивенс Л. М., Тонг Икс, Стейн Д. (февраль 2004 г.). «Дрозофила dMyc необходима для роста и эндорепликации клеток яичников». Разработка . 131 (4): 775–86. дои : 10.1242/dev.00932 . ПМИД 14724122 . S2CID 721144 .
- ^ Джонстон Л.А., Пробер Д.А., Эдгар Б.А., Эйзенман Р.Н., Галлант П. (сентябрь 1999 г.). «Drosophila myc регулирует рост клеток во время развития» (PDF) . Клетка . 98 (6): 779–90. дои : 10.1016/S0092-8674(00)81512-3 . ПМЦ 10176494 . ПМИД 10499795 . S2CID 5215149 . Архивировано из оригинала (PDF) 3 апреля 2022 г. Проверено 20 марта 2020 г.
- ^ Авраам С.А., Хопкрофт Л.Е., Каррик Э., Дротар М.Е., Данн К., Уильямсон А.Дж. и др. (июнь 2016 г.). «Двойное воздействие на p53 и c-MYC избирательно уничтожает лейкемические стволовые клетки» . Природа . 534 (7607): 341–6. Бибкод : 2016Natur.534..341A . дои : 10.1038/nature18288 . ПМЦ 4913876 . ПМИД 27281222 .
- ^ «Ученые идентифицируют лекарства, воздействующие на «ахиллесову пяту» клеток хронического миелолейкоза» . мояНаука . 08.06.2016. Архивировано из оригинала 27 июля 2018 г. Проверено 9 июня 2016 г.
- ^ Нопфлер П.С., Ченг П.Ф., Эйзенман Р.Н. (октябрь 2002 г.). «N-myc необходим во время нейрогенеза для быстрого расширения популяций клеток-предшественников и ингибирования дифференцировки нейронов» . Гены и развитие . 16 (20): 2699–712. дои : 10.1101/gad.1021202 . ЧВК 187459 . ПМИД 12381668 .
- ^ Уилсон А., Мерфи М.Дж., Оскарссон Т., Калулис К., Беттесс М.Д., Озер Г.М. и др. (ноябрь 2004 г.). «c-Myc контролирует баланс между самообновлением и дифференцировкой гемопоэтических стволовых клеток» . Гены и развитие . 18 (22): 2747–63. дои : 10.1101/gad.313104 . ПМК 528895 . ПМИД 15545632 .
- ^ Уилсон А., Мерфи М.Дж., Оскарссон Т., Калулис К., Беттесс М.Д., Озер Г.М. и др. (ноябрь 2004 г.). «c-Myc контролирует баланс между самообновлением и дифференцировкой гемопоэтических стволовых клеток» . Гены и развитие . 18 (22): 2747–63. дои : 10.1101/gad.313104 . ПМК 528895 . ПМИД 15545632 .
- ^ Влахопулос С., Пан Л., Варисли Л., Данчик Г.М., Карантанос Т., Болдог И. (декабрь 2023 г.). «OGG1 как эпигенетический считыватель влияет на NFκB: что это значит для рака» . Раков (Базель) . 16 (1): 148. doi : 10.3390/cancers16010148 . ПМЦ 10778025 . ПМИД 38201575 .
- ^ Такахаши К., Яманака С. (март 2016 г.). «Десятилетие перепрограммирования к плюрипотентности, опосредованного транскрипционными факторами». Обзоры природы. Молекулярно-клеточная биология . 17 (3): 183–93. дои : 10.1038/номер.2016.8 . ПМИД 26883003 . S2CID 7593915 .
- ^ Перейти обратно: а б с д Парк Дж., Вуд Массачусетс, Коул Доктор медицины (март 2002 г.). «BAF53 образует отдельные ядерные комплексы и действует как критический ядерный кофактор, взаимодействующий с c-Myc, для онкогенной трансформации» . Молекулярная и клеточная биология . 22 (5): 1307–16. дои : 10.1128/mcb.22.5.1307-1316.2002 . ПМЦ 134713 . ПМИД 11839798 .
- ^ Перейти обратно: а б Ли Х, Ли Т.Х., Авраам Х (июнь 2002 г.). «Новый трикомплекс BRCA1, Nmi и c-Myc ингибирует c-Myc-индуцированную активность промотора гена обратной транскриптазы теломеразы человека (hTERT) при раке молочной железы» . Журнал биологической химии . 277 (23): 20965–73. дои : 10.1074/jbc.M112231200 . ПМИД 11916966 .
- ^ Сюн Дж., Фань С., Мэн К., Шрамм Л., Ван С., Бузаза Б., Чжоу Дж., Зафонте Б., Голдберг И.Д., Хаддад Б.Р., Пестель Р.Г., Розен Э.М. (декабрь 2003 г.). «Ингибирование теломеразной активности BRCA1 в культивируемых клетках» . Молекулярная и клеточная биология . 23 (23): 8668–90. дои : 10.1128/mcb.23.23.8668-8690.2003 . ПМК 262673 . ПМИД 14612409 .
- ^ Чжоу С., Лю Дж. (март 2003 г.). «Ингибирование экспрессии гена обратной транскриптазы теломеразы человека с помощью BRCA1 в клетках рака яичников человека». Связь с биохимическими и биофизическими исследованиями . 303 (1): 130–6. дои : 10.1016/s0006-291x(03)00318-8 . ПМИД 12646176 .
- ^ Ван Ц, Чжан Х, Каджино К., Грин М.И. (октябрь 1998 г.). «BRCA1 связывает c-Myc и ингибирует его транскрипционную и трансформирующую активность в клетках». Онкоген . 17 (15): 1939–48. дои : 10.1038/sj.onc.1202403 . ПМИД 9788437 . S2CID 30771256 .
- ^ Перейти обратно: а б Цзинь З, Гао Ф, Флэгг Т, Дэн Икс (сентябрь 2004 г.). «Табак-специфичный нитрозамин 4-(метилнитрозамино)-1-(3-пиридил)-1-бутанон способствует функциональному сотрудничеству Bcl2 и c-Myc посредством фосфорилирования, регулируя выживание и пролиферацию клеток» . Журнал биологической химии . 279 (38): 40209–19. дои : 10.1074/jbc.M404056200 . ПМИД 15210690 .
- ^ Канадзава С., Соучек Л., Эван Г., Окамото Т., Петерлин Б.М. (август 2003 г.). «c-Myc привлекает P-TEFb для транскрипции, клеточной пролиферации и апоптоза». Онкоген . 22 (36): 5707–11. дои : 10.1038/sj.onc.1206800 . ПМИД 12944920 . S2CID 29519364 .
- ^ Дингар Д., Калкат М., Чан П.К., Шрикумар Т., Бэйли С.Д., Ту В.Б., Койо Э., Понциелли Р., Коляр М., Юришика И., Хуанг А., Люпиен М., Пенн Л.З., Раут Б (апрель 2015 г.). «BioID идентифицирует новых партнеров, взаимодействующих с c-MYC, в культивируемых клетках и ксенотрансплантатных опухолях». Журнал протеомики . 118 (12): 95–111. дои : 10.1016/j.jprot.2014.09.029 . ПМИД 25452129 .
- ^ Бреннер С, Деплюс Р, Дидло С, Лорио А, Вире Е, Де Смет С, Гутьеррес А, Данови Д, Бернар Д, Бун Т, Пеличчи П.Г., Амати Б, Кузаридес Т, де Лонуа Ю, Ди Кроче Л, Фукс Ф (январь 2005 г.). «Myc подавляет транскрипцию посредством рекрутирования корепрессора ДНК-метилтрансферазы» . Журнал ЭМБО . 24 (2): 336–46. дои : 10.1038/sj.emboj.7600509 . ПМК 545804 . ПМИД 15616584 .
- ^ Перейти обратно: а б Фукс М., Гербер Дж., Драпкин Р., Сиф С., Икура Т., Огрызко В., Лейн В.С., Накатани Ю., Ливингстон Д.М. (август 2001 г.). «Комплекс p400 является важной мишенью трансформации E1A» . Клетка . 106 (3): 297–307. дои : 10.1016/s0092-8674(01)00450-0 . ПМИД 11509179 . S2CID 15634637 .
- ^ Рой А.Л., Каррутерс К., Гутьяр Т., Редер Р.Г. (сентябрь 1993 г.). «Прямая роль Myc в инициации транскрипции, опосредованная взаимодействием с TFII-I». Природа . 365 (6444): 359–61. Бибкод : 1993Natur.365..359R . дои : 10.1038/365359a0 . ПМИД 8377829 . S2CID 4354157 .
- ^ Франк С.Р., Паризи Т., Тауберт С., Фернандес П., Фукс М., Чан Х.М., Ливингстон Д.М., Амати Б. (июнь 2003 г.). «MYC рекрутирует комплекс гистонацетилтрансферазы TIP60 в хроматин» . Отчеты ЭМБО . 4 (6): 575–80. дои : 10.1038/sj.embor.embor861 . ПМЦ 1319201 . ПМИД 12776177 .
- ^ Чанг Т.С., Ю Д., Ли Ю.С., Вентцель Э.А., Аркинг Д.Э., Вест К.М., Данг К.В., Томас-Тихоненко А., Менделл Дж.Т. (январь 2008 г.). «Широко распространенная репрессия микроРНК с помощью Myc способствует онкогенезу» . Природная генетика . 40 (1): 43–50. дои : 10.1038/ng.2007.30 . ПМЦ 2628762 . ПМИД 18066065 .
- ^ Косцианска Е, Баев В, Скрека К, Ойкономаки К, Русинов В, Таблер М, Калантидис К (2007). «Прогнозирование и предварительная проверка регуляции онкогенов с помощью микроРНК» . BMC Молекулярная биология . 8:79 . дои : 10.1186/1471-2199-8-79 . ПМК 2096627 . ПМИД 17877811 .
- ^ Иоаннидис П., Махайра Л.Г., Перес С.А., Грицапис А.Д., Сотиропулу П.А., Кавалакис Г.Дж., Анцаклис А.И., Баксеванис К.Н., Папамихаил М. (май 2005 г.). «Экспрессия CRD-BP/IMP1 характеризует стволовые клетки CD34+ пуповинной крови и влияет на экспрессию c-myc и IGF-II в раковых клетках MCF-7» . Журнал биологической химии . 280 (20): 20086–93. дои : 10.1074/jbc.M410036200 . ПМИД 15769738 .
- ^ Гупта С., Дэвис Р.Дж. (октябрь 1994 г.). «MAP-киназа связывается с NH2-концевым доменом активации c-Myc» . Письма ФЭБС . 353 (3): 281–5. дои : 10.1016/0014-5793(94)01052-8 . ПМИД 7957875 . S2CID 45404088 .
- ^ Турнье С., Уитмарш А.Дж., Кавана Дж., Барретт Т., Дэвис Р.Дж. (июль 1997 г.). «Митоген-активируемая протеинкиназа-киназа 7 является активатором NH2-концевой киназы c-Jun» . Труды Национальной академии наук Соединенных Штатов Америки . 94 (14): 7337–42. Бибкод : 1997PNAS...94.7337T . дои : 10.1073/pnas.94.14.7337 . ПМК 23822 . ПМИД 9207092 .
- ^ Ногучи К., Китанака С., Ямана Х., Кокубу А., Мотидзуки Т., Кучино Ю. (ноябрь 1999 г.). «Регуляция c-Myc посредством фосфорилирования Ser-62 и Ser-71 N-концевой киназой c-Jun» . Журнал биологической химии . 274 (46): 32580–7. дои : 10.1074/jbc.274.46.32580 . ПМИД 10551811 .
- ^ Перейти обратно: а б Юинг Р.М., Чу П., Элизма Ф., Ли Х., Тейлор П., Клими С., МакБрум-Серажевски Л., Робинсон М.Д., О'Коннор Л., Ли М., Тейлор Р., Дарси М., Хо Ю, Хейлбут А., Мур Л., Чжан С., Орнацкий О, Бухман Ю.В., Этьер М., Шэн Ю., Василеску Дж., Абу-Фарха М., Ламберт Дж.П., Дьюэл Х.С., Стюарт II, Кюль Б., Хог К., Колвилл К., Гладвиш К., Маскат Б., Кинач Р., Адамс С.Л., Моран М.Ф., Морин ГБ, Топалоглу Т., Фигейс Д. (2007). «Крупномасштабное картирование белково-белковых взаимодействий человека методом масс-спектрометрии» . Молекулярная системная биология . 3 : 89. дои : 10.1038/msb4100134 . ПМЦ 1847948 . ПМИД 17353931 .
- ^ Перейти обратно: а б МакМахон С.Б., Вуд Массачусетс, Коул Мэриленд (январь 2000 г.). «Незаменимый кофактор TRRAP рекрутирует гистон-ацетилтрансферазу hGCN5 в c-Myc» . Молекулярная и клеточная биология . 20 (2): 556–62. дои : 10.1128/mcb.20.2.556-562.2000 . ПМК 85131 . ПМИД 10611234 .
- ^ Перейти обратно: а б МакМахон С.Б., Ван Баскирк Х.А., Дуган К.А., Коупленд Т.Д., Коул, доктор медицинских наук (август 1998 г.). «Новый белок TRRAP, родственный ATM, является важным кофактором онкопротеинов c-Myc и E2F» . Клетка . 94 (3): 363–74. дои : 10.1016/s0092-8674(00)81479-8 . ПМИД 9708738 . S2CID 17693834 .
- ^ Перейти обратно: а б Ченг С.В., Дэвис К.П., Юнг Э., Белтран Р.Дж., Ю Дж., Калпана Г.В. (май 1999 г.). «c-MYC взаимодействует с INI1/hSNF5 и требует комплекса SWI/SNF для функции трансактивации». Природная генетика . 22 (1): 102–5. дои : 10.1038/8811 . ПМИД 10319872 . S2CID 12945791 .
- ^ Перейти обратно: а б Мак Партлин М., Гомер Э., Робинсон Х., Маккормик С.Дж., Крауч Д.Х., Дюрант С.Т., Мэтисон Э.К., Холл А.Г., Гиллеспи Д.А., Браун Р. (февраль 2003 г.). «Взаимодействие белков репарации несоответствия ДНК MLH1 и MSH2 с c-MYC и MAX» . Онкоген . 22 (6): 819–25. дои : 10.1038/sj.onc.1206252 . ПМИД 12584560 .
- ^ Блэквуд Э.М., Эйзенман Р.Н. (март 1991 г.). «Макс: белок застежки-молнии спираль-петля-спираль, который образует специфичный для последовательности ДНК-связывающий комплекс с Myc». Наука . 251 (4998): 1211–7. Бибкод : 1991Sci...251.1211B . дои : 10.1126/science.2006410 . ПМИД 2006410 .
- ^ Ли CM, Онисим Д., Reddy CD, Дханасекаран Н., Reddy EP (октябрь 2002 г.). «JLP: каркасный белок, который связывает сигнальные модули JNK/p38MAPK и факторы транскрипции» . Труды Национальной академии наук Соединенных Штатов Америки . 99 (22): 14189–94. Бибкод : 2002PNAS...9914189L . дои : 10.1073/pnas.232310199 . ПМЦ 137859 . ПМИД 12391307 .
- ^ Биллин А.Н., Эйлерс А.Л., Кева С., Айер Д.Э. (декабрь 1999 г.). «Mlx, новый Max-подобный белок BHLHZip, который взаимодействует с сетью транскрипционных факторов Max» . Журнал биологической химии . 274 (51): 36344–50. дои : 10.1074/jbc.274.51.36344 . ПМИД 10593926 .
- ^ Гупта К., Ананд Г., Инь Х, Гроув Л., Проховник Е.В. (март 1998 г.). «Mmip1: новый белок лейциновой молнии, который обращает вспять подавляющее действие членов семьи Mad на c-myc». Онкоген . 16 (9): 1149–59. дои : 10.1038/sj.onc.1201634 . ПМИД 9528857 . S2CID 30576019 .
- ^ Мерони Дж., Реймонд А., Алкалай М., Борсани Г., Танигами А., Тонлоренци Р., Ло Нигро С., Мессали С., Золло М., Ледбеттер Д.Х., Брент Р., Баллабио А., Карроццо Р. (май 1997 г.). «Rox, новый белок bHLHZip, экспрессируемый в покоящихся клетках, который гетеродимеризуется с Max, связывает неканонический E-бокс и действует как репрессор транскрипции» . Журнал ЭМБО . 16 (10): 2892–906. дои : 10.1093/emboj/16.10.2892 . ПМЦ 1169897 . ПМИД 9184233 .
- ^ Наир С.К., Берли С.К. (январь 2003 г.). «Рентгеновские структуры Myc-Max и Mad-Max, узнающих ДНК. Молекулярные основы регуляции протоонкогенными факторами транскрипции» . Клетка . 112 (2): 193–205. дои : 10.1016/s0092-8674(02)01284-9 . ПМИД 12553908 . S2CID 16142388 .
- ^ Фитцджеральд М.Дж., Арсура М., Беллас Р.Э., Ян В., Ву М., Чин Л., Манн К.К., ДеПиньо Р.А., Соненшейн Г.Е. (апрель 1999 г.). «Дифференциальные эффекты широко экспрессируемого сплайс-варианта dMax Max на E-box и регуляцию, опосредованную элементом-инициатором, с помощью c-Myc» . Онкоген . 18 (15): 2489–98. дои : 10.1038/sj.onc.1202611 . ПМИД 10229200 .
- ^ Мерони Дж., Каиро С., Мерла Г., Мессали С., Брент Р., Баллабио А., Реймонд А. (июль 2000 г.). «Mlx, новый Max-подобный член семейства bHLHZip: центральная стадия нового пути регуляции факторов транскрипции?». Онкоген . 19 (29): 3266–77. дои : 10.1038/sj.onc.1203634 . ПМИД 10918583 . S2CID 17891130 .
- ^ Го Ц, Се Дж, Данг К.В., Лю Э.Т., Бишоп Дж.М. (август 1998 г.). «Идентификация большого Myc-связывающего белка, содержащего RCC1-подобные повторы» . Труды Национальной академии наук Соединенных Штатов Америки . 95 (16): 9172–7. Бибкод : 1998PNAS...95.9172G . дои : 10.1073/pnas.95.16.9172 . ПМК 21311 . ПМИД 9689053 .
- ^ Тайра Т., Маэда Дж., Ониши Т., Китаура Х., Ёсида С., Като Х., Икеда М., Тамаи К., Игучи-Арига С.М., Арига Х. (август 1998 г.). «AMY-1, новый белок, связывающий C-MYC, который стимулирует транскрипционную активность C-MYC» . Гены в клетки . 3 (8): 549–65. дои : 10.1046/j.1365-2443.1998.00206.x . ПМИД 9797456 . S2CID 41886122 .
- ^ Идзуми Х., Моландер С., Пенн Л.З., Ишисаки А., Коно К., Фуна К. (апрель 2001 г.). «Механизм репрессии транскрипции c-Myc на бета-рецепторе PDGF». Журнал клеточной науки . 114 (Часть 8): 1533–44. дои : 10.1242/jcs.114.8.1533 . ПМИД 11282029 .
- ^ Тайра Т., Савай М., Икеда М., Тамаи К., Игучи-Арига С.М., Арига Х. (август 1999 г.). «Зависимое от клеточного цикла переключение повышающей и понижающей регуляции экспрессии гена hsp70 человека путем взаимодействия между c-Myc и CBF/NF-Y» . Журнал биологической химии . 274 (34): 24270–9. дои : 10.1074/jbc.274.34.24270 . ПМИД 10446203 .
- ^ Урамото Х., Идзуми Х., Исе Т., Тада М., Учиуми Т., Кувано М., Ясумото К., Фуна К., Коно К. (август 2002 г.). «p73 взаимодействует с c-Myc, регулируя экспрессию Y-бокс-связывающего белка-1» . Журнал биологической химии . 277 (35): 31694–702. дои : 10.1074/jbc.M200266200 . ПМИД 12080043 .
- ^ Перейти обратно: а б с д и ж Лю X, Тесфай Дж., Эврард Ю.А., Дент С.Ю., Мартинес Э. (май 2003 г.). «Домен трансформации c-Myc рекрутирует человеческий комплекс STAGA и требует активности ацетилазы TRRAP и GCN5 для активации транскрипции» . Журнал биологической химии . 278 (22): 20405–12. дои : 10.1074/jbc.M211795200 . ПМК 4031917 . ПМИД 12660246 .
- ^ Мори К., Маэда Ю., Китаура Х., Тайра Т., Игучи-Арига С.М., Арига Х. (ноябрь 1998 г.). «ММ-1, новый белок, ассоциированный с c-Myc, который подавляет транскрипционную активность c-Myc» . Журнал биологической химии . 273 (45): 29794–800. дои : 10.1074/jbc.273.45.29794 . ПМИД 9792694 .
- ^ Фудзиока Ю., Тайра Т., Маэда Ю., Танака С., Нишихара Х., Игучи-Арига С.М., Нагасима К., Арига Х. (ноябрь 2001 г.). «MM-1, c-Myc-связывающий белок, является кандидатом на роль супрессора опухоли при лейкемии/лимфоме и раке языка» . Журнал биологической химии . 276 (48): 45137–44. дои : 10.1074/jbc.M106127200 . ПМИД 11567024 .
- ^ Перейти обратно: а б Фэн XH, Лян YY, Лян М, Чжай В, Линь X (январь 2002 г.). «Прямое взаимодействие c-Myc с Smad2 и Smad3 для ингибирования TGF-бета-опосредованной индукции ингибитора CDK p15 (Ink4B)» . Молекулярная клетка . 9 (1): 133–43. дои : 10.1016/s1097-2765(01)00430-0 . ПМИД 11804592 .
- ^ Оцуки Ю, Танака М, Камо Т, Китанака С, Кучино Ю, Сугимура Х (февраль 2003 г.). «Фактор обмена гуаниновых нуклеотидов, Tiam1, напрямую связывается с c-Myc и препятствует c-Myc-опосредованному апоптозу в фибробластах крысы-1» . Журнал биологической химии . 278 (7): 5132–40. дои : 10.1074/jbc.M206733200 . ПМИД 12446731 .
- ^ Гаубац С., Имхоф А., Дош Р., Вернер О., Митчелл П., Бюттнер Р., Эйлерс М. (апрель 1995 г.). «Активация транскрипции Myc находится под отрицательным контролем транскрипционного фактора AP-2» . Журнал ЭМБО . 14 (7): 1508–19. дои : 10.1002/j.1460-2075.1995.tb07137.x . ПМЦ 398238 . ПМИД 7729426 .
- ^ Томас Л.Р., Ван К., Гриб Б.С., Фан Дж., Фошейдж А.М., Сан К., Олейничак Е.Т., Кларк Т., Дей С., Лори С., Алиси Б., Ховард Г.К., Коутон Б., Эсс К.С., Эйшен К.М., Чжао З., Фесик С.В. , Тэнси В.П. (май 2015 г.). «Взаимодействие с WDR5 способствует распознаванию целевых генов и онкогенезу с помощью MYC» . Молекулярная клетка . 58 (3): 440–52. doi : 10.1016/j.molcel.2015.02.028 . ПМЦ 4427524 . ПМИД 25818646 .
- ^ Шривастава А., Салеке С., Калпана Г.В., Артанди С., Гофф С.П., Каламе К. (декабрь 1993 г.). «Ингибирование регулятора транскрипции Инь-Ян-1 за счет ассоциации с c-Myc». Наука . 262 (5141): 1889–92. Бибкод : 1993Sci...262.1889S . дои : 10.1126/science.8266081 . ПМИД 8266081 .
- ^ Сталлер П., Пойкерт К., Кирмайер А., Сеоан Дж., Лукас Дж., Карсунки Х., Мёрой Т., Бартек Дж., Массаги Дж., Ханель Ф., Эйлерс М. (апрель 2001 г.). «Репрессия экспрессии p15INK4b с помощью Myc посредством ассоциации с Miz-1». Природная клеточная биология . 3 (4): 392–9. дои : 10.1038/35070076 . ПМИД 11283613 . S2CID 12696178 .
- ^ Пойкерт К., Сталлер П., Шнайдер А., Кармайкл Г., Ханель Ф., Эйлерс М. (сентябрь 1997 г.). «Альтернативный путь регуляции генов с помощью Myc» . Журнал ЭМБО . 16 (18): 5672–86. дои : 10.1093/emboj/16.18.5672 . ПМК 1170199 . ПМИД 9312026 .
- ^ «ПСИКИКВИД» . ebi.ac.uk. Проверено 2 мая 2019 г.
Дальнейшее чтение
[ редактировать ]- Руф И.К., Райн П.В., Ян Х., Борза К.М., Хатт-Флетчер Л.М., Кливленд Дж.Л., Сэмпл Дж.Т. (2001). «EBV регулирует c-MYC, апоптоз и туморогенность при лимфоме Беркитта». Вирус Эпштейна-Барра и рак человека . Актуальные темы микробиологии и иммунологии. Том. 258. стр. 153–60. дои : 10.1007/978-3-642-56515-1_10 . ISBN 978-3-642-62568-8 . ПМИД 11443860 .
- Люшер Б. (октябрь 2001 г.). «Функция и регуляция факторов транскрипции сети Myc/Max/Mad». Джин . 277 (1–2): 1–14. дои : 10.1016/S0378-1119(01)00697-7 . ПМИД 11602341 .
- Хоффман Б., Аманулла А., Шафаренко М., Либерман Д.А. (май 2002 г.). «Протоонкоген c-myc в развитии кроветворения и лейкемогенезе». Онкоген . 21 (21): 3414–21. дои : 10.1038/sj.onc.1205400 . ПМИД 12032779 . S2CID 8720539 .
- Пеленгарис С., Хан М., Эван Г. (октябрь 2002 г.). «c-MYC: больше, чем просто вопрос жизни и смерти». Обзоры природы. Рак . 2 (10): 764–76. дои : 10.1038/nrc904 . ПМИД 12360279 . S2CID 13226062 .
- Нильссон Дж. А., Кливленд Дж. Л. (декабрь 2003 г.). «Пути Myc, провоцирующие клеточное самоубийство и рак». Онкоген . 22 (56): 9007–21. дои : 10.1038/sj.onc.1207261 . ПМИД 14663479 . S2CID 24758874 .
- Данг К.В., О'доннелл К.А., Юоппери Т. (сентябрь 2005 г.). «Великий побег MYC в онкогенезе» . Раковая клетка . 8 (3): 177–8. дои : 10.1016/j.ccr.2005.08.005 . ПМИД 16169462 .
- Данг К.В., Ли Ф., Ли Л.А. (ноябрь 2005 г.). «Может ли индукция MYC митохондриального биогенеза быть связана с производством АФК и нестабильностью генома?» . Клеточный цикл . 4 (11): 1465–6. дои : 10.4161/cc.4.11.2121 . ПМИД 16205115 .
- Коллер Х.А., Форман Дж.Дж., Легесс-Миллер А. (август 2007 г.). « Сообщения Myc'ed»: myc индуцирует транскрипцию E2F1, ингибируя его трансляцию через полицистрон микроРНК» . ПЛОС Генетика . 3 (8): е146. дои : 10.1371/journal.pgen.0030146 . ЧВК 1959363 . ПМИД 17784791 .
- Астрин С.М., Лоуренс Дж (май 1992 г.). «Вирус иммунодефицита человека активирует c-myc и вирус Эпштейна-Барра в В-лимфоцитах человека». Анналы Нью-Йоркской академии наук . 651 (1): 422–32. Бибкод : 1992NYASA.651..422A . дои : 10.1111/j.1749-6632.1992.tb24642.x . ПМИД 1318011 . S2CID 31980333 .
- Бернштейн П.Л., Херрик Д.Д., Прокипчак Р.Д., Росс Дж. (апрель 1992 г.). «Контроль периода полураспада мРНК c-myc in vitro с помощью белка, способного связываться с детерминантой стабильности кодирующей области» . Гены и развитие . 6 (4): 642–54. дои : 10.1101/gad.6.4.642 . ПМИД 1559612 .
- Иидзима С., Тераока Х., Дате Т., Цукада К. (июнь 1992 г.). «ДНК-активируемая протеинкиназа в клетках лимфомы Раджи Беркитта. Фосфорилирование онкопротеина c-Myc» . Европейский журнал биохимии . 206 (2): 595–603. дои : 10.1111/j.1432-1033.1992.tb16964.x . ПМИД 1597196 .
- Сет А., Альварес Э., Гупта С., Дэвис Р.Дж. (декабрь 1991 г.). «Сайт фосфорилирования, расположенный в NH2-концевом домене c-Myc, увеличивает трансактивацию экспрессии генов» . Журнал биологической химии . 266 (35): 23521–4. дои : 10.1016/S0021-9258(18)54312-X . ПМИД 1748630 .
- Такахаши Э., Хори Т., О'Коннелл П., Лепперт М., Уайт Р. (1991). «Картирование гена MYC с полосой 8q24.12----q24.13 с помощью R-бэндинга и дистально от fra(8)(q24.11), FRA8E, с помощью флуоресцентной гибридизации in situ». Цитогенетика и клеточная генетика . 57 (2–3): 109–11. дои : 10.1159/000133124 . ПМИД 1914517 .
- Блэквуд Э.М., Эйзенман Р.Н. (март 1991 г.). «Макс: белок застежки-молнии спираль-петля-спираль, который образует специфичный для последовательности ДНК-связывающий комплекс с Myc». Наука . 251 (4998): 1211–7. Бибкод : 1991Sci...251.1211B . дои : 10.1126/science.2006410 . ПМИД 2006410 .
- Газин С., Риголе М., Бриан Ж.П., Ван Регенмортель М.Х., Галиберт Ф. (сентябрь 1986 г.). «Иммунохимическое обнаружение белков, родственных экзону 1 c-myc человека» . Журнал ЭМБО . 5 (9): 2241–50. дои : 10.1002/j.1460-2075.1986.tb04491.x . ПМЦ 1167107 . ПМИД 2430795 .
- Люшер Б., Куэнзель Э.А., Кребс Э.Г., Эйзенман Р.Н. (апрель 1989 г.). «Онкопротеины Myc фосфорилируются казеинкиназой II» . Журнал ЭМБО . 8 (4): 1111–9. дои : 10.1002/j.1460-2075.1989.tb03481.x . ПМК 400922 . ПМИД 2663470 .
- Финвер С.Н., Нисикура К., Фингер Л.Р., Халуска Ф.Г., Финан Дж., Ноуэлл ПК, Кроче СМ (май 1988 г.). «Анализ последовательности онкогена MYC, участвующего в транслокации хромосомы t(8;14)(q24;q11) в линии Т-клеток лейкемии человека, показывает, что предполагаемые регуляторные области не изменяются» . Труды Национальной академии наук Соединенных Штатов Америки . 85 (9): 3052–6. Бибкод : 1988PNAS...85.3052F . дои : 10.1073/pnas.85.9.3052 . ПМК 280141 . ПМИД 2834731 .
- Шоу LC, Мур RC, Эриксон Дж, Кроче CM (май 1987 г.). «Онкоген MYC, участвующий в транслокации хромосомы at(8;22), не изменяется в своих предполагаемых регуляторных областях» . Труды Национальной академии наук Соединенных Штатов Америки . 84 (9): 2824–8. Бибкод : 1987PNAS...84.2824S . дои : 10.1073/pnas.84.9.2824 . ПМК 304752 . ПМИД 3033665 .
- Гийо С., Петриду Б., Сайед-Хусейн С., Галиберт Ф. (декабрь 1988 г.). «Нуклеотидная последовательность 3' онкогена c-myc человека; наличие длинного инвертированного повтора». Джин . 72 (1–2): 105–8. дои : 10.1016/0378-1119(88)90131-X . ПМИД 3243428 .
- Ханн С.Р., Кинг М.В., Бентли Д.Л., Андерсон К.В., Эйзенман Р.Н. (январь 1988 г.). «Инициация трансляции, не связанная с AUG, в экзоне 1 c-myc генерирует отдельный на N-конце белок, синтез которого нарушается при лимфомах Беркитта». Клетка . 52 (2): 185–95. дои : 10.1016/0092-8674(88)90507-7 . ПМИД 3277717 . S2CID 3012009 .
Внешние ссылки
[ редактировать ]- Сигнатуры InterPro для семейства белков: IPR002418 , IPR011598 , IPR003327.
- Myc-белок
- Белок Myc человека NCBI
- Ген рака Myc
- myc + протоонкоген + белки в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)
- Создание iPS-клеток из MEFS посредством принудительной экспрессии Sox-2, Oct-4, c-Myc и Klf4
- Drosophila Myc - Интерактивная муха
- FactorBook C-Myc
- PDBe-KB предоставляет обзор всей информации о структуре, доступной в PDB для протоонкогенного белка Myc человека.