ЭТВ6
| ЭТВ6 | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Псевдонимы | ETV6 , TEL, TEL/ABL, THC5, вариант 6 ETS, вариант транскрипционного фактора 6 ETS | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Внешние идентификаторы | Опустить : 600618 ; МГИ : 109336 ; Гомологен : 37560 ; Генные карты : ETV6 ; ОМА : ETV6 – ортологи | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Викиданные | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
Белок ETV6 (т.е. вируса транслокационного Ets-лейкоза) представляет собой фактор транскрипции , который у человека кодируется геном ( ранее известным как TEL ) ETV6 . Белок ETV6 регулирует развитие и рост различных типов клеток, особенно клеток гематологических тканей. Однако его ген ETV6 часто подвергается различным мутациям, которые приводят к множеству потенциально смертельных видов рака, т.е. ETV6 является клинически значимым протоонкогеном , поскольку он может сливаться с другими генами, вызывая развитие и/или прогрессирование определенных видов рака. Однако ETV6 также является антионкогеном или геном-супрессором опухолей , поскольку его мутации, кодирующие усеченный и, следовательно, неактивный белок, также связаны с определенными типами рака.
Ген
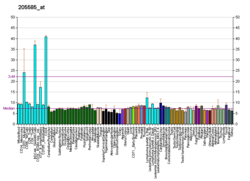
[ редактировать ]человека Ген ETV6 расположен в положении «13.2» на коротком (т.е. «p») плече хромосомы 12, т.е. его обозначенная позиция — 12p13.2. Ген имеет 8 экзонов и два стартовых кодона , один из которых расположен в экзоне 1 в начале гена, а альтернативный расположен выше экзона 3. ETV6 кодирует полноразмерный белок, состоящий из 452 аминокислот; ген экспрессируется практически во всех типах клеток и тканях. [5] [6] Мыши, лишенные гена ETV6 в результате нокаута гена, умирают между 10,5 и 11,5 днями эмбриональной жизни с дефектным желточного мешка ангиогенезом и обширными потерями мезенхимальных и нервных клеток из-за апоптоза . Другие исследования генетических манипуляций на мышах показывают, что этот ген необходим для развития и поддержания костного мозга на основе образования клеток крови и сосудистой сети. [5] [7]
Белок
[ редактировать ]Человеческий белок ETV6 является членом семейства транскрипционных факторов ETS ; однако он чаще ингибирует, чем стимулирует транскрипцию генов-мишеней. Белок ETV6 содержит 3 домена : а) заостренный N-концевой (т.е. PNT) домен, который образует олигомерных партнеров с самим собой, а также с другими факторами транскрипции (например, FLI1 ) и необходим для репрессирующей транскрипции активности ETV6; б) центральный регуляторный домен; и в) С-концевой ДНК-связывающий домен , ETS, который связывается с консенсусной последовательностью ДНК , 5-GGAA/T-3, в пределах последовательности длиной от 9 до 10 п.о. в генах-мишенях, которые он регулирует. [5] [8] ETV6 взаимодействует с другими белками, регулирующими дифференцировку и рост клеток. Он связывается и тем самым ингибирует , другой член транскрипционных факторов ETS , который активно способствует созреванию тромбоцитообразующих мегакариоцитов семейства и блокирует клеточную дифференцировку эритробластов эритроциты в FLI1 ; это приводит к чрезмерной пролиферации и аномальной морфологии эритробластов. [9] [7] ETV6 также связывается с HTATIP , гистон-ацетилтрансферазой , которая регулирует экспрессию различных генов, участвующих в транскрипции генов, репарации ДНК и клеточном апоптозе ; это связывание способствует репрессирующей транскрипцию активности ETV6. [10]
Медицинское значение
[ редактировать ]Наследственные мутации
[ редактировать ]Редкие миссенс-мутации и другие мутации с потерей функции в ETV6 вызывают тромбоцитопению 5, аутосомно-доминантное семейное заболевание, характеризующееся различной тромбоцитопенией ( количество тромбоцитов в крови от 5% до 90% от нормы), склонностью к кровотечениям от легкой до умеренной степени и костного мозга аномальными результатами биопсии эритроцитов . появление мегакариоцитов (т.е. ядер с меньшим количеством долек, чем обычно) и макроцитоз . [7] [11] Тромбоцитопения 5 связана с увеличением частоты развития гематологических (например, хронического миеломоноцитарного лейкоза , острого миелоцитарного лейкоза , острого В-клеточного лимфобластного лейкоза , острого лейкоза смешанного фенотипа, миелодиспластического синдрома и множественной миеломы ) и негематологических (например, кожи и толстой кишки) раковых заболеваний. а также доброкачественные заболевания, такие как рефрактерные анемии, миопатии и гастроэзофагеальная рефлюксная болезнь . [11] [12]
Было обнаружено, что у двух неродственных родственников имеются аутосомно-доминантно наследуемые мутации в гене ETV6 : одна семья с заменой ДНК зародышевой линии, названной L349P, которая приводит к замене лейцина на пролин в аминокислоте 349 в ДНК-связывающем домене ETV6, вторая - N385fs. , в ДНК зародышевой линии вызвало потерю пяти пар оснований ETV6 и укороченного белка ETV6. Оба мутантных белка не смогли нормально проникнуть в ядра клеток и имели пониженную способность воздействовать на гены, регулируемые нормальным белком ETV6. У больных членов этих семей было низкое количество тромбоцитов (т.е. тромбоцитопения) и острый лимфобластный лейкоз . У пятнадцати представителей этих двух родственников была тромбоцитопения, у пятерых из них также был острый лимфобластный лейкоз. У родственников L249P также был один член семьи с почечно-клеточной карциномой и еще один член семьи с раком двенадцатиперстной кишки . Связь этих двух видов рака с мутацией L249P не исследована. В любом случае эти два синдрома семейной тромбоцитопении заметно отличаются от синдрома тромбоцитопении 5. [13]
Уход
[ редактировать ]Члены семьи с тромбоцитопенией 5 нуждаются в регулярном наблюдении с проведением общего анализа крови и мазков крови для выявления ранних изменений, вызванных злокачественной трансформацией этого заболевания в гематологические новообразования. Пациентов, у которых развились эти трансформации, обычно лечили так же, как пациентов с теми же гематологическими новообразованиями, но на несемейной основе. Пациентов, у которых развиваются доброкачественные гематологические или негематологические солидные опухолевые проявления тромбоцитопении 5, также лечат так же, как пациентов с таким же, но несемейным заболеванием. [11] [12]
Острый лимфобластный лейкоз, связанный с мутациями L349P или N385fs в ETV6, оказался гораздо менее чувствительным к стандартной химиотерапии острого лимфобластного лейкоза: 2 из 3 членов семьи довольно быстро перешли от химиотерапии к трансплантации костного мозга , а третий член семьи умер. Это позволяет предположить, что эти мутационно-зависимые формы острого лимфобластного лейкоза требуют агрессивной терапии. [13]
Приобретенные мутации
[ редактировать ]Ген ETV6 склонен к развитию широкого спектра приобретенных мутаций в гематологических клетках-предшественниках, которые приводят к различным типам лейкемии и/или лимфомы . Он также может страдать от меньшего количества мутаций в негематологических тканях, что приводит к солидным опухолям . Эти мутации включают хромосомные транслокации , которые сливают ETV6 на коротком (то есть «p») плече хромосомы 12 («q» означает «длинное плечо») в положении p13.2 (обозначение сайта: 12p12.2) рядом со вторым геном на другом хромосому или, реже, собственную хромосому. В результате создается слитый ген категории онкогенов , который кодирует химерный белок , способствующий злокачественному росту родительских клеток. Может быть неясно, какая часть вновь образованного онкопротеина способствует развитию злокачественного новообразования, но слияние между ETV6 и белками с тирозинкиназной активностью обычно преобразуется из белка с жестко регулируемой тирозинкиназной активностью в неконтролируемую и постоянно активную тирозинкиназу, которая тем самым способствует злокачественная трансформация родительских клеток. [14]
Гематологические злокачественные новообразования
[ редактировать ]В следующей таблице перечислены наиболее часто встречающиеся гены, с которыми сливается ETV6, функция этих генов, хромосомное расположение этих генов, обозначения, обозначающие наиболее распространенные места транслокаций этих слитых генов, а также злокачественные новообразования, возникающие в результате этих транслокаций. Эти транслокационные мутации обычно возникают в плюрипотентных гемопоэтических стволовых клетках , которые дифференцируются в различные типы зрелых гематологических клеток. Следовательно, данная мутация может привести к различным типам гематологических злокачественных новообразований . [5] [14] В таблице приведены сокращения для рецептора тирозинкиназы (рецептор ТК), нерецепторной тирозинкиназы (нерецептора ТК), гомеобоксного белка типа транскрипционного фактора (гомеобоксного белка), острого лимфоцитарного лейкоза (ОЛЛ), хронического миелогенного лейкоза с отрицательной филадельфийской хромосомой ( Ph(-)ХМЛ), миелодиспластический синдром (МДС), миелопролиферативное новообразование (МПН) и острый миелоидный лейкоз (ОМЛ). Наличие мутаций гена ETV6 при миелодиспластических синдромах связано с сокращением выживаемости. [15]
| Ген | функция | расположение | обозначение | злокачественные новообразования | ген | функция | расположение | обозначение | злокачественные новообразования | |
|---|---|---|---|---|---|---|---|---|---|---|
| ПДГФРА | ТК-рецептор | 4q12 | т(4;12)(q27?3;p13) | От 40% до 50% с клональной эозинофилией пациентов | ПДГФРБ | ТК-рецептор | 5q32 | т(5;12)(q31-33;p13) | редкие с клональной эозинофилией пациенты | |
| ФЛТ3 | ТК-рецептор | 13q12.2 | т(12;13)(q13.1;p12.3-13) | редкие с ОМЛ , ОЛЛ и клональной эозинофилией пациенты | АБЛ1 | нерецепторные ТЗ | 9q34.12 | т(9;12)(q34;p13) | редкие с ОМЛ , В-клеточным или Т-клеточным ОЛЛ , Ph(-) ХМЛ пациенты | |
| РУНХ1 | транскрипционный фактор | 21q22.12 | т(12;21)(p13;q22) | 20-25% педиатрических с ОЛЛ пациентов | ПАКС5 | гомеобоксный белок | 9p13.2 | т(9;12)(q11;p13) | 1% педиатрических с ОЛЛ пациентов | |
| МНХ1 | гомеобоксный белок | 7q36.3 | т(7:12)(q36;p13) | 20-30% педиатрических пациентов с ОЛЛ в возрасте до 18 месяцев | со мной | Транскрипционный фактор | 3q26.2 | т(3;12)(д26;р13) | редкие с МДС , МПН и ОМЛ пациенты |
Сообщалось , что помимо транслокаций, продуцирующих слитые гены, представленных в таблице, ETV6 в очень редких случаях (т.е. 1-10 опубликованных отчетов) сливался с другими генами. Эти транслокации приводят к одному или нескольким типам гематологических злокачественных новообразований, перечисленных в таблице. Таким образом, сообщается, что ген ETV6 образует индуцированные транслокацией слитые гены с: [5] а) ген рецептора тирозинкиназы FGFR3 ; б) гены тирозинкиназы ABL2 , NTRK3 , JAK2 , SYK , FRK и LYN ; нерецепторные в) гены транскрипционных факторов MN1 и PER1 ; г) фактор транскрипции белка гомеобокса CDX2 ; д) рецептора белковой тирозинфосфатазы типа R ген PTPRR ; [16] е) транскрипционный коактиватор ядерных рецепторов гормонов ген NCOA2 ; f) ген тяжелой цепи иммуноглобулина IGH; [17] г) гены фермента TTL (добавляют и удаляют остатки тирозина на α-тубулине ), [18] GOT1 ( аспартат-трансаминаза ) и ACSL6 ( лигаза жирных кислот с длинной цепью — КоА ); h) ген-транспортер ARNT (связывается с лиганд -связанным арилуглеводородным рецептором, помогая его перемещению к ядру, где он способствует экспрессии генов, участвующих в метаболизме ксенобиотиков); i) неизвестные функциональные гены CHIC2 , [19] МДС2 , [20] ФЧО2 [21] и БАЗ2А .; [22] и j) неаннотированный ген STL (который не имеет длинной открытой рамки считывания) . [23] ).
По крайней мере 9 мутаций сдвига рамки считывания в гене ETV6 были связаны с ~ 12% случаев острого лимфобластного лейкоза взрослых Т-клеток . Эти мутации включают вставки или делеции гена, которые приводят к тому, что он кодирует усеченный и, следовательно, неактивный белок ETV6. Эти мутации обычно происходят наряду с мутациями в другом онкогене, NOTCH1 , который связан с острой Т-клеточной лимфобластной лимфомой совершенно независимо от ETV6. Предполагается, что супрессорные мутации в гене ETV6 могут быть фактором, способствующим развитию и/или прогрессированию этого типа лейкоза. [8] [24] [25]
Уход
[ редактировать ]Пациенты, у которых развиваются гематологические злокачественные новообразования вследствие слияния гена ETV6 с рецепторными тирозинкиназами и нерецепторными тирозинкиназами, могут быть чувствительны к терапии ингибиторами тирозинкиназ . [26] Например, у пациентов с клональной эозинофилией, вызванной слитыми генами PDGFRA или PDGFRB, наблюдается длительная полная ремиссия при лечении высокочувствительным ингибитором тирозинкиназы гливеком . [14] Ларотректиниб , энтректиниб , мерестиниб и другие ингибиторы тирозинкиназы широкого действия нацелены на ген NTRK3 . Многие из этих препаратов проходят фазу 1 или фазу 2 клинических испытаний для лечения солидных опухолей, связанных с ETV6-NTRK3 , и в конечном итоге могут оказаться полезными для лечения гематологических злокачественных новообразований, связанных с этим слитым геном. [27] Клинические испытания показали, что ингибиторы тирозинкиназы первого поколения сорафениб , сунитиниб , мидостаурин , лестауртиниб показали некоторую перспективность в лечении острого миелогенного лейкоза, связанного со слитым геном FLT3-TKI ; Ингибиторы тирозинкиназы второго поколения кизартиниб и креноланиб, которые высокоселективно ингибируют белок FLT3, показали значительные перспективы в лечении рецидивирующего и рефрактерного острого миелогенного лейкоза, связанного со слитым геном FLT3-TKI . [28] У одного пациента с миелоидным/лимфоидным новообразованием, связанным с ETV6-FLT3, наблюдалась кратковременная ремиссия на сунитинибе, а после рецидива - на сорафенибе, что позволяет предположить, что указанные ингибиторы протеинтирозинкиназы FLT3 могут оказаться полезными для лечения гематологических злокачественных новообразований, связанных с ETV6-FLT . [29] У двух пациентов, страдающих гематологическими злокачественными новообразованиями, связанными со слитыми генами PCM1-JAK2 или BCR-JAK2, наблюдалась полная цитогенетическая ремиссия в ответ на ингибитор тирозинкиназы руксолитиниб ; хотя обе ремиссии были кратковременными (12 месяцев), эти результаты позволяют предположить, что ингибиторы тирозинкиназы, нацеленные на JAK2, могут быть полезны для лечения гематологических злокачественных новообразований, связанных со слитыми стволами ETV6-JAK2 . [14] Ингибитор тирозинкиназы SYK, TAK-659 в настоящее время проходит I фазу клинических испытаний на предмет злокачественных новообразований лимфомы и может оказаться полезным при лечении этого заболевания, если он связан со слитым геном ETV6-SYK . [30] Вполне возможно, что гематологические злокачественные новообразования, связанные со ETV6 слиянием гена с генами тирозинкиназы SYK или FRK, когда-нибудь могут оказаться восприимчивыми к терапии ингибиторами тирозинкиназы. Однако дети с ETV6-RUNX1, ассоциированным с острым лимфобластным лейкозом, относятся к подгруппе особенно высокого риска и, следовательно, практически всегда лечатся по протоколам химиотерапии стандартного риска . [31]
Гематологические злокачественные новообразования, связанные со слиянием гена ETY6 с генами других факторов транскрипции, по-видимому, отражают потерю или усиление функции ETV6 и/или других генов в регуляции экспрессии их генов-мишеней; это приводит к образованию или отсутствию образования продуктов, влияющих на рост, пролиферацию и/или выживаемость клеток. Исследования in vitro слитых генов ETV6-RUNX, ETV6-MN1, ETV6-PER1 и ETV6-MECOM подтверждают это мнение. Таким образом, слитый ген ETV6-MECOM сверхэкспрессируется, поскольку он управляется промотором, полученным из ETV6. [5] тогда как слитые гены ETV6-RUNX, ETV6-MN1 и ETV6-PER1 продуцируют химерные белки, у которых отсутствует геносупрессорная активность белка ETV6. [32] Химерные белковые продукты слияний генов ETV6 с ARNT, TTL, BA22A, FCHO2, MDS2 и CHIC2 также лишены активности транскрипционного фактора белка ETV6. [32] Слияние генов между ETV6 и генами гомеобокса (т.е. CDX2, PAX5 и MNX1) приводит к образованию химерных белков с отсутствием активности транскрипционных факторов ETV6 и/или CDX2, PAX5 или MNX1. [5] Во всех случаях гематологические злокачественные новообразования, связанные с этими слитыми генами, лечились с помощью стандартных протоколов химиотерапии, выбранных на основе фенотипа злокачественных новообразований .
Солидные опухоли
[ редактировать ]Мутации в гене ETV6 также связаны с солидными опухолями . В частности, слитый ген ETV6- NTRK3 встречается и считается или предполагается, что он вызывает определенные типы рака. Эти виды рака включают секреторный рак молочной железы также называемый ювенильным раком молочной железы), аналог секреторной карциномы молочной железы околоушных ( и других слюнных желез , врожденную фибросаркому , врожденную мезобластную нефрому , воспалительную миофибробластическую опухоль и радиационно-индуцированную папиллярную карциному щитовидной железы . [8] [33] [34] [35] [27] [36] [32] [37]
Уход
[ редактировать ]Лечение солидных опухолей, ассоциированных с геном ETV6, не продвинулось так далеко, как лечение ETV6 гематологических злокачественных новообразований, ассоциированных с геном . Предполагается, что ингибиторы тирозинкиназы со специфичностью к тирозинкиназной активности NTRK3 в солидных опухолях, ассоциированных с геном ETV6-NTRK3, могут иметь терапевтическую ценность. Энтектиниб , пан-NTRK, а также ингибитор тирозинкиназы ALK и ROS1, оказался полезным при лечении одного пациента с ETV6-NRTK3 , связанной со слитым геном секреторной карциномой аналога молочной железы , и оказывает поддержку клинической разработке NTRK3-направленной тирозинкиназы ингибиторы для лечения злокачественных новообразований, связанных со слитым белком ETV6-NTRK3. [27] Три клинических исследования находятся на этапе набора персонала для определения эффективности лечения широкого спектра солидных опухолей, связанных с мутированными сверхактивными белками тирозинкиназы, включая белок ETV6-TRK3, с помощью ларотректиниба , неселективного ингибитора NTRK1, NTRK2 и Тирозинкиназы NTRK3. [38]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Перейти обратно: а б с GRCh38: Версия Ensembl 89: ENSG00000139083 – Ensembl , май 2017 г.
- ^ Перейти обратно: а б с GRCm38: выпуск Ensembl 89: ENSMUSG00000030199 – Ensembl , май 2017 г.
- ^ «Ссылка на Human PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ «Ссылка на Mouse PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ Перейти обратно: а б с д и ж г Де Брекелер Э., Дуэ-Гильбер Н., Морель Ф., Ле Брис М.Дж., Басинко А., Де Брекелер М. (август 2012 г.). «Слитые гены ETV6 при гематологических злокачественных новообразованиях: обзор». Исследования лейкемии . 36 (8): 945–61. doi : 10.1016/j.leukres.2012.04.010 . ПМИД 22578774 .
- ^ Интернет-менделевское наследование у человека (OMIM): вариант ETS, ген 6; ЭТВ6 - 600618
- ^ Перейти обратно: а б с Сонгдей Н., Рао АК (май 2017 г.). «Мутации гематопоэтических транскрипционных факторов: важные игроки в наследственных дефектах тромбоцитов» . Кровь . 129 (21): 2873–2881. дои : 10.1182/blood-2016-11-709881 . ПМЦ 5445569 . ПМИД 28416505 .
- ^ Перейти обратно: а б с Сайзмор ГМ, Питарреси-младший, Балакришнан С., Островски М.К. (июнь 2017 г.). «Семейство онкогенных транскрипционных факторов ETS в солидных опухолях». Обзоры природы. Рак . 17 (6): 337–351. дои : 10.1038/nrc.2017.20 . ПМИД 28450705 . S2CID 32483397 .
- ^ Квятковский Б.А., Бастиан Л.С., Бауэр Т.Р., Цай С., Зелинска-Квятковска А.Г., Хикштейн Д.Д. (июль 1998 г.). «Член семейства ets Tel связывается с онкобелком Fli-1 и ингибирует его транскрипционную активность» . Журнал биологической химии . 273 (28): 17525–30. дои : 10.1074/jbc.273.28.17525 . ПМИД 9651344 .
- ^ Нордентофт I, Йоргенсен П. (август 2003 г.). «Транс-действующий регуляторный белок ацетилтрансферазы массой 60 кДа белка, взаимодействующего с ВИЧ типа 1 (Tip60), взаимодействует с транслокационным геном лейкемии, трансформирующим специфическую транслокацию E26 (TEL), и действует как ко-репрессор транскрипции» . Биохимический журнал . 374 (Часть 1): 165–73. дои : 10.1042/BJ20030087 . ПМЦ 1223570 . ПМИД 12737628 .
- ^ Перейти обратно: а б с Bannon SA, компакт-диск DiNardo (май 2016 г.). «Наследственная предрасположенность к миелодиспластическому синдрому» . Международный журнал молекулярных наук . 17 (6): 838. doi : 10.3390/ijms17060838 . ПМЦ 4926372 . ПМИД 27248996 .
- ^ Перейти обратно: а б Чжан М.Ю., Чурпек Дж.Э., Кил С.Б., Уолш Т., Ли М.К., Леб КР., Гульсунер С., Притчард С.С., Санчес-Бонилья М., Делроу Дж.Дж., Басом Р.С., Форухар М., Гюркоча Б., Шварц Б.С., Нейштадт Б., Маркес Р., Мариани С.Дж., Коутс С.А., Хофманн И., Линдсли Р.К., Уильямс Д.А., Абковиц Дж.Л., Хорвиц М.С., Кинг МС, Годли Л.А., Шимамура А. (февраль 2015 г.). «Зародышевые мутации ETV6 при семейной тромбоцитопении и гематологических злокачественных новообразованиях» . Природная генетика . 47 (2): 180–5. дои : 10.1038/ng.3177 . ПМЦ 4540357 . ПМИД 25581430 .
- ^ Перейти обратно: а б Топка С, Виджай Дж, Уолш МФ, Джейкобс Л, Мария А, Виллано Д, Гаддам П, Ву Дж, МакГи РБ, Куинн Э, Инаба Х, Хартфорд С, Пуй Ч., Паппо А, Эдмонсон М, Чжан М.Ю., Степенский П. , Штайнгерц П., Шредер К., Линкольн А., Бассел Дж., Липкин С.М., Голдгур Ю., Харит М., Стадлер З.К., Маллиган С., Вайнтрауб М., Шимамура А., Чжан Дж., Даунинг Дж.Р., Николс К.Э., Оффит К. (июнь 2015 г.). «Мутации зародышевой линии ETV6 повышают восприимчивость к острому лимфобластному лейкозу и тромбоцитопении» . ПЛОС Генетика . 11 (6): e1005262. дои : 10.1371/journal.pgen.1005262 . ПМЦ 4477877 . ПМИД 26102509 .
- ^ Перейти обратно: а б с д Рейтер А., Готлиб Дж. (февраль 2017 г.). «Миелоидные новообразования с эозинофилией» . Кровь . 129 (6): 704–714. дои : 10.1182/blood-2016-10-695973 . ПМИД 28028030 .
- ^ Гангат Н., Патнаик М.М., Теффери А. (январь 2016 г.). «Миелодиспластические синдромы: современный обзор и как мы лечим» . Американский журнал гематологии . 91 (1): 76–89. дои : 10.1002/ajh.24253 . ПМИД 26769228 .
- ^ «Протеин PTPRR тирозинфосфатаза, рецептор типа R (человек0» . Entrez Gene) .
- ^ «Тяжелый локус иммуноглобулина IGH (человека)» . Энтрез Джин .
- ^ «ТТЛ тубулин-тирозинлигаза (человеческая)» . Энтрез Джин .
- ^ «CHIC2 богатый цистеином гидрофобный домен 2 (человек)» . Энтрез Джин .
- ^ «Связанный с транслокацией миелодиспластический синдром MDS2 2» . Энтрез Джин .
- ^ «FCHO2 FCH домен только 2» . Энтрез Джин .
- ^ «Бромодомен BAZ2A, соседний с доменом 2А цинкового пальца» . Энтрез Джин .
- ^ Суто Ю., Сато Ю., Смит С.Д., Роули Дж.Д., Боландер С.К. (апрель 1997 г.). «t(6;12)(q23;p13) приводит к слиянию ETV6 с новым геном STL в линии В-клеточных ALL». Гены, хромосомы и рак . 18 (4): 254–68. doi : 10.1002/(sici)1098-2264(199704)18:4<254::aid-gcc3>3.0.co;2-# . ПМИД 9087565 . S2CID 196600869 .
- ^ Ван Влиерберге П., Амбези-Импиомбато А., Перес-Гарсия А., Хайду Дж.Э., Риго И., Хадлер М., Тоселло В., Делла Гатта Дж., Пайетта Е., Рачевскис Дж., Верник П.Х., Люгер С.М., Роу Дж.М., Рю М., Феррандо А.А. (декабрь 2011 г.). «Мутации ETV6 при ранних незрелых Т-клеточных лейкозах человека» . Журнал экспериментальной медицины . 208 (13): 2571–9. дои : 10.1084/jem.20112239 . ПМК 3244026 . ПМИД 22162831 .
- ^ Санчес-Мартин М., Феррандо А. (март 2017 г.). «Шоссе NOTCH1-MYC к острому Т-клеточному лимфобластному лейкозу» . Кровь . 129 (9): 1124–1133. дои : 10.1182/blood-2016-09-692582 . ПМИД 28115368 .
- ^ Готлиб Дж. (декабрь 2015 г.). «Ингибиторы тирозинкиназы и терапевтические антитела при прогрессирующих эозинофильных заболеваниях и системном мастоцитозе». Текущие отчеты о гематологических злокачественных новообразованиях . 10 (4): 351–61. дои : 10.1007/s11899-015-0280-3 . ПМИД 26404639 . S2CID 36630735 .
- ^ Перейти обратно: а б с Хоцкая Ю.Б., Холла В.Р., Фараго А.Ф., Миллс Шоу К.Р., Мерик-Бернстам Ф., Хонг Д.С. (май 2017 г.). «Нацеливание на белки семейства TRK при раке». Фармакология и терапия . 173 : 58–66. doi : 10.1016/j.pharmthera.2017.02.006 . ПМИД 28174090 . S2CID 4243668 .
- ^ Цапогас П., Муни С.Дж., Браун Дж., Ролинк А. (май 2017 г.). «Цитокин Flt3-лиганд в нормальном и злокачественном кроветворении» . Международный журнал молекулярных наук . 18 (6): 1115. doi : 10.3390/ijms18061115 . ПМЦ 5485939 . ПМИД 28538663 .
- ^ Вальц С, Эрбен П, Риттер М, Блур А, Мецгерот Г, Телфорд Н, Хаферлах С, Хаферлах Т, Геск С, Скор Дж, Хофманн ВК, Хоххаус А, Кросс NC, Райтер А (август 2011 г.). «Ответ ETV6-FLT3-положительного миелоидного / лимфоидного новообразования с эозинофилией на ингибиторы FMS-подобной тирозинкиназы 3» . Кровь . 118 (8): 2239–42. дои : 10.1182/blood-2011-03-343426 . ПМИД 21705501 .
- ^ Лам Б., Арикава И., Крамлетт Дж., Донг К., де Йонг Р., Фехер В., Гримшоу С.Э., Фаррелл П.Дж., Хоффман И.Д., Дженнингс А., Джонс Б., Матушкевич Дж., Миура Дж., Мияке Х., Натала С.Р., Ши Л., Такахаши М., Тейлор Э., Уайрик С., Яно Дж., Залевский Дж., Ни З. (декабрь 2016 г.). «Открытие TAK-659, доступного для перорального применения исследовательского ингибитора тирозинкиназы селезенки (SYK)» . Письма по биоорганической и медицинской химии . 26 (24): 5947–5950. дои : 10.1016/j.bmcl.2016.10.087 . ПМИД 27839918 .
- ^ Харрисон Си Джей (2013). «Нацеливание на сигнальные пути при остром лимфобластном лейкозе: новые идеи» (PDF) . Гематология. Американское общество гематологии. Образовательная программа . 2013 : 118–25. doi : 10.1182/asheducation-2013.1.118 . ПМИД 24319172 . S2CID 24762855 .
- ^ Перейти обратно: а б с Кар А., Гутьеррес-Хартманн А. (2013). «Молекулярные механизмы онкогенеза, опосредованного транскрипционным фактором ETS» . Критические обзоры по биохимии и молекулярной биологии . 48 (6): 522–43. дои : 10.3109/10409238.2013.838202 . ПМК 4086824 . ПМИД 24066765 .
- ^ Тоньон С., Кнезевич С.Р., Хантсман Д., Роскелли С.Д., Мельник Н., Мазерс Дж.А., Беккер Л., Карнейро Ф., Макферсон Н., Хорсман Д., Поремба С., Соренсен П.Х. (ноябрь 2002 г.). «Экспрессия слияния генов ETV6-NTRK3 как первичное событие секреторной карциномы молочной железы человека» . Раковая клетка . 2 (5): 367–76. дои : 10.1016/S1535-6108(02)00180-0 . ПМИД 12450792 .
- ^ Маевска Х., Скалова А., Стодульский Д., Климкова А., Штайнер П., Станкевич С., Бирнат В. «Аналог секреторной карциномы молочной железы слюнных желез: новый объект, связанный с перестройкой гена ETV6». Арка Вирхова. Март 2015 г.;466(3):245-54. дои: 10.1007/s00428-014-1701-8. Epub 2014, 12 декабря.
- ^ Аргани П., Фрич М., Кадкол С.С., Шустер А., Беквит Дж.Б., Перлман Э.Дж. (январь 2000 г.). «Обнаружение химерной РНК ETV6-NTRK3 инфантильной фибросаркомы/клеточной врожденной мезобластной нефромы в парафиновой ткани: применение для лечения сложных стромальных опухолей почек у детей» . Современная патология . 13 (1): 29–36. doi : 10.1038/modpathol.3880006 . ПМИД 10658907 .
- ^ Скалова А., Михал М., Симпсон Р.Х. (январь 2017 г.). «Недавно описанные опухоли слюнных желез» . Современная патология . 30 (с1): С27–С43. дои : 10.1038/modpathol.2016.167 . ПМИД 28060365 .
- ^ Алассири А.Х., Али Р.Х., Шен Ю., Лум А., Стралендорф С., Дейелл Р., Рассех Р., Соренсен П.Х., Ласкин Дж., Марра М., Йип С., Ли CH, Нг ТЛ (август 2016 г.). «ETV6-NTRK3 экспрессируется в подмножестве ALK-негативных воспалительных миофибробластических опухолей». Американский журнал хирургической патологии . 40 (8): 1051–61. doi : 10.1097/PAS.0000000000000677 . ПМИД 27259007 . S2CID 25165398 .
- ^ «Поиск ЕТВ6-НТРК» . ClinicalTrials.gov .
Дальнейшее чтение
[ редактировать ]- Кеунг Ю.К., Бити М., Стюард В., Джекл Б., Петтнати М. (октябрь 2002 г.). «Хронический миелоцитарный лейкоз с эозинофилией, t(9;12)(q34;p13) и перестановкой гена ETV6-ABL: отчет о случае и обзор литературы». Генетика рака и цитогенетика . 138 (2): 139–42. дои : 10.1016/S0165-4608(02)00609-X . ПМИД 12505259 .
- Файнштейн Э., Эйнат М., Гоккель Э., Марсель С., Кроче С.М., Гейл Р.П., Канаани Э. (декабрь 1989 г.). «Анализ нуклеотидных последовательностей кДНК abl и bcr-abl человека». Онкоген . 4 (12): 1477–81. ПМИД 2687768 .
- Буйс А., Шерр С., ван Баал С., ван Безу С., ван дер Плас Д., Гертс ван Кессель А., Ригман П., Леканн Депре Р., Звартхофф Е., Хагемейер А. (апрель 1995 г.). «Транслокация (12;22) (p13;q11) при миелопролиферативных заболеваниях приводит к слиянию ETS-подобного гена TEL на 12p13 с геном MN1 на 22q11». Онкоген . 10 (8): 1511–9. ПМИД 7731705 .
- Голуб Т.Р., Баркер Г.Ф., Боландер С.К., Хиберт С.В., Уорд Д.С., Брей-Уорд П., Морган Э., Раймонди С.К., Роули Дж.Д., Гиллиланд Д.Г. (май 1995 г.). «Слияние гена TEL на 12p13 с геном AML1 на 21q22 при остром лимфобластном лейкозе» . Труды Национальной академии наук Соединенных Штатов Америки . 92 (11): 4917–21. Бибкод : 1995PNAS...92.4917G . дои : 10.1073/pnas.92.11.4917 . ПМК 41818 . ПМИД 7761424 .
- Романа С.П., Мошофе М., Ле Кониа М., Чумаков И., Ле Паслье Д., Бергер Р., Бернар О.А. (июнь 1995 г.). «t(12;21) острого лимфобластного лейкоза приводит к слиянию гена tel-AML1» . Кровь . 85 (12): 3662–70. doi : 10.1182/blood.V85.12.3662.bloodjournal85123662 . ПМИД 7780150 .
- Пападопулос П., Ридж С.А., Баучер К.А., Стокинг С., Видеманн Л.М. (январь 1995 г.). «Новая активация ABL путем слияния с геном, связанным с ets, TEL». Исследования рака . 55 (1): 34–8. ПМИД 7805037 .
- Голуб Т.Р., Баркер Г.Ф., Ловетт М., Гиллиланд Д.Г. (апрель 1994 г.). «Слияние бета-рецептора PDGF с новым ets-подобным геном tel при хроническом миеломоноцитарном лейкозе с хромосомной транслокацией t (5;12)». Клетка . 77 (2): 307–16. дои : 10.1016/0092-8674(94)90322-0 . ПМИД 8168137 . S2CID 30073372 .
- Влодарска И., Баенс М., Петерс П., Эрсенс Дж., Мекуччи С., Брок П., Маринен П., Ван ден Берге Х. (июнь 1996 г.). «Двуаллельные изменения генов ETV6 и CDKN1B в случае острого лимфобластного лейкоза у детей (12;21)». Исследования рака . 56 (11): 2655–61. ПМИД 8653712 .
- Баенс М., Петерс П., Го С., Эрссенс Дж., Маринен П. (май 1996 г.). «Геномная организация TEL: ген 6 варианта ETS человека» . Геномные исследования . 6 (5): 404–13. дои : 10.1101/гр.6.5.404 . ПМИД 8743990 .
- Бональдо М.Ф., Леннон Дж., Соарес М.Б. (сентябрь 1996 г.). «Нормализация и вычитание: два подхода к открытию генов» . Геномные исследования . 6 (9): 791–806. дои : 10.1101/гр.6.9.791 . ПМИД 8889548 .
- Хиллиер Л.Д., Леннон Дж., Беккер М., Бональдо М.Ф., Кьяпелли Б., Чиссо С., Дитрих Н., Дюбук Т., Фавелло А., Гиш В., Хокинс М., Хультман М., Кукаба Т., Лейси М., Ле М., Ле Н., Мардис Э. , Мур Б, Моррис М, Парсонс Дж, Прейндж С, Рифкин Л, Ролфинг Т, Шелленберг К, Бенто Соареш М, Тан Ф, Тьерри-Мэг Дж, Треваскис Э, Андервуд К, Уолдман П, Уотерстон Р, Уилсон Р, Марра М (сентябрь 1996 г.). «Создание и анализ 280 000 меток экспрессируемых последовательностей человека» . Геномные исследования . 6 (9): 807–28. дои : 10.1101/гр.6.9.807 . ПМИД 8889549 .
- Андреассон П., Йоханссон Б., Археден К., Биллстрем Р., Мительман Ф., Хёглунд М. (июнь 1997 г.). «Делеции CDKN1B и ETV6 при остром миелолейкозе и миелодиспластических синдромах без цитогенетических доказательств нарушений 12p». Гены, хромосомы и рак . 19 (2): 77–83. doi : 10.1002/(SICI)1098-2264(199706)19:2<77::AID-GCC2>3.0.CO;2-X . ПМИД 9171997 . S2CID 27083284 .
- Лакроник В., Буре А., Валле В.Д., Пуарель Х., Куанг С.Т., Мошофе М., Берту С., Лессард М., Бергер Р., Гисдал Дж., Бернар О.А. (ноябрь 1997 г.). «Слитый белок TEL-JAK2 с конститутивной киназной активностью при лейкемии человека». Наука . 278 (5341): 1309–12. Бибкод : 1997Sci...278.1309L . дои : 10.1126/science.278.5341.1309 . ПМИД 9360930 .
- Кнезевич С.Р., Макфадден Д.Э., Тао В., Лим Дж.Ф., Соренсен П.Х. (февраль 1998 г.). «Новый слияние генов ETV6-NTRK3 при врожденной фибросаркоме». Природная генетика . 18 (2): 184–7. дои : 10.1038/ng0298-184 . ПМИД 9462753 . S2CID 7390311 .
- Квятковский Б.А., Бастиан Л.С., Бауэр Т.Р., Цай С., Зелинска-Квятковска А.Г., Хикштейн Д.Д. (июль 1998 г.). «Член семейства ets Tel связывается с онкобелком Fli-1 и ингибирует его транскрипционную активность» . Журнал биологической химии . 273 (28): 17525–30. дои : 10.1074/jbc.273.28.17525 . ПМИД 9651344 .
- Ханнеманн-младший, Макманус Д.М., Кабаровский Дж.Х., Видеманн Л.М. (июль 1998 г.). «Гемопоэтическая трансформация онкогеном TEL/ABL». Британский журнал гематологии . 102 (2): 475–85. дои : 10.1046/j.1365-2141.1998.00803.x . ПМИД 9695962 . S2CID 25904172 .
- Чакрабарти С.Р., Суд Р., Гангули С., Боландер С., Шен З., Нуцифора Г. (июнь 1999 г.). «Модуляция транскрипционной активности TEL путем взаимодействия с убиквитин-конъюгирующим ферментом UBC9» . Труды Национальной академии наук Соединенных Штатов Америки . 96 (13): 7467–72. Бибкод : 1999PNAS...96.7467R . дои : 10.1073/pnas.96.13.7467 . ПМК 22109 . ПМИД 10377438 .
- Кулс Дж., Бильоу-Набера С., Влодарска И., Каброль С., Талмант П., Бернард П., Хагемейер А., Маринен П. (сентябрь 1999 г.). «Слияние нового гена BTL с ETV6 при остром миелоидном лейкозе с at(4;12)(q11-q12;p13)». Кровь . 94 (5): 1820–4. дои : 10.1182/blood.V94.5.1820 . ПМИД 10477709 .
- Ягасаки Ф, Джиннаи И, Ёсида С, Ёкояма Ю, Мацуда А, Кусумото С, Кобаяши Х, Терасаки Х, Охясики К, Асо Н, Мурохаси И, Бессё М, Хирасима К (ноябрь 1999 г.). «Слияние TEL/ETV6 с новым ACS2 при миелодиспластическом синдроме и остром миелолейкозе с t(5;12)(q31;p13)» . Гены, хромосомы и рак . 26 (3): 192–202. doi : 10.1002/(SICI)1098-2264(199911)26:3<192::AID-GCC2>3.0.CO;2-E . ПМИД 10502316 .
- Вай Д.Х., Кнезевич С.Р., Лукас Т., Янсен Б., Кей Р.Дж., Соренсен П.Х. (февраль 2000 г.). «Слияние генов ETV6-NTRK3 кодирует химерную протеинтирозинкиназу, которая трансформирует клетки NIH3T3» . Онкоген . 19 (7): 906–15. дои : 10.1038/sj.onc.1203396 . ПМИД 10702799 .
Внешние ссылки
[ редактировать ]- ETV6+белок+человек Национальной медицинской библиотеки США по медицинским предметным рубрикам (MeSH)
- дрозофила Передняя открытая - The Interactive Fly
Эта статья включает текст из Национальной медицинской библиотеки США , который находится в свободном доступе .