Апротинин
 | |
| Клинические данные | |
|---|---|
| Другие имена | Трасилол, ингибитор бычьего трипсина поджелудочной железы |
| AHFS / Drugs.com | Монография |
| Беременность категория |
|
| Зависимость обязанность | Никто |
| Маршруты администрация | внутривенный |
| код АТС | |
| Юридический статус | |
| Юридический статус |
|
| Фармакокинетические данные | |
| Биодоступность | 100% ( внутривенно ) |
| Идентификаторы | |
| Номер CAS | |
| ИЮФАР/БПС | |
| Лекарственный Банк | |
| ХимическийПаук |
|
| НЕКОТОРЫЙ | |
| КЕГГ | |
| ХЭМБЛ | |
| Информационная карта ECHA | 100.029.983 |
| Химические и физические данные | |
| Формула | С 284 Ч 432 Н 84 О 79 С 7 |
| Молярная масса | 6 511 .51 g·mol −1 |
| | |
Препарат апротинин (Трасилол, ранее выпускаемый компанией Bayer , а теперь фармацевтической компанией Nordic Group) представляет собой небольшой белковый ингибитор трипсина поджелудочной железы крупного рогатого скота ( BPTI ) или основной ингибитор трипсина поджелудочной железы крупного рогатого скота , который представляет собой антифибринолитическую молекулу, ингибирующую трипсин и связанные с ним протеолитические ферменты . Под торговым названием «Трасилол » апротинин использовался в качестве препарата инъекционного . для уменьшения кровотечения во время сложных операций , таких как операции на сердце и печени Его основной эффект – замедление фибринолиза – процесса, приводящего к разрушению тромбов. Целью его применения было снижение необходимости переливания крови во время операции, а также повреждения органов-мишеней вследствие гипотонии (пониженного артериального давления) в результате выраженной кровопотери. Препарат был временно запрещен во всем мире в 2007 году после того, как исследования показали, что его использование увеличивает риск осложнений или смерти; [ 1 ] это было подтверждено последующими исследованиями. Продажи трасилола были приостановлены в мае 2008 года, за исключением очень ограниченного исследовательского использования. В феврале 2012 года научный комитет Европейского агентства по лекарственным средствам (EMA) изменил свою прежнюю точку зрения в отношении апротинина и рекомендовал отменить его приостановку. [ 2 ] Nordic стала дистрибьютором апротинина в 2012 году. [ 3 ]
Химия
[ редактировать ]| Ингибитор бычьего панкреатического трипсина | |||
|---|---|---|---|
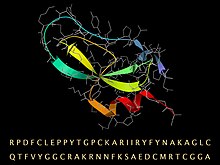 Последовательность BPTI со свернутой трехмерной структурой, представленной лентой для вторичной структуры и моделью палочки (серая) для основной цепи и боковых цепей. | |||
| Идентификаторы | |||
| Организм | |||
| Символ | ПТИ | ||
| Входить | 404172 | ||
| ПДБ | 4PTI Больше структур | ||
| RefSeq (мРНК) | НМ_001001554 | ||
| RefSeq (защита) | НП_001001554 | ||
| ЮниПрот | P00974 | ||
| Другие данные | |||
| хромосома | 13: 75.02 - 75.03 Мб | ||
| |||
Апротинин представляет собой мономерный (одноцепочечный) глобулярный полипептид, полученный из легочной ткани крупного рогатого скота. Он имеет молекулярную массу 6512 Да и состоит из 16 различных типов аминокислот , расположенных в цепочке длиной 58 остатков. [ 4 ] [ 5 ] которая сворачивается в стабильную компактную третичную структуру типа «маленькая SS-богатая», содержащую 3 дисульфида, скрученную β-шпильку и С-концевую α-спираль . [ 6 ]
Аминокислотная последовательность бычьего BPTI представляет собой RPDFC LEPPY TGPCK ARIIR YFYNA KAGLC QTFVY GGCRA KRNNF KSAED CMRTC GGA. [ 7 ] Имеет 10 положительно заряженных боковых цепей лизина (K) и аргинина (R) и только 4 отрицательных аспартата (D) и глутаматов (E), что делает белок сильноосновным , что и объясняет основное в его названии. (Из-за обычного организма-источника BPTI иногда называют ингибитором бычьего панкреатического трипсина.) [ нужна ссылка ]
Высокая стабильность молекулы обусловлена 3 дисульфидными связями, связывающими 6 членов цистеиновой цепи (Cys5-Cys55, Cys14-Cys38 и Cys30-Cys51). [ 8 ] Длинная основная боковая цепь лизина 15 на открытой петле (вверху слева на изображении) очень прочно связывается с карманом специфичности в активном центре трипсина и ингибирует его ферментативное действие. BPTI синтезируется как более длинная последовательность-предшественник, которая сворачивается и затем расщепляется на зрелую последовательность, указанную выше. [ нужна ссылка ]
BPTI является классическим членом белкового семейства типа Кунитца ингибиторов сериновых протеаз . Его физиологические функции включают защитное ингибирование основного пищеварительного фермента трипсина, когда он вырабатывается в небольших количествах, путем расщепления предшественника трипсиногена во время хранения в поджелудочной железе. [ нужна ссылка ]
Механизм действия препарата
[ редактировать ]Апротинин является конкурентным ингибитором нескольких сериновых протеаз , в частности трипсина , химотрипсина и плазмина в концентрации около 125 000 МЕ/мл и калликреина в концентрации 300 000 МЕ/мл. [ 5 ] Его действие на калликреин приводит к ингибированию образования фактора XIIa . В результате ингибируется как внутренний путь коагуляции, так и фибринолиз. Его действие на плазмин самостоятельно замедляет фибринолиз. [ 4 ]
Эффективность препарата
[ редактировать ]В кардиохирургических операциях с высоким риском значительной кровопотери апротинин значительно снижал кровотечение, смертность и длительность пребывания в стационаре. [ 5 ] Сообщалось также о положительных эффектах в ортопедической хирургии высокого риска. [ 5 ] При трансплантации печени первоначальные сообщения о пользе были омрачены опасениями по поводу токсичности. [ 9 ]
По данным метаанализа, проведенного в 2004 году, потребность в переливании крови снизилась на 39% при операции аортокоронарного шунтирования (АКШ). [ 10 ] В ортопедической хирургии также было подтверждено снижение количества переливаний крови. [ 11 ]
Безопасность лекарств
[ редактировать ]Были опасения по поводу безопасности апротинина. [ 5 ] Анафилаксия (тяжелая аллергическая реакция) возникает с частотой 1:200 при первом использовании, но серологическое исследование (измерение антител против апротинина в крови) на практике не проводится для прогнозирования риска анафилаксии, поскольку правильная интерпретация этих тестов трудный. [ 5 ]
Тромбоз , предположительно из-за чрезмерного ингибирования фибринолитической системы, может возникать с более высокой частотой, но до 2006 года доказательства этой связи были ограничены. [ 5 ] [ 10 ] Аналогичным образом, хотя было известно, что биохимические показатели функции почек иногда ухудшаются, не было никаких доказательств того, что это сильно влияло на исходы. [ 5 ] Исследование, проведенное среди кардиохирургических пациентов, о котором сообщалось в 2006 году, показало, что действительно существует риск острой почечной недостаточности , инфаркта миокарда и сердечной недостаточности , а также инсульта и энцефалопатии . [ 12 ] Авторы исследования рекомендуют старые антифибринолитики (такие как транексамовая кислота ), для которых подобные риски не были документированы. [ 12 ] Та же группа обновила свои данные в 2007 году и продемонстрировала аналогичные результаты. [ 13 ]
В сентябре 2006 года FDA обвинило компанию Bayer AG в том, что она не раскрыла во время дачи показаний о существовании заказанного ретроспективного исследования 67 000 пациентов, 30 000 из которых получали апротинин, а остальные - другие антифибринолитики. Исследование пришло к выводу, что апротинин несет больший риск. FDA было предупреждено об исследовании одним из участвовавших исследователей. Хотя FDA выступило с заявлением о обеспокоенности, они не изменили своей рекомендации о том, что препарат может принести пользу определенным группам пациентов. [ 14 ] В консультативном обновлении общественного здравоохранения от 3 октября 2006 г. FDA рекомендовало «врачам рассмотреть возможность ограничения использования трасилола теми ситуациями, в которых клиническая польза от снижения кровопотери необходима для медицинского лечения и перевешивает потенциальные риски», и тщательно наблюдать за пациентами. [ 15 ]
25 октября 2007 г. FDA опубликовало заявление относительно рандомизированного исследования «Сохранение крови с использованием антифибринолитиков» (BART) среди кардиохирургических пациентов. Предварительные результаты позволяют предположить, что по сравнению с другими антифибринолитическими препаратами (эпсилон-аминокапроновой кислотой и транексамовой кислотой) апротинин может увеличивать риск смерти. [ 16 ] 29 октября 2006 г. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов выпустило предупреждение о том, что апротинин может иметь серьезную токсичность для почек и сердечно-сосудистой системы. Производитель Bayer сообщил FDA, что дополнительные исследования показали, что он может увеличить вероятность смерти, серьезного повреждения почек, застойной сердечной недостаточности и инсульта. FDA предупредило врачей, что следует рассмотреть возможность ограничения использования препарата теми ситуациями, когда клиническая польза от снижения кровопотери важна для медицинского лечения и перевешивает потенциальные риски. [ 17 ] 5 ноября 2007 года компания Bayer объявила, что прекращает прием апротинина из-за канадского исследования, которое показало, что он увеличивает риск смерти при использовании для предотвращения кровотечения во время операций на сердце. [ 18 ]
Два исследования, опубликованные в начале 2008 года, в которых сравнивали апротинин с аминокапроновой кислотой , показали, что смертность увеличилась на 32 человека. [ 19 ] и 64%, [ 20 ] соответственно. Одно исследование выявило повышенный риск необходимости диализа и реваскуляризации. [ 20 ]
Случаев передачи губчатой энцефалопатии крупного рогатого скота апротинином не зарегистрировано, хотя в Италии препарат был отозван из-за опасений по этому поводу. [ 5 ]
Использование in vitro
[ редактировать ]Небольшие количества апротинина можно добавлять в пробирки с взятой кровью, чтобы обеспечить лабораторное измерение некоторых быстро разлагаемых белков, таких как глюкагон . [ нужна ссылка ]
В клеточной биологии апротинин используется в качестве ингибитора ферментов для предотвращения деградации белка во время лизиса или гомогенизации клеток и тканей. [ нужна ссылка ]
Апротинин можно пометить изотиоцианатом флуоресцеина. Конъюгат сохраняет свои антипротеолитические и углеводсвязывающие свойства. [ 21 ] и использовался в качестве флуоресцентного гистохимического реагента для окрашивания гликоконъюгатов (слизистых веществ), богатых уроновыми или сиаловыми кислотами. [ 22 ]
История
[ редактировать ]Первоначально названный «инактиватором калликреина», апротинин был впервые выделен из околоушных желез коровы в 1930 году. [ 23 ] и независимо в качестве ингибитора трипсина из бычьей поджелудочной железы в 1936 году. [ 24 ] Его выделили из бычьих легких в 1964 году. [ 25 ] Поскольку он ингибирует ферменты поджелудочной железы, его первоначально использовали при лечении острого панкреатита , при котором разрушение железы собственными ферментами считается частью патогенеза. [ 26 ] Его использование в серьезной хирургии началось в 1960-х годах. [ 27 ]
BPTI — один из наиболее тщательно изученных белков с точки зрения структурной биологии , экспериментальной и вычислительной динамики, мутагенеза и пути сворачивания . Это была одна из первых кристаллических структур белка, решенная в 1970 году в лаборатории Роберта Хубера . [ 28 ] и этот тип субстратно-подобного взаимодействия был расшифрован в контексте комплекса бычьего трипсина в 1974 году. [ 29 ] Позже он также прославился как первый белок, структура которого была определена с помощью ЯМР-спектроскопии в лаборатории Курта Вутриха в ETH в Цюрихе в начале 1980-х годов. [ 30 ] [ 31 ]
Поскольку это небольшой стабильный белок, структура которого была определена с высоким разрешением к 1975 году. [ 32 ] это была первая макромолекула, представляющая научный интерес, которая была смоделирована с использованием вычислений молекулярной динамики в 1977 году Дж. Эндрю Маккаммоном и Брюсом Гелином в группе Карплюс в Гарварде. [ 33 ] Это исследование подтвердило удивительный на тот момент факт, обнаруженный в работе ЯМР. [ 34 ] что даже хорошо упакованные ароматические боковые цепи внутри стабильного белка могут переворачиваться довольно быстро (в масштабе времени от микросекунды до миллисекунды). Константы скорости были определены с помощью ЯМР для водородного обмена отдельных пептидных групп NH вдоль цепи: от слишком быстрой для измерения на наиболее открытой поверхности до многих месяцев для наиболее скрытых групп с водородными связями в центре β-листа и эти значения также довольно хорошо коррелируют со степенью движения, наблюдаемой в динамическом моделировании.
BPTI сыграл важную роль в развитии знаний о процессе сворачивания белка , самосборке полипептидной цепи в определенное расположение в 3D. Было показано, что проблема достижения правильных спариваний между 6 боковыми цепями Cys оказалась особенно сложной для двух похороненных, близко расположенных друг к другу SS вблизи концов цепи BPTI, требуя ненативного промежуточного соединения для сворачивания зрелой последовательности in vitro (позже это было обнаружено). обнаружили, что последовательность предшественников легче сворачивается in vivo ). BPTI было изображением на обложке тома сборника по сворачиванию белков Томаса Крейтона в 1992 году. [ 35 ]
Текущие результаты
[ редактировать ]Одно научное исследование на крысах показало, что лечение апротинином предотвращает нарушение гематоэнцефалического барьера во время инфекции C. neoformans . [ 36 ] Другое исследование на культурах клеток показало, что препарат ингибирует репликацию SARS-CoV-2. [ 37 ]
Ссылки
[ редактировать ]- ^ «Bayer временно приостанавливает глобальный маркетинг трасилола» (PDF) (пресс-релиз). Трасилол.com. 05.11.2007. Архивировано из оригинала (PDF) 17 июля 2011 г. Проверено 3 декабря 2007 г.
- ^ «Европейское агентство лекарственных средств рекомендует отменить приостановку приема апротинина» . Европейское агентство лекарственных средств. 17 февраля 2012 г. Архивировано из оригинала 18 февраля 2014 г. Проверено 22 февраля 2012 г.
- ^ «The Nordic Group приобретает права на Трасилол® у компании Bayer HealthCare» . The Nordic Group BV Архивировано из оригинала 1 февраля 2014 года . Проверено 28 января 2014 г.
- ^ Перейти обратно: а б Маннуччи ПМ (июль 1998 г.). «Гемостатические препараты». Медицинский журнал Новой Англии . 339 (4): 245–53. дои : 10.1056/NEJM199807233390407 . ПМИД 9673304 .
- ^ Перейти обратно: а б с д и ж г час я Махди А.М., Вебстер Н.Р. (декабрь 2004 г.). «Периоперационные системные гемостатики» . Британский журнал анестезии . 93 (6): 842–58. дои : 10.1093/bja/aeh227 . ПМИД 15277296 .
- ^ Ричардсон Дж.С. (1981). «Анатомия и систематика структуры белка». Достижения в области химии белков, том 34 . Достижения в химии белков. Том. 34. стр. 167–339. дои : 10.1016/S0065-3233(08)60520-3 . ISBN 978-0-12-034234-1 . ПМИД 7020376 .
- ^ Касселл Б., Радичевич М., Энсфилд М.Дж., Ласковски М. (январь 1965 г.). «Основной ингибитор трипсина поджелудочной железы крупного рогатого скота. IV. Линейная последовательность из 58 аминокислот». Связь с биохимическими и биофизическими исследованиями . 18 (2): 255–8. дои : 10.1016/0006-291X(65)90749-7 . ПМИД 14282026 .
- ^ Касселл Б., Ласковски М. (август 1965 г.). «Основной ингибитор трипсина поджелудочной железы крупного рогатого скота. V. Дисульфидные связи». Связь с биохимическими и биофизическими исследованиями . 20 (4): 463–8. дои : 10.1016/0006-291X(65)90601-7 . ПМИД 5860161 .
- ^ Ся Фольксваген, Стедман Р.Х. (январь 2005 г.). «Антифибринолитики при ортотопической трансплантации печени: современное состояние и противоречия» . Трансплантация печени . 11 (1): 10–8. дои : 10.1002/lt.20275 . ПМИД 15690531 .
- ^ Перейти обратно: а б Седракян А., Трежер Т., Элефтериадес Дж.А. (сентябрь 2004 г.). «Влияние апротинина на клинические результаты при аортокоронарном шунтировании: систематический обзор и метаанализ рандомизированных клинических исследований» . Журнал торакальной и сердечно-сосудистой хирургии . 128 (3): 442–8. дои : 10.1016/j.jtcvs.2004.03.041 . ПМИД 15354106 .
- ^ Сига Т., Вадзима З., Иноуэ Т., Сакамото А. (декабрь 2005 г.). «Апротинин в большой ортопедической хирургии: систематический обзор рандомизированных контролируемых исследований» . Анестезия и анальгезия . 101 (6): 1602–7. дои : 10.1213/01.ANE.0000180767.50529.45 . ПМИД 16301226 . S2CID 33762135 .
- ^ Перейти обратно: а б Мангано Д.Т., Тюдор И.С., Дитцель С. (январь 2006 г.). «Риск, связанный с апротинином в кардиохирургии» . Медицинский журнал Новой Англии . 354 (4): 353–65. doi : 10.1056/NEJMoa051379 . ПМИД 16436767 .
- ^ Мангано Д.Т., Мяо Ю., Вуйлстеке А., Тюдор И.С., Джунеха Р., Филипеску Д. и др. (февраль 2007 г.). «Смертность, связанная с апротинином, в течение 5 лет после операции аортокоронарного шунтирования». ДЖАМА . 297 (5): 471–9. дои : 10.1001/jama.297.5.471 . ПМИД 17284697 .
- ^ Харрис Дж. (30 сентября 2006 г.). «FDA заявляет, что компания Bayer не представила данные об исследовании риска применения лекарств — New York Times» . Нью-Йорк Таймс . Проверено 5 ноября 2007 г.
- ^ «Факты и сравнения: обновленная информация о трасилоле для общественного здравоохранения» . Архивировано из оригинала 22 июля 2012 г. Проверено 5 ноября 2007 г.
- ^ «Раннее сообщение о продолжающемся обзоре безопасности инъекции апротинина (продаваемого как трасилол)» . Управление по контролю за продуктами и лекарствами . Архивировано из оригинала 30 октября 2007 г. Проверено 28 октября 2007 г.
- ^ «Информация для медицинских работников; Апротинин (продается как Трасилол)» . Управление по контролю за продуктами и лекарствами . Архивировано из оригинала 10 октября 2006 г. Проверено 30 октября 2006 г.
- ^ Харрис Дж. (5 ноября 2007 г.). «Bayer отзывает препарат для кардиохирургии» . Нью-Йорк Таймс . Проверено 5 ноября 2007 г.
- ^ Шоу А.Д., Стаффорд-Смит М., Уайт В.Д., Филлипс-Бьют Б., Сваминатан М., Милано С. и др. (февраль 2008 г.). «Влияние апротинина на исход после аортокоронарного шунтирования» . Медицинский журнал Новой Англии . 358 (8): 784–93. doi : 10.1056/NEJMoa0707768 . ПМИД 18287601 .
- ^ Перейти обратно: а б Шневайс С., Сигер Дж. Д., Лэндон Дж., Уокер А. М. (февраль 2008 г.). «Апротинин при аортокоронарном шунтировании и риск смерти» . Медицинский журнал Новой Англии . 358 (8): 771–83. doi : 10.1056/NEJMoa0707571 . ПМИД 18287600 .
- ^ Стоддарт Р.В., Кернан Дж.А. (март 1973 г.). «Апротинин, углеводсвязывающий белок». Гистохимия. Гистохимия. Гистохимия . 34 (4): 275–80. дои : 10.1007/BF00306299 . ПМИД 4266832 . S2CID 44549220 .
- ^ Кирнан Дж.А., Стоддарт Р.В. (1973). «Апротинин, меченный флуоресцентной меткой: новый реагент для гистохимического обнаружения кислых слизистых веществ». Гистохимия . 34 (1): 77–84. дои : 10.1007/BF00304309 . ПМИД 4119444 . S2CID 32032724 .
- ^ Краут Х., Фрей Е.К., Бауэр Э. (1930). «Об инактивации калликреина». Z Physiol Chem Хоппе-Зейлера (на немецком языке). 192 : 1–21. дои : 10.1515/bchm2.1930.192.1-3.1 .
- ^ Куниц М., Нортроп Дж. Х. (июль 1936 г.). «Выделение из поджелудочной железы говядины кристаллического трипсиногена, трипсина, ингибитора трипсина и соединения-ингибитора трипсина» . Журнал общей физиологии . 19 (6): 991–1007. дои : 10.1085/jgp.19.6.991 . ПМК 2141477 . ПМИД 19872978 .
- ^ Краут Х., Бхаргава Н. (1964). «Опыты по выделению инактиватора калликреина из легких крупного рогатого скота и его идентификация с инактиватором из околоушной железы крупного рогатого скота» [Опыты по выделению инактиватора калликреина. V. Выделение калликреинового инактиватора из легких крупного рогатого скота и его идентификация с ингибитором из околоушной железы крупного рогатого скота. Журнал физиологической химии Хоппе-Зейлера (на немецком языке). 338 : 231–7. дои : 10.1515/bchm2.1964.338.1-2.231 . ПМИД 14330402 .
- ^ Ньюджент Ф.В., Уоррен К.В., Джонассон Х., Гарсиадепаредес Дж. (ноябрь 1964 г.). «Ранний опыт применения трасилола в лечении острого панкреатита». Южный медицинский журнал . 57 (11): 1317–21. дои : 10.1097/00007611-196411000-00012 . ПМИД 14195953 . S2CID 5286289 .
- ^ Тайс Д.А., Уорт М.Х., Клаусс Р.Х., Рид Г.Х. (июль 1964 г.). «Ингибирование трасилолом фибринолитической активности, связанной с сердечно-сосудистыми операциями». Хирургия, гинекология и акушерство . 119 : 71–4. ПМИД 14179354 .
- ^ Хубер Р., Кукла Д., Рюльманн А., Эпп О., Форманек Х. (август 1970 г.). «Основной ингибитор трипсина поджелудочной железы крупного рогатого скота. I. Анализ структуры и конформации полипептидной цепи». Die Naturwissenschaften . 57 (8): 389–92. Бибкод : 1970NW.....57..389H . дои : 10.1007/BF00599976 . ПМИД 5447861 . S2CID 6261274 .
- ^ Хубер Р., Кукла Д., Боде В., Швагер П., Бартельс К., Дайзенхофер Дж., Штайгеманн В. (октябрь 1974 г.). «Структура комплекса, образованного бычьим трипсином и ингибитором бычьего панкреатического трипсина. II. Кристаллографическое уточнение при разрешении 1,9 А». Журнал молекулярной биологии . 89 (1): 73–101. дои : 10.1016/0022-2836(74)90163-6 . ПМИД 4475115 .
- ^ Вагнер Г., Вютрих К. (март 1982 г.). «Последовательные резонансные назначения в спектрах ядерного магнитного резонанса белка 1H. Основной ингибитор трипсина поджелудочной железы». Журнал молекулярной биологии . 155 (3): 347–66. дои : 10.1016/0022-2836(82)90009-2 . ПМИД 6176717 .
- ^ Гавел Т.Ф., Вютрих К. (март 1985 г.). «Оценка совместного использования ядерного магнитного резонанса и геометрии расстояния для определения конформаций белка в растворе». Журнал молекулярной биологии . 182 (2): 281–94. дои : 10.1016/0022-2836(85)90346-8 . ПМИД 2582141 .
- ^ Дайзенхофер Дж, Штайгеманн В (1975). «Кристаллографическое уточнение структуры ингибитора бычьего панкреатического трипсина при разрешении 1,5 ангстрем» (PDF) . Акта Кристаллографика Б. 31 : 238. дои : 10.1107/S0567740875002415 .
- ^ Маккаммон Дж. А., Гелин Б. Р., Карплюс М. (июнь 1977 г.). «Динамика свернутых белков». Природа . 267 (5612): 585–90. Бибкод : 1977Natur.267..585M . дои : 10.1038/267585a0 . ПМИД 301613 . S2CID 4222220 .
- ^ Вютрих К., Вагнер Г. (февраль 1975 г.). «ЯМР-исследования динамики остатков ароматических аминокислот в основном ингибиторе панкреатического трипсина». Письма ФЭБС . 50 (2): 265–8. дои : 10.1016/0014-5793(75)80504-7 . ПМИД 234403 . S2CID 46084481 .
- ^ Крейтон Т.Э. (1992). Складывание белка . У. Х. Фриман. ISBN 978-0-7167-7027-5 .
- ^ Сюй С.И., Чжу Х.М., Ву Дж.Х., Вэнь Х., Лю С.Дж. (февраль 2014 г.). «Повышение проницаемости гематоэнцефалического барьера опосредовано сериновой протеазой при криптококковом менингите» . Журнал международных медицинских исследований . 42 (1): 85–92. дои : 10.1177/0300060513504365 . ПМИД 24398759 .
- ^ Бойкова Д., Бектель М., Маклафлин К.М., МакГрейг Дж.Э., Кланн К., Беллинхаузен С. и др. (октябрь 2020 г.). «Апротинин ингибирует репликацию SARS-CoV-2» . Клетки . 9 (11): 2377. doi : 10.3390/cells9112377 . ПМЦ 7692688 . ПМИД 33143316 .