Йодид висмута(III)
| |

| |

| |

| |
| Имена | |
|---|---|
| Название ИЮПАК
Йодид висмута(III)
| |
| Другие имена
Йодид висмута, трийодид висмута
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| ХимическийПаук | |
| Информационная карта ECHA | 100.029.207 |
| Номер ЕС |
|
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| БИ 3 | |
| Молярная масса | 589,69 г/моль |
| Появление | Зеленовато-черные кристаллы |
| Плотность | 5,778 г/см 3 |
| Температура плавления | 408,6 ° С (767,5 ° F; 681,8 К) |
| Точка кипения | 542 ° C (1008 ° F; 815 К) [ 2 ] |
| 0,7761 мг/100 мл (20 °С) | |
Произведение растворимости ( K sp )
|
7.71 × 10 −19 [ 1 ] |
| Растворимость | 50 г/100 мл этанола 50 г/100 мл 2 М соляной кислоты |
| −200.5·10 −6 см 3 /моль | |
| Структура | |
| Тригональный , hR24 | |
| Р-3, № 148 | |
| Опасности | |
| СГС Маркировка : | |

| |
| Опасность | |
| H314 | |
| P260 , P264 , P280 , P301+P330+P331 , P303+P361+P353 , P304+P340 , P305+P351+P338 , P310 , P321 , P363 , P405 , P501 | |
| NFPA 704 (огненный алмаз) | |
| Родственные соединения | |
Другие анионы
|
Фторид висмута(III) Хлорид висмута(III) Бромид висмута(III) |
Другие катионы
|
Азотные триоды трииодид фосфора Трийодид сурьмы |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
) представляет собой неорганическое соединение формулы I Bi Йодид висмута( III 3 . Эта серо-черная соль — продукт реакции висмута и йода, который когда-то представлял интерес для качественного неорганического анализа . [ 3 ] [ 4 ]
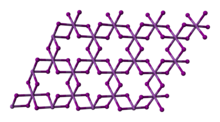
Йодид висмута (III) имеет характерную кристаллическую структуру: йодидные центры занимают гексагональную плотноупакованную решетку, а центры висмута не занимают ни одной октаэдрической дырки или две трети (чередуясь по слоям), поэтому говорят, что она занимает одну треть. общего числа октаэдрических отверстий. [ 5 ] [ 6 ]
Синтез
[ редактировать ]Йодид висмута(III) образуется при нагревании однородной смеси порошка йода и висмута: [ 7 ] [ 8 ]
- 2Би + 3И 2 → 2БиI 3
BiI 3 также можно получить реакцией оксида висмута с водным раствором иодистоводородной кислоты : [ 9 ]
- Bi 2 O 3 (тв) + 6HI(водн.) → 2BiI 3 (тв) + 3H 2 O(л)
Реакции
[ редактировать ]Поскольку йодид висмута (III) нерастворим в воде, водный раствор можно проверить на наличие Bi. 3+ ионы путем добавления источника йодида, такого как йодид калия . Черный осадок йодида висмута(III) указывает на положительный результат теста. [ 10 ]
Йодид висмута (III) образует анионы йодовисмута (III) при нагревании с донорами галогенидов: [ 11 ]
- 2 NaI + BiI 3 → Na 2 [BiI 5 ]
Йодид висмута(III) катализирует альдольную реакцию Мукаямы . Bi(III) также используется при аллилировании карбонильных соединений по типу Барбье в сочетании с восстановителем, таким как цинк или магний .
Ссылки
[ редактировать ]- ^ Джон Рамбл (18 июня 2018 г.). Справочник CRC по химии и физике (99 изд.). ЦРК Пресс. стр. 5–188. ISBN 978-1138561632 .
- ^ Норман, Николас К. (1998), Химия мышьяка, сурьмы и висмута , Springer, с. 95, ISBN 0-7514-0389-Х , получено 3 июня 2008 г.
- ^ «Йодид висмута», Словарь научных и технических терминов McGraw-Hill , McGraw-Hill, 2003 г. , получено 19 июня 2008 г.
- ^ Тернер-младший, Фрэнсис М.; Берольцхаймер, Дэниел Д.; Каттер, Уильям П.; Хелфрич, Джон (1920), Сокращенный химический словарь , Нью-Йорк: Компания химического каталога, стр. 107 , получено 19 июня 2008 г.
- ^ Умно, Лесли; Мур, Элейн А. (2005), Химия твердого тела: Введение , CRC Press, стр. 40, ISBN 0-7487-7516-1 , получено 19 июня 2008 г.
- ^ Маккей, Розмари Энн; Хендерсон, В. (2002), Введение в современную неорганическую химию , CRC Press, стр. 122–6, ISBN 0-7487-6420-8 , получено 19 июня 2008 г.
- ^ Ватт, Джордж В.; Хакки, Вафаи В.; Чоппин, Грегори Р. (1953). «Йодид висмута(III)». Неорганические синтезы . Неорганические синтезы . Том. 4. С. 114–116. дои : 10.1002/9780470132357.ch38 . ISBN 978-0-470-13163-3 .
- ^ Эрдманн, Хьюго ; Данлэп, Фредерик Ливи (1900), Справочник основных таблиц для химического анализа , Нью-Йорк: John Wiley & Sons, стр. 76 , получено 19 июня 2008 г.
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . п. 559. ИСБН 978-0-08-037941-8 .
- ^ Бруно, Томас Дж.; Своронос, Пэрис Д.Н. (2003), Справочник основных таблиц для химического анализа , CRC Press, стр. 549, ISBN 0-8493-1573-5 , получено 19 июня 2008 г.
- ^ Норман, Николас К. (1998), Химия мышьяка, сурьмы и висмута , Springer, стр. 168–70, ISBN 0-7514-0389-Х , получено 19 июня 2008 г.
