Глюкуроновая кислота
 | |
 | |
| Имена | |
|---|---|
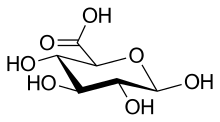
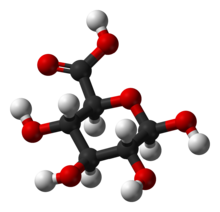
| Название ИЮПАК β- D -глюкопирануроновая кислота | |
| Систематическое название ИЮПАК (2S , 3S , 4S , 5R , 6R ) -3,4,5,6-Тетрагидроксиоксан-2-карбоновая кислота | |
| Другие имена β- D -глюкуроновая кислота, GlcA | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ЧЭБИ | |
| ХимическийПаук | |
| Лекарственный Банк | |
| Информационная карта ECHA | 100.026.807 |
| КЕГГ | |
| МеШ | Глюкуроновая+кислота |
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| С 6 Н 10 О 7 | |
| Молярная масса | 194.139 g·mol −1 |
| Температура плавления | От 159 до 161 ° C (от 318 до 322 ° F; от 432 до 434 К) [1] |
| Родственные соединения | |
Родственные уроновые кислоты | Аллуроновая кислота , Альтруроновая кислота , Арабинуроновая кислота , Фруктуроновая кислота , Галактуроновая кислота , Гулуроновая кислота , Идуроновая кислота Ликсуроновая кислота , Маннуроновая кислота , Псикуроновая кислота , Рибуроновая кислота , Рибулуроновая кислота , Сорбуроновая кислота , Тагатуроновая кислота , , Ксилуроновая Талуроновая кислота , кислота , Ксилуроновая кислота |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Глюкуроновая кислота (от греческого γλεῦκος « сладкое вино, сусло » и οὖρον « моча ») — уроновая кислота , впервые выделенная из мочи (отсюда и название «уроновая кислота»). Он содержится во многих камедях, таких как гуммиарабик ( около 18%), ксантан и чайный гриб , и важен для метаболизма микроорганизмов, растений и животных.
Характеристики
[ редактировать ]Этот раздел нуждается в дополнительных цитатах для проверки . ( Март 2023 г. ) |

Глюкуроновая кислота — это сахарная кислота, полученная из глюкозы , шестой атом углерода которой окислен до карбоновой кислоты. У живых существ это первичное окисление происходит с помощью УДФ-α- D -глюкозы (УДФГ), а не со свободным сахаром.
Глюкуроновая кислота, как и ее предшественник глюкоза , может существовать в виде линейной (карбоксо-) альдогексозы (<1%) или в виде циклического полуацеталя ( фуранозы или пиранозы ). Альдогексозы, такие как D -глюкоза, способны образовывать две формы фуранозы (α и β) и две формы пиранозы (α и β). По соглашению Фишера глюкуроновая кислота имеет два стереоизомера ( энантиомера ), D- и L -глюкуроновую кислоту, в зависимости от ее конфигурации при С-5. Большинство физиологических сахаров имеют D -конфигурацию. Из-за замыкания кольца циклические сахара имеют еще один асимметричный атом углерода (C-1), в результате чего образуются еще два стереоизомера, называемые аномерами . В зависимости от конфигурации С-1 существуют два аномера глюкуроновой кислоты: α- и β-форма. В β- D- глюкуроновой кислоте гидроксильная группа C-1 находится на той же стороне пиранозного кольца, что и карбоксильная группа. В свободной сахарной кислоте преобладает β-форма (~64%), тогда как в организме преобладает α-форма УДФ-α- D -глюкуроновой кислоты (УДПГК).
Стереоизомеры углеводов, которые различаются конфигурацией только по одному (другому) асимметричному атому С, называются эпимерами . Например, D -маннуроновая (С-2), D -аллуроновая (С-3), D -галактуроновая (С-4) и L -идуроновая кислота (С-5) являются эпимерами глюкуроновой кислоты.
Неплоские пиранозные кольца могут принимать форму стула (в двух вариантах) или лодочки. Предпочтительная конформация зависит от пространственной интерференции или других взаимодействий заместителей. Пиранозная форма D -глюкозы и ее производное D -глюкуроновая кислота предпочитают стул. 4 С 1 .
Дополнительное окисление по С-1 до карбоксильного уровня дает дикарбоновую глюкаровую кислоту . Глюкуронолактон представляет собой самоэфир ( лактон ) глюкуроновой кислоты.
Прямое окисление альдозы в первую очередь затрагивает альдегидную группу. Лабораторный синтез уроновой кислоты из альдозы требует защиты альдегидных и гидроксильных групп от окисления, например, путем превращения в циклические ацетали (например, ацетониды ).
Глюкуронат натрия можно получить прямым окислением крахмала концентрированной азотной кислотой. В этом препарате низкая доступность воды удерживает полимеры крахмала от гидролиза и окисляет только свободные гидроксилы, почти так же, как диоксид азота окисляет крахмал. Как только эта реакция завершится и смесь крахмала и азотной кислоты станет прозрачной (после выделения газообразного диоксида азота), раствор можно разбавить и гидролизовать другой минеральной кислотой. Затем окисление медленно гасят гидроксидом натрия (или бикарбонатом натрия), образуя глюкуронат натрия, который можно кристаллизовать из раствора. С переходными металлами он образует такие комплексы, как глюкуронат железа (III) , глюкуронат железа (II) и глюкуронат меди (II) .
Функции
[ редактировать ]Протеогликаны
[ редактировать ]Глюкуроновая кислота является распространенным строительным блоком протеогликанов и гликоглицеролипидов : [ нужна ссылка ]
- Гепарин является ингибитором свертывания крови и встречается в тучных клетках, легких и печени.
- Хондроитинсульфат содержится в больших количествах в хрящах, аорте, соединительной ткани, костях и коже.
- Дерматансульфат представляет собой протеогликан кожи, сердца и кровеносных сосудов.
- Кератансульфат содержится в роговице, хрящах и костях.
- Гиалуроновая кислота содержится в больших количествах в соединительных тканях, коже, хрящах и синовиальной жидкости.
- Гликоглицеролипиды глюкуроновой или галактуроновой кислот образуют клеточные стенки бактерий.
глюкуронидация
[ редактировать ]
УДФ-α -D- глюкуроновая кислота (УДПГК) часто участвует во II фазе метаболизма ( конъюгации ) липофильных ксено- и эндобиотиков . Эти связи включают гликозидные связи с тиоловыми, аминными и гидроксильными группами или этерификацию с карбоксильными и гидроксильными группами. Этот процесс связывания известен как глюкуронидация (или конъюгация глюкуронида). Глюкуронидация происходит главным образом в печени, хотя ферменты, ответственные за ее катализ, УДФ-глюкуронилтрансферазы (УДФ-ГТ), обнаружены во всех основных органах тела, например, в кишечнике, почках, головном мозге, надпочечниках, селезенке и тимусе. [2] [3] Аналогичные реакции происходят и с другими УДФ - уроновыми кислотами (например, D -галактуроновой кислотой ).
Гликозиды, образующиеся в результате глюкуронидации, называются β- D -глюкуронидами, а их соли и эфиры — глюкуронатами. Человеческий организм использует глюкуронидацию, чтобы сделать спирты , фенолы , карбоновые кислоты , меркаптаны , первичные и вторичные алифатические амины и карбаматы более водорастворимыми и, таким образом, обеспечивает их последующее выведение из организма через мочу или кал (с желчью). из печени) со значительно повышенной скоростью. Карбоксильная группа ионизируется при физиологическом pH, что делает сопряженное соединение водорастворимым. Соединения с молекулярной массой > 60 000 слишком велики для выведения почками и выводятся с желчью в кишечник. У новорожденных наблюдается дефицит этой конъюгирующей системы, что делает их особенно уязвимыми для таких препаратов, как хлорамфеникол , который инактивируется добавлением глюкуроновой кислоты, что приводит к синдрому серого ребенка . Билирубин выводится с желчью в виде диглюкуронида билирубина (80%), глюкуронида билирубина (20%) и неконъюгированного билирубина (<1%). В При синдроме Криглера-Найяра и синдроме Гилберта активность UDPGT снижена или почти отсутствует из-за мутаций, что приводит к желтухе .
Запасы глюкуроновой кислоты в организме можно исчерпать путем комбинирования нескольких препаратов/веществ, метаболизм и выведение которых в первую очередь или полностью зависят от глюкуронидации. Хотя большинство таких веществ имеют вторичные пути метаболизма, которые становятся заметными после истощения ГКА, скорость метаболизма снижается настолько, что приводит к заметному накоплению всех субстратов ГКА в системе; это часто увеличивает концентрацию лекарства в крови на величину, значимую с медицинской точки зрения. Известно, что в наиболее тяжелых случаях происходит необратимое и изнурительное повреждение органов (особенно печени, почек, сердца и мозга) и даже смерть. Этанол , морфин , парацетамол (ацетаминофен) , ингибиторы циклооксигеназы ( НПВП ), эндогенные стероиды и некоторые бензодиазепины способны способствовать истощению запасов ГКА, при этом этанол и ацетаминофен являются наиболее часто встречающимися веществами, участвующими в случаях случайной передозировки, что имело положительные результаты. связано с истощением запасов глюкуроновой кислоты.
Чрезмерное количество GCA также может быть опасно для здоровья. [ нужна ссылка ] табачный дым, большинство барбитуратов Известно, что и некоторые карбаматы фактически стимулируют выработку ГКА. Повышенная активность ГКА приводит к снижению концентрации и метаболического периода полувыведения субстратов глюкуроновой кислоты, в результате чего уровни глюкуронидированных препаратов в плазме падают ниже их терапевтического порога. Чрезмерное глюкуронидирование субстратов может привести к неадекватному ответу на традиционные дозы затронутых препаратов и, если препарат не имеет очень широкого терапевтического индекса, обычно приводит к острой неэффективности фармакотерапии и вызывает необходимость перехода одного или нескольких задействованных препаратов на эквивалентный режим неглюкуронидных альтернатив. Некоторые антидепрессанты и широкий спектр антипсихотических средств являются лигандами глюкуронидации, но из-за их замедленного механизма действия и фармакокинетических свойств снижение их концентраций в плазме может быть не сразу очевидным и имеет тенденцию проявляться как внезапный и интенсивный рецидив симптомы вместо постепенной регрессии к поведению и мышлению пациента, проявленному до начала фармакологического лечения.
Глюкурониды могут гидролизоваться присутствующей β-глюкуронидазой, в кишечной микрофлоре, до соответствующего агликона, который может реабсорбироваться из кишечника и транспортироваться обратно в печень с кровью. Возникающий цикл называется энтерогепатической циркуляцией . Соединения, которые подвергаются энтерогепатической циркуляции, выводятся из организма медленно и обычно имеют более длительный период полураспада в организме.
Некоторые глюкурониды электрофильны и могут участвовать в интоксикации процессах . Известно, что ковалентное связывание агликоновых частей некоторых глюкуронидов (эфиров) карбоновых кислот происходит с нуклеофильными сайтами сывороточного альбумина посредством реакций трансацилирования . , например, [4]
Фенолы , количественно важные P450 метаболиты ароматических углеводородов, производные , являются субстратами как для UDP-GT, так и для сульфотрансфераз . Глюкурониды преобладают с фенолом или предшественником фенола ( бензолом ) у млекопитающих, поскольку образование сульфатов представляет собой систему с высоким сродством и низкой емкостью (из-за истощения запасов сульфатов), тогда как глюкуронидация представляет собой систему с низким сродством и высокой производительностью (хотя все еще исчерпаемую). . [4]
Роль в болезни
[ редактировать ]Глюкуроновая кислота, а также глюкуронидированный метаболит этанола , этилглюкуронид (ETG), действуют на толл-подобный рецептор 4, усугубляя как острые, так и хронические воспалительные состояния, а также увеличивая воспринимаемую тяжесть боли у пациентов с хроническими болевыми состояниями, посредством активация производства и высвобождения эндогенных воспалительных сигнальных молекул в организме. Длительный агонизм рецептора TLR4 (например, вызываемый GCA, ETG и опиатами ) приводит к тому, что хронические болезненные состояния воспринимаются как значительно более тяжелые, чем раньше, в то время как ранее существовавшие терпимые, но иногда болезненные действия могут стать более болезненными. чем раньше, и начнет усугубляться более короткими и менее физически тяжелыми занятиями. Это также может вызывать столь же болезненные реакции на все менее вредные (раздражающие) раздражители, что в конечном итоге приводит к значительной агонии от раздражителей, которые не причиняют никакой боли большинству людей. [5]
Использовать
[ редактировать ]Определение стероидов в моче и стероидных конъюгатов в крови. Этилглюкуронид и этилсульфат выводятся с мочой в виде метаболитов этанола и используются для контроля употребления алкоголя или зависимости.
Глюкуроновая кислота и глюконовая кислота являются ферментации продуктами чая Чайный гриб . [6]
Глюкуроновая кислота является предшественником аскорбиновой кислоты ( витамина С , ранее называемого L-гексуроновой кислотой). Аскорбат может биосинтезироваться высшими растениями, водорослями, дрожжами и большинством животных. Взрослая коза производит около 13 г витамина С в день. Эта способность отсутствует у некоторых млекопитающих (включая человека и морских свинок), а также у насекомых, беспозвоночных и большинства рыб. Этим видам требуется внешнее снабжение аскорбатом, поскольку у них отсутствует биосинтетический фермент L - гулонолактоноксидаза . [7]
Глюкуронид 4-метилумбеллиферил-β- D -глюкуронид (MUG) используется для проверки на наличие Escherichia coli . E. coli вырабатывает фермент β-глюкуронидазу, которая гидролизует молекулу MUG до флуоресцентного продукта, который можно обнаружить в ультрафиолетовом свете .
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ D-глюкуроновая кислота в Sigma-Aldrich
- ^ Оно С., Накаджин, Шизуо (6 октября 2008 г.). «Определение экспрессии мРНК УДФ-глюкуронозилтрансфераз человека и их применение для локализации в различных тканях человека с помощью обратной транскриптазно-полимеразной цепной реакции в реальном времени» . Метаболизм и распределение лекарств . 37 (1). Американское общество фармакологии и экспериментальной терапии : 32–40. дои : 10.1124/dmd.108.023598 . ПМИД 18838504 . S2CID 5150289 . Проверено 7 ноября 2010 г.
- ^ Бок К., Кёле С. (2005). «UDP-глюкуронозилтрансфераза 1A6: структурные, функциональные и регуляторные аспекты». Ферменты конъюгации фазы II и транспортные системы . Методы энзимологии. Том. 400. стр. 57–75. дои : 10.1016/S0076-6879(05)00004-2 . ISBN 978-0-12-182805-9 . ПМИД 16399343 .
- ^ Jump up to: а б Таня С. Маккарти, Кристофер Дж. Синал (2005), «Биотрансформация», Энциклопедия токсикологии , том. 1 (2-е изд.), Elsevier, стр. 299–312, ISBN. 0-12-745354-7
- ^ Льюис С.С., Хатчинсон М.Р., Чжан Й., Хунд Д.К., Майер С.Ф., Райс К.К., Уоткинс Л.Р. (2013). «Глюкуроновая кислота и метаболит этанола этилглюкуронид вызывают активацию толл-подобного рецептора 4 и усиление боли» . Мозг, поведение и иммунитет . 30 : 24–32. дои : 10.1016/j.bbi.2013.01.005 . ПМК 3641160 . ПМИД 23348028 .
- ^ Блан П. (февраль 1996 г.). «Характеристика метаболитов чайного гриба». Письма о биотехнологиях . 18 (2): 139–142. дои : 10.1007/BF00128667 . S2CID 34822312 .
- ^ Герхард Михал, Дитмар Шомбург (2012), Биохимические пути: Атлас биохимии и молекулярной биологии (2-е изд.), Wiley, с. 145а, ISBN 978-0-470-14684-2