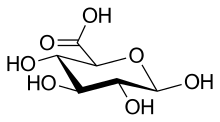
Глюкуроновая кислота
| |
| |
| Имена | |
|---|---|
| Имя IUPAC
β -d -глюкопирануроновая кислота
| |
| Систематическое имя IUPAC
(2 с , 3 с , 4 с , 5 r , 6 r ) -3,4,5,6-тетрагидроксиксан-2-карбоновая кислота | |
| Другие имена
β -d -глюкуроновая кислота, GLCA
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| Чеби | |
| Chemspider | |
| Наркоман | |
| Echa Infocard | 100.026.807 |
| Кегг | |
| Сетка | Глюкуронный+кислота |
PubChem CID
|
|
| НЕКОТОРЫЙ | |
Comptox Dashboard ( EPA )
|
|
| Характеристики | |
| C 6 H 10 O 7 | |
| Молярная масса | 194.139 g·mol −1 |
| Точка плавления | 159 до 161 ° C (от 318 до 322 ° F; от 432 до 434 К) [ 1 ] |
| Связанные соединения | |
Связанные уронические кислоты
|
Alluronic acid , Altruronic acid , Arabinuronic acid , Fructuronic acid , Galacturonic acid , Guluronic acid , Iduronic acid , Lyxuronic acid , Mannuronic acid , Psicuronic acid , Riburonic acid , Ribuluronic acid , Sorburonic acid , Tagaturonic acid , Taluronic acid , Xyluluronic acid , Xyluronic acid |
За исключением случаев, когда отмечены, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа).
| |
Глюкуроновая кислота (от греческого γλεῦκος « сладкое вино, должно » и ὖρον « моча ») - это уроновая кислота , которая была сначала изолирована от мочи (отсюда и название «Мороновая кислота»). Он обнаруживается во многих деснах , таких как Gumbricic ( около 18%), ксантхан и чай из Комбуча , и важен для метаболизма микроорганизмов, растений и животных.
Характеристики
[ редактировать ]В этом разделе нужны дополнительные цитаты для проверки . ( Март 2023 г. ) |

Глюкуроновая кислота представляет собой сахарную кислоту, полученную из глюкозы , с ее шестым атом углерода, окисленным до карбоновой кислоты. У живых существа это первичное окисление происходит с UDP-α- d- глюкозой (UDPG), а не со свободным сахаром.
Глюкуроновая кислота, как и ее предшественница , глюкоза , может существовать в виде линейной (карбобо-) альдогексозы (<1%) или в виде циклического гемиацетали ( фураноза или пиранозы ). Альдогесозы, такие как D -глюкоза, способны образовывать две фуранозные формы (α и β) и две пиранозные формы (α и β). По соглашению Фишера , глюкуроновая кислота имеет две стереоизомеры ( энантиомеры ), D -и L -глюкуроновую кислоту, в зависимости от ее конфигурации в C -5. Большинство физиологических сахаров имеют D -Конфигурацию. Из-за закрытия кольца циклические сахара имеют еще один асимметричный атом углерода (C-1), что приводит к еще двум стереоизомерам, названным Anomers . В зависимости от конфигурации в C-1 есть два аномера глюкуроновой кислоты, α- и β-формы. В β -D -глюкуроновой кислоте группа гидрокси C-1 находится на той же стороне пиранозного кольца, что и карбоксильная группа. В свободной сахарной кислоте β-форма распространена (~ 64%), тогда как в организме преобладает α-форма UDP-α- D- глюкуроновая кислота (UDPGA).
Углеводные стереоизомеры, которые различаются по конфигурации только в одном (другом) асимметричном C-атом, называются эпимерами . Например, d -маннороническая (C -2), D -аллуронная (C -3), D -галактуронная (C -4) и L -идуроновая кислота (C -5) являются эпимерами глюкуроновой кислоты.
Непланарные пиранозные кольца могут предположить либо стул (в 2 вариантах), либо конформацию лодки. Предпочтительная конформация зависит от пространственных помех или других взаимодействий заместителей. Пиранозная форма D -глюкозы и ее производной D -глюкуроновой кислоты предпочитают кресло 4 C 1 .
Дополнительное окисление при C-1 до уровня карбоксила дает дикарбоксильную глюкариновую кислоту . Глюкуронолактон -это самостоятельный ( лактон ) глюкуроновой кислоты.
Прямое окисление альдоза сначала влияет на группу альдегидов. Лабораторный синтез мороновой кислоты из альдозы требует защиты групп альдегида и гидрокси от окисления, например, путем превращения в циклические ацеталы (например, ацетониды ).
Глюкуронат натрия может продуцироваться путем прямого окисления крахмала концентрированной азотной кислотой. В этом препарате низкая доступность воды удерживает полимеры крахмала от гидролиза и окисляет только свободные гидроксилы, так же, как диоксид азота окисляет крахмал. Как только эта реакция завершена, и смесь крахмала/азотной кислоты становится прозрачной (из -за испускания газа диоксида азота), раствор может быть разбавлен и гидролизован другой минеральной кислотой. Затем окисление медленно гасит гидроксидом натрия (или бикарбонат натрия), образуя глюкуронат натрия, который может быть кристаллизован из раствора. С переходными металлами он образует такие комплексы, как глюкуронат железа (III) , глюкуронат железа (II) и глюкуронат меди (II) .
Функции
[ редактировать ]Протеогликаны
[ редактировать ]Глюкуроновая кислота является общим строительным блоком протеогликанов и гликоглицерипидов : [ Цитация необходима ]
- Гепарин является ингибитором коагуляции крови и встречается в тучных клетках, легких и печени.
- Хонруитинсульфат обнаруживается в больших количествах в хряще, аорте, соединительной ткани, кости и коже.
- Дерматан сульфат является протеогликаном в коже, сердце и кровеносных сосудах.
- Кератан сульфат встречается в роговице, хряще и кости.
- Гиалуроновая кислота встречается в больших количествах в соединительных тканях, коже, хряще и синовиальной жидкости.
- Гликоглицеролипиды глюкуронических или галактуроновых кислот образуют клеточные стенки бактерий.
Глюкуронидация
[ редактировать ]
UDP -α -D -глюкуроновая кислота (UDPGA) часто участвует в метаболизме фазы II ( конъюгация ) липофильных ксено и эндобиотиков . Эти связи включают гликозидные связи с группами тиола, амина и гидрокси или этерификации с карбоксильными и гидроксильными группами. Этот процесс сцепления известен как глюкуронидация (или конъюгация глюкуронида). Глюкуронидирование встречается в основном в печени, хотя ферменты, ответственные за его катализ, были обнаружены UDP-глюкуронилтрансферазы (UDP-GT), были обнаружены во всех основных органах тела, например, кишечника, почек, мозга, надпочечниц, селезенки и тимуса. [ 2 ] [ 3 ] Аналогичные реакции встречаются с другими UDP -уроническими кислотами (например, D -галактуроновая кислота ).
Гликозиды, возникающие в результате глюкуронидации, называются β -d -глюкуронидами, его соли и сложные эфиры называются глюкуронатами. Человеческое тело использует глюкуронидирование для изготовления спиртов , фенолов , карбоновых кислот , мерканедов , первичных и вторичных алифатических аминов и карбаматов более растворимыми в воде, и, таким образом из печени) с значительно повышенной скоростью. Карбоксильная группа ионизирована при физиологическом pH, что делает сопряженное соединение водорастворимым. Соединения с молекулярными массами> 60 000 слишком велики для выведения почек и будут выводиться с желтой в кишечник. Новороты дефицит в этой конъюгирующей системе, что делает их особенно уязвимыми для препаратов, таких как хлорамфеникол , который инактивируется добавлением глюкуроновой кислоты, что приводит к синдрому серого ребенка . Билирубин выделяется в желчи, как билирубин диглукуронид (80%), глюкуронид билирубина (20%) и неконъюгированный билирубин (<1%). В Синдром Криглера -Наджар и синдром Гилберта , активность UDPGT снижается или почти отсутствует из -за мутаций, что приводит к желтухи .
Можно исчерпать поставку тела глюкуроновой кислоты, объединив несколько лекарств/веществ, метаболизм и экскреция, в первую очередь или полностью зависят от глюкуронидации. Хотя большинство таких веществ имеют вторичные метаболические маршруты, которые становятся заметными после истощения GCA, скорость метаболизма достаточно снижается, чтобы получить заметное накопление всех субстратов GCA в системе; Это часто увеличивает концентрации лекарств в крови за счет с медицинской точки зрения. В наиболее тяжелых случаях известно, что постоянное и изнурительное повреждение органов (особенно печень, почки, сердце и мозг) и даже смерть. Этанол , морфин , парацетамол (ацетаминофен) , ингибиторы циклооксигеназы ( НПВП ), эндогенные стероиды и некоторые бензодиазепины способны способствовать истощению GCA, причем этанол и ацетаминофы наиболее подвержены веществам, вовлеченными в случаи случайных переводов, которые были проживающими, которые были проживающими. приписывается глюкуроновой кислоте истощение.
Чрезмерное количество GCA также может быть опасно для здоровья [ Цитация необходима ] Полем табачный дым, большинство барбитуратов Известно, что и некоторых карбаматов фактически стимулируют выработку GCA. Повышенная активность GCA приводит к снижению концентрации и метаболического периода полураспада субстратов глюкуроновой кислоты, вызывая плазму уровни глюкуронидированных препаратов падать ниже их терапевтического порога. Чрезмерное глюкуронидирование субстратов может привести к неадекватному ответу на традиционные дозы пораженных препаратов и, если препарат не имеет очень широкого терапевтического индекса, обычно приведет к острой неудаче фармакотерапии и потребует перехода от одного или нескольких влиятельных препаратов к препаратам к препаратам к препаратам к препаратам к препаратам к препаратам. эквивалентный режим не глюкуронидированных альтернатив. Избранное количество антидепрессантов и широкий спектр антипсихотических агентов-это лиганды глюкуронидации, но из-за их отсроченного механизма действия и фармакокинетических свойств снижение их концентраций в плазме не может быть сразу очевидным и имеет тенденцию представлять в качестве внезапного и интенсивного рецидива. симптомов вместо постепенной регрессии к поведению и моделям мышления, проявляемым пациентом до начала их фармакологического лечения.
Глюкурониды могут гидролизоваться присутствующей β-глюкуронидазой, в микрофлоре кишечника в соответствующий агликон, который может быть реабсорбирован из кишечника и перемещен в печень с кровью. Полученный цикл называется энтерогепатической циркуляцией . Соединения, которые подвергаются энтерогепатической циркуляции, только медленно выделяются и обычно имеют более длительный период полураспада в организме.
Некоторые глюкурониды являются электрофильными и могут функционировать в токсирования процессах . Известно, что ковалентное связывание агликоновых участков нескольких глюкуронидов карбоновой кислоты (сложная эфир) встречается с нуклеофильными участками на сывороточном альбумине посредством транс -ацилирования реакций. [ 4 ]
Фенолы , количественно важные метаболиты P450 ароматических углеводородов, являются субстратами как для UDP -GT, так и для сульфотрансфераз . Глюкурониды преобладают фенолом или предшественником фенола ( бензол ) у млекопитающих, потому что образование сульфата представляет собой систему с низкой аффинностью с низкой емкость Полем [ 4 ]
Роль в болезнях
[ редактировать ]Глюкуроновая кислота, а также глюкуронидированный метаболит этанола , этил глюкуронид (ETG), действуйте на рецептор, похожий на Toll, усугублять как острые, так и хронические воспалительные состояния, а также увеличение воспринимаемого тяжести боли у пациентов с хроническими заболеваниями, с помощью заболеваний с помощью заболеваний с помощью заболеваний с помощью хронических боль Повышенная регуляция продукции и высвобождения эндогенных воспалительных сигнальных молекул в организме. Долгосрочный агонизм рецептора TLR4 (например, то, что происходит от GCA, ETG и опиатов ), приводит к тому, что хронически болезненные состояния воспринимаются как значительно более тяжелые, чем они делали ранее, в то время как ранее существовавшие терпимые, но иногда болезненные действия могут стать более болезненными более болезненными, могут стать более болезненными более болезненными, чем ранее чем раньше, и начнет усугубляться, и менее физически требовательными действиями. Это также может вызвать одинаково болезненные реакции на снижение вредных (раздражающих) стимулов, в конечном итоге приводя к значительной агонии от стимулов, которые не вызывают никакой боли для большинства людей. [ 5 ]
Использовать
[ редактировать ]Определение мочевых стероидов и стероидных конъюгатов в крови. Этиллюкуронид и этилсульфат выделяются в моче в качестве метаболитов этанола и используются для мониторинга употребления спирта или зависимости.
Глюкуроновая кислота и глюконовая кислота являются ферментации продуктами в чай в чай . [ 6 ]
Глюкуроновая кислота является предшественником аскорбиновой кислоты ( витамин С , ранее называемой L-гексуроновой кислотой). Аскорбат может быть биосинтезирован более высокими растениями, водорослями, дрожжами и большинством животных. Взрослый козел производит ~ 13 г витамина С в день. Эта способность отсутствует у некоторых млекопитающих (включая людей и морских свинок), а также у насекомых, беспозвоночных и большинства рыб. Эти виды требуют внешнего аскорбатного снабжения, потому что им не хватает биосинтетического фермента L - Глулонолактон оксидазы . [ 7 ]
Глюкуронид 4-метилумбеллиферил-β- d -глюкуронид (кружка) используется для проверки наличия Escherichia coli . E. coli продуцирует фермент β-глюкуронидазу, которая гидролизует молекулу кружки в флуоресцентный продукт, который обнаруживается при ультрафиолетовом свете .
Смотрите также
[ редактировать ]Ссылки
[ редактировать ]- ^ D-глюкуроновая кислота в Sigma-Aldrich
- ^ Ohno S, Nakajin, Shizuo (2008-10-06). «Определение экспрессии мРНК UDP-глюкуронозилтрансферазы человека и применение для локализации в различных тканях человека с помощью обратной транскриптазы-полимеразной цепной реакции в реальном времени» . Метаболизм и расположение наркотиков . 37 (1). Американское общество фармакологии и экспериментальной терапии : 32–40. doi : 10.1124/dmd.108.023598 . PMID 18838504 . S2CID 5150289 . Получено 2010-11-07 .
- ^ Bock K, Köhle C (2005). «UDP-глюкуронозилтрансфераза 1A6: структурные, функциональные и регуляторные аспекты». Фаза II конъюгационные ферменты и транспортные системы . Методы в фермере. Тол. 400. С. 57–75. doi : 10.1016/s0076-6879 (05) 00004-2 . ISBN 978-0-12-182805-9 Полем PMID 16399343 .
- ^ Jump up to: а беременный Таня С Маккарти, Кристофер Дж. Синал (2005), «Биотрансформация», Энциклопедия токсикологии , вып. 1 (2 -е изд.), Elsevier, с. 299–312, ISBN 0-12-745354-7
- ^ Льюис С.С., Хатчинсон М.Р., Чжан Ю., Хунд Д.К., Майер С.Ф., Райс К.С., Уоткинс Л.Р. (2013). «Глюкуроновая кислота и метаболит этанол этил-глюкуронид вызывают активацию рецептора 4 и усиливают боль» . Мозг, поведение и иммунитет . 30 : 24–32. doi : 10.1016/j.bbi.2013.01.005 . PMC 3641160 . PMID 23348028 .
- ^ Blanc P (февраль 1996 г.). «Характеристика метаболитов чайного гриба». Биотехнологические письма . 18 (2): 139–142. doi : 10.1007/bf00128667 . S2CID 34822312 .
- ^ Gerhard Michal, Dietmar Schomburg (2012), Биохимические пути: атлас биохимии и молекулярной биологии (2 -е изд.), Wiley, p. 145a, ISBN 978-0-470-14684-2