Стимулятор генов интерферона
| СТИНГ1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Псевдонимы | STING1 , ERIS, MITA, MPYS, NET23, SAVI, STING, hMITA, hSTING, Стимулятор генов интерферона, трансмембранный белок 173, STING-бета, TMEM173, стимулятор интерферонового ответа, интерактор cGAMP 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Внешние идентификаторы | Опустить : 612374 ; МГИ : 1919762 ; Гомологен : 18868 ; GeneCards : STING1 ; OMA : STING1 — ортологи | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Викиданные | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
Стимулятор генов интерферона ( STING ), также известный как трансмембранный белок 173 ( TMEM173 ) и MPYS / MITA / ERIS — белок , который у человека кодируется геном STING1 . [5]
ЖАЛО играет важную роль во врожденном иммунитете . STING индуцирует выработку интерферона I типа , когда клетки инфицированы внутриклеточными патогенами, такими как вирусы , микобактерии и внутриклеточные паразиты . [6] Интерферон I типа , опосредованный STING, защищает инфицированные клетки и близлежащие клетки от местного заражения, связываясь с той же клеткой, которая его секретирует ( аутокринная передача сигналов), и близлежащими клетками ( паракринная передача сигналов). Таким образом, он играет важную роль, например, в контроле норовирусная инфекция. [7]
STING работает как прямой цитозольный ДНК-сенсор (CDS), так и белок-адаптер в передаче сигналов интерферона I типа посредством различных молекулярных механизмов. Было показано, что он активирует нижестоящие факторы транскрипции STAT6 и IRF3 через TBK1 , которые отвечают за противовирусный ответ и врожденный иммунный ответ против внутриклеточного патогена . [8]
Структура
[ редактировать ]
Аминокислоты 1–379 человеческого STING включают 4 трансмембранные области (TM) и С-концевой домен . ( С-концевой домен CTD: аминокислоты 138–379) содержит домен димеризации (DD) и карбокси-концевой хвост (CTT: аминокислоты 340–379). [8]
ЖАЛО образует в клетке симметричный димер. Димер STING напоминает бабочку с глубокой щелью между двумя протомерами. Гидрофобные . остатки каждого протомера STING образуют гидрофобные взаимодействия между собой на границе раздела [8] [9]
Выражение
[ редактировать ]STING экспрессируется в гемопоэтических клетках периферических лимфоидных тканей , включая Т-лимфоциты , NK-клетки , миелоидные клетки и моноциты . Также было показано, что STING высоко экспрессируется в легких, яичниках , сердце, гладких мышцах , сетчатке , костном мозге и влагалище. [10] [11]
Локализация
[ редактировать ]Субклеточная локализация STING была выяснена как белок эндоплазматической сети . Кроме того, вполне вероятно, что STING ассоциируется в непосредственной близости с митохондриально-ассоциированной мембраной ЭР (МАМ) - границей раздела между митохондриями и ЭР. [12] Во время внутриклеточной инфекции STING способен перемещаться из эндоплазматического ретикулума в перинуклеарные везикулы, потенциально участвующие в транспорте, опосредованном экзоцистами . [12] Также было показано, что STING колокализуется с белками аутофагии, легкой цепью 3 белка 1, ассоциированного с микротрубочками (LC3), и белком 9A, связанным с аутофагией , после стимуляции двухцепочечной ДНК, что позволяет предположить его присутствие в аутофагосоме . [13]
Функция
[ редактировать ]STING опосредует выработку интерферона I типа в ответ на внутриклеточную ДНК и различные внутриклеточные патогены, включая вирусы , внутриклеточные бактерии и внутриклеточные паразиты . [14] При заражении STING из инфицированных клеток может ощущать присутствие нуклеиновых кислот внутриклеточных патогенов, а затем индуцировать выработку интерферона β и более 10 форм интерферона α . Интерферон I типа, продуцируемый инфицированными клетками, может находить и связываться с рецепторами интерферона-альфа/бета близлежащих клеток, защищая клетки от местной инфекции.
Противовирусный иммунитет
[ редактировать ]STING вызывает мощный иммунитет к интерферону I типа против вирусной инфекции. После проникновения вируса вирусные нуклеиновые кислоты присутствуют в цитозоле инфицированных клеток. Некоторые ДНК-сенсоры, такие как DAI , РНК-полимераза III , IFI16 , DDX41 и cGAS , могут обнаруживать чужеродные нуклеиновые кислоты . После распознавания вирусной ДНК сенсоры ДНК инициируют последующие сигнальные пути, активируя STING-опосредованный интерфероновый ответ. [15]
Было показано, что аденовирус , вирус простого герпеса , ВПГ-1 и ВПГ-2, а также вирус с отрицательной цепью РНК , вирус везикулярного стоматита (ВВС), способны активировать STING-зависимый врожденный иммунный ответ . [14]
Дефицит STING у мышей привел к летальной восприимчивости к инфекции HSV-1 из-за отсутствия успешного ответа интерферона I типа. [16]
Точечная мутация серина-358 ослабляет активацию STING-IFN у летучих мышей и, как предполагается, дает летучим мышам способность служить резервуарными хозяевами. [17]
Против внутриклеточных бактерий
[ редактировать ]внутриклеточные бактерии Listeria monocytogenes стимулируют иммунный ответ хозяина посредством STING. Было показано, что [18] STING может играть важную роль в выработке хемокинов MCP-1 и CCL7 . Моноциты с дефицитом STING по своей природе неспособны мигрировать в печень во время инфекции Listeria monocytogenes . Таким образом, STING защищает хозяина от инфекции Listeria monocytogenes , регулируя миграцию моноцитов . Активация STING, вероятно, опосредуется циклическим ди-АМФ, секретируемым внутриклеточными бактериями. [18] [19]
Другой
[ редактировать ]STING может быть важной молекулой для защитного иммунитета против инфекционных организмов. Например, животные, которые не могут выражать STING, более восприимчивы к инфекции, вызываемой VSV , HSV-1 и Listeria monocytogenes , что позволяет предположить ее потенциальную связь с инфекционными заболеваниями человека. [20]
Роль в иммунитете хозяина
[ редактировать ]Хотя IFN типа I абсолютно необходим для устойчивости к вирусам, появляется все больше литературы о негативной роли интерферона I типа в иммунитете хозяина, опосредованном STING. Было показано , что богатый АТ мотив ДНК «стебель-петля» в геноме Plasmodium falciparum и Plasmodium berghei, а также внеклеточная ДНК Mycobacterium Tuberculosis активирует интерферон I типа посредством STING. [21] [22] Перфорация мембраны фагосомы, опосредованная системой секреции ESX1, позволяет внеклеточной микобактериальной ДНК получить доступ к цитозольным ДНК-сенсорам хозяина, тем самым индуцируя выработку интерферона I типа в макрофагах. Высокая сигнатура интерферона I типа приводит к патогенезу туберкулеза и длительному инфицированию. [22] , опосредованная STING-TBK1-IRF, Реакция интерферона I типа занимает центральное место в патогенезе экспериментальной церебральной малярии у лабораторных животных, инфицированных Plasmodium berghei . Лабораторные мыши с дефицитом реакции интерферона I типа устойчивы к экспериментальной церебральной малярии. [21]
Сигнальные механизмы STING
[ редактировать ]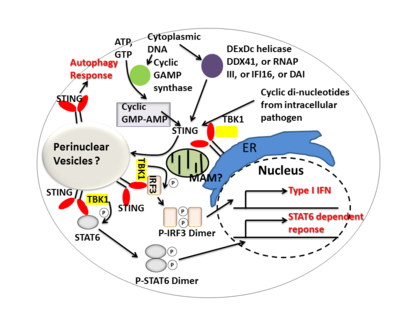
STING опосредует иммунный ответ на интерферон I типа , действуя как прямой сенсор ДНК, так и сигнальный адаптерный белок . После активации STING стимулирует активность TBK1 фосфорилировать IRF3 или STAT6 . Фосфорилированные IRF3 и STAT6 димеризуются, а затем проникают в ядро, чтобы стимулировать экспрессию генов, участвующих в иммунном ответе хозяина, таких как IFNB , CCL2 , CCL20 и т. д. [8] [23]
В нескольких отчетах предполагается, что STING связан с активацией селективной аутофагии. [13] микобактерии туберкулеза Было показано, что продуцируют цитозольные ДНК-лиганды, которые активируют STING, что приводит к убиквитинированию бактерий и последующему привлечению белков, связанных с аутофагией , все из которых необходимы для «селективного» аутофагического нацеливания и врожденной защиты от M.tuberculosis . [24]
Таким образом, STING координирует множественные иммунные ответы на инфекцию, включая индукцию интерферонов и STAT6-зависимый ответ, а также селективный ответ аутофагии. [8]
В качестве цитозольного сенсора ДНК
[ редактировать ]Циклические динуклеотиды - сигнальные молекулы второго мессенджера, продуцируемые различными видами бактерий, были обнаружены в цитозоле клеток млекопитающих при внутриклеточной инфекции патогена; это приводит к активации TBK1 - IRF3 и последующей выработке интерферона I типа . [8] [25] Было показано, что STING напрямую связывается с циклическим ди-ГМФ , и это узнавание приводит к выработке цитокинов , таких как интерферон I типа , которые необходимы для успешной элиминации патогена. [26]
В качестве сигнального адаптера
[ редактировать ]DDX41 , член семейства геликаз DEXDc, в миелоидных дендритных клетках распознает внутриклеточную ДНК и опосредует врожденный иммунный ответ посредством прямой ассоциации с STING. [27] другие ДНК-сенсоры — DAI , РНК-полимераза III , IFI16 — активируют STING посредством прямых или непрямых взаимодействий. Было показано, что [15]
Циклическая GMP-AMP-синтаза (cGAS), принадлежащая к семейству нуклеотидилтрансфераз, способна распознавать содержимое цитозольной ДНК и индуцировать STING-зависимый интерфероновый ответ, продуцируя вторичный мессенджер циклический гуанозинмонофосфат-аденозинмонофосфат (циклический GMP-AMP или cGAMP). После циклическим GMP-AMP активации STING, связанного с IRF3 , он усиливает активность TBK1 по фосфорилированию и STAT6 для последующего ответа интерферона I типа . [28] [29]
Было высказано предположение, что внутриклеточный кальций играет важную роль в ответе пути STING. [30]
См. также
[ редактировать ]- Агонист STING – компонент врожденной иммунной системы.
Ссылки
[ редактировать ]- ^ Jump up to: а б с ENSG00000288243 GRCh38: выпуск Ensembl 89: ENSG00000184584, ENSG00000288243 — Ensembl , май 2017 г.
- ^ Jump up to: а б с GRCm38: выпуск Ensembl 89: ENSMUSG00000024349 – Ensembl , май 2017 г.
- ^ «Ссылка на Human PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ «Ссылка на Mouse PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ «STING1 стимулятор интерферонового ответа, интерактор 1 cGAMP [Homo sapiens (человек)]» .
- ^ Нахаи П., Хискотт Дж., Лин Р. (июнь 2010 г.). «УЖАЛЕНИЕ противовирусного пути» . Журнал молекулярно-клеточной биологии . 2 (3): 110–2. дои : 10.1093/jmcb/mjp048 . ПМИД 20022884 .
- ^ Нью П., Мяо З., Ли Ю., Бансал Р., Пеппеленбош, член парламента, Пан К. (2021). «cGAS-STING эффективно ограничивает мышиную норовирусную инфекцию, но противодействует противовирусному действию N-конца RIG-I в мышиных макрофагах» . Кишечные микробы . 13 (1): 1959839. doi : 10.1080/19490976.2021.1959839 . ISSN 1949-0976 . ПМЦ 8344765 . ПМИД 34347572 .
- ^ Jump up to: а б с д и ж Бердетт Д.Л., Вэнс Р.Э. (январь 2013 г.). «ЖАЛО и врожденный иммунный ответ на нуклеиновые кислоты в цитозоле». Природная иммунология . 14 (1): 19–26. дои : 10.1038/ni.2491 . ПМИД 23238760 . S2CID 7968532 .
- ^ Шу С., Йи Джи, Уоттс Т., Као CC, Ли П. (июль 2012 г.). «Структура STING, связанного с циклическим ди-ГМФ, раскрывает механизм распознавания циклических динуклеотидов иммунной системой» . Структурная и молекулярная биология природы . 19 (7): 722–4. дои : 10.1038/nsmb.2331 . ПМЦ 3392545 . ПМИД 22728658 .
- ^ «Профиль экспрессии EST TMEM173» . биогпс орг . biogps.org.
- ^ «ГЕОпрофиль выражения NCBI TMEM173» . НКБИ . www.ncbi.nlm.nih.gov/geoprofiles.
- ^ Jump up to: а б Исикава Х., Барбер Г.Н. (октябрь 2008 г.). «STING — это адаптер эндоплазматической сети, который облегчает передачу сигналов врожденного иммунитета» . Природа . 455 (7213): 674–8. Бибкод : 2008Natur.455..674I . дои : 10.1038/nature07317 . ПМК 2804933 . ПМИД 18724357 .
- ^ Jump up to: а б Сайто Т., Фудзита Н., Хаяси Т., Такахара К., Сато Т., Ли Х., Мацунага К., Кагеяма С., Омори Х., Нода Т., Ямамото Н., Каваи Т., Исии К., Такеучи О., Ёсимори Т., Акира С. (декабрь 2009 г.) ). «Atg9a контролирует управляемую дцДНК динамическую транслокацию STING и врожденный иммунный ответ» . Труды Национальной академии наук Соединенных Штатов Америки . 106 (49): 20842–6. Бибкод : 2009PNAS..10620842S . дои : 10.1073/pnas.0911267106 . ПМК 2791563 . ПМИД 19926846 .
- ^ Jump up to: а б Барбер Г.Н. (февраль 2011 г.). «Пути восприятия ДНК врожденного иммунитета: STING, AIMII и регуляция выработки интерферона и воспалительных реакций» . Современное мнение в иммунологии . 23 (1): 10–20. дои : 10.1016/j.coi.2010.12.015 . ПМЦ 3881186 . ПМИД 21239155 .
- ^ Jump up to: а б Китинг С.Э., Бэран М., Боуи А.Г. (декабрь 2011 г.). «Цитозольные ДНК-сенсоры, регулирующие индукцию интерферона I типа» (PDF) . Тенденции в иммунологии . 32 (12): 574–81. дои : 10.1016/j.it.2011.08.004 . hdl : 2262/68041 . ПМИД 21940216 .
- ^ Ма З., Дамания Б. (февраль 2016 г.). «Путь защиты cGAS-STING и его противодействие вирусам» . Клетка-хозяин и микроб . 19 (2): 150–8. дои : 10.1016/j.chom.2016.01.010 . ПМЦ 4755325 . ПМИД 26867174 .
- ^ Се Дж, Ли Ю, Шен Х, Гот Г, Чжу Ю, Цуй Дж, Ван Л, Ши З, Чжоу П (март 2018 г.). «Подавленная STING-зависимая активация интерферона у летучих мышей» . Клетка-хозяин и микроб . 23 (3): 297–301.е4. дои : 10.1016/j.chom.2018.01.006 . ПМК 7104992 . ПМИД 29478775 .
- ^ Jump up to: а б Джин Л., Гетахун А., Ноулз Х.М., Моган Дж., Акерлунд Л.Дж., Паккард Т.А., Перро А.Л., Камбье Дж.К. (март 2013 г.). «STING/MPYS опосредует защиту хозяина от инфекции Listeria monocytogenes, регулируя миграцию моноцитов Ly6C(hi)» . Журнал иммунологии . 190 (6): 2835–43. doi : 10.4049/jimmunol.1201788 . ПМЦ 3593745 . ПМИД 23378430 .
- ^ Вудворд Дж.Дж., Иавароне А.Т., Портной Д.А. (июнь 2010 г.). «c-ди-АМФ, секретируемый внутриклеточными Listeria monocytogenes, активирует ответ интерферона I типа хозяина» . Наука . 328 (5986): 1703–5. Бибкод : 2010Sci...328.1703W . дои : 10.1126/science.1189801 . ПМК 3156580 . ПМИД 20508090 .
- ^ Исикава Х., Ма З., Барбер Г.Н. (октябрь 2009 г.). «STING регулирует внутриклеточный ДНК-зависимый интерферон-зависимый врожденный иммунитет» . Природа . 461 (7265): 788–92. Бибкод : 2009Natur.461..788I . дои : 10.1038/nature08476 . ПМЦ 4664154 . ПМИД 19776740 .
- ^ Jump up to: а б Шарма С., ДеОливейра Р.Б., Калантари П., Паррош П., Гутаньи Н., Цзян З., Чан Дж., Бартоломеу Д.К., Лау Ф., Холл Дж.П., Барбер Г.Н., Газзинелли Р.Т., Фицджеральд К.А., Голенбок Д.Т. (август 2011 г.). «Врожденное иммунное распознавание богатого АТ мотива ДНК «стебель-петля» в геноме Plasmodium falciparum» . Иммунитет . 35 (2): 194–207. doi : 10.1016/j.immuni.2011.05.016 . ПМК 3162998 . ПМИД 21820332 .
- ^ Jump up to: а б Мансанильо П.С., Шайло М.Ю., Портной Д.А., Кокс Дж.С. (май 2012 г.). «Микобактерия туберкулеза активирует ДНК-зависимый путь цитозольного надзора внутри макрофагов» . Клетка-хозяин и микроб . 11 (5): 469–80. дои : 10.1016/j.chom.2012.03.007 . ПМЦ 3662372 . ПМИД 22607800 .
- ^ Чен Х, Сунь Х, Ю Ф, Сунь В, Чжоу Х, Чэнь Л, Ян Дж, Ван Ю, Тан Х, Гуань Ю, Ся В, Гу Дж, Исикава Х, Гутман Д, Барбер Дж, Цинь Цзи, Цзян Цзи (октябрь 2011 г.). «Активация STAT6 с помощью STING имеет решающее значение для врожденного противовирусного иммунитета» . Клетка . 147 (2): 436–46. дои : 10.1016/j.cell.2011.09.022 . ПМИД 22000020 .
- ^ Уотсон Р.О., Мансанильо П.С., Кокс Дж.С. (август 2012 г.). «Внеклеточная ДНК M. Tuberculosis нацелена на бактерии для аутофагии, активируя путь восприятия ДНК хозяина» . Клетка . 150 (4): 803–15. дои : 10.1016/j.cell.2012.06.040 . ПМЦ 3708656 . ПМИД 22901810 .
- ^ МакВиртер С.М., Барбалат Р., Монро К.М., Фонтана М.Ф., Хиодо М., Джонкер Н.Т., Исии К.Дж., Акира С., Колонна М., Чен З.Дж., Фицджеральд К.А., Хаякава Ю., Вэнс Р.Э. (август 2009 г.). «Реакция интерферона типа I хозяина индуцируется цитозольным восприятием бактериального вторичного мессенджера циклического ди-ГМФ» . Журнал экспериментальной медицины . 206 (9): 1899–911. дои : 10.1084/jem.20082874 . ПМЦ 2737161 . ПМИД 19652017 .
- ^ Бердетт Д.Л., Монро К.М., Сотело-Троха К., Ивиг Дж.С., Эккерт Б., Хёдо М., Хаякава Ю., Вэнс Р.Э. (октябрь 2011 г.). «СТИНГ — это прямой врожденный иммунный сенсор циклического ди-ГМФ» . Природа . 478 (7370): 515–8. Бибкод : 2011Natur.478..515B . дои : 10.1038/nature10429 . ПМК 3203314 . ПМИД 21947006 .
- ^ Чжан Цз, Юань Б, Бао М, Лу Н, Ким Т, Лю Юй Джей (октябрь 2011 г.). «Геликаза DDX41 распознает внутриклеточную ДНК, опосредованную адаптером STING в дендритных клетках» . Природная иммунология . 12 (10): 959–65. дои : 10.1038/ni.2091 . ПМЦ 3671854 . ПМИД 21892174 .
- ^ Ву Дж, Сунь Л, Чен X, Ду Ф, Ши Х, Чен С, Чен ZJ (февраль 2013 г.). «Циклический GMP-AMP является эндогенным вторичным мессенджером в передаче сигналов врожденного иммунитета с помощью цитозольной ДНК» . Наука . 339 (6121): 826–30. Бибкод : 2013Sci...339..826W . дои : 10.1126/science.1229963 . ПМЦ 3855410 . ПМИД 23258412 .
- ^ Сунь Л, Ву Дж, Ду Ф, Чен X, Чен ZJ (февраль 2013 г.). «Циклическая GMP-AMP-синтаза представляет собой цитозольный сенсор ДНК, который активирует путь интерферона I типа» . Наука . 339 (6121): 786–91. Бибкод : 2013Sci...339..786S . дои : 10.1126/science.1232458 . ПМЦ 3863629 . ПМИД 23258413 .
- ^ Ким С., Кох П., Ли Л., Пешкин Л., Митчисон Т.Дж. (4 июня 2017 г.). «Доказательства роли кальция в передаче сигналов STING». bioRxiv 10.1101/145854 .
Дальнейшее чтение
[ редактировать ]- Ван Ю, Тонг Икс, Омореги Э.С., Лю В., Мэн С., Йе Икс (октябрь 2012 г.). «Тетраспанин 6 (TSPAN6) отрицательно регулирует индуцируемую ретиноевой кислотой передачу иммунных сигналов, опосредованную геном I-подобным рецептором, убиквитин-зависимым способом» . Журнал биологической химии . 287 (41): 34626–34. дои : 10.1074/jbc.M112.390401 . ПМЦ 3464568 . ПМИД 22908223 .
- Инь Ц, Тянь Ю, Кабалисваран В, Цзян Х, Ту Д, Эк МДж, Чен ЗДж, Ву Х (июнь 2012 г.). «Циклическое определение ди-ГМФ через врожденный иммунный сигнальный белок STING» . Молекулярная клетка . 46 (6): 735–45. doi : 10.1016/j.molcel.2012.05.029 . ПМЦ 3697849 . ПМИД 22705373 .
- Агирре С., Маэстре А.М., Паньи С., Патель Дж.Р., Сэвидж Т., Гутман Д., Маринджер К., Бернал-Рубио Д., Шабман Р.С., Саймон В., Родригес-Мадос Дж.Р., Малдер Л.С., Барбер Г.Н., Фернандес-Сесма А. (2012) . «DENV ингибирует выработку IFN типа I в инфицированных клетках путем расщепления человеческого STING» . ПЛОС Патогены . 8 (10): e1002934. дои : 10.1371/journal.ppat.1002934 . ПМЦ 3464218 . ПМИД 23055924 .
- Ли Ю, Ли С, Сюэ П, Чжун Б, Мао А. П., Ран Ю, Чен Х, Ван Ю, Ян Ф, Шу Х. Б. (май 2009 г.). «ISG56 является регулятором отрицательной обратной связи, запускаемой вирусом, и клеточным противовирусным ответом» . Труды Национальной академии наук Соединенных Штатов Америки . 106 (19): 7945–50. Бибкод : 2009PNAS..106.7945L . дои : 10.1073/pnas.0900818106 . ПМЦ 2683125 . ПМИД 19416887 .
- Конлон Дж., Бердетт Д.Л., Шарма С., Бхат Н., Томпсон М., Цзян З., Ратинам В.А., Монкс Б., Джин Т., Сяо Т.С., Фогель С.Н., Вэнс Р.Э., Фицджеральд К.А. (май 2013 г.). «Мышь, но не человеческое STING, связывается и подает сигнал в ответ на агент, разрушающий сосуды, 5,6-диметилксантенон-4-уксусную кислоту» . Журнал иммунологии . 190 (10): 5216–25. doi : 10.4049/jimmunol.1300097 . ПМЦ 3647383 . ПМИД 23585680 .
- Абэ Т., Харашима А., Ся Т., Конно Х., Конно К., Моралес А., Ан Дж., Гутман Д., Барбер Г.Н. (апрель 2013 г.). «Распознавание цитоплазматической ДНК STING запускает клеточную защиту» . Молекулярная клетка . 50 (1): 5–15. doi : 10.1016/j.molcel.2013.01.039 . ПМЦ 3881179 . ПМИД 23478444 .
- Назми А., Мухопадьяй Р., Дутта К., Басу А. (2012). «STING опосредует врожденный иммунный ответ нейронов после заражения вирусом японского энцефалита» . Научные отчеты . 2 : 347. Бибкод : 2012NatSR...2E.347N . дои : 10.1038/srep00347 . ПМЦ 3317237 . ПМИД 22470840 .
- Чжан Дж., Ху М.М., Ван Ю.И., Шу Х.Б. (август 2012 г.). «Белок TRIM32 модулирует индукцию интерферона I типа и клеточный противовирусный ответ, нацеливаясь на белок MITA/STING для K63-связанного убиквитинирования» . Журнал биологической химии . 287 (34): 28646–55. дои : 10.1074/jbc.M112.362608 . ПМЦ 3436586 . ПМИД 22745133 .
- Исикава Х., Барбер Г.Н. (октябрь 2008 г.). «STING — это адаптер эндоплазматической сети, который облегчает передачу сигналов врожденного иммунитета» . Природа . 455 (7213): 674–8. Бибкод : 2008Natur.455..674I . дои : 10.1038/nature07317 . ПМК 2804933 . ПМИД 18724357 .



