Стрептококк пневмонии
| Стрептококк пневмонии | |
|---|---|
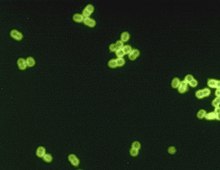 | |
| S. pneumoniae в спинномозговой жидкости. Морилка FA (цифровая окраска). | |
| Научная классификация | |
| Домен: | Бактерии |
| Тип: | Бациллота |
| Сорт: | Бациллы |
| Заказ: | лактобактерии |
| Семья: | Стрептококковые |
| Род: | Стрептококк |
| Разновидность: | С. пневмонии |
| Биномиальное имя | |
| Стрептококк пневмонии (Маленький 1884 г.) Честер 1901 г. | |
Streptococcus pneumoniae , или пневмококк , — грамположительные сферические бактерии, альфа-гемолитические представители рода Streptococcus . [1] Обычно они встречаются парами ( диплококки ), не образуют спор и неподвижны. [2] , являющаяся важной патогенной Бактерия S. pneumoniae для человека, была признана основной причиной пневмонии в конце 19 века и является предметом многих гуморального иммунитета . исследований [ нужна ссылка ]
Streptococcus pneumoniae бессимптомно обитает у здоровых носителей, обычно колонизируя дыхательные пути, пазухи и полость носа . Однако у восприимчивых людей с более слабой иммунной системой , таких как пожилые люди и маленькие дети, бактерия может стать патогенной и распространиться в другие места, вызывая заболевание. Он распространяется при прямом контакте от человека к человеку воздушно-капельным путем и при аутоинокуляции у лиц, несущих бактерии в верхних дыхательных путях. [3] Это может быть причиной неонатальных инфекций . [4]
Streptococcus pneumoniae является основной причиной внебольничной пневмонии и менингита у детей и пожилых людей. [5] и сепсиса у лиц, инфицированных ВИЧ . Этот организм также вызывает многие виды пневмококковых инфекций, помимо пневмонии . К таким инвазивным пневмококковым заболеваниям относятся бронхит , ринит , острый синусит , средний отит , конъюнктивит , менингит , сепсис, остеомиелит , септический артрит , эндокардит , перитонит , перикардит , целлюлит и абсцесс головного мозга . [6]

Streptococcus pneumoniae можно отличить от стрептококков viridans , некоторые из которых также являются альфа-гемолитическими , с помощью оптохинового теста, поскольку S. pneumoniae чувствителен к оптохину. S. pneumoniae также можно отличить по его чувствительности к лизису желчью . , так называемому «тесту на растворимость в желчи» Инкапсулированные бактерии грамположительные кокковидные имеют характерную морфологию при окраске по Граму — ланцетной диплококки формы. Они имеют полисахаридную капсулу, которая действует как фактор вирулентности для организма; более 100 различных серотипов известно , различающихся по вирулентности , распространенности и степени лекарственной устойчивости .
Капсулярный полисахарид (CPS) служит важным защитным механизмом против иммунной системы хозяина. Он составляет внешний слой инкапсулированных штаммов S. pneumoniae и обычно прикрепляется к пептидогликану клеточной стенки. [7] Он состоит из вязкого вещества, полученного из высокомолекулярного полимера, состоящего из повторяющихся олигосахаридных звеньев, связанных ковалентными связями с клеточной стенкой. Вирулентность и инвазивность различных штаммов S. pneumoniae различаются в зависимости от их серотипов, что определяется их химическим составом и количеством продуцируемого ими CPS. Вариации между различными S. pneumoniae штаммами существенно влияют на патогенез , определяя выживаемость бактерий и вероятность возникновения инвазивного заболевания. [8] Кроме того, CPS ингибирует фагоцитоз , предотвращая доступ гранулоцитов к клеточной стенке. [9]
История
[ редактировать ]В 1881 году был обнаружен микроорганизм, известный позже, в 1886 году, как пневмококк. [10] из-за его роли в причине пневмонии, был впервые выделен одновременно и независимо врачом армии США Джорджем Штернбергом. [11] и французский химик Луи Пастер . [12]
этот организм был назван Diplococcus pneumoniae. В 1920 году [13] из-за его характерного появления в , окрашенной по Граму мокроте . В 1974 году он был переименован в Streptococcus pneumoniae, поскольку был очень похож на стрептококки . [10] [14]
Streptococcus pneumoniae сыграл центральную роль в демонстрации того, что генетический материал состоит из ДНК . В 1928 году Фредерик Гриффит продемонстрировал трансформацию жизни, превратив безвредный пневмококк в смертельную форму, путем совместной инокуляции живых пневмококков мышам вместе с убитыми нагреванием вирулентными пневмококками. [15] В 1944 году Освальд Эйвери , Колин МакЛауд и Маклин Маккарти продемонстрировали, что преобразующим фактором в эксперименте Гриффита был не белок , как широко считалось в то время, а ДНК. [16] Работа Эйвери ознаменовала рождение молекулярной эры генетики . [17]
Генетика
[ редактировать ]Геном пар S. pneumoniae представляет собой замкнутую кольцевую структуру ДНК, содержащую от 2,0 до 2,1 миллиона оснований в зависимости от штамма . Его основной набор состоит из 1553 генов , плюс 154 гена в вируломе , которые способствуют вирулентности, и 176 генов, поддерживающих неинвазивный фенотип . Генетическая информация может варьироваться до 10% между штаммами. [18] Известно, что пневмококковый геном содержит большой и разнообразный репертуар антимикробных пептидов, включая 11 различных лантибиотиков . [19]
Трансформация
[ редактировать ]Естественная бактериальная трансформация включает перенос ДНК от одной бактерии к другой через окружающую среду. Трансформация — это сложный процесс развития, требующий энергии и зависящий от экспрессии многочисленных генов. У S. pneumoniae для трансформации требуется не менее 23 генов. Чтобы бактерия могла связать, принять и рекомбинировать экзогенную ДНК в свою хромосому , она должна войти в особое физиологическое состояние, называемое компетентностью . [20] Компетентность S. pneumoniae индуцируется агентами, повреждающими ДНК, такими как митомицин С , фторхинолоновые антибиотики ( норфлоксацин , левофлоксацин и моксифлоксацин ) и ингибиторы топоизомеразы . [21] Трансформация защищает S. pneumoniae от бактерицидного действия митомицина С. [22] Мишо и др. [23] обобщены доказательства того, что индукция компетентности у S. pneumoniae связана с повышенной устойчивостью к окислительному стрессу и повышенной экспрессией белка RecA, ключевого компонента механизма рекомбинационной репарации для устранения повреждений ДНК . На основании этих результатов они предположили, что трансформация — это адаптация для восстановления окислительных повреждений ДНК. Инфекция S. pneumoniae стимулирует полиморфно-ядерные лейкоциты (гранулоциты), вызывая окислительный взрыв, который потенциально смертелен для бактерий. Способность S. pneumoniae восстанавливать окислительные повреждения ДНК в своем геноме, вызванные этой защитой хозяина, вероятно, способствует вирулентности возбудителя. В соответствии с этой предпосылкой, Li et al. [24] сообщили, что среди различных высокотрансформируемых изолятов S. pneumoniae приспособленность к назальной колонизации и вирулентность (инфекционность легких) зависят от интактной компетентностной системы.
Инфекция
[ редактировать ]Streptococcus pneumoniae является частью нормальной верхних дыхательных путей флоры . иммунной системы хозяина Как и многие другие виды естественной флоры, он может стать патогенным при определенных условиях, обычно при подавлении . Инвазины , такие как пневмолизин , антифагоцитарная капсула , различные адгезины и иммуногенные компоненты клеточной стенки , являются основными факторами вирулентности . После того, как pneumoniae колонизирует воздушные мешочки легких S. , организм реагирует стимуляцией воспалительной реакции, вызывая заполнение альвеол плазмой, кровью и лейкоцитами. Это состояние называется бактериальной пневмонией. [25]
S. pneumoniae претерпевает спонтанные фазовые изменения , меняя фенотипы колоний между прозрачными и непрозрачными. Прозрачный фенотип имеет более тонкую капсулу и экспрессирует большое количество фосфорилхолина (ChoP) и холинсвязывающего белка А (CbpA), что способствует способности бактерий прикрепляться и колонизировать носоглотку. [26] Непрозрачный фенотип характеризуется более толстой капсулой, что приводит к повышенной устойчивости к выведению из организма хозяина. [26] Он экспрессирует большое количество капсульного и пневмококкового поверхностного белка А (PspA), который помогает бактериям выжить в крови. [27] Фазовая изменчивость между этими двумя фенотипами позволяет S. pneumoniae выживать в различных системах организма человека.
Болезни и симптомы
[ редактировать ]Пневмония является наиболее распространенным заболеванием, вызванным S. pneumoniae , которое включает такие симптомы, как лихорадка и озноб, кашель, учащенное дыхание, затрудненное дыхание и боль в груди. У пожилых людей они могут включать спутанность сознания, низкую концентрацию внимания и в меньшей степени предыдущие перечисленные симптомы. [ нужна ссылка ]
Пневмококковый менингит – это инфекция тканей, покрывающих головной и спинной мозг. Симптомы включают ригидность шеи, лихорадку, головную боль, спутанность сознания и светобоязнь . [ нужна ссылка ]
Сепсис вызывается подавляющей реакцией на инфекцию и приводит к повреждению тканей, недостаточности органов и даже смерти. Симптомы включают спутанность сознания, одышку, учащенное сердцебиение, боль или дискомфорт, повышенное потоотделение, лихорадку, дрожь или ощущение холода. [28]
Вакцина
[ редактировать ]Из-за важности заболевания, вызываемого S. pneumoniae несколько вакцин , было разработано для защиты от инвазивной инфекции. Всемирная организация здравоохранения рекомендует плановую вакцинацию детей от пневмококковой инфекции; [29] он включен в календарь прививок детей в ряде стран, включая Великобританию, [30] Соединенные Штаты, [31] Греция, [32] и Южная Африка. [33]
В настоящее время против S. pneumoniae доступны две вакцины: пневмококковая полисахаридная вакцина (PPV23) и пневмококковая конъюгированная вакцина (PCV13). PPV23 функционирует, используя CPS для стимуляции выработки типоспецифичных антител, инициируя такие процессы, как активация комплемента, опсонизация и фагоцитоз для борьбы с бактериальными инфекциями. Он вызывает гуморальный иммунный ответ, направленный на CPS, присутствующий на поверхности бактерий. [34] PPSV23 обеспечивает иммунитет, независимый от Т-клеток , и требует ревакцинации через 5 лет после первой вакцинации из-за ее временного характера. [35] PCV13 был разработан при определении его низкой эффективности у детей и младенцев. PCV13 вызывает Т-клеточно-зависимый ответ и обеспечивает стойкий иммунитет, способствуя взаимодействию между В- и Т-клетками, что приводит к усиленному и продолжительному иммунному ответу. [35]
Биотехнология
[ редактировать ]Компоненты S. pneumoniae нашли применение в различных сферах биотехнологии. Благодаря конструированию поверхностных молекул этой бактерии белки могут быть необратимо связаны с помощью сортазы . фермента [36] или используя реакцию SnoopTag/SnoopCatcher. [37] Различные гликозидгидролазы также были клонированы из S. pneumoniae, чтобы помочь в анализе клеточного гликозилирования . [38]
Взаимодействие с Haemophilus influenzae
[ редактировать ]Исторически Haemophilus influenzae была важной причиной инфекции, и как H. influenzae , так и S. pneumoniae можно обнаружить в верхних дыхательных путях человека. Исследование конкуренции in vitro показало, что S. pneumoniae одолела H. influenzae, атакуя его перекисью водорода . [39] Есть также свидетельства того, что S. pneumoniae использует перекись водорода в качестве фактора вирулентности. [40] Однако в исследовании, в котором обе бактерии были добавлены в полость мыши носовую в течение двух недель, только H. influenzae выжил ; дальнейший анализ показал, что нейтрофилы, подвергшиеся воздействию мертвого H. influenzae, были более агрессивны в атаке на S. pneumoniae . [41]
Диагностика
[ редактировать ]
Диагноз обычно ставится на основании клинического подозрения, а также положительного результата культуры из образца практически из любого места тела. S. pneumoniae , как правило, чувствителен к оптохину , хотя наблюдалась резистентность к оптохину. [42]
Последние достижения в области секвенирования нового поколения и сравнительной геномики позволили разработать надежные и надежные молекулярные методы обнаружения и идентификации S. pneumoniae . Например, ген Xisco недавно был описан как биомаркер для обнаружения S. pneumoniae с помощью ПЦР и дифференциации от близкородственных видов. [43]
Атроментин и лейкомелон обладают антибактериальной активностью, ингибируя фермент еноилацил-переносящую протеинредуктазу (необходимую для биосинтеза жирных кислот ) у S. pneumoniae . [44]
Сопротивление
[ редактировать ]Устойчивые штаммы пневмококков называются пенициллинрезистентными пневмококками ( PRP ). [45] пенициллинрезистентный Streptococcus pneumoniae ( PRSP ), [46] Streptococcus pneumoniae, устойчивый к пенициллину ( SPPR ) [47] или устойчивый к лекарствам Streptococcus pneumoniae ( DRSP ). В 2015 году в США было зарегистрировано около 30 000 случаев, и в 30% из них штаммы были устойчивы к одному или нескольким антибиотикам. [48]
См. также
[ редактировать ]- Трансформация (генетика)
- Совет экспертов по осведомленности о пневмококковой инфекции
- Факультативно-анаэробный организм
Ссылки
[ редактировать ]- ^ Райан К.Дж., Рэй К.Г., ред. (2004). Шеррис Медицинская микробиология . МакГроу Хилл. ISBN 978-0-8385-8529-0 .
- ^ «Стрептококк пневмонии» . microbewiki.kenyon.edu . Проверено 24 октября 2017 г.
- ^ "Передача инфекции" . cdc.org . Проверено 24 октября 2017 г.
- ^ Бауселс Б., Меркадаль Халли М., Альварес Санчес А., Фигерас Алой Дж. (2015). «Ассоциации пробиотиков для профилактики некротизирующего энтероколита и снижения позднего сепсиса и неонатальной смертности у недоношенных новорожденных с массой тела менее 1500 г: систематический обзор» . Анналы педиатрии . 85 (5): 247–255. дои : 10.1016/j.anpedi.2015.07.038 . ISSN 1695-4033 . ПМИД 26611880 .
- ^ ван де Бек Д., де Ганс Дж., Тункель А.Р., Вейдикс Э.Ф. (5 января 2006 г.). «Внебольничный бактериальный менингит у взрослых». Медицинский журнал Новой Англии . 354 (1): 44–53. дои : 10.1056/NEJMra052116 . ISSN 0028-4793 . ПМИД 16394301 .
- ^ Семенюк Р.А., Грегсон, Дэн Б., Гилл, М. Джон (ноябрь 2011 г.). «Сохраняющееся бремя инвазивной пневмококковой инфекции у пациентов с ВИЧ: наблюдательное когортное исследование» . БМК Инфекционные болезни . 11 : 314. дои : 10.1186/1471-2334-11-314 . ПМК 3226630 . ПМИД 22078162 .
- ^ Патон Х.К., Траппетти К. (12 апреля 2019 г.). Фишетти В.А., Новик Р.П., Ферретти Дж.Дж., Портной Д.А., Браунштейн М., Руд Дж.И. (ред.). «Капсулярный полисахарид Streptococcus pneumoniae» . Микробиологический спектр . 7 (2). doi : 10.1128/microbiolspec.GPP3-0019-2018 . ISSN 2165-0497 . ПМИД 30977464 .
- ^ Мораис В., Ди В., Суарес Н. (12 октября 2018 г.). «Очистка капсульных полисахаридов Streptococcus pneumoniae: традиционные и новые методы» . Границы биоинженерии и биотехнологии . 6 : 145. дои : 10.3389/fbioe.2018.00145 . ISSN 2296-4185 . ПМК 6194195 . ПМИД 30370268 .
- ^ Дион CF, Ashurst JV (2024 г.), «Streptococcus pneumoniae» , StatPearls , Остров сокровищ (Флорида): StatPearls Publishing, PMID 29261971 , получено 15 апреля 2024 г.
- ^ Перейти обратно: а б Плоткин С. , Оренштейн В. , Оффит П.А. (22 сентября 2012 г.). Вакцина . Эльзевир – Сондерс. п. 542 . ISBN 978-1-4557-0090-5 . Проверено 2 июля 2015 г.
- ^ Штернберг Г.М. (30 апреля 1881 г.). «Смертельная форма сепсиса у кроликов, вызванная подкожным введением человеческой слюны. Экспериментальное исследование». Бюллетень Национального совета здравоохранения . .
- ^ Пастор Л. (1881 г.). «О новом заболевании, вызванном слюной ребенка, умершего от бешенства». Доклады Парижской академии наук . 92 :159 .
- ^ Уинслоу, К., Дж. Бродхерст (1920). «Семейства и роды бактерий: заключительный отчет комитета Общества американских бактериологов по характеристике и классификации типов бактерий» . J Бактериол . 5 (3): 191–229. дои : 10.1128/JB.5.3.191-229.1920 . ПМЦ 378870 . ПМИД 16558872 .
- ^ Вайнер Х (2014). Медицинское освещение: использование фактических данных, визуализации и статистического мышления для улучшения здравоохранения . Издательство Оксфордского университета. п. 53 . ISBN 978-0-19-966879-3 . Проверено 4 июля 2015 г.
- ^ Гриффит Ф. (январь 1928 г.). «Значение типов пневмококков» . Журнал гигиены . 27 (2): 113–159. дои : 10.1017/S0022172400031879 . ПМК 2167760 . ПМИД 20474956 .
- ^ Эйвери ОТ, Маклауд СМ, Маккарти М (1944). «Исследование химической природы вещества, индуцирующего трансформацию пневмококков типа: индукция трансформации фракцией дезоксирибонуклеиновой кислоты, выделенной из пневмококка III типа» . Джей Эксп Мед . 79 (2): 137–158. дои : 10.1084/jem.79.2.137 . ПМК 2135445 . ПМИД 19871359 .
- ^ Ледерберг Дж. (1994). «Трансформация генетики с помощью ДНК: празднование юбилея Эйвери, Маклауда и Маккарти (1944)» . Генетика . 136 (2): 423–6. дои : 10.1093/генетика/136.2.423 . ПМЦ 1205797 . ПМИД 8150273 .
- ^ ван дер Полл Т., Опал С.М. (2009). «Патогенез, лечение и профилактика пневмококковой пневмонии». Ланцет . 374 (9700): 1543–56. дои : 10.1016/S0140-6736(09)61114-4 . ПМИД 19880020 . S2CID 28676845 .
- ^ Резаи Джаван Р., Ван Тондер А., Кинг Дж., Харролд С., Брюггеманн А. (август 2018 г.). «Секвенирование генома раскрывает большой и разнообразный набор антимикробных пептидов» . Границы микробиологии . 2012 (9): 2012. doi : 10.3389/fmicb.2018.02012 . ПМК 6120550 . ПМИД 30210481 .
- ^ Бернштейн Х, Бернштейн С, Мишо Р.Э. Пол у микробных возбудителей. Заразить Генет Эвол. Январь 2018 г.;57:8-25. дои: 10.1016/j.meegid.2017.10.024. Epub, 27 октября 2017 г. PMID 29111273
- ^ Клаверис Дж. П., Прюдом М., Мартин Б. (2006). «Индукция компетентных регулонов как общий ответ на стресс у грамположительных бактерий». Анну. Преподобный Микробиол . 60 : 451–75. дои : 10.1146/annurev.micro.60.080805.142139 . ПМИД 16771651 .
- ^ Энгельмоер DJ, Розен Д.Е. (декабрь 2011 г.). «Компетентность увеличивает выживаемость во время стресса у Streptococcus pneumoniae» . Эволюция . 65 (12): 3475–85. дои : 10.1111/j.1558-5646.2011.01402.x . ПМИД 22133219 . S2CID 24634666 .
- ^ Мишод Р.Э., Бернштейн Х., Недельку А.М. (май 2008 г.). «Адаптационное значение пола у микробных патогенов» (PDF) . Заразить. Жене. Эвол . 8 (3): 267–85. дои : 10.1016/j.meegid.2008.01.002 . ПМИД 18295550 .
- ^ Ли Г, Лян З, Ван Х, Ян И, Шао З, Ли М, Ма Ю, Цюй Ф, Моррисон Д.А., Чжан-младший (2016). «Пристрастие гипертрансформируемых пневмококковых изолятов к естественной трансформации для обеспечения пригодности и вирулентности in vivo» . Заразить. Иммунитет . 84 (6): 1887–901. дои : 10.1128/IAI.00097-16 . ПМЦ 4907133 . ПМИД 27068094 .
- ^ Андерсон К. «Патогенные свойства (факторы вирулентности) некоторых распространенных патогенов» (PDF) .
- ^ Перейти обратно: а б Ван Дж., Ли Дж.В., Ли Дж., Хуан Ю., Ван С., Чжан Дж.Р. (18 марта 2020 г.). Весселс М.Р. (ред.). «Регуляция пневмококковой эпигенетической и колониальной фаз с помощью множественных двухкомпонентных регуляторных систем» . ПЛОС Патогены . 16 (3): e1008417. дои : 10.1371/journal.ppat.1008417 . ISSN 1553-7374 . ПМЦ 7105139 . ПМИД 32187228 .
- ^ Логран А.Дж., Ориуэла С.Дж., Туоманен Э.И. (12 апреля 2019 г.). Фишетти В.А., Новик Р.П., Ферретти Дж.Дж., Портной Д.А., Браунштейн М., Руд Дж.И. (ред.). «Streptococcus pneumoniae: инвазия и воспаление» . Микробиологический спектр . 7 (2). doi : 10.1128/microbiolspec.GPP3-0004-2018 . ISSN 2165-0497 . ПМК 6422050 . ПМИД 30873934 .
- ^ «Симптомы и осложнения» . Центры по контролю и профилактике заболеваний . 24 июля 2023 г.
- ^ «Документ с изложением позиции ВОЗ по пневмококковым вакцинам, 2012 г.» (PDF) . Еженедельная эпидемиологическая рекомендация . 87 (14): 129–44. 6 апреля 2012 г. PMID 24340399 .
- ^ «Детям сделают новую вакцину» . Новости Би-би-си . 8 февраля 2006 г.
- ^ «Пневмококковая вакцинация: информация для медицинских работников» . cdc.org . Архивировано из оригинала 23 июля 2016 года . Проверено 26 июля 2016 г.
- ^ «Календарь прививок для детей и подростков Министерства здравоохранения Греции на 2023 год» . Проверено 16 июля 2024 г.
- ^ «Критическое снижение заболеваемости пневмококковой инфекцией и устойчивостью к антибиотикам в Южной Африке» . НИКД . Проверено 20 июля 2015 г.
- ^ Алиберти С., Мантеро М., Мирсаиди М., Блази Ф. (май 2014 г.). «Роль вакцинации в профилактике пневмококковой инфекции у взрослых» . Клиническая микробиология и инфекции . 20 (5): 52–58. дои : 10.1111/1469-0691.12518 . ПМЦ 4473770 . ПМИД 24410778 .
- ^ Перейти обратно: а б Брукс Л.Р., Миас Г.И. (22 июня 2018 г.). «Вирулентность Streptococcus pneumoniae и иммунитет хозяина: старение, диагностика и профилактика» . Границы в иммунологии . 9 : 1366. дои : 10.3389/fimmu.2018.01366 . ISSN 1664-3224 . ПМК 6023974 . ПМИД 29988379 .
- ^ Никгалб, Кевьян Д. (2018). «Расширение области лигирования, опосредованного сортазой, за счет использования гомологов сортазы». ХимБиоХим . 19 (7): 185–195. дои : 10.1002/cbic.201700517 . ПМИД 29124839 . S2CID 23874288 .
- ^ Веджиани, Джанлука (2014). «Программируемые полипротеамы, построенные с использованием двойных пептидных суперклеев» . ПНАС . 113 (5): 1202–1207. Бибкод : 2016ПНАС..113.1202В . дои : 10.1073/pnas.1519214113 . ПМЦ 4747704 . ПМИД 26787909 .
- ^ Грегг, Кэти Дж (16 октября 2015 г.). «Структурный анализ гликозидгидролазы семейства 101 в комплексе с углеводами позволяет лучше понять ее механизм» . Журнал биологической химии . 290 (42): 25657–69. дои : 10.1074/jbc.M115.680470 . ПМЦ 4646209 . ПМИД 26304114 .
- ^ Перикон, Кристофер Д., Овервег, Карин, Херманс, Питер ВМ, Вайзер, Джеффри Н. (2000). «Ингибирующее и бактерицидное действие продукции пероксида водорода Streptococcus pneumoniae на других обитателей верхних дыхательных путей» . Заразить иммунитет . 68 (7): 3990–3997. дои : 10.1128/IAI.68.7.3990-3997.2000 . ПМК 101678 . ПМИД 10858213 .
- ^ Мрахейл, Массачусетс. (2021). «Двойная роль перекиси водорода как окислителя при пневмококковой пневмонии» . Антиоксидно-окислительно-восстановительный сигнал . 20 (34): 962–978. дои : 10.1089/ars.2019.7964 . ПМЦ 8035917 . ПМИД 32283950 .
- ^ Лысенко Е.С., Ратнер А.Дж., Нельсон А.Л., Вайзер Дж.Н. (2005). «Роль врожденных иммунных реакций в исходе межвидовой конкуренции за колонизацию поверхностей слизистых оболочек» . ПЛОС Патог . 1 (1): е1. дои : 10.1371/journal.ppat.0010001 . ПМЦ 1238736 . ПМИД 16201010 . Полный текст
- ^ Пикис А., Кампос Х.М., Родригес В.Дж., Кейт Дж.М. (2001). «Резистентность к оптохину у Streptococcus pneumoniae: механизм, значение и клинические последствия» . Журнал инфекционных болезней . 184 (5): 582–90. дои : 10.1086/322803 . ISSN 0022-1899 . JSTOR 30137322 . ПМИД 11474432 .
- ^ Сальва-Серра Ф., Коннолли Дж., Мур Э.Р., Гонсалес-Сайлс Л. (15 декабря 2017 г.). «Обнаружение гена «Xisco» для идентификации изолятов Streptococcus pneumoniae» . Диагностическая микробиология и инфекционные болезни . 90 (4): 248–250. doi : 10.1016/j.diagmicrobio.2017.12.003 . ISSN 1879-0070 . ПМИД 29329755 .
- ^ Чжэн С.Дж., Сон М.Дж., Ким В.Г. (2006). «Атроментин и лейкомелон — первые ингибиторы, специфичные к еноил-АПБ-редуктазе (FabK) Streptococcus pneumoniae » . Журнал антибиотиков . 59 (12): 808–12. дои : 10.1038/ja.2006.108 . ПМИД 17323650 .
- ^ Нильссон П., Лорел М.Х. (2001). «Носительство устойчивого к пенициллину Streptococcus pneumoniae детьми в детских садах во время программы вмешательства в Мальмё, Швеция». Журнал детских инфекционных заболеваний . 20 (12): 1144–9. дои : 10.1097/00006454-200112000-00010 . ПМИД 11740321 .
- ^ Блок С.Л., Харрисон С.Дж., Хедрик Дж.А., Тайлер Р.Д., Смит Р.А., Киган Э., Чартранд С.А. (1995). «Пенициллинорезистентный Streptococcus pneumoniae при остром среднем отите: факторы риска, особенности чувствительности и антимикробная терапия». Журнал детских инфекционных заболеваний . 14 (9): 751–9. дои : 10.1097/00006454-199509000-00005 . ПМИД 8559623 .
- ^ Коюшко С, Белуча А, Господирек Е (2007). «Лекарственная чувствительность пенициллинрезистентного Streptococcus pneumoniae ». Экспериментальная медицина и микробиология . 59 (4): 293–300. ПМИД 18416121 .
- ^ «Лекарственная устойчивость» . cdc.gov . Проверено 17 февраля 2019 г.
Внешние ссылки
[ редактировать ]- Альянс ГАВИ. Архивировано 20 августа 2014 г. в Wayback Machine.
- ПневмоАДИП
- Библиотека ресурсов по вакцинам PATH, ресурсы по пневмококку
- Центры по контролю и профилактике заболеваний (2012). «Глава 16: Пневмококковая болезнь» . В Аткинсон В., Вулф С., Хамборски Дж. (ред.). Эпидемиология и профилактика болезней, предупреждаемых с помощью вакцин (12-е изд.). Вашингтон, округ Колумбия: Фонд общественного здравоохранения. стр. 233–248. Архивировано из оригинала 10 марта 2017 г.
- Типовой штамм Streptococcus pneumoniae в Bac Dive - база метаданных бактериального разнообразия. Архивировано 20 апреля 2020 г. в Wayback Machine.