Нейроэндокринология
Нейроэндокринология — раздел биологии (особенно физиологии ), изучающий взаимодействие нервной и эндокринной систем ; т.е. как мозг регулирует гормональную активность в организме. [1] Нервная и эндокринная системы часто действуют вместе в процессе, называемом нейроэндокринной интеграцией , для регулирования физиологических процессов человеческого организма. Нейроэндокринология возникла в результате признания того, что мозг, особенно гипоталамус , контролирует секрецию гормонов гипофиза , и впоследствии расширилась , чтобы исследовать многочисленные взаимосвязи эндокринной и нервной систем.
Эндокринная гормоны система состоит из многочисленных желез по всему телу, которые производят и секретируют разнообразной химической структуры, включая пептиды , стероиды и нейроамины . В совокупности гормоны регулируют многие физиологические процессы. Нейроэндокринная система — это механизм, с помощью которого гипоталамус поддерживает гомеостаз , регулируя размножение , обмен веществ , в еде поведение и питье, использование энергии , осмолярность и кровяное давление .
Нейроэндокринная система
[ редактировать ]Гипоталамус
[ редактировать ]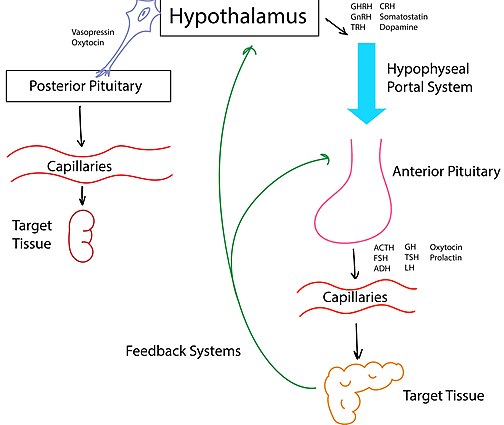
Гипоталамус широко известен как релейный центр мозга из-за его роли в интеграции сигналов от всех областей мозга и выработке специфической реакции. В нейроэндокринной системе гипоталамус получает электрические сигналы из разных частей мозга и переводит эти электрические сигналы в химические сигналы в форме гормонов или рилизинг-факторов. Эти химические вещества затем транспортируются в гипофиз, а оттуда в системный кровоток. [2]
Гипофиз
[ редактировать ]Гипофиз делится на три доли: переднюю долю гипофиза , промежуточную долю гипофиза и заднюю долю гипофиза . Гипоталамус контролирует секрецию гормонов передней доли гипофиза, направляя рилизинг-факторы, называемые тропными гормонами , вниз по гипоталамо-гипофизарной портальной системе. [3] Например, тиреотропин-рилизинг-гормон, выделяемый гипоталамусом в портальную систему, стимулирует секрецию тиреотропного гормона передней долей гипофиза. [ нужна ссылка ]
Задняя доля гипофиза непосредственно иннервируется гипоталамусом; Гормоны окситоцин и вазопрессин синтезируются нейроэндокринными клетками гипоталамуса и хранятся в нервных окончаниях задней доли гипофиза. Они секретируются непосредственно в большой круг кровообращения нейронами гипоталамуса. [3]
Основные нейроэндокринные оси
[ редактировать ]Окситоцин и вазопрессин (также называемый антидиуретическим гормоном), два нейрогипофизарных гормона задней доли гипофиза (нейрогипофиза), секретируются из нервных окончаний крупноклеточных нейросекреторных клеток в большой круг кровообращения. Клеточные тела нейронов окситоцина и вазопрессина находятся в паравентрикулярном ядре и супраоптическом ядре гипоталамуса соответственно. [2] и электрическая активность этих нейронов регулируется афферентными синаптическими входами из других областей мозга. [4]
Напротив, гормоны передней доли гипофиза (аденогипофиза) секретируются эндокринными клетками, которые у млекопитающих не имеют прямой иннервации, однако секреция этих гормонов ( адренокортикотропный гормон , лютеинизирующий гормон, фолликулостимулирующий гормон, тиреотропный гормон) гормон, пролактин и гормон роста ) остается под контролем гипоталамуса. Гипоталамус контролирует переднюю долю гипофиза посредством рилизинг-факторов и факторов, ингибирующих высвобождение ; это вещества, выделяемые нейронами гипоталамуса в кровеносные сосуды у основания мозга, на срединном возвышении . [5] Эти сосуды, гипоталамо-гипофизарные портальные сосуды, доставляют гипоталамические факторы в переднюю долю гипофиза, где они связываются со специфическими рецепторами на поверхности клеток, продуцирующих гормоны. [3]
Например, секреция гормона роста контролируется двумя нейроэндокринными системами: нейронами гормона роста (GHRH) и нейронами соматостатина , которые стимулируют и ингибируют секрецию гормона роста соответственно. [6] Нейроны GHRH расположены в дугообразном ядре гипоталамуса, тогда как клетки соматостатина, участвующие в регуляции гормона роста, находятся в перивентрикулярном ядре . Эти две нейрональные системы проецируют аксоны к срединному возвышению, где они высвобождают свои пептиды в портальные кровеносные сосуды для транспортировки в переднюю долю гипофиза. Гормон роста секретируется импульсами, которые возникают в результате чередующихся эпизодов высвобождения GHRH и высвобождения соматостатина, что может отражать нейрональные взаимодействия между GHRH и клетками соматостатина, а также отрицательную обратную связь со стороны гормона роста. [6]
Функции
[ редактировать ]Нейроэндокринная система контролирует репродукцию. [7] во всех его аспектах, от привязанности до сексуального поведения. Они контролируют сперматогенез и овариальный цикл, роды , лактацию и материнское поведение . Они контролируют реакцию организма на стресс. [8] и инфекция . [9] в организме Они регулируют обмен веществ , влияя на пищевое и питьевое поведение, а также влияют на то, как используется поступающая энергия, то есть на то, как метаболизируется жир. [10] Они влияют и регулируют настроение, [11] гомеостаз жидкости и электролитов организма, [12] и кровяное давление . [13]
Нейроны нейроэндокринной системы крупные; это мини -фабрики по производству секреторной продукции; их нервные окончания большие и организованы в когерентные терминальные поля; их выход часто можно легко измерить в крови; а что делают эти нейроны и на какие стимулы они реагируют, легко открыть для гипотез и экспериментов. Следовательно, нейроэндокринные нейроны являются хорошими «модельными системами» для изучения общих вопросов, таких как «как нейрон регулирует синтез, упаковку и секрецию своего продукта?» и «как информация кодируется в электрической активности?» [ нужна ссылка ] [Похоже, что это наблюдение из первоисточника.]
История
[ редактировать ]Пионеры
[ редактировать ]Уолтер Ли Гейнс отметил активность гипофиза при лактации коров в 1915 году. [14] Он также отметил, что анестезия может блокировать лактацию и реакцию на сосательный рефлекс. [15]
Эрнст и Берта Шаррер , [16] считается университета Мюнхенского Медицинский колледж Альберта Эйнштейна соучредителем области нейроэндокринологии благодаря своим первоначальным наблюдениям и предложениям в 1945 году, касающимся нейропептидов .
Джеффри Харрис [17] многие считают его «отцом» нейроэндокринологии. Харрису, профессору анатомии доктора Ли в Оксфордском университете , приписывают открытие того, что гипофиза млекопитающих передняя доля регулируется гормонами, секретируемыми нейронами гипоталамуса в гипоталамо-гипофиза портальную циркуляцию . Напротив, гормоны задней доли гипофиза секретируются в большой круг кровообращения непосредственно из нервных окончаний нейронов гипоталамуса. Эта плодотворная работа была проделана в сотрудничестве с Дорой Якобсон из Лундского университета . [18]
Первыми из этих факторов, которые необходимо идентифицировать, являются тиреотропин-рилизинг-гормон (ТРГ) и гонадотропин-рилизинг-гормон (ГнРГ). TRH — небольшой пептид , который стимулирует секрецию тиреотропного гормона ; ГнРГ (также называемый рилизинг-гормоном лютеинизирующего гормона) стимулирует секрецию лютеинизирующего гормона и фолликулостимулирующего гормона .
Роджер Гиймен , [19] Студент-медик медицинского факультета Лиона и Эндрю В. Шалли из Тулейнского университета выделили эти факторы из гипоталамуса овец и свиней, а затем определили их структуры. Гиймен и Шалли были удостоены Нобелевской премии по физиологии и медицине в 1977 году за вклад в понимание «выработки пептидных гормонов мозгом». [ нужна ссылка ]
В 1952 году Андор Сентивани из Университета Южной Флориды и Геза Филипп написали первую в мире исследовательскую работу, показывающую, как нейронный контроль иммунитета происходит через гипоталамус. [20]
Современный размах
[ редактировать ]Сегодня нейроэндокринология охватывает широкий спектр тем, которые прямо или косвенно возникли из основной концепции нейроэндокринных нейронов. Нейроэндокринные нейроны контролируют половые железы , стероиды которых , в свою очередь, влияют на мозг, как и кортикостероиды, секретируемые надпочечниками под влиянием адренокортикотропного гормона. Изучение этих обратных связей стало прерогативой нейроэндокринологов. Пептиды, секретируемые нейроэндокринными нейронами гипоталамуса в кровь, высвобождались также и в мозг, и центральное действие часто дополняло периферическое действие. Таким образом, понимание этих центральных действий также стало прерогативой нейроэндокринологов, иногда даже тогда, когда эти пептиды появлялись в совершенно разных частях мозга, которые, по-видимому, выполняли функции, не связанные с эндокринной регуляцией. В периферической нервной системе были обнаружены нейроэндокринные нейроны , регулирующие, например, пищеварение . Клетки мозгового слоя надпочечников, выделяющие Было доказано, что адреналин и норадреналин обладают свойствами взаимодействия между эндокринными клетками и нейронами и оказались выдающимися модельными системами, например, для изучения молекулярных механизмов экзоцитоза . И они тоже стали, в более широком смысле, нейроэндокринными системами. [ нужна ссылка ]
Нейроэндокринные системы сыграли важную роль в нашем понимании многих основных принципов нейробиологии и физиологии , например, нашего понимания связи между стимулом и секрецией . [21] Происхождение и значение формирования паттернов нейроэндокринной секреции по-прежнему являются доминирующими темами в нейроэндокринологии сегодня.
Нейроэндокринология также используется как неотъемлемая часть понимания и лечения нейробиологических заболеваний головного мозга . Одним из примеров является усиление лечения симптомов настроения гормоном щитовидной железы. [22] Другим примером является обнаружение проблем с транстиретином (транспортом тироксина) в спинномозговой жидкости у некоторых пациентов с диагнозом шизофрения. [23]
Экспериментальные методы
[ редактировать ]Со времени первых экспериментов Джеффри Харриса по изучению связи гипоталамуса с гипофизом многое было изучено о механистических деталях этого взаимодействия. Использовались различные экспериментальные техники. Ранние эксперименты в значительной степени опирались на методы электрофизиологии, используемые Ходжкиным и Хаксли . Недавние подходы включали различные математические модели для понимания ранее выявленных механизмов и прогнозирования системной реакции и адаптации при различных обстоятельствах. [ нужна ссылка ]
Электрофизиология
[ редактировать ]Электрофизиологические эксперименты использовались на заре нейроэндокринологии для выявления физиологических процессов в гипоталамусе и особенно в задней доле гипофиза. В 1950 году Джеффри Харрис и Барри Кросс описали путь окситоцина, изучая высвобождение окситоцина в ответ на электрическую стимуляцию. [24] В 1974 году Уолтерс и Хаттон исследовали эффект обезвоживания воды путем электрической стимуляции супраоптического ядра — гипоталамического центра, ответственного за высвобождение вазопрессина. [24] Гленн Хаттон посвятил свою карьеру изучению физиологии нейрогипофизарной системы, которое включало изучение электрических свойств нейронов гипоталамуса. [24] Это позволило изучить поведение этих нейронов и связанные с этим физиологические эффекты. Изучение электрической активности нейроэндокринных клеток позволило в конечном итоге различить нейроны центральной нервной системы, нейроэндокринные нейроны и эндокринные клетки. [25]
Математические модели
[ редактировать ]Модель Ходжкина-Хаксли
[ редактировать ]Модель Ходжкина-Хаксли переводит данные о токе системы при определенном напряжении в зависящие от времени данные, описывающие мембранный потенциал . Эксперименты с использованием этой модели обычно основаны на одном и том же формате и предположениях, но различаются дифференциальными уравнениями, чтобы ответить на конкретные вопросы. Благодаря использованию этого метода многое было изучено о вазопрессине, ГнРГ, соматотрофах, кортикотрофах и лактотрофных гормонах. [8]
Модель интеграции и запуска
[ редактировать ]Модель «интеграция и запуск» направлена на математическую простоту описания биологических систем, фокусируясь только на пороговой активности нейрона. Таким образом, модель успешно снижает сложность сложной системы; однако он игнорирует реальные механизмы действия и заменяет их функциями, которые определяют, как выходные данные системы зависят от ее входных данных. [8] Эта модель использовалась для описания выброса гормонов задней доли гипофиза, в частности окситоцина и вазопрессина. [9]
Модель функциональных или средних полей
[ редактировать ]Модель функциональных или средних полей основана на предпосылке «чем проще, тем лучше». [8] Он стремится упростить моделирование многогранных систем, используя одну переменную для описания всей популяции клеток. Альтернативой было бы использование разного набора переменных для каждой совокупности. При попытке смоделировать систему, в которой взаимодействуют несколько популяций клеток, использование нескольких наборов быстро становится слишком сложным. Эта модель использовалась для описания нескольких систем, особенно связанных с репродуктивным циклом (менструальные циклы, лютеинизирующий гормон, выбросы пролактина). [9] Также существуют функциональные модели для представления секреции кортизола и секреции гормона роста. [9]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ «Эндокринная система и нейроэндокринология :: Центр обучения ДНК» . www.dnalc.org . Проверено 12 мая 2018 г.
- ^ Перейти обратно: а б Уоттс, Алан Дж. (01 августа 2015 г.). «60 лет нейроэндокринологии: структура нейроэндокринного гипоталамуса: нейроанатомическое наследие Джеффри Харриса» . Журнал эндокринологии . 226 (2): Т25–Т39. дои : 10.1530/JOE-15-0157 . ISSN 0022-0795 . ПМЦ 4574488 . ПМИД 25994006 .
- ^ Перейти обратно: а б с Маленка Р.К., Нестлер Э.Дж., Хайман С.Е. (2009). «Глава 10: Нейронный и нейроэндокринный контроль внутренней среды». В Сидоре А., Брауне Р.Ю. (ред.). Молекулярная нейрофармакология: фонд клинической неврологии (2-е изд.). Нью-Йорк: McGraw-Hill Medical. стр. 246, 248–259. ISBN 9780071481274 .
- ^ Хонда, Казумаса; Чжан, Уильям; Томияма, Кейта (июнь 2014 г.). «Клетки окситоцина в паравентрикулярном ядре получают возбуждающие синаптические сигналы от контрлатеральных паравентрикулярных и супраоптических ядер у лактирующих крыс» . Письма по неврологии . 572 : 44–47. дои : 10.1016/j.neulet.2014.04.040 . ПМИД 24792395 . S2CID 25107850 .
- ^ Книгге, К.М.; Джозеф, ЮАР; Сладек, младший; Ноттер, МФ; Моррис, М.; Сундберг, ДК; Хольцварт, Массачусетс; Хоффман, GE; О'Брайен, Л. (1 января 1976 г.), Борн, GH; Даниэлли, Дж. Ф.; Чон, К.В. (ред.), Поглощение и транспортная активность срединного возвышения гипоталамуса , International Review of Cytology, vol. 45, Academic Press, стр. 383–408, номер документа : 10.1016/s0074-7696(08)60082-0 , ISBN. 9780123643452 , получено 15 ноября 2021 г.
- ^ Перейти обратно: а б МакГрегор, диджей; Ленг, Г. (декабрь 2005 г.). «Моделирование гипоталамического контроля секреции гормона роста» . Журнал нейроэндокринологии . 17 (12): 788–803. дои : 10.1111/j.1365-2826.2005.01370.x . ISSN 0953-8194 . ПМИД 16280026 . S2CID 36712187 .
- ^ Бласкес М., Босма П.Т., Фрейзер Э.Дж., Ван Лук К.Дж., Трюдо В.Л. (июнь 1998 г.). «Рыбы как модель нейроэндокринной регуляции размножения и роста». Сравнительная биохимия и физиология. Часть C. Фармакология, токсикология и эндокринология . 119 (3): 345–64. дои : 10.1016/S0742-8413(98)00023-1 . ПМИД 9827007 .
- ^ Перейти обратно: а б с д Ратка А., Сутанто В., Блумерс М., де Клоет Э.Р. (август 1989 г.). «О роли минералокортикоидных (тип I) и глюкокортикоидных (II тип) рецепторов головного мозга в нейроэндокринной регуляции». Нейроэндокринология . 50 (2): 117–23. дои : 10.1159/000125210 . ПМИД 2550833 .
- ^ Перейти обратно: а б с д Вебстер Дж.И., Тонелли Л., Штернберг Э.М. (2002). «Нейроэндокринная регуляция иммунитета» (PDF) . Ежегодный обзор иммунологии . 20 : 125–63. doi : 10.1146/annurev.immunol.20.082401.104914 . ПМИД 11861600 . Архивировано из оригинала (PDF) 12 декабря 2013 г.
- ^ Макминн Дж. Э., Баскин Д. Г., Шварц М. В. (май 2000 г.). «Нейроэндокринные механизмы, регулирующие потребление пищи и массу тела». Обзоры ожирения . 1 (1): 37–46. дои : 10.1046/j.1467-789x.2000.00007.x . ПМИД 12119644 . S2CID 33202919 .
- ^ Дэвидсон Р.Дж., Льюис Д.А., Эллой Л.Б., Амарал Д.Г., Буш Дж., Коэн Дж.Д. и др. (сентябрь 2002 г.). «Нейральные и поведенческие субстраты настроения и регуляции настроения». Биологическая психиатрия . 52 (6): 478–502. CiteSeerX 10.1.1.558.6231 . дои : 10.1016/S0006-3223(02)01458-0 . ПМИД 12361665 . S2CID 39992433 .
- ^ Антунес-Родригеш Х., де Кастро М., Элиас Л.Л., Валенса М.М., Макканн С.М. (январь 2004 г.). «Нейроэндокринный контроль обмена жидкостей организма». Физиологические обзоры . 84 (1): 169–208. doi : 10.1152/physrev.00017.2003 . ПМИД 14715914 .
- ^ Ленкей З., Корвол П., Льоренс-Кортес С. (май 1995 г.). «Подтип AT1A рецептора ангиотензина преобладает в областях переднего мозга крыс, участвующих в кровяном давлении, гомеостазе жидкости организма и нейроэндокринном контроле». Исследования мозга. Молекулярные исследования мозга . 30 (1): 53–60. дои : 10.1016/0169-328X(94)00272-G . ПМИД 7609644 .
- ^ Медвей, ВК (2012). История эндокринологии . Спрингер. п. 409.
- ^ Дрейфус, Жан Жак (1981). «У.Л. Гейнс, предшественник концепции нейроэндокринного рефлекса». Геснерус (на французском языке). 38 (3–4): 331–338. дои : 10.1163/22977953-0380304004 .
- ^ Шаррер Э, Шаррер Б (1 января 1945 г.). «Нейросекреция» . Физиологические обзоры . 25 (1): 171–181. дои : 10.1152/physrev.1945.25.1.171 . ISSN 1522-1210 .
- ^ Райсман Г. (1997). «Желание объяснить непостижимое: Джеффри Харрис и открытие нейронного контроля гипофиза» (PDF) . Ежегодный обзор неврологии . 20 : 533–66. дои : 10.1146/annurev.neuro.20.1.533 . ПМИД 9056724 . Архивировано из оригинала (PDF) 3 июля 2007 г. Проверено 10 февраля 2006 г.
- ^ Бретнак CS, Мойнихан Дж. Б. (март 2013 г.). «Первые леди в закладке основ нейроэндокринологии» (PDF) . Ирландский журнал медицинских наук . 182 (1): 143–7. дои : 10.1007/s11845-012-0830-9 . ПМИД 22581099 . S2CID 8177884 . Архивировано из оригинала (PDF) 24 декабря 2018 г.
- ^ Гиймен Р., Шалли А.В., Липскомб Х.С., Андерсен Р.Н., Лонг Дж.М. (апрель 1962 г.). «О наличии в гипоталамусе свиней рилизинг-фактора 3-кортикотропина, альфа- и бета-меланоцитстимулирующих гормонов, адренокортикотропина, лизин-вазопрессина и окситоцина» . Эндокринология . 70 (4): 471–7. дои : 10.1210/endo-70-4-471 . ПМИД 13902822 .
- ^ Берчи I (2010). «Мемориал доктора Андора Сентивани» . Университет Манитобы. Архивировано из оригинала 10 февраля 2009 г. (Внимание: автоматическая фоновая музыка)
- ^ Мислер С. (сентябрь 2009 г.). «Объединение концепций взаимодействия стимула и секреции в эндокринных клетках и некоторые последствия для терапии» . Достижения в области физиологического образования . 33 (3): 175–86. дои : 10.1152/advan.90213.2008 . ПМЦ 3747786 . ПМИД 19745043 .
- ^ Герачиоти ТД (2006). «Выявление психиатрических проявлений гипотиреоза» . Современная психиатрия . 5 (11): 98–117.
- ^ Хуанг Дж.Т., Левеке Ф.М., Оксли Д., Ван Л., Харрис Н., Кете Д. и др. (ноябрь 2006 г.). «Биомаркеры заболеваний в спинномозговой жидкости пациентов с впервые возникшим психозом» . ПЛОС Медицина . 3 (11): е428. doi : 10.1371/journal.pmed.0030428 . ПМЦ 1630717 . ПМИД 17090210 .
- ^ Перейти обратно: а б с Ленг, Г.; Моос, ФК; Армстронг, МЫ (01 мая 2010 г.). «Адаптивный мозг: Гленн Хаттон и супраоптическое ядро» . Журнал нейроэндокринологии . 22 (5): 318–329. дои : 10.1111/j.1365-2826.2010.01997.x . ПМЦ 5713484 . ПМИД 20298459 .
- ^ Кандел, скорая помощь (1 марта 1964 г.). «Электрические свойства нейроэндокринных клеток гипоталамуса» . Журнал общей физиологии . 47 (4): 691–717. дои : 10.1085/jgp.47.4.691 . ISSN 1540-7748 . ПМК 2195356 . ПМИД 14127607 .
