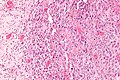
Эпителиоидная саркома
| Эпителиоидная саркома | |
|---|---|
 | |
| Микрофотография эпителиоидной саркомы. Пятно H&E . | |
| Специальность | онкология |
Эпителиоидная саркома — редкая саркома мягких тканей, возникающая из мезенхимальной ткани и характеризующаяся эпителиоидоподобными признаками. Составляет менее 1% всех сарком мягких тканей . Впервые он был окончательно охарактеризован Ф.М. Энцингером в 1970 году. [ 1 ] У молодых людей он обычно проявляется на дистальных отделах конечностей (пальцы, руки, предплечья или стопы) в виде небольшого мягкого образования или скопления шишек. конечностях . Также описан проксимальный вариант, часто встречающийся в верхних [ 2 ] Реже случаи регистрируются в области таза, вульвы, полового члена и позвоночника.
Гистологически эпителиоидная саркома образует узелки с центральным некрозом, окруженные мягкими полигональными клетками с эозинофильной цитоплазмой и периферическими веретенами. [ 3 ] Эпителиоидные саркомы обычно экспрессируют виментин , цитокератины , антиген эпителиальной мембраны и CD34 , тогда как они обычно отрицательны в отношении S100 , десмина и FLI1 (FLI-1). [ 3 ] Им характерно отсутствие белка INI1 (см. ниже). Эпителиоидные саркомы обычно окрашиваются положительно на CA125 . [ 4 ]
Эпителиоидная саркома чаще всего поражает молодых людей, однако ни одна возрастная группа не застрахована от нее. Заболевание имеет тенденцию к развитию местных рецидивов и метастазированию впоследствии в регионарные лимфатические узлы, легкие, кости, мозг и другие места. [ 3 ] Вообще говоря, эпителиоидная саркома имеет высокую частоту рецидивов после первоначального лечения и имеет тенденцию к локальному или региональному рецидиву (в месте исходной опухоли или вблизи нее). Эпителиоидная саркома также характеризуется лимфатическим распространением (в 22-48% случаев) и метастазированием (в 21-63% случаев). [ 5 ] Эти события, а также продвинутая стадия (прогрессирование) и степень (агрессивность) являются предикторами общего худшего результата. С более положительным исходом связаны более молодой возраст, женский или мужской пол, дистальное или проксимальное расположение, меньший размер опухоли и отрицательные границы после резекции опухоли. [ 1 ] [ 6 ] [ 7 ]
Признаки и симптомы
[ редактировать ]Эпителиоидная саркома представляет собой медленно растущую и относительно безболезненную опухоль, часто приводящую к длительному периоду времени между манифестацией и постановкой диагноза. [ 8 ] Из-за сложности отличить этот рак от более распространенных видов рака, таких как рак кожи (плоскоклеточный рак или базальноклеточный рак), его часто ошибочно диагностируют, ошибочно принимая за персистирующую бородавку или кисту. Чаще всего он проявляется на дистальных отделах конечностей (пальцы, руки, предплечья или стопы) в виде небольшого мягкого образования или скопления узелков. Чаще всего его описывают как твердое пальпируемое образование, расположенное либо в глубоких мягких тканях, либо в дерме. Эти виды рака могут образовывать кратер или язву, что приводит к ошибочному диагнозу плохо заживающей травматической раны или бородавки. Около 13% пациентов имеют мультифокальные опухоли и около 13% пациентов имеют метастатическое заболевание. [ 9 ]
Генетика
[ редактировать ]Наиболее распространенной генетической мутацией (встречающейся в 80-90% эпителиоидных сарком) является инактивация гена SMARCB1 , или утрата функции белка INI1. [ 10 ] [ 11 ] Эпителиоидная саркома обычно содержит мутации или делеции хромосомы 22q11.2 и прирост хромосомы 8q. Также наблюдались аберрации 18q, а также периодические приросты 11q13. [ 12 ] [ 13 ] [ 14 ]
Ген SMARCB1 (белковый продукт которого называется BAF47, INI1 или hSNF5) расположен на хромосоме 22q11.2 . [ 10 ] Он кодирует член комплекса ремоделирования хроматина SWI/SNF . Потеря функции SMARCB1 является наиболее распространенной генетической мутацией, наблюдаемой при эпителиоидной саркоме, и эта дисфункция, вероятно, является основным фактором прогрессирования заболевания. SMARCB1 представляет собой основную белковую субъединицу 15-субъединичного комплекса SWI/SNF (или BAF), участвующего в регуляции упаковки ДНК в ядре клетки. [ 10 ] Было доказано, что он является мощным геном-супрессором опухолей . [ 11 ] [ 15 ] это означает, что его основная роль заключается в контроле деления клеток. Поскольку этот супрессор опухоли обычно инактивируется при эпителиоидной саркоме, деление клеток может не остановить должным образом, что приводит к неконтролируемому росту рака. Исследовательские группы пытаются найти способы обратить вспять потерю генетической функции, характерную для эпителиоидной саркомы. [ 8 ]
Молекулярная биология
[ редактировать ]Ряд важных белков, по-видимому, активен при эпителиоидной саркоме. Некоторые из них описаны ниже.
ВЭФР
[ редактировать ]VEGF (фактор роста эндотелия сосудов) часто сверхэкспрессируется при эпителиоидной саркоме. [ 16 ] Это критический путь ангиогенеза — процесса, который раковые клетки используют для формирования новых кровеносных сосудов, которые обеспечивают опухоль необходимыми элементами для ее выживания. Агенты против VEGF, такие как пазопаниб, одобрены для использования при карциномах и саркомах мягких тканей, таких как эпителиоидная саркома, хотя доступ к этим препаратам варьируется от страны к стране. [ 17 ]
ИЗ
[ редактировать ]МЕТ (мезенхимально-эпителиальный переход) представляет собой биологический путь, который, по-видимому, важен для развития и прогрессирования эпителиоидной саркомы. [ 18 ] [ 19 ] МЕТ является тирозинкиназы онкогеном , и его сигнальный путь участвует в различных злокачественных новообразованиях, включая многие виды рака. [ 20 ]
Ежик Соник и Нотч
[ редактировать ]Сигнальные пути Sonic hedgehog (SHH) и Notch , по-видимому, активны при эпителиоидной саркоме. Эти клеточные сигнальные пути контролируют клеточную пролиферацию и дифференцировку. Они также участвуют в координации раковых стволовых клеток , инвазивности заболеваний и метастазировании. Ингибиторы Hhat (такие как RU-SKI 43) блокируют путь SHH, ингибируя пальмитоилацитл-трансферазу ежа. В исследованиях ингибиторы Notch исследовались при саркомах, таких как эпителиоидная саркома. [ 21 ]
мТОР
[ редактировать ]Частая сверхактивация передачи сигналов mTOR (мишень рапамицина у млекопитающих) также наблюдалась при эпителиоидной саркоме. [ 19 ] [ 22 ] Путь mTOR был описан как «главный переключатель» клеточного катаболизма и анаболизма , и он может усиливать прогрессирование клеточного цикла , выживаемость клеток и блокировать нормальную гибель клеток ( апоптоз ). [ 17 ] Было продемонстрировано, что простая блокировка передачи сигналов mTOR может привести к реактивации пути AKT , сводя на нет большую часть блокады mTOR. [ 19 ] Было показано, что реактивация АКТ зависит от МЕТ. [ 19 ] Это привело к выводу, что одновременное блокирование mTOR и MET должно быть полезным подходом к лечению эпителиоидной саркомы.
РЭФР
[ редактировать ]о сверхэкспрессии рецептора эпидермального фактора роста (EGFR) в большинстве эпителиоидных сарком. Сообщается [ 22 ] [ 23 ] EGFR является членом семейства HER-рецепторов . При связывании лиганда фосфорилирование EGFR запускает активацию нижестоящих сигнальных путей, участвующих в важнейших клеточных функциях, таких как пролиферация , выживание и ангиогенез . [ 24 ] Лабораторные эксперименты in vitro и in vivo показали, что блокада EGFR при эпителиоидной саркоме приводит к снижению пролиферации клеток, усилению апоптоза и прекращению инвазионной и миграционной способности. [ 22 ] Хотя блокада EGFR с помощью лекарства показала ограниченные результаты в клинических условиях, при использовании в составе комбинации с другими препаратами, такими как ингибитор mTOR, наблюдался синергизм и было продемонстрировано превосходное ингибирование роста опухоли. [ 22 ]
CD109
[ редактировать ]CD109 , обычно обнаруживаемый на лимфоцитах, также экспрессируется при эпителиоидной саркоме и, как полагают, маркирует раковые стволовые клетки (или клетки, инициирующие рак) заболевания. [ 25 ] Также было показано, что его экспрессия позволяет предсказать результат. Раковые стволовые клетки представляют собой небольшую популяцию опухолевых клеток, характеризующуюся общей химиорезистентностью, способностью к самообновлению, потенциалом мультидифференцировки, способностью к состоянию покоя и онкогенезом. Таким образом, считается, что раковые стволовые клетки играют ключевую роль в прогрессировании и рецидиве рака.
Циклин Д1
[ редактировать ]Циклин D1 является белком, необходимым для развития клеточного цикла, и было показано, что его активность повышается при эпителиоидной саркоме. [ 14 ] Циклин D1 является регулятором циклинзависимых киназ (в частности, CDK4 и CDK6 ). Было показано, что он взаимодействует, среди прочего, с белком ретинобластомы (геном-супрессором опухоли), CDK4 и CDK6, бета-рецептором гормона щитовидной железы и коактиватором ядерного рецептора 1 . [ 14 ] Циклин D и CDK способствуют развитию клеточного цикла, высвобождая факторы транскрипции , которые важны для инициации репликации ДНК . Аномальные уровни циклина D1 могут быть связаны с более быстрым делением клеток при эпителиоидной саркоме.
Диагностика
[ редактировать ]ткани Биопсия является методом выбора в диагностике. Из-за высокой частоты поражения лимфатических узлов может быть выполнена биопсия сторожевого лимфатического узла . Общей характеристикой эпителиоидной саркомы (наблюдается в 80% всех случаев) является утрата функции гена SMARCB1 (белковый продукт которого называется BAF47, INI1 или hSNF5). Доступно иммуногистохимическое окрашивание INI1, которое помогает диагностировать эпителиоидную саркому. МРТ является методом выбора для диагностики перед биопсией и патологоанатомической диагностикой для большинства пациентов.
Постановка
[ редактировать ]Стадирование эпителиоидной саркомы учитывает размер и расположение первичной опухоли, поражение лимфатических узлов, наличие и расположение метастазов, а также гистологическую степень (показатель агрессивности заболевания). [ 26 ]
Уход
[ редактировать ]Хирургическое вмешательство, лучевая терапия и системная терапия, такая как химиотерапия, в разное время используются при лечении пациентов с эпителиоидной саркомой. Поскольку саркомы считаются очень редкими, неудивительно, что результаты лечения пациентов с этим типом рака лучше, когда пациентов обследуют в экспертных центрах и, если возможно, лечат там. [ 27 ]
Хирургическое удаление эпителиоидных сарком с широкими краями остается предпочтительным методом лечения. [ 28 ] и по состоянию на 2023 год остается единственным методом лечения рака, иногда в сочетании с лучевой или химиотерапией. [ 28 ] [ 29 ] [ 30 ] Хирургия с сохранением конечностей является стандартом лечения всех сарком, а также, где это возможно, используется для лечения эпителиоидной саркомы. [ 31 ]
В случаях запущенного, рецидивирующего или метастазирующего заболевания, а также если опухоль неоперабельна, стандартом лечения являются химиотерапия и лучевая терапия. [ 32 ] Польза от стандартных лекарств, таких как доксорубицин, ифосфамид и комбинации с гемцитабином, обычно измеряется месяцами, а не годами. [ 33 ]
В январе 2020 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США одобрило пероральный препарат таземетостат (торговое название Тазверик), препарат, блокирующий метилтрансферазу EZH2 , для лечения эпителиоидной саркомы у пациентов в возрасте 16 лет и старше с метастатической или местно-распространенной (невозможной полностью удалить хирургическим путем) заболевание. [ 34 ] Данные, которые привели к регистрации препарата, были подтверждены постмаркетинговыми исследованиями. Как и при стандартной химиотерапии, эффективность таземетостата обычно измеряется месяцами, хотя некоторые пациенты чувствуют себя лучше в течение более длительного периода времени.
Прогноз
[ редактировать ]Пятилетняя выживаемость пациентов с эпителиоидной саркомой обычно оценивается как 50-70%, а 10-летняя выживаемость составляет 42-55%. Дети с эпителиоидной саркомой могут иметь несколько лучшие результаты, чем взрослые: 5-летняя выживаемость составляет около 65%. [ 6 ] У детей с этим диагнозом также реже наблюдаются лимфатическое распространение и метастазы, чем у взрослых. [ 6 ] Было показано, что помимо стадии и степени опухоли на прогноз влияют пол, локализация, возраст на момент постановки диагноза, размер опухоли и микроскопическая патология. [ 9 ] [ 35 ] Неудивительно, что поздняя стадия и степень связаны с худшими результатами. Женщины, как правило, имеют более благоприятные результаты, чем мужчины, проксимальные случаи показывают худшие результаты, чем дистальные. Опухоли диаметром более 2 см и опухоли с некрозом и сосудистой инвазией также коррелируют с худшим исходом. [ 35 ]
Лучевая терапия также является вариантом лечения, когда опухоли считаются неоперабельными или широкие хирургические границы недостижимы. Лучевая терапия в сочетании с химиотерапией до сих пор приводила лишь к минимальному улучшению показателей ответа. Испытания брахитерапии (внутренняя лучевая терапия, которая доставляет высокую дозу радиации непосредственно к опухоли и, как полагают, имеет меньше долгосрочных побочных эффектов) дали некоторые положительные результаты. [ нужна ссылка ]
Исследовать
[ редактировать ]Было показано, что эпителиоидная саркома (особенно на поздней стадии, рецидивирующая или метастазирующая болезнь) становится устойчивой к традиционным методам лечения рака, что требует дальнейшего изучения новых методов и методов лечения. Из-за относительно небольшой продолжительности эффекта от лечения эпителиоидной саркомы традиционными методами лечения рака (такими как химиотерапия и лучевая терапия) изучаются новые стратегии лечения.
Химиотерапия
[ редактировать ]В текущих клинических исследованиях изучаются новые методы химиотерапии эпителиоидной саркомы, хотя до сих пор ни один из них не продемонстрировал значительного улучшения эффективности по сравнению с доксорубицином и/или ифосфамидом. Новые препараты включают гемцитабин, таксаны, винорелбин и пазопаниб. [ 32 ]
Альдоксорубицин — это новая пролекарства изученная версия доксорубицина. Доксорубицин является стандартом лечения распространенной или метастатической эпителиоидной саркомы, но он обладает дозолимитирующей токсичностью, а именно острой и хронической кардиотоксичностью . [ 36 ] [ 37 ] Альдоксорубицин был разработан для безопасной доставки более высокой дозы препарата непосредственно в опухоль, что приводит к меньшей токсичности. Были проведены исследования фазы I и II альдоксорубицина, в ходе которых наблюдалась небольшая кардиотоксичность. Хотя полезность была замечена у некоторых пациентов, место альдоксорубицина в лечении пациентов с эпителиоидной саркомой или другими саркомами, в частности по сравнению с доксорубицином, не определено.
TH-302 был еще одним исследовательским препаратом, изучавшимся при таких саркомах, как эпителиоидная саркома. Он нацелен на опухолевую гипоксию , распространенное явление в онкогенезе, когда микроокружение опухоли обедняется кислородом и становится гипоксическим . [ 38 ] Были проведены исследования фазы I, II и III с использованием TH-302 отдельно и в комбинации. [ 39 ] но два испытания фазы 3 в 2015 году провалились, так что препарат больше не изучается активно.
Иммунотерапия
[ редактировать ]Иммунотерапия – это стратегия использования собственной иммунной системы организма для борьбы с раком. Обычно это включает в себя «обучение» или «настройку» иммунной системы, чтобы она могла лучше распознавать и отвергать раковые клетки. организма Различные иммунотерапии могут включать манипуляции с Т-клетками , NK-клетками или дендритными клетками , чтобы они были более эффективны против раковых клеток. Они также могут включать введение полученных в лаборатории антител, специфичных к опухолевым антигенам, для создания или усиления иммунного ответа . [ нужна ссылка ]
Вакцинотерапия , пожалуй, самая простая иммунотерапевтическая стратегия. [ 40 ] хотя до сих пор практически не появилось доказательств того, что вакцинация любым соединением приводит к уменьшению размеров эпителиоидной саркомы или других сарком. [ 41 ] В настоящее время изучаются многочисленные методы и стратегии лечения многих видов рака с целью повышения эффективности вакцинотерапии. [ 40 ] Вакцины могут доставлять в иммунную систему различные опухолеассоциированные факторы (опухолевые антигены), что приводит к образованию естественных антител и Т-клеточного ответа на опухоль. К сожалению, не было идентифицировано ни одной молекулы, специфичной для эпителиоидной саркомы, для тестирования такого подхода. [ 40 ] [ 42 ]
Адоптивная иммунотерапия направлена на расширение популяции Т-клеток организма, которые будут распознавать специфический опухолевый антиген. Т-клетки можно собирать, а затем размножать и подвергать генетическим манипуляциям для распознавания определенных опухолевых маркеров. [ 40 ] [ 42 ] В одном случае у пациента с запущенной эпителиоидной саркомой, у которого не удалось пройти многократную терапию, наблюдался сильный ответ на увеличенные лимфоциты и естественные клетки-киллеры. [ 43 ] Однако по состоянию на 2023 год не проводится никаких конкретных клинических исследований, посвященных клеточной терапии именно эпителиоидной саркомы.
Ингибиторы иммунных контрольных точек одобрены для использования при многих типах рака, хотя FDA не одобрило такие препараты для пациентов с эпителиоидной саркомой. Известно, что некоторые виды рака препятствуют распознаванию иммунной системой и позволяют опухоли ускользнуть от иммунного надзора. [ 41 ] Воздействие на эти ингибирующие белки открывает путь иммунной системе к распознаванию опухоли. Двумя из этих ингибирующих белков являются CTLA-4 и PD1. [ 41 ] и лекарства, нацеленные на эти блокаторы иммунной системы, исследуются у пациентов с саркомами, такими как эпителиоидная саркома.
Антиангиогенная терапия
[ редактировать ]Несколько антиангиогенных агентов исследуются при эпителиоидной саркоме. [ нужна ссылка ] рак, который, вероятно, зависит от ангиогенеза для выживания и прогрессирования. Эти агенты взаимодействуют с различными проангиогенными факторами, некоторые из которых, как известно, сверхэкспрессируются при эпителиоидной саркоме. [ 16 ] [ 23 ] (например, VEGF и EGFR). [ 44 ] [ 45 ] Опухолям требуется кровоснабжение, чтобы обеспечить их кислородом и питательными веществами, необходимыми для их выживания. По мере того, как опухоли расширяются и растут, они посылают различные сигналы (например, HIF1), которые способствуют развитию новых кровеносных сосудов в опухоли. [ 46 ] Антиангиеновый препарат пазопаниб одобрен во многих странах для применения при таких саркомах, как эпителиоидная саркома.
«Таргетная» терапия
[ редактировать ]Учитывая множественные генетические аномалии и нарушения биологических путей, наблюдаемые при эпителиоидной саркоме, в настоящее время изучаются препараты, нацеленные на уникальные характеристики опухоли, для более эффективного лечения.
Ингибиторы тирозинкиназы
[ редактировать ]Ингибиторы тирозинкиназы (такие как сунитиниб , пазопаниб и дазатиниб ) показали некоторый эффект против нескольких типов рака, одним из примеров сарком является иматиниб при стромальных опухолях желудочно-кишечного тракта (ГИСО). [ 47 ] Тирозинкиназа (подкласс протеинкиназ) — фермент , переносящий фосфатную группу с молекулы АТФ на белок в клетке. [ 48 ] Он действует как переключатель «включения» или «выключения» для многих клеточных функций, включая передачу сигналов внутри клетки и деление клеток.
Тирозинкиназы могут содержать мутации, которые заставляют их становиться конститутивно активными. [ 49 ] или застревает во включенном положении, что приводит к нерегулируемому делению клеток (признак рака). Ингибиторы тирозинкиназы блокируют действие этих ферментов. Было показано, что ингибиторы тирозинкиназы ингибируют VEGF, EGFR и MET. [ 48 ] пути, которые часто сверхэкспрессируются при эпителиоидной саркоме. Их также можно использовать против сигнальных путей KIT и JAK-STAT . [ 48 ] которые участвуют во многих раковых заболеваниях и могут быть вовлечены в эпителиоидную саркому. Темсиролимус представляет собой ингибитор тирозинкиназы, который блокирует действие белка mTOR и ингибирует путь mTOR. Из-за перекрестных помех между клеточными сигнальными путями было показано, что, хотя вмешательство только в путь mTOR дает лишь ограниченные результаты в остановке онкогенеза, одновременное ингибирование путей mTOR и EGFR дает повышенный эффект. [ 22 ]
ЕГО
[ редактировать ]Селективные ингибиторы ядерного экспорта ( SINE ), такие как селинексор и CBS9106 , исследуются при нескольких саркомах и показали многообещающие результаты как при гематологических злокачественных новообразованиях , так и при солидных опухолях . [ 50 ] [ 51 ] Однако рандомизированное исследование селинексора при липосаркоме, дальнем родственнике эпителиоидной саркомы, дало отрицательный результат. У Селинексора есть одобрение для лечения других диагнозов рака.
Ингибиторы HDAC
[ редактировать ]Ингибиторы гистондеацетилазы ( HDAC ), такие как вориностат , показали некоторую перспективность при эпителиоидной саркоме. Исследователи из Техаса изучают, могут ли ингибиторы HDAC обратить вспять потерю функции INI1, характерную для эпителиоидной саркомы. [ 8 ] Ингибиторы HDAC блокируют события, участвующие в репликации ДНК и, следовательно, в делении клеток. [ 52 ] Было показано, что блокирование HDAC стимулирует раковые клетки к апоптозу. [ 8 ] некоторые диетические фитохимические вещества являются эффективными ингибиторами HDAC. Было показано, что [ 53 ] К ним относятся сульфорфан, индол-3-карбинол и фенэтилизотиоцианаты, содержащиеся в брокколи, капусте и кресс-салате, а также эпигаллокацехин-3-галлат, содержащийся в зеленом чае. [ нужна ссылка ]
Ингибиторы CDK
[ редактировать ]Из-за связи (см. выше) с циклином D1 ингибиторы CDK изучаются при различных видах рака. Палбоциклиб является ингибитором CDK (одобрен для лечения некоторых видов рака молочной железы благодаря блокаде CDK4 и CDK6). Другие экспериментальные ингибиторы CDK4/6 включают абемациклиб и рибоциклиб .
Нацеливание на раковые стволовые клетки
[ редактировать ]раковые стволовые клетки Считается, что (или клетки, инициирующие рак) представляют собой небольшую популяцию клеток внутри опухоли, которые непосредственно ответственны за образование опухоли. Считается, что они устойчивы к лечению и обладают способностью образовывать все клетки, необходимые для развития опухоли. Предполагается, что они являются фактором, способствующим прогрессированию рака и рецидивам после лечения. В эпителиоидной саркоме были обнаружены определенные «стволоподобные» клетки, меченные CD109 (кластер дифференцировки 109). [ 25 ] обеспечивая теоретически эффективную мишень для лечения эпителиоидной саркомы. Однако CD109 экспрессируется во многих нормальных клетках организма, таких как Т-клетки и эндотелиальные клетки, выстилающие каждый кровеносный сосуд, что делает CD109 плохой мишенью для иммунотерапии.
Онколитическая вирусная терапия
[ редактировать ]Онколитическая вирусная терапия — это новый метод лечения рака, целью которого является заражение раковых клеток генетически модифицированным вирусом, способным проникать в ДНК клетки. В этом случае вирус (1) не может нанести прямой ущерб раковой клетке, (2) передается по клеткам опухоли посредством репродукции вируса и (3) становится мишенью для иммунного ответа пациента. [ 17 ] [ 54 ]
Отмечено, что терапевтический потенциал онколитической виротерапии не является простым следствием цитопатического действия , а во многом зависит от активации собственного иммунного ответа организма против инфицированных клеток. [ 54 ] [ 55 ] Превосходные противораковые эффекты наблюдались, когда онколитические вирусы были созданы для экспрессии (или совместного применения) иммуностимулирующих молекул, таких как GM-CSF. [ 55 ]
Теломелизин (OBP-301) представляет собой аденовирус, нацеленный на теломеразу . [ 56 ] фермент, который экспрессируется практически во всех раковых клетках, но не экспрессируется в нормальных клетках. OBP-301 не одобрен для использования у онкологических больных, но он был изучен при эпителиоидной саркоме и в лабораторных условиях было показано, что он способствует апоптозу и гибели клеток. [ 56 ]
CGTG-102 (разработанный Oncos Therapeutics) представляет собой аденовирус, в настоящее время находящийся в статусе орфанного препарата для лечения сарком мягких тканей. Он модифицирован для избирательной репликации в p16/Rb-дефектных клетках, к которым относится большинство раковых клеток человека. Кроме того, CGTG-102 кодирует гранулоцитарно-макрофагальный колониестимулирующий фактор ( GM-CSF ), [ 55 ] [ 57 ] мощная иммуностимулирующая молекула. Хотя CGTG-102 показал эффективность в качестве отдельного средства против нескольких сарком мягких тканей в лаборатории, по состоянию на 2023 год клинические исследования по нему, по-видимому, остановились. [ 58 ]
Дополнительные изображения
[ редактировать ]-
Интермед. маг.
-
Высокая маг.
-
Высокая маг. (СМАРКБ1)
См. также
[ редактировать ]- Саркома мягких тканей
- Саркома
- Злокачественная рабдоидная опухоль
- Атипичная тератоидная/рабдоидная опухоль
Ссылки
[ редактировать ]- ^ Jump up to: а б Энцингер, FM (1970). «Эпителиоидная саркома. Саркома, симулирующая гранулему или карциному» . Рак . 26 (5): 1029–41. doi : 10.1002/1097-0142(197011)26:5<1029::AID-CNCR2820260510>3.0.CO;2-R . ПМИД 5476785 .
- ^ Гийу, Л; Вадден, К; Коиндре, Дж. М.; Крауш, Т; Флетчер, компакт-диск (1997). « Эпителиоидная саркома проксимального типа, характерное агрессивное новообразование с рабдоидными признаками. Клинико-патологическое, иммуногистохимическое и ультраструктурное исследование серии». Американский журнал хирургической патологии . 21 (2): 130–46. дои : 10.1097/00000478-199702000-00002 . ПМИД 9042279 .
- ^ Jump up to: а б с Арма, Генри Б. Арма; Парвани, Анил В. (2009). «Эпителиоидная саркома» . Архивы патологии и лабораторной медицины . 133 (5): 814–9. дои : 10.5858/133.5.814 . ПМИД 19415960 .
- ^ Като, Масахито; Ватанабе, Мика; Огосе, Акира; Морита, Такаши, Сэцуя (2004). ". Японский журнал клинической онкологии . 34 (3): 149–54. doi : 10.1093/jjco/hyh027 . PMID 15078911 .
- ^ Леви, Антонин; Ле Пешу, Сесиль; Терьер, Филипп; Буайта, Райан; Домон, Жюльен; Мир, Оливье; Коппола, Сара; Оноре, Шарль; Ле Сесн, Аксель; Бонвало, Сильви (2014). «Эпителиоидная саркома: необходимость мультимодального подхода для максимизации шансов на радикальное консервативное лечение». Анналы хирургической онкологии . 21 (1): 269–76. дои : 10.1245/s10434-013-3247-4 . ПМИД 24046109 . S2CID 21163484 .
- ^ Jump up to: а б с Казанова, Микела; Феррари, Андреа; Коллини, Паола; Нужно, Джанни; Перевозка, Рита; Чекетто, Джованни; Гронки, Алессандро; Меацца, Кристина; Гаравента, Альберто; Ди Катальдо, Андреа; Карли, Модесто (2006). «Эпителиоидная саркома у детей и подростков». Рак . 106 (3): 708–17. дои : 10.1002/cncr.21630 . ПМИД 16353216 . S2CID 25321347 .
- ^ Джавад, Мухаммад Умар; Экстейн, Джейсон; Мин, Элайджа С.; Скалли, Шон П. (2009). «Прогностические факторы выживаемости пациентов с эпителиоидной саркомой: 441 случай из базы данных SEER» . Клиническая ортопедия и связанные с ней исследования . 467 (11): 2939–48. дои : 10.1007/s11999-009-0749-2 . ПМЦ 2758965 . ПМИД 19224301 .
- ^ Jump up to: а б с д Лев, Дина. «Эпигенетическое перепрограммирование эпителиолдной саркомы: роль перекрестных помех INI1-HDAC» . Архивировано из оригинала 22 апреля 2015 г.
- ^ Jump up to: а б Бос, Грузия; Причард, диджей; Рейман, HM; Добинс, Дж. Х.; Иструп, ДМ; Лэндон, GC (1988). «Эпителиоидная саркома. Анализ пятидесяти одного случая» . Журнал костной и суставной хирургии. Американский том . 70 (6): 862–70. дои : 10.2106/00004623-198870060-00011 . ПМИД 3392084 . Архивировано из оригинала 28 марта 2020 г. Проверено 06 октября 2015 г.
- ^ Jump up to: а б с Хорник, Джейсон Л .; Дал Син, Паола; Флетчер, Кристофер DM (2009). «Потеря экспрессии INI1 характерна как для обычной, так и для эпителиоидной саркомы проксимального типа». Американский журнал хирургической патологии . 33 (4): 542–50. дои : 10.1097/PAS.0b013e3181882c54 . ПМИД 19033866 . S2CID 5167769 .
- ^ Jump up to: а б Модена, Пьерджорджо; Луальди, Елена; Факкинетти, Федерика; Галли, Лиза; Тейшейра, Мануэль Р.; Пилотти, Сильвана; Соцци, Габриэлла (2005). « Ген-супрессор опухоли SMARCB1/INI1 часто инактивируется при эпителиоидных саркомах» . Исследования рака . 65 (10): 4012–9. дои : 10.1158/0008-5472.CAN-04-3050 . ПМИД 15899790 .
- ^ Лушникова Тамара; Кнуутила, Сакари; Миеттинен, Маркку (2000). «Изменение числа копий ДНК при эпителиоидной саркоме и ее вариантах: сравнительное исследование геномной гибридизации» . Современная патология . 13 (10): 1092–6. doi : 10.1038/modpathol.3880203 . ПМИД 11048803 . S2CID 23521276 .
- ^ Нисио, Джун; Ивасаки, Хироши; Набэсима, Кадзуки; Исигуро, Масако; Науманн, Сабина; Исаяма, Теруто; Наито, Масатоши; Канеко, Ясухико; Кикучи, Масахиро; Мост, Джулия (2005). «Создание новой линии клеток эпителиоидной саркомы человека, FU-EPS-1: молекулярно-цитогенетическая характеристика с использованием спектрального кариотипирования и сравнительной геномной гибридизации». Международный журнал онкологии . 27 (2): 361–9. дои : 10.3892/ijo.27.2.361 . ПМИД 16010416 .
- ^ Jump up to: а б с Лин, Лин; Хикс, Дэвид; Сюй, Бо; Сигел, Джессика Э; Бергфельд, Вильма Ф; Монтгомери, Элизабет; Фишер, Сирил; Хартке, Мэрибет; Таббс, Рэймонд; Голдблюм, Джон Р. (2005). «Профиль экспрессии и молекулярно-генетическая регуляция экспрессии циклина D1 при эпителиоидной саркоме». Современная патология . 18 (5): 705–9. doi : 10.1038/modpathol.3800349 . ПМИД 15578074 . S2CID 24821026 .
- ^ Кахали, Бхаскар; Ю, Цзиньлун; Маркес, Стефани Б.; Томпсон, Кеннет В.; Лян, Шерми Ю.; Лу, Ли; Райсман, Дэвид (2014). «Замалчивание субъединицы SWI/SNF и противоракового гена BRM в рабдоидных опухолях» . Онкотаргет . 5 (10): 3316–32. doi : 10.18632/oncotarget.1945 . ПМК 4102812 . ПМИД 24913006 .
- ^ Jump up to: а б Кунен, Корнелиус; Ленхардт, Маркус; Толнай, Эдина; Мюльбергер, Томас; Фогт, Питер М.; Мюллер, Клаус-Майкл (2000). «Закономерности экспрессии и секреции фактора роста эндотелия сосудов при злокачественных опухолях мягких тканей». Журнал исследований рака и клинической онкологии . 126 (4): 219–25. дои : 10.1007/s004320050036 . ПМИД 10782895 . S2CID 21613610 .
- ^ Jump up to: а б с Мартин Либерал, Хуан; Лагарес-Тена, Лаура; Сайнс-Хаспеадо, Мигель; Матео-Лозано, Сильвия; Гарсия дель Муро, Ксавьер; Тирадо, Оскар М. (2012). «Таргетная терапия сарком: бросая вызов» . Саркома . 2012 : 1–13. дои : 10.1155/2012/626094 . ПМЦ 3372278 . ПМИД 22701332 .
- ^ Кунен, К.; Толнай, Эдина; Штайнау, Ганс Ульрих; Восс, Бруно; Мюллер, Клаус-Майкл (1998). «Экспрессия рецептора c-Met и фактора роста гепатоцитов/фактора рассеяния при синовиальной саркоме и эпителиоидной саркоме». Архив Вирхова . 432 (4): 337–42. дои : 10.1007/s004280050175 . ПМИД 9565343 . S2CID 30726514 .
- ^ Jump up to: а б с д Имура, Хирохико; Вакамацу, Тору; Ямада, Сютаро; Араки, Нобухито; Ито, Кадзуюки; Норифуми (2014 г.) «Комбинированное нацеливание mTOR и Сигнальные пути c-MET для эффективного лечения эпителиоидной саркомы» . Molecular Cancer . 13 : 185. doi : /1476-4598-13-185 . PMC 4249599. . PMID 25098767 10.1186
- ^ Имура, Хирохико; Вакамацу, Тору; Ямада, Сютаро; Араки, Нобухито; Ито, Кадзуюки; Норифуми (07.08.2014). «Комбинированный таргетинг» . сигнальных путей mTOR и c-MET для эффективного лечения эпителиоидной саркомы» . Molecular Cancer . 13 : 185. doi : /1476-4598-13-185 . ISSN 1476-4598 . PMC 4249599. . PMID 25098767 10.1186
- ^ Номер клинического исследования NCT01154452 «Висмодегиб и ингибитор сигнального пути гамма-секретазы/Notch RO4929097 в лечении пациентов с распространенной или метастатической саркомой» на сайте ClinicalTrials.gov.
- ^ Jump up to: а б с д и Се, X.; Гадими, магистр здравоохранения; Янг, ЭД; Белоусов Р.; Чжу, К.-с.; Лю, Дж.; Лопес, Г.; Коломбо, К.; Пэн, Т.; Рейносо, Д.; Хорник, Дж.Л.; Лазар, Эй Джей; Лев, Д. (2011). «Сочетание блокады EGFR и mTOR для лечения эпителиоидной саркомы» . Клинические исследования рака . 17 (18): 5901–12. дои : 10.1158/1078-0432.CCR-11-0660 . ПМК 3176924 . ПМИД 21821699 .
- ^ Jump up to: а б Касио, Майкл Дж; О'Доннелл, Ричард Дж; Хорвай, Эндрю Э (2010). «Эпителиоидная саркома экспрессирует рецептор эпидермального фактора роста, но амплификация генов и мутации киназного домена встречаются редко» . Современная патология . 23 (4): 574–80. дои : 10.1038/modpathol.2010.2 . ПМИД 20118913 . S2CID 11592703 .
- ^ Ян, Ж.-Л.; Ханнан, Монтана; Рассел, П.Дж.; Кроу, Пи Джей (2006). «Экспрессия белка HER1/EGFR в саркомах мягких тканей человека». Европейский журнал хирургической онкологии . 32 (4): 466–8. дои : 10.1016/j.ejso.2006.01.012 . ПМИД 16524687 .
- ^ Jump up to: а б Ахмад, Аамир, Макото, Томохидэ; Кано, Масанобу, Кенджи; Кубо, Асанума, Хироко; Сонода, Томоко; Ториго, Тошихико; Ямасита, Тошихико, Нориюки (2013). Сатоши, Джун; Ивасаки , Подобно клеткам/клеткам, инициирующим рак, в новой клеточной линии эпителиоидной саркомы ESX и связано с плохим прогнозом саркомы мягких тканей» . PLOS ONE . 8 (12): e84187. Bibcode : 2013PLoSO...884187E . doi : 10.1371 /журнал . PMC 3869840 .pone.0084187 PMID 24376795 .
- ^ Стадия саркомы мягких тканей в eMedicine
- ^ Блей, Дж.-Ю.; Оноре, К.; Стокль, Э.; Меус, П.; Джафари, М.; Гуэн, Ф.; Анракт, П.; Феррон, Г.; Рохвергер, А.; Ропарс, М.; Каррере, С.; Маршал, Ф.; Сирво, Ф.; Ди Марко, А.; Ле Наиль, LR (01 июля 2019 г.). «Хирургия в справочных центрах улучшает выживаемость пациентов с саркомой: общенациональное исследование» . Анналы онкологии . 30 (7): 1143–1153. дои : 10.1093/annonc/mdz124 . ISSN 1569-8041 . ПМК 6637376 . ПМИД 31081028 .
- ^ Jump up to: а б де Вишер, Себастьян AHJ; ван Гинкель, Робберт Дж.; Воббес, Тео; Вет, Рене П.Х.; тен Хевел, Сюзанна Э.; Суурмейер, Альберт Дж. Х.; Хоекстра, Харад Дж. (2006). «Эпителиоидная саркома: все еще единственное заболевание, излечимое хирургическим путем» . Рак . 107 (3): 606–12. дои : 10.1002/cncr.22037 . ПМИД 16804932 . S2CID 25833518 .
- ^ Рао, Бхаскар Н.; Родригес-Галиндо, Карлос (2003). «Местный контроль сарком конечностей у детей: сохранение конечностей и щадящая функция». Медицинская и детская онкология . 41 (6): 584–7. дои : 10.1002/mpo.10405 . ПМИД 14595726 .
- ^ Феррари, Андреа; Мичели, Розальба; Рей, Энни; Оберлин, Одиль; Орбах, Дэниел; Бреннан, Бернадетт; Мариани, Луиджи; Карли, Модесто; Нужно, Джанни; Чекетто, Джованни; Сальво, Джан Лука Де; Казанова, Микела; Ваннозель, Макс М.; Келси, Анна; Стивенс, Майкл С.; Девидас, Минакши; Паппо, Альберто С.; Спунт, Шери Л. (2011). «Неметастатические нерезецированные педиатрические нерабдомиосаркомные саркомы мягких тканей: результаты объединенного анализа групп из США и Европы» . Европейский журнал рака . 47 (5): 724–31. дои : 10.1016/j.ejca.2010.11.013 . ПМЦ 3539303 . ПМИД 21145727 .
- ^ ДеГрут, Генри; Эллисон, Брюс. «Хирургия спасения конечностей при саркомах конечностей» . Архивировано из оригинала 8 февраля 2015 г. Проверено 23 апреля 2015 г. [ ненадежный медицинский источник? ]
- ^ Jump up to: а б Саркома мягких тканей . Клинические рекомендации по онкологии. Национальная комплексная онкологическая сеть. Архивировано из оригинала 5 августа 2018 г. Проверено 06 октября 2015 г. [ нужна страница ]
- ^ Вольф, Патрик С.; Флум, Дэвид Р.; Танас, Мунир Р.; Рубин, Брайан П.; Манн, Гэри Н. (2008). «Эпителиоидная саркома: опыт Вашингтонского университета». Американский журнал хирургии . 196 (3): 407–12. дои : 10.1016/j.amjsurg.2007.07.029 . ПМИД 18436180 .
- ^ «FDA одобряет первый вариант лечения специально для пациентов с эпителиоидной саркомой, редким раком мягких тканей» (пресс-релиз). FDA. 23 января 2020 г. . Проверено 3 марта 2020 г.
- ^ Jump up to: а б Чейз, ДР; Энцингер, FM (1985). «Эпителиоидная саркома. Диагностика, прогностические показатели и лечение» . Американский журнал хирургической патологии . 9 (4): 241–63. дои : 10.1097/00000478-198504000-00001 . ПМИД 4014539 . S2CID 36504524 .
- ^ Лефрак, Эдвард А.; Питха, Ян; Розенхайм, Сидней; Готлиб, Джеффри А. (1973). «Клинико-патологический анализ кардиотоксичности адриамицина». Рак . 32 (2): 302–14. doi : 10.1002/1097-0142(197308)32:2<302::AID-CNCR2820320205>3.0.CO;2-2 . ПМИД 4353012 . S2CID 41537913 .
- ^ Липшульц, Стивен Э.; Колан, Стивен Д.; Гелбер, Ричард Д.; Перес-Атайде, Антонио Р.; Саллан, Стивен Э.; Сандерс, Стивен П. (1991). «Поздние сердечные эффекты терапии доксорубицином при остром лимфобластном лейкозе в детском возрасте» . Медицинский журнал Новой Англии . 324 (12): 808–15. дои : 10.1056/NEJM199103213241205 . ПМИД 1997853 .
- ^ Мэн, Ф.; Эванс, Дж.В.; Бхупати, Д.; Баника, М.; Лан, Л.; Лоренте, Г.; Дуань, Ж.-Х.; Цай, X.; Моудей, AM; Гиз, КП; Мароз, А.; Андерсон, РФ; Паттерсон, А.В.; Стачелек, ГК; Глейзер, премьер-министр; Маттеуччи, доктор медицины; Харт, КП (2012). «Молекулярная и клеточная фармакология пролекарства, активируемого гипоксией TH-302» . Молекулярная терапия рака . 11 (3): 740–51. дои : 10.1158/1535-7163.MCT-11-0634 . ПМИД 22147748 . S2CID 11701323 .
- ^ Чавла, СП; Кранмер, Л.Д.; Ван Тайн, бакалавр; Рид, доктор медицинских наук; Окуно, SH; Бутринский, Дж. Э.; Адкинс, Д.Р.; Хендифар, А.Е.; Кролл, С.; Ганджу, КН (2014). «Исследование фазы II безопасности и противоопухолевой активности активируемого гипоксией пролекарства TH-302 в комбинации с доксорубицином у пациентов с распространенной саркомой мягких тканей» . Журнал клинической онкологии . 32 (29): 3299–306. дои : 10.1200/JCO.2013.54.3660 . ПМЦ 4588714 . ПМИД 25185097 .
- ^ Jump up to: а б с д Уилки, Брилин; Голдберг, Джон М. (14 апреля 2014 г.). «Иммунотерапия саркомы: новый рубеж» . Медицина открытий . 17 (94): 201–6. ПМИД 24759624 .
- ^ Jump up to: а б с Ху, Джеймс С.; Скит, Джозеф Дж; Каст, Виджбе Мартин (2014). «Иммунотерапия при саркоме: краткий обзор» . Международное исследование саркомы . 1 (1): id1003.
- ^ Jump up to: а б Педраццоли, Паоло; Секондино, Симона; Прекрасно, Витторио; Комоли, Патриция; Монтанья, Даниэла (2011). «Иммунотерапевтическое вмешательство против сарком» . Журнал рака . 2 :350–6. дои : 10.7150/jca.2.350 . ПМК 3119402 . ПМИД 21716856 .
- ^ Ратнавелу, Кананатан; Субрамани, Баскар; Пуллай, Читра Раманатан; Кришнан, Кохила; Сугадан, Шила Деви; Рао, Манджунатх Садананда; Виракумарасивам, Абхи; Дэн, Сювэнь; Хироши, Терунума (2013). «Аутологичная иммунная терапия против распространенной эпителиоидной саркомы: отчет о случае» . Письма об онкологии . 5 (5): 1457–1460. дои : 10.3892/ол.2013.1247 . ПМЦ 3678875 . ПМИД 23761810 .
- ^ Чардиелло, Ф; Трояни, Т; Бьянко, Р; Ордитура, М; Морджилло, Ф; Мартинелли, Э; Морелли, член парламента; Касконе, Т; Тортора, Дж. (2006). «Взаимодействие между рецептором эпидермального фактора роста (EGFR) и путями фактора роста эндотелия сосудов (VEGF): рациональный подход к многоцелевой противораковой терапии» . Анналы онкологии . 17 (Приложение 7): vii109–14. дои : 10.1093/annonc/mdl962 . ПМИД 16760272 .
- ^ Хирата, Акира; Огава, Соитиро; Комета, Такуро; Кувано, Такаши; Наито, Сейджи; Кувано, Мичихико; Оно, Маюми (2002). «ZD1839 (Iressa) вызывает антиангиогенные эффекты посредством ингибирования тирозинкиназы рецептора эпидермального фактора роста» . Исследования рака . 62 (9): 2554–60. ПМИД 11980649 .
- ^ Кармелиет, Питер; Дор, Юваль; Герберт, Жан-Марк; Фукумура, Дай; Брюссельманс, Коэн; Деверчин, Мике; Нееман, Михал; Боно, Франсуаза; Абрамович, Ринат; Максвелл, Патрик; Кох, Кэмерон Дж.; Рэтклифф, Питер; Луны, Живи; Джайн, Ракеш К.; Коллен, Дезире; Кешет, Эли (1998). «Роль HIF-1α в апоптозе, опосредованном гипоксией, пролиферации клеток и опухолевом ангиогенезе». Природа . 394 (6692): 485–90. Бибкод : 1998Natur.394..485C . дои : 10.1038/28867 . ПМИД 9697772 . S2CID 4419118 .
- ^ Деметрий, Г.Д. (2002). «Идентификация и лечение химиорезистентного неоперабельного или метастатического ГИСО: опыт применения селективного ингибитора тирозинкиназы мезилата иматиниба (STI571)». Европейский журнал рака . 38 (Приложение 5): S52–9. дои : 10.1016/s0959-8049(02)80603-7 . ПМИД 12528773 .
- ^ Jump up to: а б с Арора, Амит; Ученый, Эрик М. (2005). «Роль ингибиторов тирозинкиназы в терапии рака». Журнал фармакологии и экспериментальной терапии . 315 (3): 971–9. дои : 10.1124/jpet.105.084145 . ПМИД 16002463 . S2CID 33720 .
- ^ Лендьель, Эрнст; Савада, Кенджиро; Салгия, Рави (2007). «Мутации тирозинкиназы при раке человека». Современная молекулярная медицина . 7 (1): 77–84. дои : 10.2174/156652407779940486 . ПМИД 17311534 .
- ^ Герецитано, Джон (2014). «СИНЭ (селективный ингибитор ядерного экспорта) – переводная наука в новый класс противораковых средств» . Журнал гематологии и онкологии . 7:67 . дои : 10.1186/s13045-014-0067-3 . ПМК 4197302 . ПМИД 25281264 .
- ^ Сакакибара, К.; Сайто, Н.; Сато, Т.; Сузуки, А.; Хасэгава, Ю.; Фридман, Дж. М.; Куфе, Д.В.; ФонХофф, Д.Д.; Ивами, Т.; Кавабе, Т. (2011). «CBS9106 — это новый обратимый пероральный ингибитор CRM1 с активностью, разрушающей CRM1» . Кровь 118 (14): 3922–31. дои : 10.1182/blood-2011-01-333138 . ПМИД 21841164 . S2CID 16936188 .
- ^ Демикко, Элизабет Г.; Маки, Роберт Г.; Лев, Дина С.; Лазар, Александр Дж. (2012). «Новые терапевтические цели при саркоме мягких тканей» . Достижения анатомической патологии . 19 (3): 170–80. дои : 10.1097/PAP.0b013e318253462f . ПМЦ 3353406 . ПМИД 22498582 .
- ^ Раджендран, Правин; Эй, Эмили; Уильямс, Дэвид Э; Дэшвуд, Родерик Х (2011). «Диетические фитохимические вещества, ингибирование HDAC и дефекты повреждения/восстановления ДНК в раковых клетках» . Клиническая эпигенетика . 3 (1): 4. дои : 10.1186/1868-7083-3-4 . ПМЦ 3255482 . ПМИД 22247744 .
- ^ Jump up to: а б Пол, Джонатан Дж; Рессегье, Жюльен; Личти, Брайан Д. (2012). «Онколитические вирусы: шаг в иммунотерапию рака» . Адаптация и лечение вирусов . 4 : 1–21. дои : 10.2147/VAAT.S12980 .
- ^ Jump up to: а б с Хемминки, Аксели (2014). «Онколитическая иммунотерапия: где мы находимся клинически?» . Научка . 2014 : 1–7. дои : 10.1155/2014/862925 . ПМЦ 3914551 . ПМИД 24551478 .
- ^ Jump up to: а б Ли, Гуй-Донг; Кавасима, Хироюки; Огосе, Акира; Ариизуми, Такаши; Хотта, Тецуо; Кувано, Рёзо; Урата, Ясуо; Фудзивара, Тосиёси; Эндо, Наото (2013). «Теломелизин проявляет мощную противоопухолевую активность посредством апоптотической и неапоптотической гибели клеток в клетках саркомы мягких тканей» . Раковая наука . 104 (9): 1178–88. дои : 10.1111/cas.12208 . ПМЦ 7656541 . ПМИД 23718223 . S2CID 33300842 .
- ^ Браманте, Симона; Коски, Анниина; Шкипер, Аня; Дьякону, Юлия; Лииканен, Илкка; Хемминки, Отто; Васильева, Лотта; Парвиайнен, Суви; Черулло, Винченцо; Песонен, Сайла К; Оксанен, Минна; Хейсканен, Райта; Рувинен-Лагерстрем, Нура; Мерисало-Сойккели, Майджу; Хаконен, Тиина; Йоэнсуу, Тимо; Хизер, Анна; Песонен, Сари; Хемминки, Аксели (2014). «Серотип химерного онколитического аденовируса, кодирующего GM-CSF, для лечения саркомы у грызунов и людей». Международный журнал рака . 135 (3): 720–30. дои : 10.1002/ijc.28696 . ПМИД 24374597 . S2CID 22657446 .
- ^ «CTG Labs-NCBI» . www.clinicaltrials.gov . Проверено 12 ноября 2023 г.
Дальнейшее чтение
[ редактировать ]- Ласкин, Уильям Б.; Миеттинен, Маркку (2003). «Эпителиоидная саркома: новые данные, основанные на расширенном иммуногистохимическом анализе» . Архивы патологии и лабораторной медицины . 127 (9): 1161–8. дои : 10.5858/2003-127-1161-ESNIBO . ПМИД 12946229 .