ПЭТ для визуализации костей
Позитронно-эмиссионная томография для визуализации костей, как метод отслеживания in vivo , позволяет измерять региональную концентрацию радиоактивности изображения, , пропорциональную значениям пикселей усредненным по интересующей области (ROI) в костях. Позитронно-эмиссионная томография — это метод функциональной визуализации , который использует 18 F]NaF Радиофармпрепарат для визуализации и количественной оценки регионального костного метаболизма и кровотока. [ 18 F]NaF использовался для визуализации костей в течение последних 60 лет. В данной статье основное внимание уделяется фармакокинетике [ 18 F]NaF в костях, а также различные полуколичественные и количественные методы количественной оценки регионального костного метаболизма с использованием [ 18 F]NaF ПЭТ-изображения.
Использование [ 18 Ф]НаФ ПЭТ
[ редактировать ]Измерение регионального костного метаболизма имеет решающее значение для понимания патофизиологии метаболических заболеваний костей.
- Биопсия кости считается золотым стандартом количественной оценки метаболизма костной ткани; однако его выполнение является инвазивным, сложным и дорогостоящим, а также приводит к значительным ошибкам измерений. [1]
- Измерения биомаркеров костного обмена в сыворотке или моче являются простыми, дешевыми, быстрыми и неинвазивными методами измерения изменений костного метаболизма, но предоставляют информацию только о глобальном скелете. [2]
- Метод функциональной визуализации динамического [ 18 ПЭТ-сканирование F]NaF может количественно оценить региональный обмен костной ткани в определенных участках, имеющих клиническое значение, таких как поясничный отдел позвоночника и бедро. [3] и был подтвержден сравнением с золотым стандартом биопсии кости. [4] [5] [6]
Фармакокинетика [ 18 Ф]НаФ
[ редактировать ]Химически стабильный анион фтора -18-фторида является радиофармпрепаратом, ищущим кости, при визуализации скелета. [ 18 F]NaF имеет склонность откладываться в областях, где кость вновь минерализуется. [5] [7] [8] [9] [10] Многие исследования [ 18 F]NaF ПЭТ для измерения метаболизма костной бедра ткани , [3] поясничный отдел позвоночника и плечевая кость . [11] [ 18 F]NaF поглощается экспоненциально, что представляет собой уравновешивание индикатора с пространствами внеклеточной и клеточной жидкости с периодом полураспада 0,4 часа и почками с периодом полураспада 2,4 часа. [12] Однопроходное извлечение [ 18 F]NaF в кости составляет 100%. [13] Через час в крови остается только 10% введенной активности . [14]
18 Считается, что ионы F- занимают пространства внеклеточной жидкости, потому что, во-первых, они уравновешиваются с пространствами трансклеточной жидкости и, во-вторых, они не являются полностью внеклеточными ионами. [15] [16] [17] Фторид находится в равновесии с фтористым водородом , который имеет высокую проницаемость, позволяющую фториду проникать через плазматическую мембрану крови . [18] Циркуляция фтора в эритроцитах составляет 30%. [19] Однако он свободно доступен для поглощения поверхностью кости, поскольку равновесие между эритроцитами и плазмой происходит намного быстрее, чем время капиллярного транзита. Это подтверждается исследованиями, сообщающими о 100% экстракции цельной крови за один проход. 18 F- ион кости [13] и быстрое высвобождение 18 Ионы F- из эритроцитов с константой скорости 0,3 в секунду. [20]
[ 18 F]NaF также поглощается незрелыми эритроцитами костного мозга . [21] который играет роль в кинетике фторидов. [22] Связывание с белками плазмы [ 18 F]NaF незначительно. [23] [ 18 Почечный клиренс F]NaF зависит от диеты. [24] и pH , уровень [25] за счет его реабсорбции в нефроне, опосредованной фтористым водородом. [26] Однако большие различия в скорости потока мочи [19] в контролируемых экспериментах избегают, сохраняя патенты хорошо увлажненными. [21]
Обменный пул и размер метаболически активных поверхностей в костях определяют количество накопленного или обмененного индикатора. [27] с костной внеклеточной жидкостью , [28] хемосорбция на кристаллах гидроксиапатита с образованием фторапатита, [14] [29] [9] как показано в уравнении-1: [30] [31]
Уравнение-1
Ионы фтора из кристаллического матрикса кости высвобождаются при ремоделировании кости, что позволяет оценить скорость костного метаболизма. [32] [33] [34]
Измерительный внедорожник
[ редактировать ]Определение
[ редактировать ]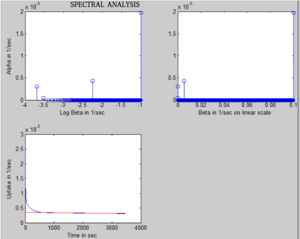
Стандартизированное значение поглощения (SUV) определяется как концентрация в тканях (КБк/мл), деленная на инъецированную активность, нормализованную по массе тела . [35]
Соответствие
[ редактировать ]Внедорожник, измеренный по большой рентабельности инвестиций, сглаживает шум и, следовательно, более подходит для [ 18 F]NaF в исследованиях костей, поскольку радиофармпрепарат довольно равномерно распределяется по всей кости. Измерить внедорожник легко, [36] дешевле и быстрее в исполнении, что делает его более привлекательным для клинического использования. Его использовали для диагностики и оценки эффективности терапии. [37] [38] Внедорожник можно измерить на одном участке или на всем скелете с помощью серии статических сканирований и ограничить небольшим полем зрения ПЭТ-сканера. [32]
Известные проблемы
[ редактировать ]SUV стал клинически полезным, хотя и спорным, полуколичественным инструментом ПЭТ-анализа. [39] Стандартизация протоколов визуализации и измерение SUV одновременно после инъекции радиофармпрепарата необходимы для получения правильного SUV. [40] потому что визуализация до плато поглощения приводит к непредсказуемым ошибкам до 50% для внедорожников. [41] Шум, разрешение изображения и реконструкция действительно влияют на точность SUV, но коррекция с помощью фантома может минимизировать эти различия при сравнении SUV для многоцентровых клинических исследований. [42] [43] SUV может не обладать чувствительностью при измерении реакции на лечение, поскольку это простой показатель поглощения индикатора в кости, на который помимо целевой рентабельности инвестиций влияет поглощение индикатора в других конкурирующих тканях и органах. [44] [45]
Измерение K i
[ редактировать ]Количественная оценка динамических ПЭТ-исследований для измерения Ki требует измерения скелетных кривых время-активность (TAC) из области интереса (ROI) и функции артериального входа (AIF), которую можно измерить различными способами. Однако наиболее распространенным является коррекция кривых активности крови на основе изображений с использованием нескольких образцов венозной крови, взятых в дискретные моменты времени во время сканирования пациента. Расчет констант скорости или K i требует трех шагов: [3]
- Измерение функции артериального входа (AIF), которая действует как первый вход в математическую модель распределения индикатора.
- Измерение кривой время-активность (TAC) в интересующей области скелета, которая действует как второй входной сигнал для математической модели распределения индикатора.
- Кинетическое моделирование AIF и TAC с использованием математического моделирования для получения чистого плазменного клиренса (K i ) до костного минерала.

Спектральный метод
[ редактировать ]Метод был впервые описан Cunningham & Jones. [46] в 1993 году для анализа данных динамической ПЭТ, полученных в головном мозге. Предполагается, что функцию импульсного ответа ткани (IRF) можно описать как комбинацию многих экспонент. Поскольку A ткани TAC может быть выражен как свертка измеренной функции артериального входа с IRF, C кость (t) может быть выражена как:
где, — оператор свертки, Cкость ( t) — концентрация активности индикатора в костной ткани (в единицах: МБк/мл) за период времени t, Cplasma ( t) — концентрация индикатора в плазме (в единицах: МБк/мл). ml) в течение периода времени t, IRF(t) равна сумме экспонент, значения β фиксируются в пределах 0,0001 с. −1 и 0,1 сек. −1 с интервалом 0,0001 n — количество α-компонентов, полученных в результате анализа, а β 1 , β 2 ,..., β n соответствует соответствующим α 1 , α 2 ,..., α n компонентам из полученных результатов. спектр. Значения α затем оцениваются на основе анализа путем подгонки мультиэкспоненты к IRF. Точка линейной аппроксимации медленной составляющей этой экспоненциальной кривой считается плазменным клиренсом (K i ) костного минерала.
Метод деконволюции
[ редактировать ]Метод был впервые описан Williams et al. в клиническом контексте. [47] Этот метод использовался во многих других исследованиях. [48] [49] [50] Это, пожалуй, самый простой из всех математических методов расчета K i, но наиболее чувствительный к шуму, присутствующему в данных. TAC ткани моделируется как свертка измеренной функции артериального входа с IRF, оценки IRF получаются итеративно, чтобы минимизировать различия между левой и правой частями следующего уравнения:
где, — оператор свертки, Cкость ( t) — концентрация активности индикатора в костной ткани (в единицах: МБк/мл) за период времени t, Cplasma ( t) — концентрация индикатора в плазме (в единицах: МБк/мл). ml) за период времени t, а IRF(t) — это импульсный отклик системы (т.е. в данном случае ткани). K . i получают из IRF аналогично полученному для спектрального анализа, как показано на рисунке
Модель Хокинса
[ редактировать ]
Измерение Ki с помощью динамических ПЭТ-сканирований требует кинетического моделирования индикаторов для получения параметров модели, описывающих биологические процессы в кости , как описано Hawkins et al. [22] Поскольку эта модель имеет два тканевых отсека, ее иногда называют моделью с двумя тканями. Существуют различные версии этой модели; однако здесь рассматривается наиболее фундаментальный подход с двумя тканевыми компартментами и четырьмя параметрами обмена индикаторов. Весь процесс кинетического моделирования с использованием модели Хокинса можно суммировать в одном изображении, как показано справа. Для получения констант скорости решаются следующие дифференциальные уравнения:
Константа скорости К 1 (в единицах: мл/мин/мл) описывает однонаправленный клиренс фторида из плазмы во всю костную ткань, k 2 (в единицах: мин −1 ) описывает обратный транспорт фторида из отсека ECF в плазму, k 3 и k 4 (в единицах мин. −1 ) описывают прямую и обратную транспортировку фторида из минерального компартмента кости.
K i представляет собой чистый плазменный клиренс только до костных минералов. K i является функцией как K 1 , отражающего костный кровоток, так и фракции индикатора, которая подвергается специфическому связыванию с костным минералом k 3 / ( k 2 + k 3 ). Поэтому,
Хокинс и др. обнаружили, что включение дополнительного параметра, называемого фракционным объемом крови (BV), представляющего пространства сосудистой ткани в пределах ROI, улучшило проблему подбора данных, хотя это улучшение не было статистически значимым. [51]
Разнесенный метод
[ редактировать ]Разнесенный метод [52] основан на предположении, что обратный поток индикатора из костного минерала в костный ECF равен нулю (т.е. k 4 =0). Расчет K i с использованием метода Патлака проще, чем с использованием нелинейной регрессии (NLR), подгоняющей функцию артериального входа ткани и данные кривой времени-активности к модели Хокинса. Крайне важно отметить, что метод Патлака может измерять только клиренс костной плазмы ( K i ) и не может измерять отдельные кинетические параметры K 1 , k 2 , k 3 или k 4 .
Концентрацию индикатора в интересующей области ткани можно представить как сумму концентраций в костном ECF и костном минерале. Математически это можно представить как
где в интересующей области ткани на ПЭТ-изображении Cbone ( T) — концентрация активности индикатора в костной ткани (в единицах: МБк/мл) в любой момент времени T, Cplasma ( T) — концентрация в плазме индикатора (в единицах: МБк/мл) во время T, V o представляет собой долю ROI, занимаемую отделением ECF, и — площадь под плазменной кривой — чистая доставка индикатора в интересующую область ткани (в единицах: МБк.сек/мл) с течением времени T. Уравнение Патлака представляет собой линейное уравнение вида

Таким образом, линейная регрессия аппроксимируется данными, нанесенными на оси Y и X в период от 4 до 60 минут, чтобы получить m и c значения , где m — наклон линии регрессии, представляющей K i, а c — точка пересечения Y линия регрессии, представляющая V o . [52]
Метод Сиддика – Блейка
[ редактировать ]Расчет Ki с использованием функции артериального входа, кривой «время-активность» и модели Хокинса был ограничен небольшой областью скелета, охватываемой узким полем зрения ПЭТ-сканера при получении динамического сканирования. Однако Сиддик и др. [53] показали в 2012 году, что можно измерить значения K i в костях с помощью статических [ 18 F]NaF ПЭТ-сканирование. Блейк и др. [32] позже в 2019 году показал, что K i , полученный с использованием метода Сиддика – Блейка, имеет погрешность точности менее 10%. Подход Сиддика-Блейка основан на сочетании метода Патлака, [52] функция артериального входа на основе полупопуляции, [54] и информация о том, что V o существенно не меняется после лечения. Этот метод использует информацию о том, что линия линейной регрессии может быть построена с использованием данных как минимум из двух моментов времени, чтобы получить m и c, как описано в методе Патлака. Однако, если V o известно или фиксировано, требуется только одно статическое ПЭТ-изображение для получения второго момента времени для измерения m , представляющего значение K i . Этот метод следует применять с большой осторожностью в других клинических областях, где эти предположения могут оказаться неверными.
Внедорожник против К я
[ редактировать ]Наиболее фундаментальное различие между значениями SUV и K i заключается в том, что SUV представляет собой простой показатель усвоения, который нормализуется по массе тела и введенной активности. Внедорожник не учитывает доставку трассера в интересующий локальный регион, откуда проводятся измерения, поэтому на него влияет физиологический процесс, потребляющий [ 18 F]NaF в других частях тела. С другой стороны, K i измеряет плазменный клиренс костного минерала, принимая во внимание поглощение индикатора в других частях тела, влияющее на доставку индикатора в интересующую область, из которой получены измерения. Разница в измерении K i и SUV в костной ткани с помощью [ 18 F]NaF более подробно объяснены Blake et al. [34]
Важно отметить, что большинство методов расчета Ki требуют динамического ПЭТ-сканирования в течение часа, за исключением методов Сиддика-Блейка. Динамическое сканирование является сложным и дорогостоящим. Однако для расчета SUV требуется одно статическое ПЭТ-сканирование, выполняемое примерно через 45–60 минут после инъекции трассера в любой области скелета, отображаемой на изображении.
Многие исследователи показали высокую корреляцию между значениями SUV и K i в различных участках скелета. [55] [56] [57] Однако методы SUV и K i могут противоречить друг другу при измерении реакции на лечение. [45] Поскольку SUV не прошел валидацию с помощью гистоморфометрии, его полезность в исследованиях костей, измеряющих реакцию на лечение и прогрессирование заболевания, сомнительна.
См. также
[ редактировать ]- Кость
- Позитронно-эмиссионная томография
- Кривая время-активность
- Функция артериального входа
- Медицинская визуализация
- Радиология
- Молекулярная визуализация
- Медицинская визуализация
- Сцинтиграфия костей
Ссылки
[ редактировать ]- ^ Компстон, Дж. Э.; Краучер, ИП (август 1991 г.). «Гистоморфометрическая оценка ремоделирования трабекулярной кости при остеопорозе». Кость и минерал . 14 (2): 91–102. дои : 10.1016/0169-6009(91)90086-ф . ISSN 0169-6009 . ПМИД 1912765 .
- ^ Бек Дженсен, JE; Коллеруп, Г.; Оренсен, штат Ха; Нильсен, С. Порс; Соренсен, Огайо (январь 1997 г.). «Единичное измерение биохимических маркеров костного обмена имеет ограниченную полезность для отдельного человека». Скандинавский журнал клинических и лабораторных исследований . 57 (4): 351–359. дои : 10.3109/00365519709099408 . ISSN 0036-5513 . ПМИД 9249882 .
- ^ Перейти обратно: а б с Пури, Т.; Фрост, МЛ; Карран, КМ; Сиддик, М.; Мур, АЕБ; Кук, GJR; Марсден, ПК; Фогельман, И.; Блейк, генеральный менеджер (12 мая 2012 г.). «Различия в региональном костном метаболизме позвоночника и бедра: количественное исследование с использованием позитронно-эмиссионной томографии с фторидом 18F». Международный остеопороз . 24 (2): 633–639. дои : 10.1007/s00198-012-2006-x . ISSN 0937-941X . ПМИД 22581294 . S2CID 22146999 .
- ^ Аалтонен, Луиза; Берёзовая накидка, Ниина; Сеппянен, Марко; Тонг, Сяоюй; Крегер, Хейкки; Лёйттиниеми, Элииса; Метсяринне, Кай (май 2020 г.). «Корреляция между позитронно-эмиссионной томографией с фторидом натрия 18F и гистоморфометрией костей у пациентов на диализе» . Кость . 134 : 115267. doi : 10.1016/j.bone.2020.115267 . ISSN 8756-3282 . ПМИД 32058018 .
- ^ Перейти обратно: а б Месса, К. (1 октября 1993 г.). «Метаболическая активность костей, измеренная с помощью позитронно-эмиссионной томографии и иона [18F] фтора при почечной остеодистрофии: корреляция с гистоморфометрией кости». Журнал клинической эндокринологии и метаболизма . 77 (4): 949–955. дои : 10.1210/jcem.77.4.8408470 . ISSN 0021-972X . ПМИД 8408470 .
- ^ Пирт, Моран; Зиттель, Тилман Т.; Мачулла, Ханс-Юрген; Беккер, Георг Александер; Ян, Майкл; Майер, Герхард; Бэрес, Роланд; Беккер, Хорст Дитер (1 августа 1998 г.). «Измерения кровотока с помощью [15O]H2O и [18F]фторид-ионов ПЭТ в свиных позвонках» . Журнал исследований костей и минералов . 13 (8): 1328–1336. дои : 10.1359/jbmr.1998.13.8.1328 . ISSN 0884-0431 . ПМИД 9718202 . S2CID 19824951 .
- ^ Пирт, Моран; Мачулла, Ханс-Юрген; Ян, Майкл; Штальшмидт, Анке; Беккер, Георг А.; Зиттель, Тилман Т. (13 апреля 2002 г.). «Взаимосвязь кровотока и метаболизма костей свиньи при заболеваниях костей с высоким оборотом, измеренная с помощью позитронно-эмиссионной томографии с ионами [15O]H2O и [18F]». Европейский журнал ядерной медицины и молекулярной визуализации . 29 (7): 907–914. дои : 10.1007/s00259-002-0797-2 . ISSN 1619-7070 . ПМИД 12111131 . S2CID 2591493 .
- ^ Шумихен, К.; Ремпфл, Х.; Вагнер, М.; Хоффманн, Г. (1979). «Кратковременная фиксация радиофармпрепаратов в кости». Европейский журнал ядерной медицины . 4 (6): 423–428. дои : 10.1007/bf00300839 . ISSN 0340-6997 . ПМИД 520356 . S2CID 23813593 .
- ^ Перейти обратно: а б Нарита, Наоки; Като, Кадзуо; Накагаки, Харуо; Оно, Нориказу; Камеяма, Ёитиро; Уэзерелл, Джон А. (март 1990 г.). «Распределение концентрации фторида в костях крысы». Кальцифицированная ткань International . 46 (3): 200–204. дои : 10.1007/bf02555045 . ISSN 0171-967X . ПМИД 2106380 . S2CID 2707183 .
- ^ РИВ, Дж.; АРЛОТ, М.; ВУТТОН, Р.; ЭДУАРД, К.; ТЕЛЛЕЗ, М.; ХЭСП, Р.; ЗЕЛЕНЫЙ, МЛАДШИЙ; МЕНЬЕ, П.Ж. (июнь 1988 г.). «Скелетный кровоток, гистоморфометрия подвздошной кости и кинетика стронция при остеопорозе: взаимосвязь между кровотоком и скоростью скорректированной аппозиции». Журнал клинической эндокринологии и метаболизма . 66 (6): 1124–1131. doi : 10.1210/jcem-66-6-1124 . ISSN 0021-972X . ПМИД 3372678 .
- ^ Кук, Гэри-младший; Лодж, Мартин А.; Блейк, Глен М.; Марсден, Пол К.; Фогельман, Игнак (18 февраля 2010 г.). «Различия в кинетике скелета между позвонками и плечевой костью, измеренные с помощью позитронно-эмиссионной томографии с 18F-фторидом у женщин в постменопаузе». Журнал исследований костей и минералов . 15 (4): 763–769. дои : 10.1359/jbmr.2000.15.4.763 . ISSN 0884-0431 . ПМИД 10780868 . S2CID 10630967 .
- ^ Кришнамурти, GT; Хьюботтер, Р.Дж.; Тюбис, М; Блад, WH (февраль 1976 г.). «Фармакокинетика современных радиофармпрепаратов, воздействующих на скелет». Американский журнал рентгенологии . 126 (2): 293–301. дои : 10.2214/ajr.126.2.293 . ISSN 0361-803X . ПМИД 175699 .
- ^ Перейти обратно: а б Вуттон, Р.; Доре, К. (ноябрь 1986 г.). «Однопроходная экстракция 18 F из кости кролика». Клиническая физика и физиологические измерения . 7 (4): 333–343. Бибкод : 1986CPPM....7..333W . дои : 10.1088/0143-0815/7/4/003 . ISSN 0143-0815 . ПМИД 3791879 .
- ^ Перейти обратно: а б Блау, Монте; Ганатра, Раманик; Бендер, Меррилл А. (январь 1972 г.). «18F-фторид для визуализации костей». Семинары по ядерной медицине . 2 (1): 31–37. дои : 10.1016/s0001-2998(72)80005-9 . ISSN 0001-2998 . ПМИД 5059349 .
- ^ Эдельман, И.С.; Лейбман, Дж. (август 1959 г.). «Анатомия воды и электролитов организма». Американский медицинский журнал . 27 (2): 256–277. дои : 10.1016/0002-9343(59)90346-8 . ISSN 0002-9343 . ПМИД 13819266 .
- ^ Пирсон, Р.Н.; Цена, округ Колумбия; Ван, Дж.; Джайн, РК (1 сентября 1978 г.). «Измерения внеклеточной воды: кинетика органных индикаторов бромида и сахарозы у крыс и человека». Американский журнал физиологии. Почечная физиология . 235 (3): Ф254–Ф264. дои : 10.1152/ajprenal.1978.235.3.f254 . ISSN 1931-857X . ПМИД 696835 .
- ^ Стаффурт, Дж. С.; Бирчалл, И. (январь 1959 г.). «Значение определения связанного с белками радиоактивного йода при гипертиреозе». Акта Эндокринологика . 30 (1): 42–52. дои : 10.1530/acta.0.0300042 . ISSN 0804-4643 . ПМИД 13605561 .
- ^ Уитфорд, генеральный директор (июнь 1994 г.). «Потребление и метаболизм фтора». Достижения в области стоматологических исследований . 8 (1): 5–14. дои : 10.1177/08959374940080011001 . ISSN 0895-9374 . ПМИД 7993560 . S2CID 21763028 .
- ^ Перейти обратно: а б Хоскинг, диджей; Чемберлен, MJ (1 февраля 1972 г.). «Исследования человека с 18F». Клиническая наука . 42 (2): 153–161. дои : 10.1042/cs0420153 . ISSN 0009-9287 . ПМИД 5058570 .
- ^ ТОСТЕСОН, округ Колумбия (январь 1959 г.). «Транспорт галогенидов в эритроцитах». Acta Physiologica Scandinavica . 46 (1): 19–41. дои : 10.1111/j.1748-1716.1959.tb01734.x . ISSN 0001-6772 .
- ^ Перейти обратно: а б Блейк, Глен М.; Пак-Холохан, Со-Джин; Кук, Гэри-младший; Фогельман, Игнак (январь 2001 г.). «Количественные исследования костей с применением 18F-фторида и 99mTc-метилендифосфоната». Семинары по ядерной медицине . 31 (1): 28–49. дои : 10.1053/snuc.2001.18742 . ISSN 0001-2998 . ПМИД 11200203 .
- ^ Перейти обратно: а б Хо, Карл К.; Хокинс, Рэндалл А.; Дальбом, Магнус; Глэспи, Джон А.; Сигер, Линн Л.; Чой, Ён; Шиперс, Кристиан В.; Хуан, Сун-чэн; Сатьямурти, Нагичеттиар; Баррио, Хорхе Р.; Фелпс, Майкл Э. (январь 1993 г.). «Визуализация скелета всего тела с помощью [18F] фторид-ионов и ПЭТ». Журнал компьютерной томографии . 17 (1): 34–41. дои : 10.1097/00004728-199301000-00005 . ISSN 0363-8715 . ПМИД 8419436 . S2CID 42563084 .
- ^ ТЭВС, ДОНАЛЬД Р. (ноябрь 1968 г.). «Электрофоретическая подвижность фторида сыворотки». Природа . 220 (5167): 582–583. Бибкод : 1968Natur.220..582T . дои : 10.1038/220582a0 . ISSN 0028-0836 . ПМИД 5686731 . S2CID 4220484 .
- ^ Экстранд, Дж.; Спак, CJ; Эрнебо, М. (13 марта 2009 г.). «Почечный клиренс фтора в стабильном состоянии у человека: влияние мочеиспускания и изменений pH в зависимости от диеты». Acta Pharmacologica et Toxicologica . 50 (5): 321–325. дои : 10.1111/j.1600-0773.1982.tb00982.x . ISSN 0001-6683 . ПМИД 7113707 .
- ^ Экстранд, Ян; Эрнебо, Матс; Бореус, Ларс О. (март 1978 г.). «Биодоступность фторида после внутривенного и перорального введения: важность почечного клиренса и потока мочи». Клиническая фармакология и терапия . 23 (3): 329–337. дои : 10.1002/cpt1978233329 . ISSN 0009-9236 . ПМИД 627140 . S2CID 26176903 .
- ^ Уитфорд, генеральный менеджер; Пэшли, Д.Х.; Стрингер, солдат (1 февраля 1976 г.). «Почечный клиренс фтора: явление, зависящее от pH». Американский журнал физиологии. Устаревший контент . 230 (2): 527–532. дои : 10.1152/ajplegacy.1976.230.2.527 . ISSN 0002-9513 . ПМИД 1259032 .
- ^ Костеас, А.; Вудард, штаб-квартира; Лафлин, Дж. С. (май 1971 г.). «Сравнительная кинетика кальция и фторида в костях кролика». Радиационные исследования . 46 (2): 317–333. Бибкод : 1971РадР...46..317С . дои : 10.2307/3573023 . ISSN 0033-7587 . JSTOR 3573023 . PMID 5564840 .
- ^ Уокер, П.Г. (ноябрь 1958 г.). «ХИМИЧЕСКАЯ ДИНАМИКА КОСТНЫХ МИНЕРАЛОВ. Уильям Ф. Нойман и Маргарет В. Нойман. 9¼x5½ дюйма. Стр. xi + 209, с 51 рисунком и 24 таблицами. Индекс. 1958. Чикаго: The University of Chicago Press. Лондон: Кембридж. Университетское издательство. Цена 37 шиллингов 6 пенсов . Журнал костной и суставной хирургии. Британский том . 40-Б (4):846. doi : 10.1302/0301-620x.40b4.846 . ISSN 0301-620X .
- ^ Исигуро, Харуо; Като, Кадзуо, Цзянсюэ; Ёсиока, Икуо; Хосоэ, Шимано, Рёю (апрель 1993 г.). фторида в кортикальной кости ребра человека». Calcified Tissue International . 52 (4): 278–282. : 10.1007 /bf00296652 . ISSN 0171-967X . PMID 8467408. . S2CID 31137242 doi
- ^ Гринпас, Марк Д. (25 февраля 2010 г.). «Влияние фторида на костные кристаллы». Журнал исследований костей и минералов . 5 (С1): С169–С175. дои : 10.1002/jbmr.5650051362 . ISSN 0884-0431 . ПМИД 2187325 . S2CID 22713623 .
- ^ Джонс, Алан Г.; Фрэнсис, Мэрион Д.; Дэвис, Майкл А. (январь 1976 г.). «Сканирование костей: механизмы радионуклидных реакций». Семинары по ядерной медицине . 6 (1): 3–18. дои : 10.1016/s0001-2998(76)80032-3 . ISSN 0001-2998 . ПМИД 174228 .
- ^ Перейти обратно: а б с Блейк, Глен М.; Пури, Танудж; Сиддик, Мусиб; Фрост, Мишель Л.; Мур, Амелия Э.Б.; Фогельман, Игнац (февраль 2018 г.). «Измерения костеобразования на конкретных участках с использованием ПЭТ/КТ с фторидом натрия [18F]» . Количественная визуализация в медицине и хирургии . 8 (1): 47–59. дои : 10.21037/qims.2018.01.02 . ПМЦ 5835654 . ПМИД 29541623 .
- ^ Грант, Флорида; Фэйи, FH; Паккард, AB; Дэвис, RT; Алави, А.; Тревес, ST (12 декабря 2007 г.). «Скелетная ПЭТ с фторидом 18F: применение новой технологии к старому индикатору» . Журнал ядерной медицины . 49 (1): 68–78. дои : 10.2967/jnumed.106.037200 . ISSN 0161-5505 . ПМИД 18077529 .
- ^ Перейти обратно: а б Блейк, Глен М.; Сиддик, Мусиб; Фрост, Мишель Л.; Мур, Амелия Э.Б.; Фогельман, Игнак (сентябрь 2011 г.). «Радионуклидные исследования костного метаболизма: обеспечивают ли поглощение костной ткани и клиренс костной плазмы эквивалентные измерения метаболизма костной ткани?». Кость . 49 (3): 537–542. дои : 10.1016/j.bone.2011.05.031 . ISSN 8756-3282 . ПМИД 21689803 .
- ^ Хуан (Генри) Сун-Ченг (октябрь 2000 г.). «Анатомия внедорожника». Ядерная медицина и биология . 27 (7): 643–646. дои : 10.1016/s0969-8051(00)00155-4 . ISSN 0969-8051 . ПМИД 11091106 .
- ^ Басу, Сандип; Заиди, Хабиб; Хусени, Мохамед; Бурал, Гонча; Удупа, Джей; Эктон, Пол; Торигиан, Дрю А.; Алави, Абасс (май 2007 г.). «Новые количественные методы оценки региональных и глобальных функций и структуры на основе современных методов визуализации: значение для нормальных изменений, старения и болезненных состояний». Семинары по ядерной медицине . 37 (3): 223–239. doi : 10.1053/j.semnuclmed.2007.01.005 . ISSN 0001-2998 . ПМИД 17418154 .
- ^ Лучиньяни, Г.; Паганелли, Дж.; Бомбардьери, Э. (июль 2004 г.). «Использование стандартизированных значений поглощения для оценки поглощения ФДГ с помощью ПЭТ в онкологии: клиническая перспектива». Коммуникации по ядерной медицине . 25 (7): 651–656. дои : 10.1097/01.mnm.0000134329.30912.49 . ISSN 0143-3636 . ПМИД 15208491 . S2CID 38728335 .
- ^ Фрост, МЛ; Блейк, генеральный менеджер; Пак-Холохан, С.-Дж.; Кук, GJR; Карран, КМ; Марсден, ПК; Фогельман, И. (15 апреля 2008 г.). «Долгосрочная точность кинетических исследований скелета с помощью 18F-фторида ПЭТ в оценке костного метаболизма» . Журнал ядерной медицины . 49 (5): 700–707. дои : 10.2967/jnumed.107.046987 . ISSN 0161-5505 . ПМИД 18413385 .
- ^ Виссер, ЕП; Бурман, О.К.; Ойен, WJG (15 января 2010 г.). «Внедорожник: от глупой бесполезной ценности к разумной потребительской ценности» . Журнал ядерной медицины . 51 (2): 173–175. дои : 10.2967/jnumed.109.068411 . ISSN 0161-5505 . ПМИД 20080897 .
- ^ Халама, Дж; Саджак, Р; Вагнер, Р. (июнь 2006 г.). «SU-FF-I-82: Вариабельность и точность стандартизированных значений поглощения при ПЭТ-сканировании с ФДГ». Медицинская физика . 33 (6Часть 4): 2015–2016. Бибкод : 2006MedPh..33.2015H . дои : 10.1118/1.2240762 . ISSN 0094-2405 .
- ^ Фишман, Алан Дж.; Альперт, Натаниэль М.; Бабич, Джон В.; Рубин, Роберт Х. (январь 1997 г.). «Роль позитронно-эмиссионной томографии в фармакокинетическом анализе». Обзоры метаболизма лекарств . 29 (4): 923–956. дои : 10.3109/03602539709002238 . ISSN 0360-2532 . ПМИД 9421680 .
- ^ Крак, Нанда К.; Буэллард, Р.; Хукстра, Отто С.; Твиск, Джос В.Р.; Хукстра, Корнелин Дж.; Ламмертсма, Адриан А. (15 октября 2004 г.). «Влияние метода определения и реконструкции рентабельности инвестиций на количественный результат и применимость в исследовании по мониторингу ответа». Европейский журнал ядерной медицины и молекулярной визуализации . 32 (3): 294–301. дои : 10.1007/s00259-004-1566-1 . ISSN 1619-7070 . ПМИД 15791438 . S2CID 22518269 .
- ^ Вестертерп, Маринке; Прюим, Ян; Ойен, Вим; Хукстра, Отто; Паанс, Энн; Виссер, Эрик; ван Ланшот, Ян; Слуф, Геррит; Боеллаард, Рональд (11 октября 2006 г.). «Количественная оценка исследований FDG PET с использованием стандартизированных значений поглощения в многоцентровых исследованиях: влияние реконструкции изображения, разрешения и параметров определения рентабельности инвестиций». Европейский журнал ядерной медицины и молекулярной визуализации . 34 (3): 392–404. дои : 10.1007/s00259-006-0224-1 . ISSN 1619-7070 . ПМИД 17033848 . S2CID 1521701 .
- ^ Блейк, генеральный менеджер; Фрост, МЛ; Фогельман, И. (16 октября 2009 г.). «Количественные радионуклидные исследования костей» . Журнал ядерной медицины . 50 (11): 1747–1750. дои : 10.2967/jnumed.109.063263 . ISSN 0161-5505 . ПМИД 19837752 .
- ^ Перейти обратно: а б Фрост, Мишель Л; Сиддик, Мусиб; Блейк, Глен М; Мур, Амелия Э.Б.; Шлейер, Пол Дж; Данн, Джоэл Т; Сомер, Эдвард Дж; Марсден, Пол К; Истелл, Ричард; Фогельман, Игнак (май 2011 г.). «Дифференциальное влияние терипаратида на региональное костеобразование с использованием позитронно-эмиссионной томографии с фторидом 18F» . Журнал исследований костей и минералов . 26 (5): 1002–1011. дои : 10.1002/jbmr.305 . ISSN 0884-0431 . ПМИД 21542003 . S2CID 40840920 .
- ^ Каннингем, Винсент Дж.; Джонс, Терри (январь 1993 г.). «Спектральный анализ динамических ПЭТ-исследований» . Журнал церебрального кровотока и метаболизма . 13 (1): 15–23. дои : 10.1038/jcbfm.1993.5 . ISSN 0271-678X . ПМИД 8417003 .
- ^ Спеддинг, В. (2001). «Живая лаборатория будет анализировать рыночные данные в режиме реального времени». Количественные финансы . 1 (6): 568–570. дои : 10.1088/1469-7688/1/6/606 . ISSN 1469-7688 . S2CID 154537213 .
- ^ Либерати, Д.; Туркхаймер, Ф. (1999). «Линейная спектральная деконволюция снижения катаболической концентрации плазмы при диализе». Медицинская и биологическая инженерия и вычислительная техника . 37 (3): 391–395. дои : 10.1007/bf02513317 . ISSN 0140-0118 . ПМИД 10505392 . S2CID 25080033 .
- ^ Лау, Чи-хой Лун, Пак-конг Дэниел Фэн, Д. Дэвид (1998). Неинвазивная количественная оценка физиологических процессов с помощью динамической ПЭТ с использованием слепой деконволюции . IEEE. OCLC 697321031 .
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Чи-Хой Лау; Лунь, ДП-К.; Даган Фэн (1998). «Неинвазивная количественная оценка физиологических процессов с помощью динамической ПЭТ с использованием слепой деконволюции». Материалы Международной конференции IEEE по акустике, речи и обработке сигналов 1998 г., ICASSP '98 (Кат. № 98CH36181) . Том. 3. ИИЭР. стр. 1805–1808. дои : 10.1109/icassp.1998.681811 . HDL : 10397/1882 . ISBN 0-7803-4428-6 . S2CID 5947145 .
- ^ Пури, Танудж; Блейк, Глен М.; Фрост, Мишель Л.; Сиддик, Мусиб; Мур, Амелия Э.Б.; Марсден, Пол К.; Кук, Гэри-младший; Фогельман, Игнак; Карран, Кэтлин М. (июнь 2012 г.). «Сравнение шести количественных методов измерения метаболизма костной ткани в тазобедренном и поясничном отделах позвоночника с использованием ПЭТ-КТ с фторидом 18F» . Коммуникации по ядерной медицине . 33 (6): 597–606. doi : 10.1097/MNM.0b013e3283512adb . ISSN 0143-3636 . ПМИД 22441132 . S2CID 23490366 .
- ^ Перейти обратно: а б с Патлак, Клиффорд С.; Бласберг, Рональд Г.; Фенстермахер, Джозеф Д. (март 1983 г.). «Графическая оценка констант переноса крови в мозг на основе данных многократного поглощения» . Журнал церебрального кровотока и метаболизма . 3 (1): 1–7. дои : 10.1038/jcbfm.1983.1 . ISSN 0271-678X . ПМИД 6822610 .
- ^ Сиддик, Мусиб; Блейк, Глен М.; Фрост, Мишель Л.; Мур, Амелия Э.Б.; Пури, Танудж; Марсден, Пол К.; Фогельман, Игнак (8 ноября 2011 г.). «Оценка регионального костного метаболизма по статическим изображениям ПЭТ всего тела с 18F-фторидом». Европейский журнал ядерной медицины и молекулярной визуализации . 39 (2): 337–343. дои : 10.1007/s00259-011-1966-y . ISSN 1619-7070 . ПМИД 22065012 . S2CID 23959977 .
- ^ Блейк, Глен Мервин; Сиддик, Мусиб; Пури, Танудж; Фрост, Мишель Лоррейн; Мур, Амелия Элизабет; Кук, Гэри Джеймс Р.; Фогельман, Игнак (август 2012 г.). «Функция ввода полупопуляции для количественной оценки статических и динамических ПЭТ-сканирований с фторидом 18F». Коммуникации по ядерной медицине . 33 (8): 881–888. дои : 10.1097/mnm.0b013e3283550275 . ISSN 0143-3636 . ПМИД 22617486 . S2CID 42973690 .
- ^ Пури, Танудж; Блейк, Глен М.; Фрост, Мишель Л.; Сиддик, Мусиб; Мур, Амелия Э.Б.; Марсден, Пол К.; Кук, Гэри-младший; Фогельман, Игнак; Карран, Кэтлин М. (июнь 2012 г.). «Сравнение шести количественных методов измерения метаболизма костной ткани в тазобедренном и поясничном отделах позвоночника с использованием ПЭТ-КТ с фторидом 18F». Коммуникации по ядерной медицине . 33 (6): 597–606. doi : 10.1097/mnm.0b013e3283512adb . ISSN 0143-3636 . ПМИД 22441132 . S2CID 23490366 .
- ^ БРЕННЕР, В. (2004). «Сравнение различных количественных подходов к ПЭТ-сканированию с фторидом 18F» . Джей Нукл Мед . 45 (9): 1493–500. ПМИД 15347716 .
- ^ Бреннер, Винфрид; Вернон, Шерил; Конрад, Эрнест У.; Эри, Джанет Ф. (10 июня 2004 г.). «Оценка метаболической активности костных трансплантатов с помощью ПЭТ с 18F-фторидом». Европейский журнал ядерной медицины и молекулярной визуализации . 31 (9): 1291–8. дои : 10.1007/s00259-004-1568-z . ISSN 1619-7070 . ПМИД 15197502 . S2CID 10000344 .









